2. 上海体育学院 运动科学学院,上海 200438;
3. 湖北民族学院 体育学院,湖北 恩施 445300
2. School of Kinesiology, Shanghai University of Sport, Shanghai 200438, China;
3. School of Physical Education, Hubei University for Nationalities, Enshi 445300, Hubei, China
由于长期处于高强度的运动训练应激,女性运动员发生月经周期紊乱的比例要远高于普通人[1]。长期月经周期紊乱可影响骨代谢,不利于骨骼健康[2-4],并且会对运动员以后的生育健康埋下隐患[5]。研究发现,长期高强度运动训练状态下,机体摄入的能量远不能满足运动所需要的能量,造成机体可利用能量的负平衡是引起月经周期紊乱的起始因素[6-7]。因此,增加可利用能量的摄入和降低运动量及强度是缓解月经周期紊乱的方法[8]。在实际训练中,为了提高或维持运动能力,采用降低运动量及强度对于运动员而言不现实,而通过增加可利用能量摄入的方法具有实用意义[9]。本文通过补充低聚糖的方法,探讨在外源性能量补充的情况下,是否可以缓解动情周期抑制大鼠的HPO轴(hypothalamus-pituitary-ovarian axis)激素释放紊乱,为运动员月经周期紊乱的防治提供理论基础。
1 研究对象与方法 1.1 研究对象选取由上海实验动物资源中心西普尔-必凯实验动物有限公司提供的健康成熟2月龄雌性SD大鼠36只,平均体质量为(200.0±5.9) g。将符合国家饲料卫生标准的啮齿类动物饲料(由上海仕林生物科技有限公司提供,产品标准编号为Q/TJCX 1-2007)作为基础标准饲料(1 337 kJ/100 g,每100 g饲料中含有脂肪4 g、蛋白质19 g、糖类52 g)。低聚糖干预组所用的低聚糖由河北华辰淀粉糖有限公司提供,生产许可证号为QS130123010057,质量管理体系认证证书编号为00109Q23299R0M/1300。本实验设计通过上海市营养学会医学伦理委员会的鉴定,并接受其监督([伦审]2013-002)。
1.2 研究方法 1.2.1 分组及干预方法选取2月龄SD雌性大鼠36只,在适应运动2周后,随机分为4组,每组9只。为了全面观察实验组的干预效果,对照组设计为2组,分别为阴性对照组(negative control group,Nco组),该组为常规对照组,不进行运动训练,以维持正常的动情周期;阳性对照组(postive control group,Pco组),该组为动情周期抑制模型组,进行9周运动训练,前6周为递增负荷训练,后3周为恒定负荷训练,以维持动情周期抑制状态。
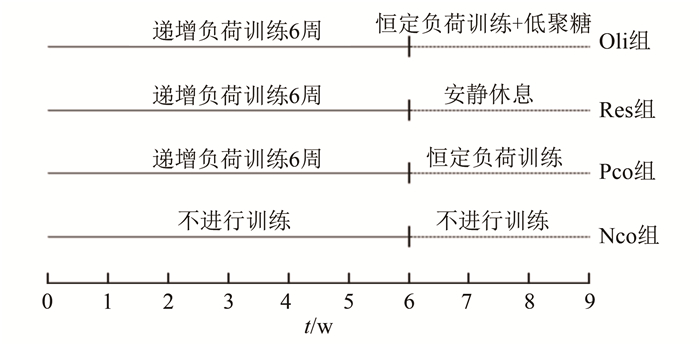
实验组设计为2组,前6周均采用递增负荷训练,后3周采取不同的干预方式,其中后3周不再进行运动训练,只进行安静休息的为安静休息组(rest intervention group,Res组),用于观察安静休息的干预方法对动情周期抑制的缓解作用,并与补充低聚糖的干预方法进行效果比较;继续进行3周恒定负荷训练,采用低聚糖进行补充的为低聚糖补充组(oligosaccharide intervention group,Oli组)。实验组的运动负荷方案同Pco组一致,后3周采用的恒定训练负荷是第6周的训练负荷(图 1)。
|
图 1 实验设计 Figure 1 Experimental design |
本实验模拟运动训练中周期性耐力跑的方式,参照Bedford大鼠运动负荷标准[10]和王人卫教授建立的大鼠动情周期抑制模型时的运动方案[11],采用段氏PT98型鼠类跑台进行训练。每笼3只,每周连续训练6 d,然后休息1 d,每天上、下午各训练1次(训练负荷见表 1),第9周最后一天下午训练结束后,晚上再加训1次。对照组和实验组前6周均采用普食喂养,每天固定为每笼投喂相同量的饲料(每天早上称量对照组一天消耗的饲料量,然后以此为参考,给实验组进行喂食)和200 mL饮用纯净水;后3周,Oli组在普食喂养的基础上,每天下午饮用含有24 g低聚糖(17.2 kJ/g)的100 mL温水(第二天早上补充100 mL饮用纯净水,以保障每组每天饮水总量相同)其余组仍200 mL饮用纯净水。总体上,Oli组平均每天增加能量摄入17.2 kJ/g×24 g/3只=137.6 kJ/只。
| 表 1 大鼠运动负荷的设定标准 Table 1 Set standard for rats exercise load |
参考Marcondes的方法[12],为避免造成待检查大鼠应激反应,检查的大鼠和待检查的大鼠分置于不同的实验室。待检查大鼠放置动物手术台后,安抚并清理大鼠毛上的垫料,用拇指和食指捏住大鼠尾巴,其余三指轻压其后腰背部,翻起尾巴露出阴道口,清理粪便后,用医用棉签蘸少许生理盐水,在大鼠阴道按照顺时针方向轻转一周。将采集物涂于玻璃载玻片后,在无水乙醇中浸泡10 min,采用常规HE染色,通过普通光学显微镜观察阴道脱落细胞的状况。
1.2.3 激素指标检测为了消除运动应急对内分泌系统产生的不必要影响,大鼠处死前安静休息36 h,并禁食12 h。大鼠称重后,采用体积分数为10%的水合氯醛作为麻醉剂,按照每千克大鼠注射40 mg麻醉剂的量进行麻醉。待大鼠完全麻醉后,将大鼠四肢固定在手术台,迅速打开腹腔,剥离下腔静脉,用一次性负压真空管采血5~8 mL,低温离心(3 000 r/min)15 min,取上清液置于-80 ℃的冰箱中,待测GnRH、FSH、LH、E2、P及PRL。GnRH采用双抗体两步夹心酶联免疫吸附法(ELISA)测定,试剂盒由美国R & D公司提供。
E2的测定采用免疫化学发光法,试剂盒由Beckman Coulter公司提供,采用Beckman Coulter公司生产的Access 2 immunoassay system(全自动化学发光免疫测定系统)进行测试。采用双抗体放射免疫分析法测定FSH、LH、P、PRL,放射免疫分析试剂盒由第二军医大学神经生物学教研室提供。
1.3 数据处理采用SPSS 20.0数据软件包对数据进行分析处理,所有结果均以均值±标准差(M±SD)表示。采用单因素方差分析进行组间比较,采用LSD法进行两两比较。P<0.05表示具有显著性差异。
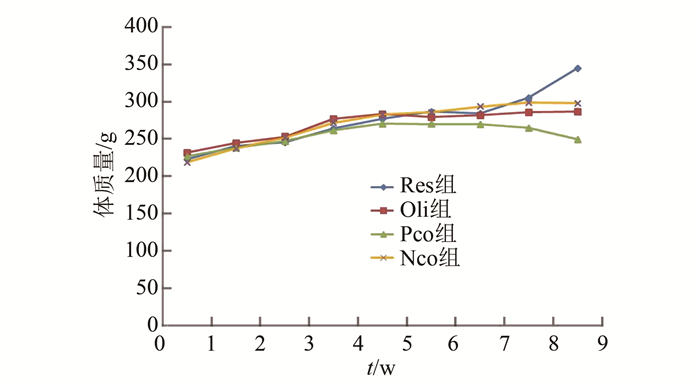
2 实验结果 2.1 大鼠体质量的变化情况由图 2可见,在前6周建立动情周期抑制状态,未进行任何干预措施前,各组大鼠的体质量的自然生长发育变化基本一致;动情周期抑制建立后,自第7周开始,体质量的不同变化趋势开始显现,Res组体质量开始迅速增加;而Oli组也呈增长趋势,但无Res组明显;Nco组体质量基本不再变化;Pco组体质量下降明显。
|
图 2 大鼠体质量的变化 Figure 2 Changes of body weight of rats |
禁食12 h后对大鼠进行处死,处死前测量大鼠的体长、体质量;处死后取大鼠内脏周围的脂肪进行称量。由表 2可见,各组大鼠的体长无组间统计学意义,但体质量、内脏脂肪含量均有统计学意义。为了避免体质量对内脏脂肪质量的影响,将内脏脂肪质量/体质量×100作为衡量大鼠体脂率的指标。经过统计发现:Pco组大鼠体脂率显著低于Nco组,但无统计学意义;Oli组大鼠体脂率显著低于Nco组;Res组合Oli组大鼠体脂率显著高于Pco组;Oli组大鼠体脂率低于Res组,但无统计学意义。
| 表 2 大鼠形态指标比较(M±SD) Table 2 Comparison of morphological parameter of rats |
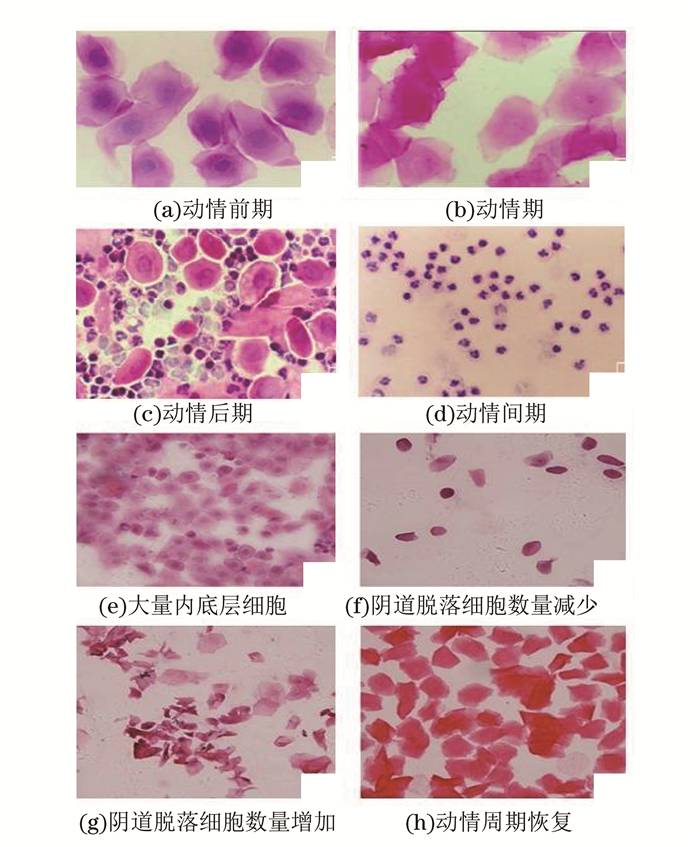
大鼠的动情周期一般为4~5 d,图 3(a)~(d)为Nco组大鼠一个动情周期的阴道脱落细胞HE染色结果,该组为动情周期正常组。由图 3可见,不同动情周期阶段表现出不同的阴道脱落细胞特征:图 3(a)为动情前期,该阶段以大量有核表层细胞为特征;图 3(b)为动情期,该阶段以大量无核表层细胞为特征;图 3(c)为动情后期,该阶段以大量有核表层细胞和白细胞为特征;图 3(d)为动情间期,该阶段以出现大量白细胞为特征。
|
图 3 大鼠阴道脱落细胞HE染色结果 Figure 3 Results of HE staining of vaginal exfoliated cells in rats |
实验开始2周后,每2天进行阴道脱落细胞学检查,结果显示:运动训练第3周后,实验干预组各组阴道涂片出现中层细胞和少量底层细胞;第4~5周时,出现大量的中层细胞和相对少量的底层细胞;第6周时,出现大量底层细胞和相对少量的中层细胞,并且阴道脱落细胞数量明显较前几周减少(图 3(e)、(f))。这表明,经过6周的递增负荷训练,动情周期开始出现抑制,这与王人卫等[11]观察到的一致。
在第7周开始进行干预,阴道脱落细胞学观察发现:Res、Oli组阴道脱落细胞数量开始增加(图 3(g));至第9周后,以上2组大鼠阴道脱落细胞数量同Nco组无显著性差异(图 3(h));随着运动的继续,Pco组阴道脱落细胞显著减少。
2.4 HPO轴激素浓度情况通过阴道脱落细胞学检查确认大鼠的动情周期抑制状态建立后,再进行3周恒定负荷训练,并采取不同的干预措施。结果显示,HPO轴释放的各激素浓度均有组间统计学差异(表 3)。两两比较的结果显示,Pco组的GnRH、FSH、LH、E2及P浓度均显著低于Nco组,而Pco组的PRL浓度则显著高于Nco组。Res组和Oli组的GnRH、FSH、LH、E2及P浓度均低于Nco组,而Nco组的PRL浓度高于Res组和Oli组,但均无统计学意义。Res组和Oli组的GnRH、FSH、LH、E2及P浓度均显著高于Pco组,而Res组和Oli组的PRL浓度则显著低于Pco组。Oli组同Res组比较发现,除释放的GnRH浓度显著高于Res组外,其余激素浓度,Res组和Nco组均无统计学差异(表 4~表 9)。
| 表 3 HPO轴激素浓度情况比较(M±SD) Table 3 Comparison of HPO axis hormone concentration |
| 表 4 GnRH组间比较结果 Table 4 Comparison of GnRH between groups |
| 表 5 FSH组间比较结果 Table 5 Comparison of FSH between groups |
| 表 6 LH组间比较结果 Table 6 Comparison of LH between groups |
| 表 7 E2组间比较结果 Table 7 Comparison of E2 between groups |
| 表 8 P组间比较结果 Table 8 Comparison of P between groups |
| 表 9 PRL组间比较结果 Table 9 Comparison of PRL between groups |
动情周期是有胎盘类哺乳动物拥有的一种经常性的生理变化,与人类的月经周期相似,是受身体性腺轴释放的性激素影响而产生的周期性变化。动情周期抑制类似于女性的闭经,是一种病理状态,长期处于这种状态,不仅会影响身体健康,还会抑制生殖功能。本文以大鼠动情周期抑制模型模拟女性闭经,通过补充低聚糖,增加外源性能量摄入,观察是否可以促进HPO轴激素释放恢复正常,以逆转动情周期抑制状态。
3.1 对内脏脂肪含量的影响体质量是早期衡量月经周期是否规律的直观指标。早期学者发现从事形体类运动项目的运动员,如体操运动员[13],普遍存在体质量过轻,月经周期不规律的问题,体质量与月经周期存在密切的相关性。本文各组雌性大鼠体质量在前6周未采取干预措施前,随着自然生长发育体质量变化基本一致,但当动情周期抑制形成后,随着不同干预措施的施行,大鼠的体质量呈现不同的变化。主要原因是由于运动训练负荷的降低和外源性可利用能量的补充,使得安静休息组和补充低聚糖组大鼠的体质量得以继续维持生长,而运动强度和饮食保持不变的阳性对照组(即动情周期抑制模型组)则由于缺乏足够的外源性能量补充,体质量呈现下降趋势。
体质量的变化只是直观现象,内脏脂肪含量的变化才是客观原因。研究表明,内脏脂肪对维持正常的动情周期具有重要作用。总结已有的研究[14-16],学者认为:①内脏脂肪是能量存储器,可以为动情周期的维持提供必需的可利用能量;②内脏脂肪也具有分泌瘦素(leptin)的作用,能直接作用于中枢神经系统的leptin受体,对中枢神经系统释放进行机体能量储存的信号,并且与下丘脑GnRH脉冲性释放密切相关,从而直接影响HPO轴。本文发现,虽然补充低聚糖组的内脏脂肪含量低于安静休息组和阴性对照组(均无统计学差异),却显著高于阳性对照组,表明通过补充低聚糖可以有效阻止内脏脂肪的消耗,并达到与安静休息近似的效果。
3.2 对阴道脱落细胞学的影响研究发现,长期力竭运动致动情周期紊乱大鼠的卵巢颗粒细胞凋亡指数显著高于正常对照组[17]。对动情周期正常的大鼠进行递增负荷训练时发现:当训练进行到第3周时,阴道涂片出现中层细胞和少量底层细胞,卵巢功能开始表现出轻度低落;当训练至第7周时,则出现大量底层细胞和相对少量的中层细胞,表现为卵巢功能大幅下降[11]。经过6周递增负荷训练后发现,阴道脱落细胞的数量急剧减少,与已有研究结果[11]基本一致,表明第6周后,动情周期抑制模型已成功建立。随后进行为期3周的不同手段的干预,根据阴道脱落细胞学可知:阳性对照组的底层细胞数量显著增加,表明动情周期抑制状态加深;而安静休息组和补充低聚糖组阴道脱落细胞数量逐渐增加,开始出现无核表层细胞,表明动情周期抑制状态逐步解除。
3.3 对HPO轴合成分泌激素的影响HPO轴是由下丘脑-垂体-性腺轴组成的神经内分泌系统,控制女性发育、正常月经和性功能,因此又称性腺轴。HPO轴的每个环节均有其独特的神经内分泌功能,并且彼此调节和影响。下丘脑分泌的GnRH作用于脑垂体,促使其分泌FSH、LH和PRL;卵巢在FSH和LH的作用下分泌E2、P;子宫内膜的周期性变化又受卵巢分泌的E2、P的控制;卵巢分泌的E2、P又可通过负反馈抑制下丘脑GnRH的释放,从而使HPO轴重新调整相应激素的释放[18]。
通过比较血清激素检查结果可以发现,阳性对照组的GnRH、FSH、LH、E2及P浓度均显著低于其余各组,而PRL则显著高于其余各组。研究发现,内分泌系统由多条内分泌轴组成,每条内分泌轴对运动负荷的反应不一致,从而引起内分泌稳态失衡,导致HPO轴分泌出现紊乱[19]。有研究报道,长期高强度的剧烈运动可导致多巴胺神经元活性降低[19]。多巴胺神经元是下丘脑和脑垂体间重要的神经递质,可以通过Kp(神经细胞产生的一类多肽类激素)保持GnRH的脉冲频率。过高的PRL通过短路反馈影响下丘脑多巴胺神经元活性,由于机体长期处于负能量平衡状态,易导致下丘脑弓状核神经元的老化、凋亡及神经递质的传递出现障碍,从而抑制GnRH的合成与释放,破坏其正常的脉冲分泌[20]。当PRL分泌升高时,其通过破坏GnRH的正常脉冲式分泌导致FSH和LH分泌的减少,使卵巢合成的E2及P分泌也减少,从而造成月经周期紊乱和闭经等问题。
本文通过补充低聚糖或采取安静休息的方法发现:补充低聚糖组或安静休息组分泌的PRL水平显著低于阳性对照组,而与阴性对照组无统计学差异;且GnRH、FSH、LH、E2及P浓度均显著高于阳性对照组,并与阴性对照组无统计学差异。表明补充低聚糖或安静休息后,多巴胺神经元活性升高,且神经递质传递增多,从而缓解了因PRL分泌增加而引起的GnRH脉冲式分泌的抑制,使性腺轴各环节激素的合成与释放恢复正常,阴道脱落细胞数量逐渐增加,无核表层细胞开始出现,动情周期的抑制状态得到缓解。
4 结论通过补充低聚糖,增加大负荷运动训练状态下雌性大鼠的外源性能量摄入,使HPO轴合成分泌激素恢复正常。由此推断大鼠能量负平衡状态得到改善,使可利用能量增加,缓解了动情周期抑制状态。
| [1] |
PRATHER H, HUNT D, MCKEON K, et al. Are elite female soccer athletes at risk for disordered eating attitudes, menstrual dysfunction, and stress fractures?[J].
PM & R:The Journal of Injury, Function, and Rehabilitation, 2015, 8(3): 208-213 (  0) 0)
|
| [2] |
MITCHELL D M, TUCK P, ACKERMAN K E, et al. Altered trabecular bone morphology in adolescent and young adult athletes with menstrual dysfunction[J].
Bone, 2015, 81: 24-30 DOI:10.1016/j.bone.2015.06.021 (  0) 0)
|
| [3] |
MARQUEZ S, MOLINERO O. Energy availability, menstrual dysfunction and bone health in sports:An overview of the female athlete triad[J].
Nutricion Hospitalaria, 2013, 28(4): 1010-1017 (  0) 0)
|
| [4] |
MAIMOUN L, GEORGOPOULOS N A, SULTAN C. Endocrine disorders in adolescent and young female athletes:Impact on growth, menstrual cycles, and bone mass acquisition[J].
The Journal of Clinical Endocrinology and Metabolism, 2014, 99(11): 4037-4050 DOI:10.1210/jc.2013-3030 (  0) 0)
|
| [5] |
HIND K. Recovery of bone mineral density and fertility in a former amenorrheic athlete[J].
Journal of Sports Science & Medicine, 2008, 7(3): 415-418 (  0) 0)
|
| [6] |
BLAUWET C A, BROOK E M, TENFORDE A S, et al. Low energy availability, menstrual dysfunction, and low bone mineral density in individuals with a disability:Implications for the para athlete population[J].
Sports Medicine (Auckland, NZ), 2017: 1-12 (  0) 0)
|
| [7] |
HAND T M, HOWE S, CIALDELLA-KAM L, et al. A pilot study:Dietary energy density is similar between active women with and without exercise-associated menstrual dysfunction[J].
Nutrients, 2016, 8(4): 230-231 DOI:10.3390/nu8040230 (  0) 0)
|
| [8] |
CIALDELLA-KAM L, GUEBELS C P, MADDALOZZO G F, et al. Dietary intervention restored menses in female athletes with exercise-associated menstrual dysfunction with limited impact on bone and muscle health[J].
Nutrients, 2014, 6(8): 3018-3039 DOI:10.3390/nu6083018 (  0) 0)
|
| [9] |
LAGOWSKA K, KAPCZUK K, FRIEBE Z, et al. Effects of dietary intervention in young female athletes with menstrual disorders[J].
Journal of the International Society of Sports Nutrition, 2014, 11(1): 21-22 (  0) 0)
|
| [10] |
BEDFORD T G, TIPTON C M, WILSON N C, et al. Maximum oxygen consumption of rats and its changes with various experimental procedures[J].
Journal of Applied Physiology:Respiratory, Environmental and Exercise Physiology, 1979, 47(6): 1278-1283 (  0) 0)
|
| [11] |
王人卫, 陆爱云, 陈佩杰, 等. 递增负荷的运动性闭经动物模型的建立[J].
中国运动医学杂志, 2000, 19(3): 293-296 (  0) 0)
|
| [12] |
MARCONDES F K, BIANCHI F J, TANNO A P. Determination of the estrous cycle phases of rats:Some helpful considerations[J].
Brazilian Journal of Biology, 2002, 62(4a): 609-614 DOI:10.1590/S1519-69842002000400008 (  0) 0)
|
| [13] |
KLENTROU P, PLYLEY M. Onset of puberty, menstrual frequency, and body fat in elite rhythmic gymnasts compared with normal controls[J].
British Journal of Sports Medicine, 2003, 37(6): 490-491 DOI:10.1136/bjsm.37.6.490 (  0) 0)
|
| [14] |
李合, 王人卫, 赵璨, 等. 补充葡萄糖或低聚糖对动情周期抑制大鼠瘦素水平的影响[J].
体育科研, 2015, 36(6): 12-16 (  0) 0)
|
| [15] |
LUO Q, LI W, LI M, et al. Leptin/leptinR-kisspeptin/kiss1r-GnRH pathway reacting to regulate puberty onset during negative energy balance[J].
Annals of Pediatric Endocrinology & Metabolism, 2016, 153: 207-212 (  0) 0)
|
| [16] |
AKHTER N, CARLLEE T, SYED M M, et al. Selective deletion of leptin receptors in gonadotropes reveals activin and GnRH-binding sites as leptin targets in support of fertility[J].
Endocrinology, 2014, 155(10): 4027-4042 DOI:10.1210/en.2014-1132 (  0) 0)
|
| [17] |
付燕, 周妙蓉, 王志杰. 长期力竭运动致动情周期紊乱大鼠卵巢颗粒细胞凋亡及Bcl-2/Bax表达变化[J].
中国运动医学杂志, 2014, 33(3): 233-237 (  0) 0)
|
| [18] |
LIU T, LI N, ZHU J, et al. Effects of di-(2-ethylhexyl) phthalate on the hypothalamus-pituitary-ovarian axis in adult female rats[J].
Reproductive Toxicology, 2014, 46(7): 141-147 (  0) 0)
|
| [19] |
HACKNEY A C, DAVIS H C, LANE A R. Growth hormone-insulin-like growth factor axis, thyroid axis, prolactin, and exercise[J].
Frontiers of Hormone Research, 2016, 47(6): 1-11 (  0) 0)
|
| [20] |
GOODMAN R L, MALTBY M J, MILLAR R P, et al. Evidence that dopamine acts via kisspeptin to hold GnRH pulse frequency in check in anestrous ewes[J].
Endocrinology, 2012, 153(12): 5918-5927 DOI:10.1210/en.2012-1611 (  0) 0)
|
 2018, Vol. 42
2018, Vol. 42


