| 荧光碳量子点/锂皂石乳化的液体石蜡Pickering乳液及其性能研究 |
乳液是常见的材料形式,常应用于食品、化妆品、药品等。乳液的适当配方将确保其对液滴聚结和宏观相分离的稳定性。Pickering发现乳液的稳定性可以通过胶体颗粒在界面上的吸附而获得[1]。因此,除了常规的表面活性剂和表面活性聚合物之外,胶体颗粒已被广泛用作稳定剂。已得到详细研究[2-6]的Pickering乳液是一种由固体粒子代替传统有机表面活性剂来稳定乳液体系的新型乳液,因其避免了表面活性剂的毒性和负面作用(例如起泡、影响材料性能)以及独有的界面粒子自组装效应,近20年来受到了学者们的广泛关注[7]。Pickering乳液中用到的固体颗粒主要有片状、球状、带状、棒状等形状。片状的固体颗粒主要是黏土类[8-11],如高岭土、蒙脱石等[12];球状的固体颗粒较普遍,纳米SiO2是其中研究较多的一种[13-14],另外,还有一些比较新颖的粒子,如高分子球(主要是聚苯乙烯球)、复合球、Janus微球等,也可用于稳定乳液。
碳点(CDs)或碳量子点是尺寸小于10 nm的一类碳基纳米颗粒[15-16],从根本上说,它们是sp2杂化石墨纳米晶体,是由几个原子层组成的CDs石墨烯量子点。与石墨烯碳量子点不同,由聚合物(包括蛋白质)制成的碳点是属于聚合物点[16]。若进行功能化/改性,CDs还可以含有氧、氢、氮和各种官能团或烷基配体[17-20]。CDs的独特性和新颖性主要归因于其下列性质:高表面积,特殊形态,独特的电子、光学、热特性,生物相容性和化学惰性,因此CDs在生物标记[21-24]、生物传感[25-27]、光催化[9, 28]等方面具有很大的潜在应用价值。
石蜡乳液是指石蜡和水在表面活性剂的作用下通过不断搅拌、降低界面张力而形成的O/W型分散体系[29]。近年来随着人们对石蜡研究的不断深入,更为有效的乳化体系的研究和开发对造纸用石蜡表面施胶剂及其他造纸化学品的生产有着重要的意义,而Pickering乳液固体微粒乳化技术为解决上述问题提供了崭新的思路。
本研究制备的具有羧基和氨基的CDs具有能够与锂皂石相互作用的潜质,CDs将导致锂皂石负ζ电位的减少并诱导锂皂石颗粒聚集,而CDs的荧光性不会因为其与锂皂石相互作用而明显减少。因此,我们可以用CDs荧光标示锂皂石颗粒并提高液体石蜡乳液的稳定性。由于其优异的生物相容性、低成本和易制备性,且能够使由纳米颗粒制成的乳液稳定化,因此CDs可以在许多领域中得到应用。
1 实验 1.1 实验材料1) 主要试剂:尿素(凯米拉化学品(兖州)有限公司);柠檬酸钠(国药集团化学试剂有限工司);溴化钾(上海晶纯试剂有限公司);锂皂石(英国Rockwood试剂公司)。实验所用水为去离子水,电阻率为18.2 MΩ·cm。其他试剂均为分析纯。
2) 主要实验仪器:傅里叶变换显微红外光谱仪(Magna560型,美国Nicolet公司);原子力显微镜(Multimode-8, 布鲁克Bruker);荧光分光光度计(F-7000,日立);Y18高速乳化机(Y18,Fluco);生物光学显微镜(BK3000,奥林巴斯);电导率测量仪(DDSJ-308 A,上海沪粤明科学仪器有限公司);接触角测量仪(SDC-100S,晟鼎精密仪器);激光粒度仪(3000E,英国马尔文仪器有限公司);激光共聚焦显微镜(SP8-X,德国Leica)。
1.2 荧光碳量子点的制备及其性能表征用电子天平准确称取尿素和柠檬酸钠,按照尿素:柠檬酸钠的摩尔比为6:1称量,然后将尿素和柠檬酸钠混合均匀;混合均匀后的固体颗粒粉末置于聚四氟乙烯反应釜(100 mL)中,在160 ℃下加热1 h,然后将所得到的固体用乙醇溶解后进行超声分散;最后用透析膜透析,得到碳量子点样品。用傅里叶变换显微红外光谱仪表征(扫描范围为400~4 000 cm-1)。将荧光碳量子点分散于去离子水中,配成浓度为0.05%的溶液,分别用Zeta电位仪和纳米粒度仪测荧光碳量子点的Zeta电位和粒径大小。将荧光碳量子点分散于去离子水中,配成浓度为0.05%的溶液。取2~3滴上述溶液,滴到云母片上,自然风干后在原子力显微镜下观察荧光碳量子点的粒径分布和形貌。将荧光碳量子点分散于去离子水中,配成具有一定浓度阶梯的稀溶液,用荧光分光光度计测其荧光强度、激发和发射波长。
1.3 液体石蜡Pickering乳液的制备将CDs和锂皂石混合均匀分散到去离子水中作为水相,设定一定的油水比,液体石蜡作为油相。将液体石蜡油相迅速倒入水相中,用Y18高速乳化机在3 000 r/min的转速下乳化5 min,制得液体石蜡Pickering乳液。
1.4 乳液性能表征用改性蒙脱石固体颗粒乳化的ASA乳液的稳定性通过析出的油相体积分数Vo(相对于初始油相体积分数)和水相体积分数Vw(相对于初始水相体积分数)来表征。乳液液滴的形态及粒径用BK3000生物电子显微镜记录和测定。
乳液类型(W/O或O/W)通过测量乳液电导率来确定。所用水相电导率约为10 μS·cm-1,ASA油电导率小于0.02 μS·cm-1。当所制得的ASA乳液电导率高于10 μS·cm-1时,乳液为水包油(O/W)型;当ASA乳液电导率低于0.1 μS·cm-1时,乳液为油包水(W/O)型。
1.5 颗粒疏水性表征复合颗粒的疏水性能用接触角测量仪来表征。将复合颗粒干燥后压制成2 mm厚、直径为5 cm的薄片,置于接触角测量仪测量台上,滴一滴去离子水(50 μL)。测量水滴在颗粒薄片表面的晶态接触角。
2 结果与讨论 2.1 荧光碳量子点的性能表征 2.1.1 傅里叶变换红外谱图制备的荧光碳量子点(CDs)的傅里叶变换红外(FT-IR)谱图如图 1所示。1410 cm-1和1452 cm-1处是—CN基团的振动吸收峰;3285 cm-1和3450 cm-1处分别是—NH2和—OH基团的振动吸收峰;1589 cm-1处的尖锐峰是羧基的不对称伸缩振动吸收峰。均说明所制备的CDs表面具有羧基、羟基及C—N键。氨基和羟基是典型的亲水性基团,并且在水中电离后带负电,可与表面带正电荷的黏土颗粒结合。而羧基是疏水性基团,可通过调控其数量达到调节颗粒或复合颗粒表面亲油亲水的目的。这为复配颗粒在Pickering乳液界面两亲性可控调节方面创造了良好的条件和基础。
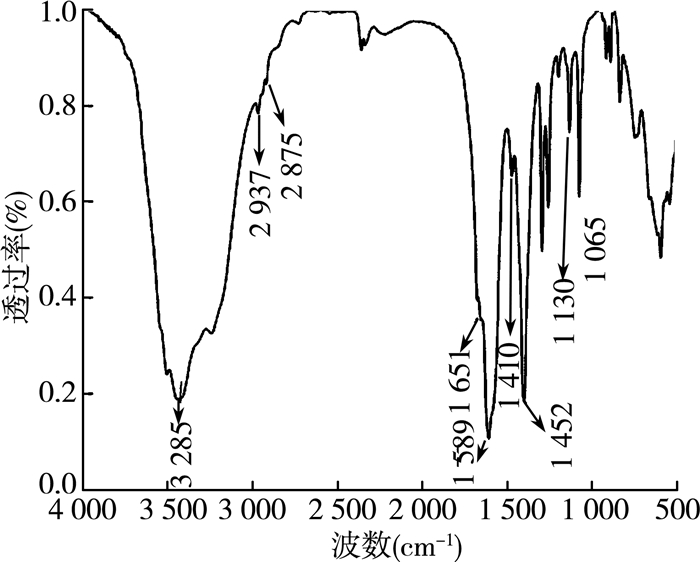 |
| 图 1 CDs的FT-IR谱图 |
2.1.2 荧光强度
利用荧光分光光度计定量测量所制备的CDs的荧光性能。图 2是固定激发波长365 nm下的荧光CDs的荧光强度曲线图。可以看出:所制备的CDs在450 nm波长处具有强烈的吸收峰,荧光强度达到3250 a.u.,可以在365 nm紫外灯照射下发出明亮的绿光,具有良好的荧光性。
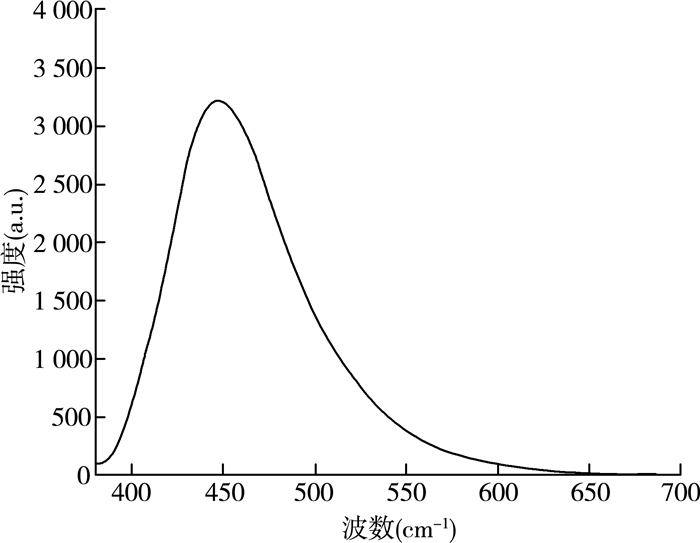 |
| 图 2 激发波长365 nm下的CDs荧光强度曲线图 |
将所制备的CDs样品浓缩或稀释至质量分数为1%,作为2#-1样本;然后用去离子水分别稀释至CDs质量分数为0.5%、0.25%、0.125%、0.05%和0.025%。固定激发波长为365 nm,测量380~700 nm发射波长范围内的碳量子点荧光强度(PL),所得结果如图 3所示。可以清楚地看到:当CDs质量分数为1%时,所制备的CDs的荧光强度最大;随着CDs浓度的降低,荧光强度逐渐降低;当CDs质量分数为0.025%时,荧光性能近乎消失。
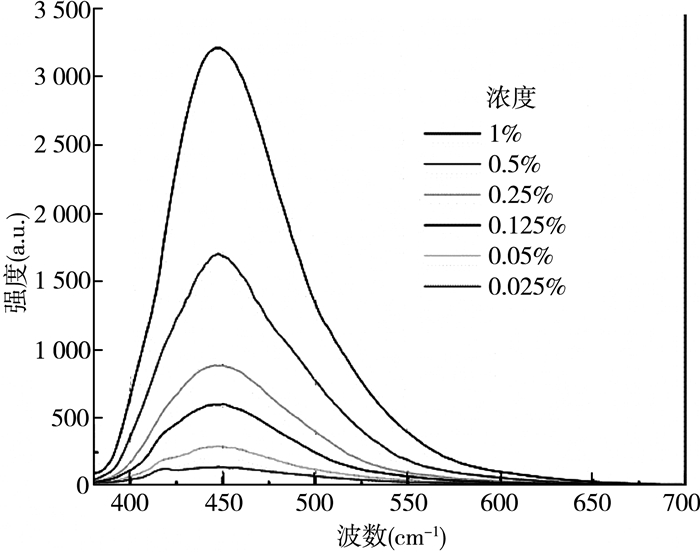 |
| 图 3 CDs在不同浓度下的荧光强度 |
2.1.3 Zeta电位和粒径分析
为了解所制备的CDs表面的带电荷情况,通过马尔文Zeta电位粒径仪对CDs的带电性能进行了测试,结果如图 4所示。可以看到:所制备的CDs带负电,Zeta电位约为-24 mV,这可能与其表面所具有的羧基和羟基基团的数量有关。所带羧基和羟基基团数量越多,CDs的负电性就越大,就越有利于跟带正电的其他颗粒相结合。
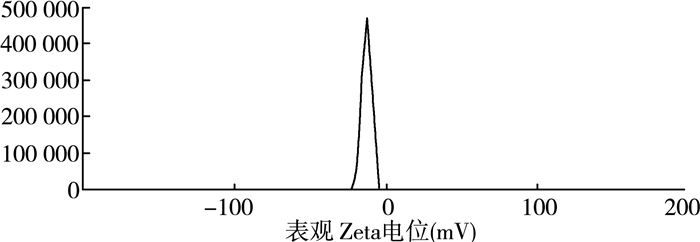 |
| 图 4 制备的CDs的Zeta电位 |
图 5是所制备的CDs纳米颗粒用马尔文Zeta电位粒径仪测得的粒度分布图。从图中可以清楚地看到,所制备的CDs在5~7 nm处具有一个很窄的强峰,这说明所制备的CDs具有良好的粒子性和粒径均一性(粒径约为6 nm)。
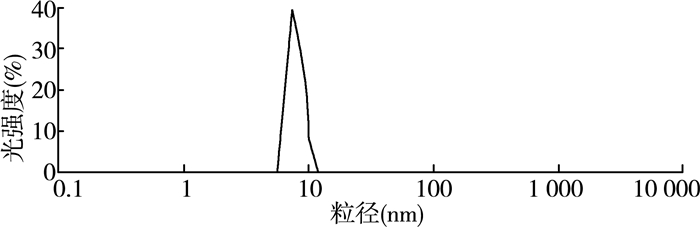 |
| 图 5 制备的CDs的粒径分布 |
利用原子力显微镜(AMF)进一步揭示所制备的CDs的粒子性,结果如图 6所示。可以看到:所制备的CDs呈圆球形,粒径为5~15 nm,具有很好的粒径分布和粒子性;CDs颗粒有部分絮聚,但总体分散良好。这为Pickering乳液界面颗粒膜的形成及稳定提供了良好的条件。
 |
| 图 6 CDs的原子力显微镜图 |
2.2 CDs和锂皂石乳化的液体石蜡Pickering乳液
首先固定锂皂石浓度为0.1%(相对于水相的质量百分比),分别配制含有不同质量(0 g、0.025 g、0.05 g、0.125 g、0.25 g、0.5 g、1 g)的CDs的混合颗粒溶液作为水相,同时保持所有乳液样品的油水比例为1:2。乳化后得到的液体石蜡乳液外观如图 7所示。
 |
| 图 7 锂皂石/CDs乳化稳定的液体石蜡Pickering乳液外观 |
图 7显示锂皂石和CDs协同作用可以将液体石蜡乳化成乳白色的乳液。当CDs用量超过0.05 g时,可以形成均一的乳白色Pickering型石蜡乳液,并且随着CDs用量的增大,乳液的乳白色越来越明显。说明CDs对锂皂石的协同乳化作用随着CDs用量的增加而增大,这可能跟CDs表面的基团(如羟基和氨基)对油水界面的协同稳定作用有关。
为了进一步观察乳液的微观形态,利用光学显微镜拍摄乳液液滴,照片如图 8所示。
 |
| 图 8 锂皂石/CDs乳化稳定的液体石蜡Pickering乳液液滴的光学显微镜照片 |
随着CDs用量的增大,乳液液滴尺寸呈现先增大后降低再增大的趋势,这可能跟锂皂石/CDs复合颗粒的絮聚程度和颗粒表面润湿程度有关。当没有CDs加入时,锂皂石单独乳化的石蜡乳液粒径很小,约为5 μm;加入CDs后,颗粒的亲水性降低,这是因为CDs带入了羧基和CN基团,使得复合颗粒的亲油性提高,导致乳液液滴变大。随着CDs用量的继续提高,达到0.125 g时,乳液液滴尺寸达到最小,这时复合颗粒的亲油亲水性达到最适宜的条件。根据Pickering乳液的接触角理论,颗粒在接触角为90°时Pickering乳液最为稳定,乳液粒径最低。再继续增大CDs用量,乳液液滴又会增大,乳液稳定性变差。液体石蜡Pickering乳液的液滴粒径分布随CDs加入量的变化如图 9所示。
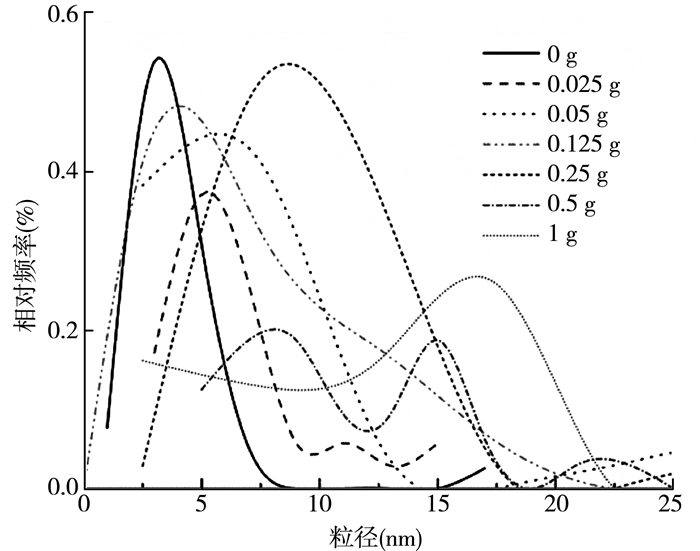 |
| 图 9 液体石蜡Pickering乳液的液滴粒径分布随CDs加入量的变化 |
从图 9中可以看出:随着CDs用量的增大,乳液液滴粒径分布呈现先增大后降低再增大的趋势;随着CDs用量的继续提高,达到0.125 g时,乳液液滴尺寸达到最小;再继续增大CDs用量,乳液液滴又会增大,乳液稳定性变差;乳液液滴粒径在CDs用量为1 g时达到最大,此时乳液的稳定性会变差。为了确定乳液的稳定性,我们将乳液放置24 h后观察乳液的分层情况。只有CDs用量为0.125 g的4#乳液样品下层没有析出水相,乳液稳定性最好,其他样品不同程度地析出了水相或者油相。这也再次证明了乳液在CDs用量为0.125 g的条件下稳定性达到最佳。
固定CDs的用量,改变锂皂石用量,观察复配颗粒中锂皂石用量对乳液稳定性的影响。固定CDs的用量为0.5 mL,质量分数为10%;依次改变加入的锂皂石的用量(mL):7、6、5、4、3、2,质量分数均为1%。固定油水比为1:1,乳化后所得乳液样品外观如图 10所示。
 |
| 注:乳液样品中的锂皂石用量(mL)从左到右依次为:2、3、4、5、6、7.5。 图 10 锂皂石/CDs乳化稳定的液体石蜡乳液外观 |
图 10显示:随着锂皂石用量的增大,乳液越来越稳定;当锂皂石用量小于3 mL时,乳液下层有浑浊水相析出,这是因为锂皂石用量不够,CDs的亲油性比锂皂石强,导致复配颗粒的亲油性较强、乳液不稳定;而当锂皂石用量超过3 mL但低于4 mL时,乳液上层有油相析出,这说明复配颗粒的亲水性大于亲油性,乳液稳定性虽有所提高,但还是不稳定;直到锂皂石用量超过5 mL后,才得到均一稳定的乳液,没有任何相体析出,这说明复合颗粒体系的亲油亲水性达到均衡。
图 11是锂皂石/CDs乳化稳定的液体石蜡Pickering乳液的光学显微镜照片。从中可以看出:随着锂皂石用量的提高,乳液粒径先降低后增大,然后保持不变。这进一步印证了随着锂皂石用量的提高,乳液稳定性先上升再下降再上升的趋势。当锂皂石用量很少的时候,乳液体系不稳定,粒径分布不均匀,乳液液滴尺寸差距很大;随着锂皂石用量的提高,上述差距逐渐降低,但乳液液滴的平均尺寸在增大,最终增大至30~50 μm。说明锂皂石的加入对提高乳化体系的稳定性具有显著效果。
 |
| 图 11 锂皂石/CDs乳化稳定的液体石蜡Pickering乳液液滴的光学显微镜照片 |
锂皂石/CDs乳化稳定的液体石蜡Pickering乳液的粒径分布随锂皂石用量的变化如图 12所示。由图 12可以看出:随着锂皂石用量的增大,乳液粒径呈现出先降低后增大、然后保持基本不变的总体趋势。说明锂皂石对于复配颗粒组成的乳化稳定体系具有良好的增益效果,但锂皂石用量并不是越大越好。锂皂石用量在5 mL时乳液粒径保持不变,乳液稳定性达到最佳;继续增大锂皂石用量可能会破坏乳液的稳定性,这是因为锂皂石和CDs可能形成的空间三维网络结构会随着锂皂石的进一步加入而被破坏,导致乳液稳定性降低。
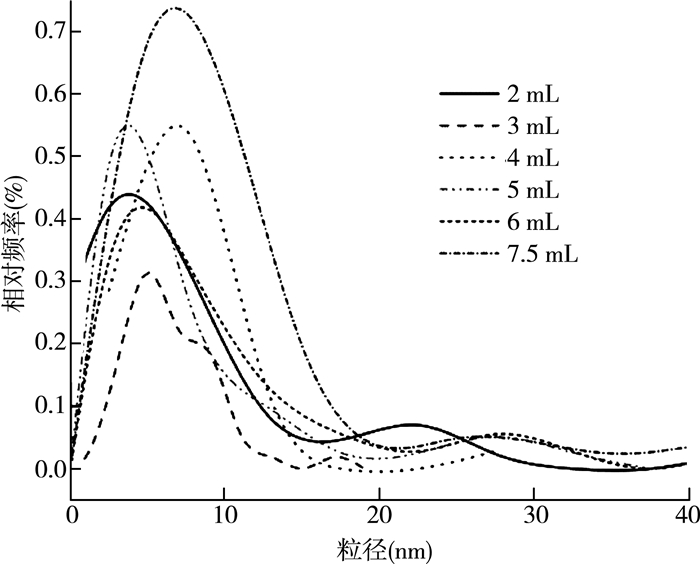 |
| 图 12 液体石蜡Pickering乳液的液滴粒径分布随锂皂石加入量的变化 |
2.3 乳液类型
Pickering乳液的油水相比例对乳液稳定性也有重要的影响。我们通过测量乳液的电导率来判断所形成的乳液是油包水型W/O还是水包油O/W型。图 13显示了固定锂皂石用量时不同CDs用量下的液体石蜡Pickering乳液的电导率。固定锂皂石的质量分数为1%,油水比为1:2,改变CDs的用量(g):0、0.025、0.05、0.125、0.25、0.5、1。
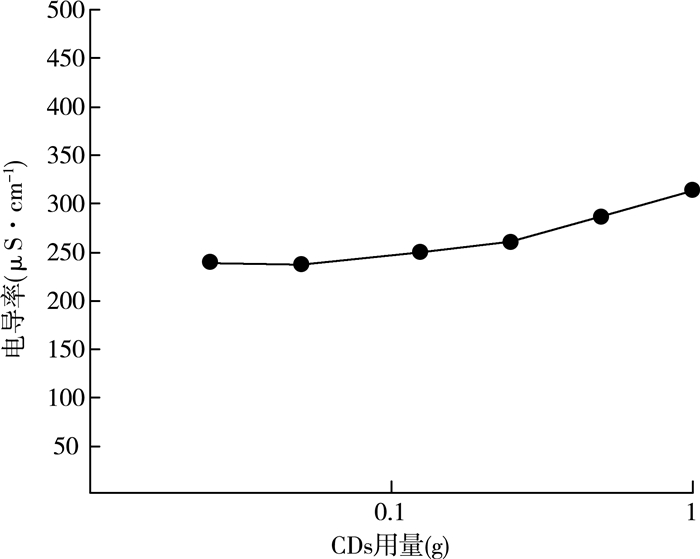 |
| 图 13 固定锂皂石用量时不同CDs用量下的液体石蜡Pickering乳液的电导率 |
从图 13中可以看出:所制备的石蜡Pickering乳液的电导率均大于10,这说明它们都是水包油型(O/W)Pickering乳液,即乳液都可以很好地分散在水中,或者加入水后可以稀释乳液。这可能是因为复配颗粒体系中的锂皂石具有很高的亲水性,在水中分散后表面电离而带有负电荷。
固定CDs的用量,改变锂皂石用量,观察了乳液类型的变化情况。固定CDs用量为1 g,改变锂皂石用量(g):0、0.01、0.02、0.05、0.1、0.25、0.5、1,油水比固定为1:2,所得乳液电导率测量结果如图 14所示。
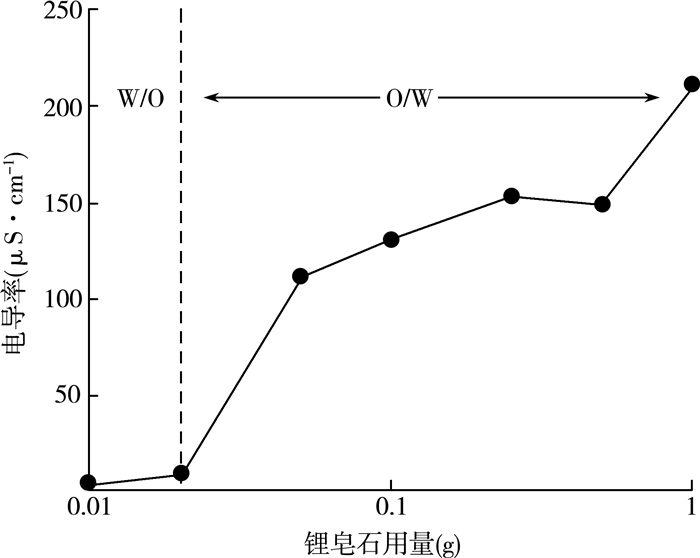 |
| 图 14 固定CDs用量时不同锂皂石用量下的液体石蜡Pickering乳液的电导率 |
可以看出:所制备的液体石蜡Pickering乳液在锂皂石用量不超过0.02 g时电导率均低于10 μS·cm-1,说明乳液是油包水(W/O)型。此时的乳液不溶于水,加入水也不能将其稀释,但加入液体石蜡油可以稀释。这可能是跟复配颗粒体系中的锂皂石用量太少而CDs用量很大有关,此时复配颗粒的亲油性要大于亲水性,使乳化的乳液表现为油包水型。当锂皂石用量超过0.05 g后,乳液电导率急剧升高且均大于10 μS·cm-1,表现为水包油型(O/W),这是因为随着锂皂石用量的提高,复配颗粒乳化体系的亲水性提高,此时复配颗粒的亲水性要大于亲油性,因而可以获得水包油型的Pickering乳液。当然,随着固体颗粒浓度的变化,乳液转相点也会随之变化。这是因为Pickering乳液液滴的形成和稳定与包裹在液滴表面的颗粒数量有关[30]。固体颗粒乳化剂浓度越高, 转相点处油水比越大;浓度越低, 转相点处油水比越小。
2.4 CDs的荧光示踪性和稳定机理Pickering乳液的形成与稳定主要是由油水界面处固体颗粒膜和连续相中固体颗粒三维网络结构产生的阻隔和保护作用决定的[31]。CDs在紫外光下会发出明亮的绿色荧光,因此可以作为理想的荧光示踪剂来应用。我们利用复配颗粒的荧光性来追踪颗粒在Pickering乳液两相(水相、油相)界面处的分布情况,从而揭示Pickering乳液的稳定机理。液体石蜡Pickering乳液的激光共聚焦显微镜(CLSM)照片如图 15所示,从左至右分别为:365 nm激发波长下的照片,460 nm激发波长下的照片,白光下的CLSM照片。
 |
| 图 15 液体石蜡Pickering乳液的激光共聚焦显微镜照片 |
从图 15的左图中可以清楚地看到乳液液滴发出的绿色荧光。这是因为由CDs和锂皂石纳米颗粒复配的颗粒吸附在油水两相的界面处,形成了一层界面颗粒膜,从而阻断了水相和油相,形成稳定的乳液。而这一层连续的绿色固体颗粒除了在油水界面处吸附以外,还在连续相中有分布,并形成3D网络结构,使乳液的液滴不能相互接触,从而有利于Pickering乳液的形成和稳定。在460 nm波长激发下的CLSM照片中也可以看到CDs发出红色的荧光,在乳滴表面和连续相中都有存在,进一步佐证了Pickering乳液的界面颗粒膜和3D网络结构的稳定理论。
3 结论利用尿素和柠檬酸钠通过高压水热法制备出具有良好荧光性能的碳量子点(CDs)纳米颗粒,并测得其在365 nm处的荧光强度。通过红外光谱发现所制备的CDs表面具有羟基、羧基、氨基和—CN基团。通过马尔文Zeta电位粒径仪发现所制备的CDs带负电,Zeta电位约为-24 mV,在5~7 nm处具有一个很窄的强峰。这说明所制备的CDs具有良好的粒子性和粒径均一性。通过AFM发现所制备的CDs具有很好的粒径分布和粒子性;CDs颗粒呈圆球形,粒径约为5~15 nm,有部分絮聚,但总体分散良好。
随着CDs用量的增大,乳液的乳白色越来越明显;CDs对锂皂石的协同乳化作用随着CDs用量的增加而增大,当用量为0.125 g时稳定性达到最佳。随着锂皂石用量的提高,乳液粒径先降低后增大、然后保持不变,乳液稳定性先上升再下降再上升。锂皂石用量在5 mL时乳液粒径保持不变,乳液稳定性达到最佳;继续增大锂皂石用量可能会破坏乳液的稳定性。锂皂石用量较低时,可以制备出油包水(W/O)型乳液;当锂皂石用量超过0.05 g后,乳液电导率急剧升高,均大于10 μS·cm-1,乳液均为水包油(O/W)型。
CDs和锂皂石纳米颗粒复配的颗粒吸附在油水两相的界面处,形成了一层界面颗粒膜和3D网络结构,从而提高了乳液的稳定性。CDs具有显著的荧光示踪性,可为Pickering乳液界面颗粒稳定机理提供崭新的研究思路。
| [1] |
PICKERING S U. CXCVI.-Emulsions[J]. J.Chem.Soc.Trans., 1907, 91: 2001-2021. DOI:10.1039/CT9079102001 |
| [2] |
HUNTER T N, PUGH R J, FRANKS G V, et al. The role of particles in stabilising foams and emulsions[J]. Advances in Colloid & Interface Science, 2008, 137(2): 57-81. |
| [3] |
BINKS B P, LIU W, RODRIGUES J A. Novel stabilization of emulsions via the heteroaggregation of nanoparticles[J]. Langmuir the Acs Journal of Surfaces & Colloids, 2008, 24(9): 4443-4446. |
| [4] |
GU G, ZHANG L, WU X A, et al. Isolation and characterization of interfacial materials in bitumen emulsions[J]. Energy & Fuels, 2006, 20(2): 673-681. |
| [5] |
HODGE S M, ROUSSEAU D. Continuous-phase fat crystals strongly influence water-in-oil emulsion stability[J]. Journal of the American Oil Chemists Society, 2005, 82(3): 159-164. DOI:10.1007/s11746-005-5166-4 |
| [6] |
LIU J, XU Z, MASLIYAH J. Role of fine clays in bitumen extraction from oil sands[J]. AIChE Journal, 2004, 50(8): 1917-1927. DOI:10.1002/(ISSN)1547-5905 |
| [7] |
周君, 乔秀颖, 孙康. Pickering乳液的制备和应用研究进展[J]. 化学通报, 2012, 75(2): 99-105. |
| [8] |
GRIM R E. Applied Clay Mineralogy[M]. MCGRAW-HILL, 1962: 39.
|
| [9] |
HANSEN E L, HEMMEN H, FONSECA D M, et al. Swelling transition of a clay induced by heating[J]. Scientific Reports, 2012, 2(8): 618. |
| [10] |
KEGEL W K, LEKKERKERKER H N. Colloidal gels:Clay goes patchy[J]. Nature Materials, 2011, 10(1): 5. DOI:10.1038/nmat2927 |
| [11] |
NADEAU P H, WILSON M J, MCHARDY W J, et al. Interstratified clays as fundamental particles:A reply[J]. Science, 1984, 225(4665): 923-925. DOI:10.1126/science.225.4665.923 |
| [12] |
PINNAVAIA T J. Intercalated clay catalysts[J]. Science, 1983, 220(4595): 365-371. DOI:10.1126/science.220.4595.365 |
| [13] |
ISOGAI A. The reason why the reactive chemical structure of alkenyl succinic anhydride is necessary for efficient paper sizing[J]. Fiber, 2001, 56(7): 334-339. |
| [14] |
AND B P B, LUMSDON S O. Catastrophic phase inversion of water-in-oil emulsions stabilized by hydrophobic silica[J]. Langmuir, 2000, 16(6): 2539-2547. DOI:10.1021/la991081j |
| [15] |
ZHANG W, FAN J. Red shift in the photoluminescence of colloidal carbon quantum dots induced by photon reabsorption[J]. Applied Physics Letters, 2014, 104(9): 6726. |
| [16] |
SONG Y, ZHU S, YANG B. Bioimaging based on fluorescent carbon dots[J]. Rsc Advances, 2014, 4(52): 27184-27200. DOI:10.1039/c3ra47994c |
| [17] |
LINEHAN K, DOYLE H. Efficient one-pot synthesis of highly monodisperse carbon quantum dots[J]. Rsc Advances, 2013, 4(1): 18-21. |
| [18] |
GLINKA Y D, LIN K, CHANG H, et al. Multiphoton-excited luminescence from diamond nanoparticles[J]. The Journal of Physical Chemistry B, 1999, 103(21): 4251-4263. DOI:10.1021/jp9835364 |
| [19] |
ZYUBIN A S, MEBEL A M, HAYASHI M, et al. Quantum chemical modeling of photoabsorption properties of two-and three-nitrogen vacancy point defects in diamond[J]. Journal of Physical Chemistry C, 2009, 113(24): 10432-10440. DOI:10.1021/jp9012703 |
| [20] |
AND L C L H, CHANG H C. Adsorption and immobilization of cytochrome c on nanodiamonds[J]. Langmuir the Acs Journal of Surfaces & Colloids, 2004, 20(14): 5879. |
| [21] |
YANG S T, WANG X, WANG H, et al. Carbon dots as nontoxic and high-performance fluorescence imaging agents[J]. Journal of Physical Chemistry C Nanomaterials & Interfaces, 2009, 113(42): 18110. |
| [22] |
YANG S, CAO L, LUO P G, et al. Carbon dots for optical imaging in vivo[J]. Journal of the American Chemical Society, 2009, 131(32): 11308-11309. DOI:10.1021/ja904843x |
| [23] |
CAO L, WANG X, MEZIANI M J, et al. Carbon dots for multiphoton bioimaging[J]. Journal of the American Chemical Society, 2007, 129(37): 11318-11319. DOI:10.1021/ja073527l |
| [24] |
LARSON D R, ZIPFEL W R, WILLIAMS R M, et al. Water-soluble quantum dots for multiphoton fluorescence imaging in vivo[J]. Science, 2003, 300(5624): 1434-1436. DOI:10.1126/science.1083780 |
| [25] |
LIU S, TIAN J, WANG L, et al. Hydrothermal treatment of grass:a low-cost, green route to nitrogen-doped, carbon-rich, photoluminescent polymer nanodots as an effective fluorescent sensing platform for label-free detection of Cu(Ⅱ) ions[J]. Advanced Materials, 2012, 24(15): 2037-2041. DOI:10.1002/adma.201200164 |
| [26] |
MING H, MA Z, LIU Y, et al. Large scale electrochemical synthesis of high quality carbon nanodots and their photocatalytic property[J]. Dalton Transactions, 2012, 41(31): 9526-9531. DOI:10.1039/c2dt30985h |
| [27] |
WEI W, XU C, REN J, et al. Sensing metal ions with ion selectivity of a crown ether and fluorescence resonance energy transfer between carbon dots and graphene[J]. Chemical Communications, 2012, 48(9): 1284-1286. DOI:10.1039/C2CC16481G |
| [28] |
ZHANG H, HUANG H, LIU Y, et al. Porous and hollow metal-layer@SiO2 nanocomposites as stable nanoreactors for hydrocarbon selective oxidation[J]. Journal of Materials Chemistry, 2012, 22(38): 20182-20185. DOI:10.1039/c2jm35031a |
| [29] |
赵国玺. 表面活性剂物理化学. 2版(修订版)[M]. 北京大学出版社, 1991.
|
| [30] |
LAGALY G, REESE M, ABEND S. Smectites as colloidal stabilizers of emulsions:Ⅰ.Preparation and properties of emulsions with smectites and nonionic surfactants[J]. Applied Clay Science, 1999, 14(1-3): 83-103. DOI:10.1016/S0169-1317(98)00051-9 |
| [31] |
BINKS B P, FLETCHER P D, THOMPSON M A, et al. Influence of propylene glycol on aqueous silica dispersions and particle-stabilized emulsions[J]. Langmuir, 2013, 29(19): 5723-5733. DOI:10.1021/la4008697 |
 2018, Vol. 32
2018, Vol. 32


