| Ag/g-C3N4复合光催化剂的制备及降解染料废水的研究 |
g-C3N4作为一种新型的无金属半导体, 因其优良的特性近年来在光催化领域得到了很大的发展和应用[1]。尽管g-C3N4自身具有许多优势, 但在光催化应用过程中仍旧存在一些挑战。例如, g-C3N4比表面积相对较低; 纯相g-C3N4的可见光吸收主要集中在蓝紫光区域, 对可见光的利用率相对低; 纯相g-C3N4存在光生电子空穴对的复合率较高, 导致其光催化活性不高; g-C3N4表面和界面上光生载流子的动力学行为及其光催化机理还有待进一步地探索[2]。为此, 我们需要通过掺杂、半导体复合、形貌改变等多种手段[3]对其进行物理和化学的改性以调节其化学组成和结构, 提高其可见光的吸收范围和吸收强度, 抑制其光生载流子的复合, 达到提高其光催化性能的目的。同时, 还需要借助多种测试手段对g-C3N4光催化剂进行表征, 以探索其光催化机理。
由于可以有效地抑制g-C3N4中光生电子空穴对的快速复合, 半导体复合与贵金属沉积是现阶段使用最多的改性方法之一。但是, 稀缺性与高成本在很大程度上限制了贵金属在g-C3N4改性方面的应用。与其他贵金属相比, Ag是一种较为便宜与来源广泛的材料, 具有优异的导电性和较强的电子捕获能力, 将Ag沉积在g-C3N4上能够改善其光催化性能, 从而提高g-C3N4的降解吸附能力[4]。模板法可以用来增加材料中的孔隙, 是提高材料比表面积的常用方法, 该方法同样适用于g-C3N4[5]。其中, 气体模板法以热分解过程中产生的气体调控材料孔隙, 可以有效解决传统硬模板的模板去除问题。
本论文使用两步法制备了Ag/g-C3N4复合光催化剂:首先使用热聚合法以三聚氰胺为前驱体、NH4Cl为气体模板在空气气氛下制备多孔g-C3N4, 然后再使用光化学沉积法将金属Ag纳米颗粒负载在多孔g-C3N4上。实验过程中, 首先探讨了不同NH4Cl加入量对多孔g-C3N4光催化性能的影响, 并通过甲基橙降解实验优选了多孔g-C3N4样品。然后, 再用不同浓度的AgNO3溶液进行Ag在多孔g-C3N4上的光化学沉积, 并对所得Ag/g-C3N4样品进行光催化性能评价。包括XRD、BET、SEM、TEM、吸收光谱、荧光光谱和电化学测试等多种手段被用来对以上光催化材料进行检测分析, 探讨了g-C3N4光催化性能提高的机理。
1 实验 1.1 实验试剂三聚氰胺, 甲醇, 氯化铵, 硝酸银和甲基橙购自国药集团化学试剂有限公司, 纯度均为分析纯。
1.2 制备多孔g-C3N41 g三聚氰胺和一定质量的氯化铵充分研磨搅拌之后加入到坩埚中, 在马弗炉中以10 ℃/min升温到550 ℃, 保温3 h, 自然冷却后将所得样品充分研磨备用。在制备过程中, 改变NH4Cl的质量为0 g、1 g、2 g、3 g。所得样品分别编号g-C3N4(对照样品)、g-C3N4-1、g-C3N4-2、g-C3N4-3。
1.3 Ag/g-C3N4光催化剂的制备通过对不同多孔g-C3N4样品光催化降解甲基橙的测试, 选出性能最好的多孔g-C3N4样品用于制备Ag/g-C3N4复合光催化剂。首先将一定质量的AgNO3溶于50 mL甲醇中, 然后向其中加入0.1 g g-C3N4, 超声分散15 min, 然后将溶液在300 W氙灯下照射20 min, 之后溶液离心3次, 洗净之后, 放入60 ℃烘箱中烘干得到复合光催化剂。改变AgNO3的质量分别为0.007 0 g(0.8 mol/L), 0.013 6 g(1.6 mol/L), 0.033 9 g(4 mol/L), 0.051 0 g(6 mol/L), 所得样品编号为0.8Ag/C3N4, 1.6Ag/C3N4, 4Ag/C3N4, 6Ag/C3N4。
1.4 表征方法使用德国布鲁克D8-ADVANCE X射线衍射仪分析材料的物相组成; 使用气体吸附分析仪测得样品的氮气吸脱附等温线, 并用BET法和BJH法从吸附支曲线计算获得材料的比表面积和孔径分布数据; 使用日立Regulus8220扫描电子显微镜和日本电子JEM-2100透射电子显微镜分析材料的形貌特征, 并通过与扫描电镜连用的能谱仪测试样品中元素分布情况; 使用日本岛津UV-2600紫外-可见漫反射光谱仪分析材料的光吸收性能; 使用CHI660E电化学工作站在分析材料的10 mV振幅、0.01~105 Hz的频率范围内、零电势条件下测得材料的电化学阻抗图谱; 使用日立F-4600荧光光谱仪测试样品的荧光性质, 激发波长为350 nm。
1.5 性能评价先制备20 mg/L的甲基橙溶液:取甲基橙粉末10 mg置于烧杯中, 加纯水溶解, 倒入500 mL容量瓶中定量, 配置成500 mL溶液, 放在阴凉处备用。随后, 取10 mg g-C3N4氮化碳样品放入250 mL烧杯中, 再量取50 mL甲基橙溶液倒入烧杯中, 超声15 min, 然后暗处搅拌30min, 用1 mL的移液枪取一次样。然后将溶液置于300 W氙灯下照射, 期间每隔10 min用1 mL的移液枪取样一次, 放入离心管中, 直至甲基橙溶液颜色消失或溶液移取完。最后, 把暗处存放的离心管放入离心机中, 在10 000 rpm转速下离心10 min, 待离心结束后用紫外可见分光光度计对离心清液进行测试, 以检测残余甲基橙的浓度。
2 结果与讨论 2.1 光催化性能评价图 1(a)是g-C3N4-2不同降解时间后甲基橙的紫外可见吸收光谱。从图中可以看出, 甲基橙溶液的显色基团的特征吸收峰在464 nm附近。随着光催化降解甲基橙溶液反应时间的逐步增加, 甲基橙溶液的特征吸收峰的强度逐渐降低, 表明溶液中甲基橙的浓度逐渐减小。100 min时甲基橙溶液的浓度下降为原浓度的24.1%。
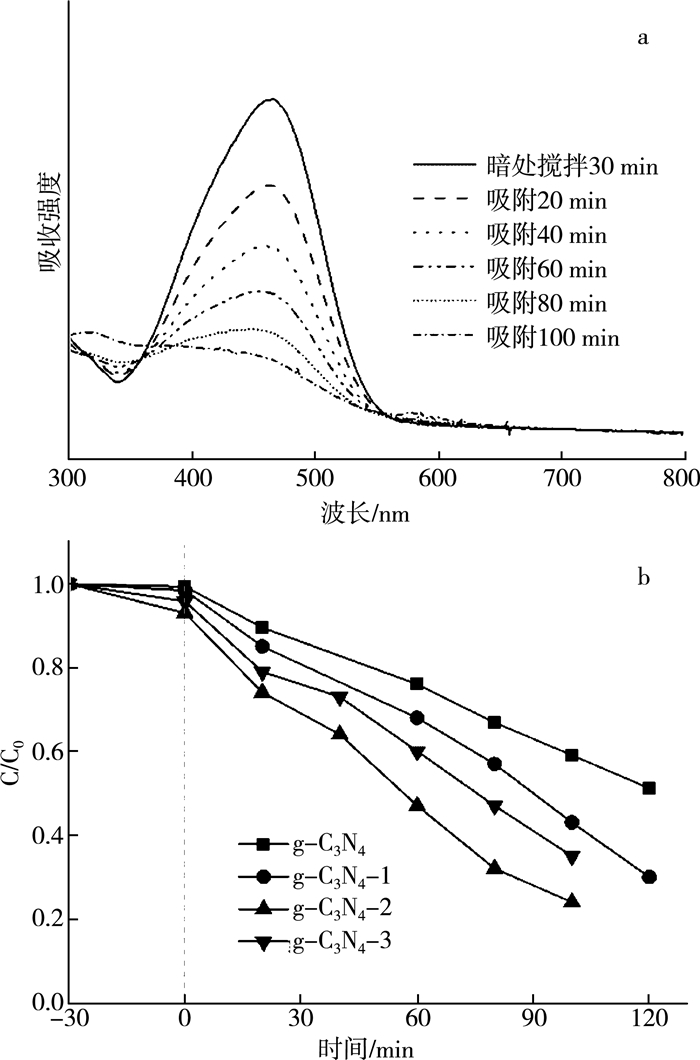 |
| 图 1 (a) g-C3N4-2不同降解时间后甲基橙的紫外可见吸收光谱; (b)不同g-C3N4在可见光下对甲基橙的光催化降解曲线图 |
图 1(b)是g-C3N4和多孔g-C3N4在可见光下降解甲基橙的曲线图。其中C0表示溶液的原始浓度, C表示溶液的检测浓度。可以看出, 多孔g-C3N4的甲基橙降解效率均比g-C3N4有所提高。其中, g-C3N4-2样品光催化降解甲基橙染料的效果最好。
图 2是几种Ag/g-C3N4样品的不同降解时间后甲基橙溶液的降解曲线图。其中C0表示溶液的原始浓度, C表示溶液的检测浓度。从图中看出, 6Ag/C3N4的样品降解甲基橙染料的效率最高, 经过60 min的光催化反应, 其甲基橙溶液在464 nm附近的特征吸收峰下降至原强度的7.5%, 使得甲基橙溶液几乎变为无色。这说明Ag负载可以明显提高g-C3N4的光催化活性。
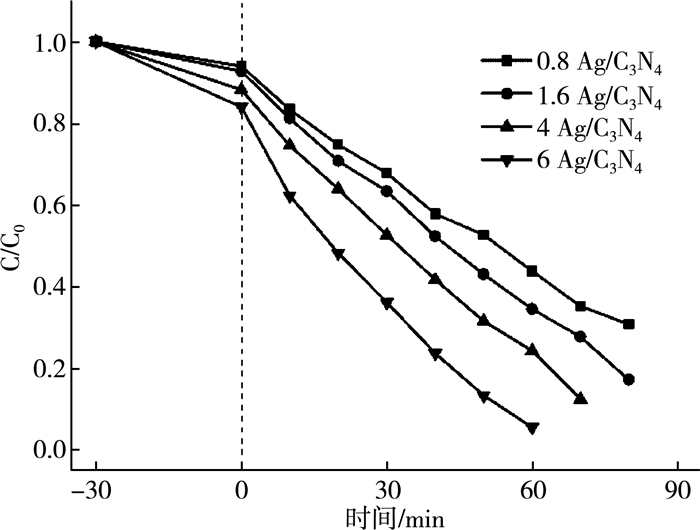 |
| 图 2 Ag/g-C3N4样品光催化降解甲基橙溶液的曲线图 |
2.2 光催化剂的表征 2.2.1 比表面积及孔径分析
使用氮气吸脱附测试对多孔g-C3N4的比表面积大小和孔结构特性进行了研究。图 3(a)是g-C3N4和多孔g-C3N4的氮气吸脱附曲线。从图中可以看出, 所有样品都是具有H3回滞环的Ⅲ型等温线:相对压力(P/P0)低于0.5时, 各个样品均没有明显的吸附; 在相对压力0.5~1.0范围内, 样品都有一个明显的回滞环, 这是由于毛细管凝聚现象导致的, 是介孔材料的典型特性。而H3回滞环常见于层状结构的聚集体, 这与g-C3N4的结构也是一致的。使用BET方法根据吸附支计算得到的g-C3N4、g-C3N4-1、g-C3N4-2和g-C3N4-3的比表面积分别为20.93、41.69、57.33、33.56 m2/g, 显然g-C3N4-2具有最大的比表面积, 因而其能够暴露更多的活性位点, 在多孔g-C3N4样品中表现出最佳的光催化活性。g-C3N4-3比表面积下降的原因可能是过多的NH4Cl分解产生大量气体, 过大的气体压力直接在正在聚合的三聚氰胺中产生了通孔, 气体直接从样品中逸出而未起到气体模板应有的作用。图 3(b)是g-C3N4和多孔g-C3N4的BJH孔径分布图。从图中可以看出, 样品的孔径集中在2~4 nm和20~30 nm两个范围内。
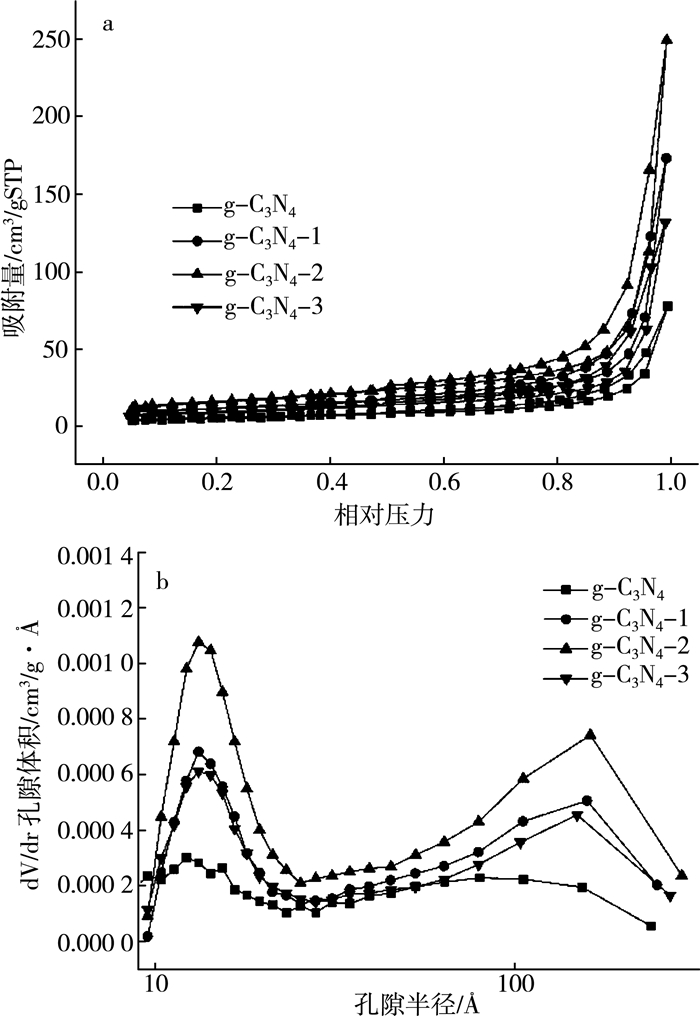 |
| 图 3 (a) g-C3N4和多孔g-C3N4的氮气吸脱附曲线; (b)BJH孔径分布图 |
2.2.2 X射线衍射分析
采用XRD图谱对材料的晶相组成进行了分析。从图 4中可以看出谱线中有两个明显的特征峰, 分别在27.5°和13.1°。据文献可知, 在27.5°附近出现的衍射峰对应于g-C3N4的(002)晶面, 出现在13.1°的衍射峰对应于g-C3N4的(100)晶面, 说明我们成功制备了g-C3N4[6]。相比于g-C3N4-2样品, g-C3N4(002)晶面的衍射峰峰形更加尖锐, 强度更强, 说明g-C3N4具有更高的结晶度, 加入气体模板后由于孔隙的产生会使g-C3N4的结晶度下降。Ag/g-C3N4样品的衍射峰强度和半高全峰宽(FWHM)与g-C3N4-2相比变化不明显, 说明光化学沉积Ag的过程对g-C3N4的晶型几乎没有影响。此外, 在1.6Ag/C3N4、4Ag/C3N4和6Ag/C3N4的38.2°附近能够发现微弱的衍射峰, 通过对比X射线衍射标准卡片可知此衍射峰对应于金属Ag的(111)晶面, 这证明了Ag/g-C3N4复合光催化剂的成功制备。0.8Ag/C3N4图谱中无法识别出Ag的衍射峰, 这可能是由于AgNO3溶液的浓度太低, 生成的Ag颗粒太小结晶较差导致的。
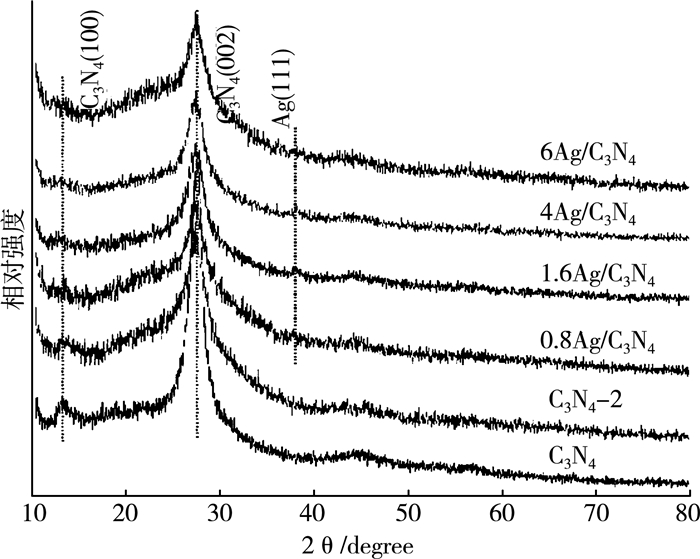 |
| 图 4 不同样品的X射线衍射图谱 |
2.2.3 电镜与能谱分析
图 5中(a)、(b)和(c)分别是g-C3N4放大10K倍、30K倍及50K倍的SEM图。从低倍照片中可以看到, g-C3N4为许多外形不规则的片状颗粒构成, 这些颗粒相互堆叠在一起。在更大的放大倍数下, 可以看到颗粒表面有一些缝隙和孔洞。当加入气体模板后, 从图(d)、(e)和(f)可以看到, 所得样品的片层结构更加明显, 片层厚度明显降低, 样品中出现了许多介孔级别的孔洞(与氮气吸脱附曲线的表征结果一致), 这表明在制备g-C3N4过程中加入的氯化铵作为气体模板起到了扩孔、增大比表面积的作用。Ag沉积在g-C3N4上后, 从图(g)、(h)和(i)可以看到, 样品形貌没有发生太大变化, 仍旧是由具有介孔孔洞的片层结构构成, 表明Ag沉积对g-C3N4的形貌没有影响, 这与XRD的表征结果也是一致的。样品中没有观察到Ag颗粒存在, 这可能是因为Ag颗粒尺寸较小且与衬度相似的g-C3N4颗粒混杂在一起, 无法分辨。尽管无法直观地从图 5(g)-(i)中看到Ag的分布, 但是通过6Ag/C3N4的EDS元素分布表征图 5(j)中可以清楚地看到Ag元素均匀分布于g-C3N4上, 证明成功合成了Ag/g-C3N4复合光催化剂。
 |
| 图 5 (a-c)g-C3N4、(d-f)g-C3N4-2和(g-i)6Ag/C3N4放大10K倍、30K倍和50K倍的扫描电镜图; (j)6Ag/C3N4中Ag的EDS元素分布图; (k)6Ag/C3N4的透射电镜照片 |
为了深入研究6Ag/C3N4样品, 我们使用透射电子显微镜对其形貌结构进行了进一步观察。图 5(k)为6Ag/C3N4光催化剂的TEM照片。从图中可以看出, 在具有多孔结构的C3N4上存在一些与其衬度明显不同的黑色颗粒, 这些颗粒的尺寸大约为10~20 nm, 应该是沉积在C3N4上的金属Ag纳米颗粒。这一表征结果再次证明了Ag/g-C3N4复合光催化剂的成功制备。
2.2.4 漫反射光谱分析图 6为g-C3N4、多孔g-C3N4和Ag/g-C3N4光催化剂的紫外-可见漫反射光谱。与g-C3N4相比, 多孔g-C3N4样品的谱线几乎没有变化, 这表明气体模板NH4Cl尽管可以调控g-C3N4的形貌结构, 但对其可见光的吸收强度没有影响。然而, 当在g-C3N4-2(光催化性能最佳的多孔g-C3N4样品)上沉积Ag后, 所得Ag/g-C3N4的可见光吸收强度明显增强, 且吸收边有一定的红移, 因而具有更广的可见光响应范围。由文献可知, Ag纳米颗粒的表面等离子激元共振(SPR)效应是Ag/g-C3N4可见光吸收强度增强的主要原因。可以看到, 随着AgNO3溶液浓度的提高, 从0.8Ag/C3N4到6 Ag/C3N4的可见光吸收强度显示出逐渐增加的趋势, 这是Ag沉积量增多导致的。
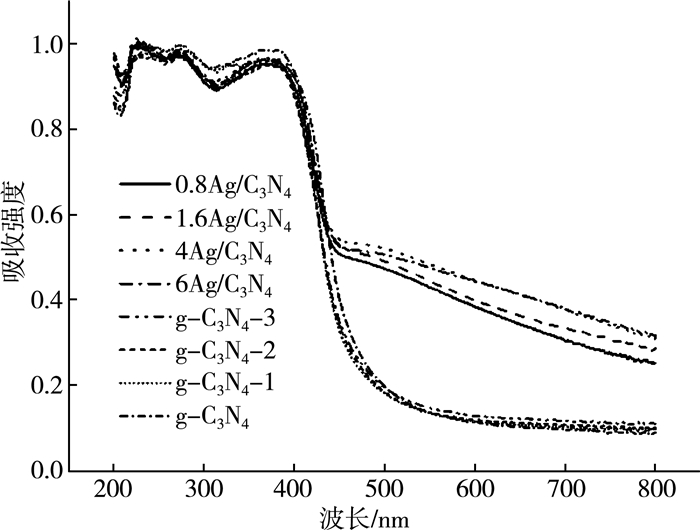 |
| 图 6 不同样品的紫外-可见漫反射光谱 |
2.2.5 荧光光谱分析
荧光是光激发后准平衡态下的电子和空穴复合产生的, 一般来说, 荧光光谱的峰值越高, 表明光催化材料中光生电子-空穴对的复合率越高, 分离效率越低, 光催化活性越低。图 7是g-C3N4, g-C3N4-2, 6Ag/C3N4的荧光光谱图。与g-C3N4相比, g-C3N4-2的荧光强度显著降低, 说明其电子-空穴对的复合率较低, 光催化活性较好。导致这一结果的原因可能是, 气体模板的加入使得g-C3N4中缺陷增加(XRD测试显示加入气体模板后g-C3N4的结晶性显著下降), 抑制了光生电子-空穴对的复合。6Ag/C3N4与g-C3N4-2相比荧光光谱强度进一步下降, 说明其电子-空穴对的复合率进一步降低。此外, 其峰位位置向短波长方向偏移, 表明Ag与g-C3N4发生了相互作用, 一定程度改变了g-C3N4的价带结构, 这与紫外-可见漫反射光谱表征结果是一致的。
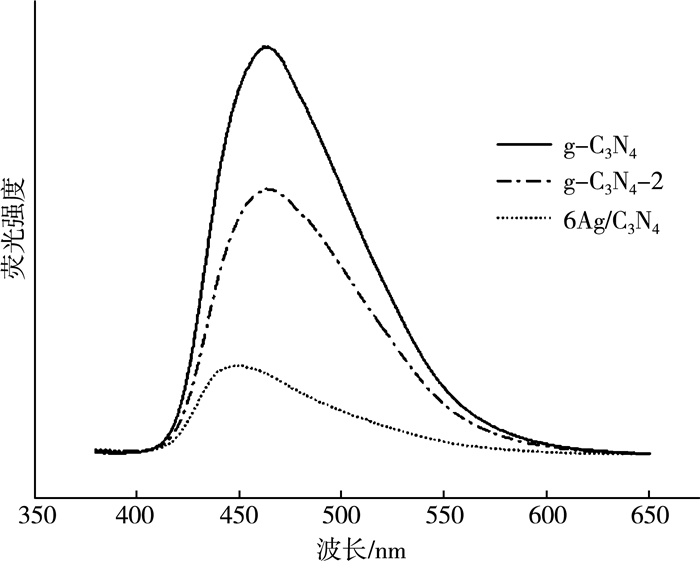 |
| 图 7 不同样品的荧光光谱 |
2.2.6 电化学阻抗谱分析
图 8是g-C3N4和6Ag/C3N4的电化学阻抗谱(EIS), 电化学阻抗谱中的圆弧半径的大小与内阻的大小密切相关, 圆弧半径越大表示样品的内阻越大, 反之则代表样品的内阻越小。6Ag/C3N4样品在电化学阻抗谱上显示出比g-C3N4更小的圆弧半径, 表明6Ag/C3N4光催化剂的内阻最小, 其中光生载流子的转移效率更高, 光生电子空穴对较不易复合。这一结论与之前荧光光谱所的结论一致, 表明Ag纳米颗粒的负载增强了g-C3N4的光催化性能。
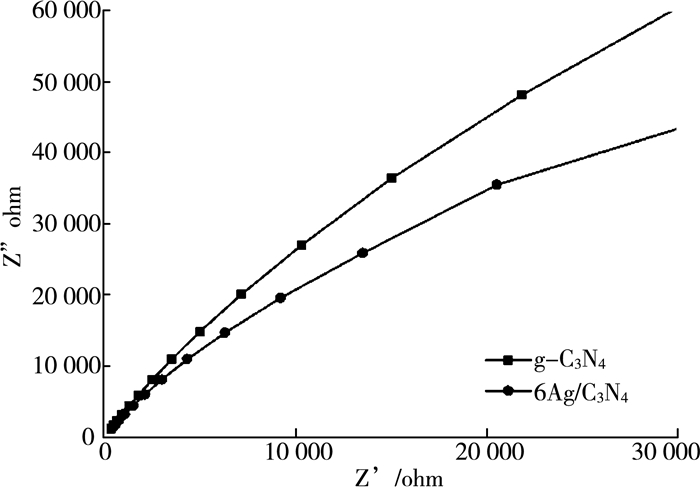 |
| 图 8 g-C3N4和6Ag/C3N4的电化学阻抗谱 |
2.3 机理分析
根据以上结果, 并结合文献, 我们给出了Ag/g-C3N4光催化机理的示意图, 如图 9所示。首先, 从光吸收的角度看, 由于Ag纳米颗粒的SPR效应, 使Ag/g-C3N4可见光吸收能力明显增强[7]。相应的, 材料中能够产生更多的光生载流子, 这对Ag/g-C3N4的光催化活性具有积极作用。其次, 从光生载流子的分离角度看, Ag与g-C3N4具有匹配的能带结构(g-C3N4的导带和价带位置为-1.3和1.4 eV, Ag的费米能级为0.4 eV [vs.NHE])[8-9], Ag纳米颗粒可以作为电子陷阱快速捕获g-C3N4上产生的光生电子, 将空穴留存在g-C3N4上, 从而抑制光生电子和空穴的复合。以上两方面原因促使复合材料的光催化性能明显提升。当光生电子和空穴分离后, 二者转换为h+、·O2-和·OH等活性物种, 将甲基橙降解为CO2、H2O和硝酸根离子等小分子, 从而使溶液褪色。
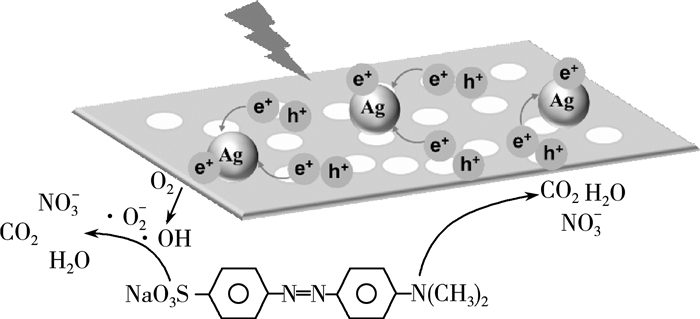 |
| 图 9 Ag/g-C3N4的光催化机理示意图 |
3 结论
本文首先利用三聚氰胺和氯化铵制备了多孔g-C3N4, 然后通过光化学沉积法将Ag负载于多孔g-C3N4上, 获得了Ag/g-C3N4复合光催化剂。气体模板的添加能够增大g-C3N4的比表面积, 但添加量应控制在合理范围之内。多孔g-C3N4沉积Ag后光催化活性可继续提高, 其中6Ag/C3N4光催化活性最优, 其在60min之内就可将甲基橙溶液降解为无色, 这主要是因为Ag能够增强光催化剂对可见光的捕获能力, 并且对光生电子-空穴的复合有明显抑制作用。本研究表明Ag/g-C3N4复合光催化剂在降解有机废水方面具有潜在的应用价值。
| [1] |
T HOMAS A, FISCHER A, GOETTMANN F, et al. ChemInform abstract:graphitic carbon nitride materials:variation of structure and morphology and their use as metal-free catalysts[J]. Journal of Materials Chemistry, 2008, 18(41): 4893-4908. DOI:10.1039/b800274f |
| [2] |
罗磊.形貌可控g-C3N4的制备及其可见光催化性能研究[D].大连: 大连理工大学, 2018. http://kns.cnki.net/KCMS/detail/detail.aspx?dbcode=CDFD&filename=1018257211.nh
|
| [3] |
WANG K, LI Q, LIU B, et al. Sulfur-doped g-C3N4 with enhanced photocatalytic CO2-reduction performance[J]. Applied Catalysis B:Environmental, 2015, 176: 44-52. |
| [4] |
YANG Y, GUO Y, LIU F, et al. Preparation and enhanced visible-light photocatalytic activity of silver deposited graphitic carbon nitride plasmonic photocatalyst[J]. Applied Catalysis B:Environmental, 2013, 142: 828-837. |
| [5] |
YUAN B, ZOU X, YAN T, et al. Green synthesis of graphitic carbon nitride nanodots using sodium chloride template[J]. Journal of Nanoparticle Research, 2016, 18(5): 110. DOI:10.1007/s11051-016-3415-0 |
| [6] |
DONG F, WU L, SUN Y, et al. Efficient synthesis of polymeric g-C3N4 layered materials as novel efficient visible light driven photocatalysts[J]. Journal of Materials Chemistry, 2011, 21(39): 15171-15174. DOI:10.1039/c1jm12844b |
| [7] |
INGRAM D B, CHRISTOPHER P, BAUER J L, et al. Predictive model for the design of plasmonic metal/semiconductor composite photocatalysts[J]. ACS Catalysis, 2011, 1(10): 1441-1447. DOI:10.1021/cs200320h |
| [8] |
LI J, CUSHING S K, BRIGHT J, et al. Ag@ Cu2O core-shell nanoparticles as visible-light plasmonic photocatalysts[J]. ACS Catalysis, 2012, 3(1): 47-51. |
| [9] |
WANG X, BLECHERT S, ANTONIETTI M. Polymeric graphitic carbon nitride for heterogeneous photocatalysis[J]. ACS Catalysis, 2012, 2(8): 1596-1606. DOI:10.1021/cs300240x |
 2019, Vol. 33
2019, Vol. 33


