| 微乳/水热法制备勃姆石 |
勃姆石是铝土矿的主要组成部分,是一种重要的化工原料,具有独特的晶体结构,化学式为γ-AlOOH[1-2]。勃姆石是制备氧化铝的前驱体材料。勃姆石在500 ℃下加热脱水,转化为γ-Al2O3相,随着温度的上升由γ相通过δ相转化为θ-Al2O3,最终可转换为稳定的α-Al2O3。
氧化铝(Al2O3)是用作研磨材料、耐火材料、保护屏障、陶瓷材料以及电子材料等的最重要的物质之一[3-5]。由于其高硬度、高导热性和良好的绝缘性能,高纯的氧化铝始终是作为一种重要的摩擦原料用于生产透明陶瓷、激光陶瓷和荧光粉[6-7]。由于过渡相Al2O3被广泛应用在催化剂及催化剂载体、汽车尾气净化、催化燃烧、石油炼制领域,因此使用勃姆石制备Al2O3具有巨大的应用价值以及经济效益[8-11]。
勃姆石的制备方法很多,包括电化学法[12-13]、溶胶-凝胶法[14-15]、气相沉积法[16]、微乳液法[17-18]、水热法[19-20]等。
微乳液法是通过表面活性剂、助表面活性剂、溶剂和水溶液形成微乳体系,经过一系列处理后获得材料的方法。微乳液法的特点是粒径分布较窄且粒径可控,粒子的表面包覆一层(或几层)表面活性剂,粒子间不易聚结,稳定性好。
水热法是指在特制的密闭反应器中,采用水溶液作为反应体系,通过对反应体系加热、加压(或自生蒸汽压),创造一个相对高温、高压的反应环境,使得通常难溶或不溶的物质溶解并重结晶而进行材料合成的方法。由于反应在相对较高的压力和温度下进行,产物为晶态,无需焙烧晶化,可以减少焙烧过程中难以避免的团聚现象。
采用微乳液为模板,结合水热法制备勃姆石。
1 实验部分 1.1 试剂曲拉通X-100(Triton-100,上海麦克林生化科技有限公司);正丁醇(天津博迪化工股份有限公司);环己烷(天津市大茂试剂厂);硝酸铝(Al(NO3)3·9H2O,天津市精细化工研究所);氨水(莱阳市康德化工有限公司)。以上试剂均为分析纯。工业氧化铝(γ-Al2O3)购自山东铝业有限公司。
1.2 表征方法XRD(日本理学电机株式会社,D/max-RA型);SEM(Tescan公司,VEGA3型)。
1.3 实验方法 1.3.1 铝源为硝酸铝将5 mL TX-100、2.5 mL正丁醇、4 mL环己烷依次混合在一起,剧烈搅拌15 min,形成均匀稳定的有机相。向其中滴加1 mol·L-1的硝酸铝水溶液3 mL,再用氨水将pH调制8.5,常温下搅拌反应2 h,然后放入50 mL水热反应釜中,在180 ℃下反应6 h。将所得液体进行抽滤,并用无水乙醇和去离子水多次洗涤,将滤饼在80 ℃下干燥12 h。
1.3.2 铝源为工业氧化铝(γ-Al2O3)取5 mL TritonX-100(表面活性剂)、2.5 mL正丁醇(助表面活性剂)、4 mL环己烷(油相)依次混合在一起,再加入3 mL蒸馏水(水相),搅拌15 min。称取0.207 5 g γ-Al2O3,加入上述溶液中,常温搅拌2 h,加入水热反应釜中,在180 ℃下反应6 h。将所得液体进行抽滤,并用无水乙醇和去离子水多次洗涤,将滤饼在80 ℃下干燥12 h。
2 结果与讨论 2.1 铝源为硝酸铝使用硝酸铝作为铝源,采用微乳-水热法制备的勃姆石的XRD图如图 1所示。所有的衍射峰可以被检索到单相γ-AlOOH斜方晶系的结构(a=3.7Å, b=12.227Å, c=2.868Å, JCPDS卡片No.21-1307)。并且从XRD图中可以看出经过洗涤后的产物中不含有杂质。其中(020)、(120)、(031)、(131)、(051)、(200)、(151) 晶面的2θ角分别为14.198°、28.222°、38.395°、45.753°、45.852°、48.963°、55.185°。
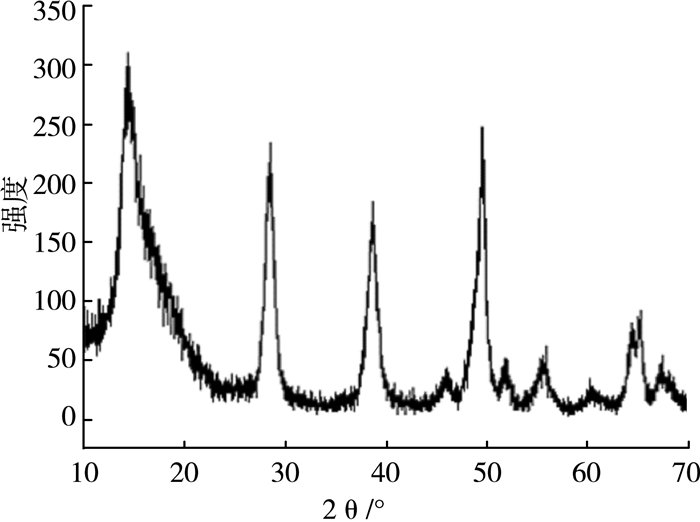 |
| 图 1 使用硝酸铝作为铝源制备的勃姆石的XRD图 |
使用硝酸铝(Al(NO3)3·9H2O)作为铝源,制备得到的氧化铝前驱体勃姆石的扫描电镜图如图 2所示。从电镜图中可以看出勃姆石的形状为不规则的块状,表面比较粗糙,整体尺寸范围为5~100 μm。
 |
| 图 2 使用硝酸铝作为铝源,制备的勃姆石的SEM图 |
使用硝酸铝为铝源,制备γ-Al2O3的过程可能发生了如下反应:
| $ {\rm{Al}}{({\rm{N}}{{\rm{O}}_{\rm{3}}})_{\rm{3}}}{\rm{ + 3}}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{Al}}{\left( {{\rm{OH}}} \right)_{\rm{3}}}{\rm{ + 3}}{{\rm{H}}^{\rm{ + }}}{\rm{ + 3NO}}_3^ - , $ | (1) |
| $ {\rm{N}}{{\rm{H}}_{\rm{3}}}{\rm{\cdot}}{{\rm{H}}_{\rm{2}}}{\rm{O + }}{{\rm{H}}^{\rm{ + }}} \to {\rm{N}}{{\rm{H}}^{\rm{ + }}}_{\rm{4}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}, $ | (2) |
| ${\rm{Al}}{\left( {{\rm{OH}}} \right)_{\rm{3}}} \to {\rm{\gamma-AlOOH + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}。$ | (3) |
将硝酸铝(Al(NO3)3·9H2O)固体加入蒸馏水中溶解,Al(NO3)3·9H2O发生水解反应生成Al(OH)3,这两者之间存在动态的水解平衡(1)。随着氨水的加入,反应(1) 生成的H+被中和。由于H+的减少而导致平衡过程被打破,使得反应(1) 向右进行,不断生成絮状的的Al(OH)3沉淀。生成的无定形Al(OH)3在180 ℃的水热条件下会发生脱水反应,转化为γ-AlOOH,如反应(3) 所示。
2.2 铝源为工业氧化铝(γ-Al2O3)使用γ-Al2O3作为铝源,在水热条件为180 ℃、反应时间6 h制备的氧化前驱体的XRD图如图 3所示。从图中可以看出:所制备的氧化铝前驱体的衍射峰位置与勃姆石γ-AlOOH的标准卡片(JCPDS21-1307) 的衍射峰位置基本一致,可以判断所制备的物质为氧化铝的前驱体γ-AlOOH。其中,(020)、(120)、(031)、(051)、(200) 晶面的2θ角分别为14.593°、28.173°、38.494°、48.963°、49.259°。
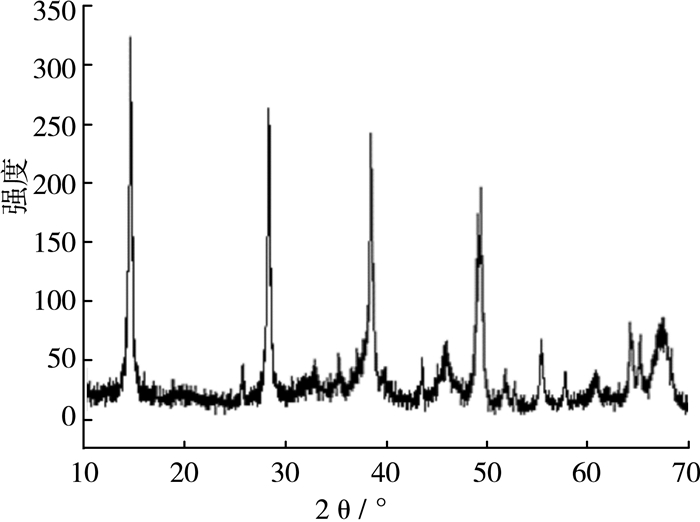 |
| 图 3 用γ-Al2O3作为铝源制备的勃姆石的XRD图 |
使用工业氧化铝(γ-Al2O3)作为铝源,制备的氧化铝前驱体勃姆石的扫描电镜图如图 4所示。从SEM图中可以看出:制备的氧化铝前驱体勃姆石(γ-AlOOH)为不规则的块状,表面不太光滑,晶粒大小不一,整体尺寸范围为5~30 μm。
 |
| 图 4 用γ-Al2O3作为铝源制备的勃姆石的SEM图 |
3 结论
采用TX-100(表面活性剂)、正丁醇(助表面活性剂)、环己烷(油相)、水(水相)组成的微乳液为模板,结合水热法制备氧化铝,通过使用硝酸铝(Al(NO3)3·9H2O)、工业氧化铝(γ-Al2O3)作为铝源,得出了以下结论:
1) 使用微乳液法结合水热法,以硝酸铝作为铝源,在水热反应釜中于180 ℃下反应6 h,可以制备成氧化铝的前驱体勃姆石相,所得勃姆石为块状,尺寸分布范围为5~100 μm。
2) 使用微乳液法结合水热法,以工业氧化铝(γ-Al2O3)作为铝源,在水热反应釜中于180 ℃下反应6 h,可以制备成氧化铝的前驱体勃姆石相。所得勃姆石为块状,尺寸分布范围为5~30 μm。
工业氧化铝的来源丰富、价格低廉,使用工业氧化铝制备勃姆石具有巨大的工业价值,应对此进行广泛而深入的研究。
| [1] |
张丽, 岳巍, 秦烟莱. 水热法制备不同形貌的勃姆石研究[J]. 铝镁通讯, 2016(4): 48-50. |
| [2] |
温俊磊, 江琦. 多种形貌勃姆石纳米材料制备的研究进展[J]. 材料导报, 2016(30): 42-48. |
| [3] |
LEVIN I, BRANDON D. Metastable alumina polymorphs:crystal structures and transition sequences[J]. Am Ceram Soc, 1998, 8: 1995-2012. |
| [4] |
WEN H L, YEN F S. Growth characteristics of boehmite-derived ultrafine theta and alpha-alumina particles during phase transformation[J]. Cryst Growth, 2000, 208: 696-708. DOI:10.1016/S0022-0248(99)00436-4 |
| [5] |
朱志斌, 郭志军, 刘英, 等. 氧化铝陶瓷的发展与应用[J]. 陶瓷, 2003(1): 5-8. |
| [6] |
童幸生, 张静. 氧化铝陶瓷摩擦磨损实验研究[J]. 江汉大学学报, 2011(2): 34-37. |
| [7] |
吴振东, 叶建东. 添加剂对氧化铝陶瓷的烧结和显微结构的影响[J]. 兵器材料科学与工程, 2002, 25(1): 68-72. |
| [8] |
惠坤龙, 张君涛, 中志兵. 介孔氧化铝的合成及应用进展[J]. 现代化工, 2015(35): 50-54. |
| [9] |
李慧, 胡燚, 苏国东, 等. 合成方法对γ-Al2O3催化剂乙醇脱水性能的影响[J]. 石油化工, 2009(38): 373-378. |
| [10] |
吴祖燊, 李齐春, 戴品中. 异丙醇铝气相燃烧法制备纳米氧化铝的实验研究[J]. 精细专用化品, 2011(19): 26-29. |
| [11] |
ASGHARI A, MOHAMMADI B. Nano-alumina coated with sodium dodecyl sulfate and modified with 4-(2-Pyridylazo) resorcinol for extraction of heavy metals in different matrixes[J]. Ind Eng Chem, 2014, 20: 824-829. DOI:10.1016/j.jiec.2013.06.012 |
| [12] |
ZHANG L, CHENG B, SHI W S, et al. In-situ electrochemical synthesis of 1-dimensional alumina nanostructures[J]. Mater.Chem, 2005(15): 4889-4893. |
| [13] |
张璐, 姚素薇, 张卫国, 等. 氧化铝纳米线的制备及其形成机理[J]. 物理化学学报, 2005(21): 1254-1258. |
| [14] |
曹凯, 沈湘黔, 王涛平, 等. 溶胶凝胶法制备纳米结构氧化铝陶瓷纤维[J]. 矿冶工程, 2004(24): 76-79. |
| [15] |
SHEN S C, CHEN Q, CHOW P S, et al. Steam-assisted solid wet-gel synthesis of h igh-quality nano rods of boehmite and alumina[J]. Phys Chem C, 2007(111): 700-707. |
| [16] |
PROOST J, Van BOXEL S. Large-scale synthesis of high purity, one-dimensional α-Al2O3 structures[J]. Mater Chem, 2004(14): 3058-3062. |
| [17] |
张彩霞, 罗序燕, 吴速英. 微乳液法制备氧化铝纳米粉体的研究[J]. 无机盐工业, 2006, 38(10): 26-28. DOI:10.3969/j.issn.1006-4990.2006.10.009 |
| [18] |
GHOSH S, NASKAR M K. Synthesis of mesoporous γ-alumina nanorods using a double surfactant system by reverse microemulsion process[J]. RSC Advances, 2013(3): 4207-4211. |
| [19] |
VITORINO N, KOVALEVSKY A V, ABRANTES J C C, et al. Hydrothermal synthesis of boehmite in cellular alumina monoliths for catalytic and separation applications[J]. Journal of the European Ceramic Society, 2015(35): 3119-3125. |
| [20] |
徐冰, 王晶, 于洪波, 等. 水热合成三维花状薄水铝石及其形成机理[J]. 无机盐工业, 2010(42): 11-13. |
 2017, Vol. 31
2017, Vol. 31


