| 刺槐豆胶在铜硫分离中的抑制作用及机理分析 |
我国铜矿资源十分丰富, 且以硫化铜矿为主, 因黄铁矿和硫化铜矿致密共生, 且两者可浮性相近, 分离效果不佳[1-3]。在铜硫矿浮选分离工艺中, 主要在强碱条件下采用石灰等无机抑制剂抑硫浮铜, 但高碱工艺的铜精矿质量较差, 且不利于伴生金属矿物富集, 此外还易造成尾矿中选硫困难[4-6]。而新型高分子有机抑制剂不仅种类多、来源广、无污染、价格低, 且抑制效果较好, 如糊精、聚丙烯酰胺、黄原酸钠、树胶、纤维素等有机抑制剂在铜硫分离中均已有理论研究[7-9]。刘斌等[10]在焦性没食子酸与单宁酸混合抑制剂对铜硫多金属实际矿浮选分离试验中得出较好指标。
刺槐豆胶(分子结构式如图 1所示)也称槐豆胶, 是由刺槐树种子加工而成的糖胶, 为白色或微黄色粉末, 无臭或稍带臭味。精制刺槐豆胶溶液透明度高[11-15]。在冷水中部分溶解, 加热至85 ℃保持10 min以上充分水化, 冷却后达到最大黏度。与黄原胶等亲水胶体有良好的凝胶协同效应, 可使复合后的用量很低并改善凝胶组织结构, 在食品工业上的应用较广泛[16-21]。但目前其在选矿领域中研究很少。
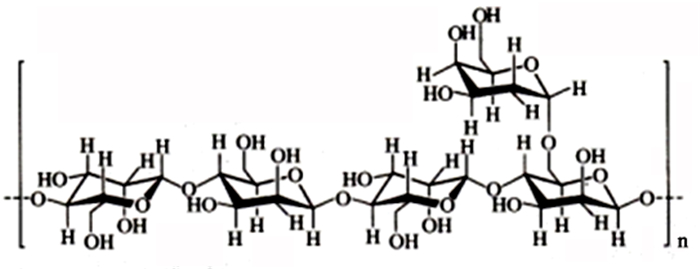 |
| 图 1 刺槐豆胶分子结构式 Fig.1 The molecular structural formula of Locust bean gum |
本文通过浮选试验、吸附量试验和动电位测试, 研究刺槐豆胶在黄铜矿及黄铁矿浮选分离中的作用, 并考察其作用机理, 为促进铜硫矿的浮选分离提供参考。
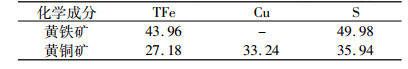
1 试验方法 1.1 试样与药剂黄铜矿取自青海赛什塘铜矿, 黄铁矿取自某矿山。较高纯度的块矿经锤碎、手选后, 用瓷球磨机磨细, 并干筛得-0.150 mm+0.037 5 mm和-0.037 5 mm粒级矿样分别用于浮选试验和机理测试。X衍射分析(见图 2)和化学分析结果(见表 1)表明黄铜矿和黄铁矿样品均较纯。
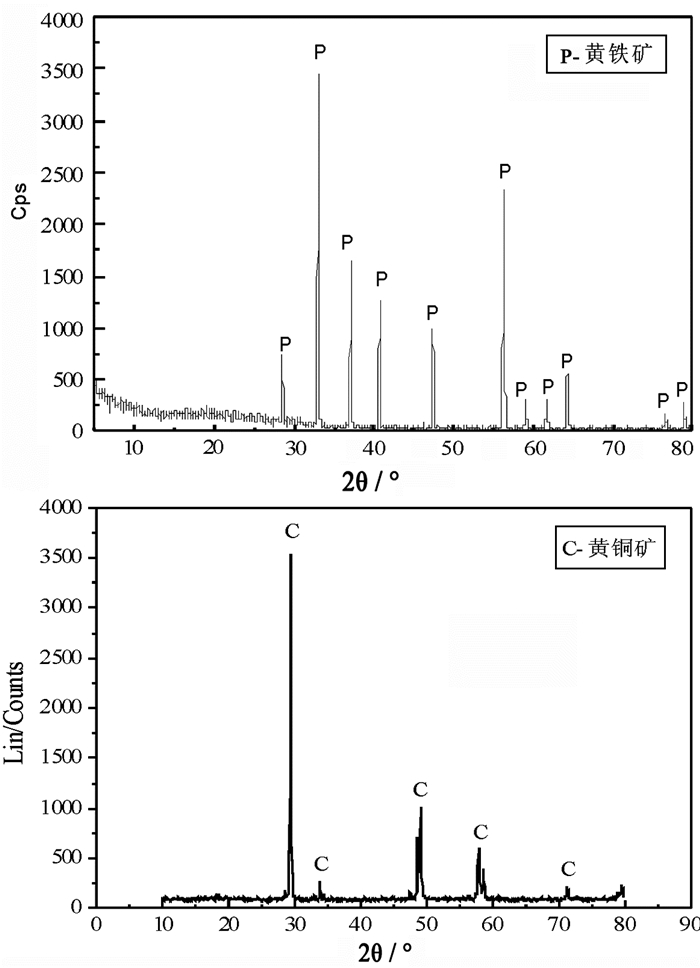 |
| 图 2 矿物X射线衍射图谱 Fig.2 X-ray diffraction of minerals |
| 表 1 矿样主要化学成分 /% Table 1 The chemical composition of chalcopyrite and pyrite |
 |
刺槐豆胶, 产自上海思域化工有限公司, 分析纯; 捕收剂丁黄药(PBX), 分析纯; 起泡剂甲基异丁基甲醇(MIBC), 分析纯; 水, 一次蒸馏水。
1.2 浮选试验每次试验称取2.0 g矿样和40 mL蒸馏水于浮选槽中, 经充分搅拌调浆, 根据要求加入浮选药剂, 用NaOH及HCl溶液调节矿浆pH值, 最后浮选刮泡3 min。单矿物试验时, 将精矿、尾矿分别烘干称重并计算回收率; 混合矿试验时, 将精矿、尾矿分别化验其铜品位后计算其回收率。
1.3 吸附量试验通过总有机碳法测量刺槐豆胶在黄铜矿及黄铁矿表面的吸附量。具体试验步骤为:先用TOC总有机碳分析仪测量绘制刺槐豆胶浓度与有机碳含量的标准曲线; 取1.0 g矿样和相应浓度刺槐豆胶溶液于烧杯中, 调节矿浆pH, 充分搅拌后离心分离, 取上层清液进行总有机碳测定; 最后根据标准曲线得出上清液中的刺槐豆胶含量。
1.4 Zeta电位测试将矿样磨至粒度小于2 μm, 称取1.0 g矿物和50 mL蒸馏水于烧杯中, 按要求加入药剂并调节pH, 再用磁力搅拌器搅拌10 min, 最后用Zeta电位分析仪测得电位值。
1.5 红外光谱分析取1.0 g磨细至-2 μm的纯矿物于干净烧杯中, 并加入适量药剂和50 mL蒸馏水, 再调节pH至合适值, 最后置于磁力搅拌器上搅拌30 min, 静置后用离心分离机固液分离, 将固体矿物真空烘干后, 取适量样品压片制样并用红外光谱测量。
2 结果与讨论 2.1 刺槐豆胶对黄铜矿及黄铁矿单矿物浮选的影响研究了以丁基黄药为捕收剂时, pH值变化对单矿物浮选回收率影响(见图 3)。结果表明:在试验所做pH范围内, 黄铜矿回收率较高, 可浮性均较好; 在pH为3~7时, 黄铁矿回收率较高且基本不变, 但pH为7~11时黄铁矿回收率急剧下降, pH为11时黄铁矿基本不可浮。
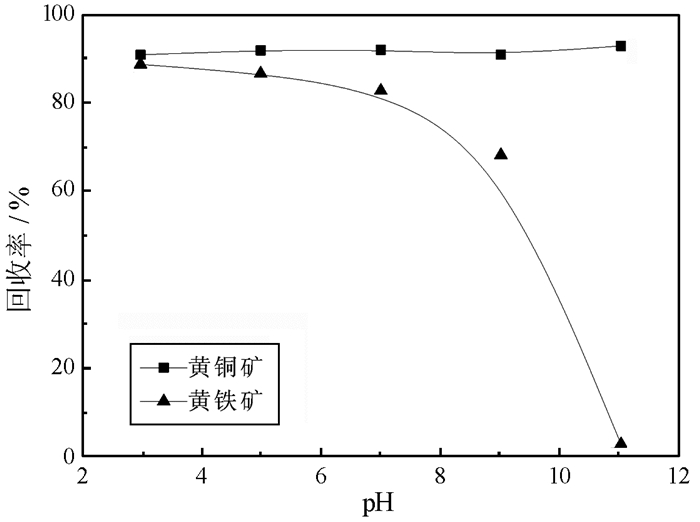 |
| 图 3 无抑制剂作用时pH对黄铜矿及黄铁矿浮选影响 Fig.3 Effect of pH on the flotation of chalcopyrite and pyrite in the absence of depressant c(PAX)=1×10-4 mol/L; c(MIBC)=1×10-4 mol/L |
图 4为pH=7时刺槐豆胶用量对单矿物浮选的影响。结果表明:随着刺槐豆胶用量的增加, 单矿物回收率均逐渐下降, 刺槐豆胶对黄铜矿及黄铁矿均有一定抑制作用; 但黄铁矿回收率下降速率更快, 所以刺槐豆胶对黄铁矿抑制效果更强, 可浮性差异较大。
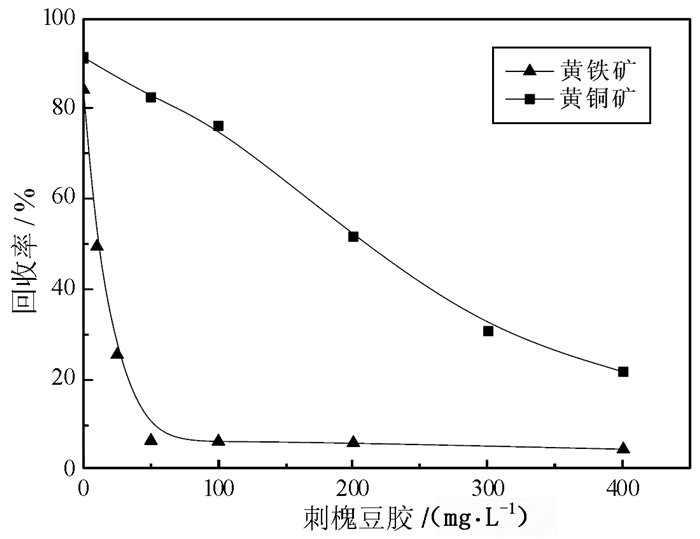 |
| 图 4 刺槐豆胶对黄铜矿及黄铁矿的浮选影响 Fig.4 Flotation of chalcopyrite and pyrite as a function of locust bean gum dosage c(PBX)=1×10-4 mol/L; c(MIBC)=1×10-4 mol/L; pH=7 |
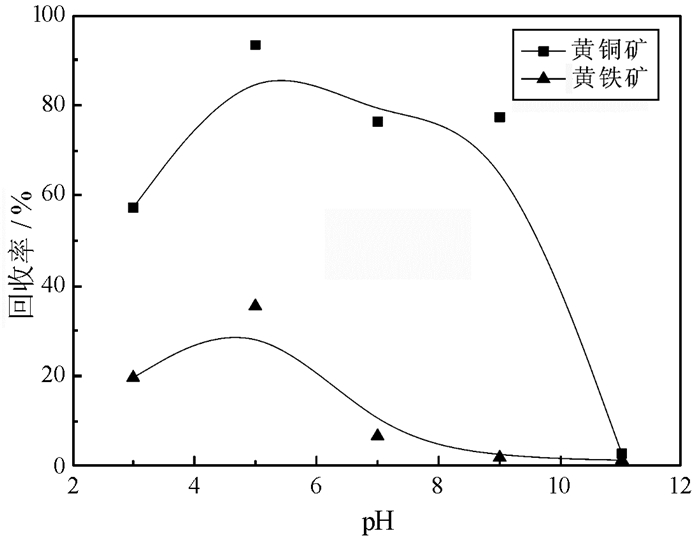
图 5为不同pH时刺槐豆胶对黄铜矿与黄铁矿浮选的影响。结果表明:在所做pH条件下, 黄铁矿的回收率较低, 说明刺槐豆胶对黄铁矿抑制作用较强且不受pH影响; 但刺槐豆胶对黄铜矿抑制作用受pH影响较大, 在强碱性条件下黄铜矿可浮性差, 说明药剂抑制作用较强, 而在其他pH条件下矿物可浮性好, 说明抑制作用较弱。
 |
|
图 5 不同pH条件下刺槐豆胶对黄铜矿及黄铁矿浮选影响 Fig.5 Flotation of chalcopyrite and pyrite as a function of pH in the presence of locust bean gum c(PBX)=1×10-4 mol/L; c(MIBC)=1×10-4 mol/L; c(locust bean gum)=100 mg/L |
2.2 刺槐豆胶在黄铜矿与黄铁矿分离中的作用
单矿物浮选试验表明刺槐豆胶在中性及弱碱性pH条件下, 对黄铁矿有强选择性抑制作用。研究了pH=7刺槐豆胶(100 mg/L)对铜品位为15.58%的混合矿分离的影响(见表 2)。
| 表 2 刺槐豆胶对混合矿浮选分离的影响 /% Table 2 Effect of locust bean gum on the flotation separation of mixture minerals |
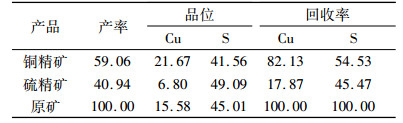 |
结果表明:在此条件下, 可获得的铜精矿铜品位为21.67%, 回收率为82.13%, 此时铜硫分离效果较好。
2.3 刺槐豆胶在黄铜矿与黄铁矿表面的吸附行为浮选药剂产生抑制作用的前提是其在矿物表面的吸附, 研究了pH为7条件下刺槐豆胶在黄铜矿及黄铁矿表面的吸附行为(见图 6)。结果表明:刺槐豆胶在矿物表面均发生了吸附, 且其在矿物表面吸附量与自身用量成正相关; 但刺槐豆胶在黄铁矿表面吸附作用更强。
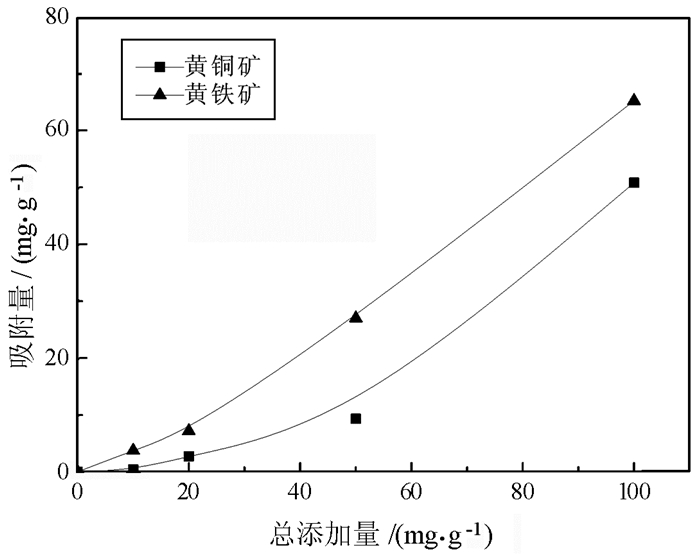 |
| 图 6 不同刺槐豆胶用量在黄铜矿及黄铁矿表面吸附行为 Fig.6 The adsorption behavior of locust bean gum on chalcopyrite and pyrite surface |
2.4 刺槐豆胶在黄铜矿与黄铁矿表面的吸附机理
图 7所示为不同pH条件下刺槐豆胶对黄铜矿与黄铁矿表面电位的影响。
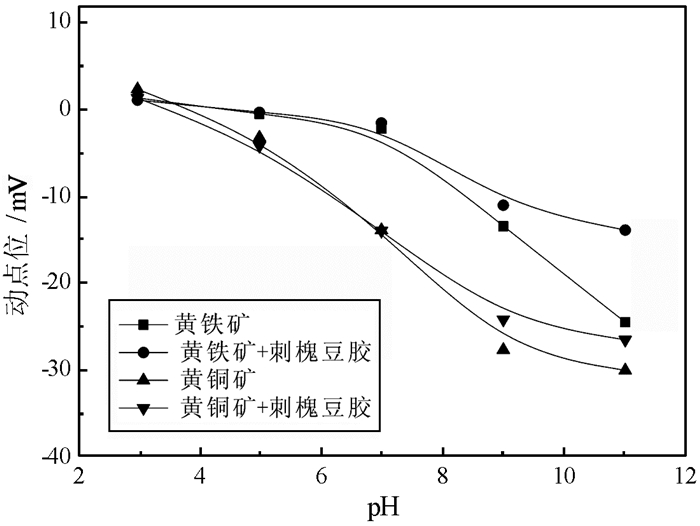 |
| 图 7 不同pH条件下刺槐豆胶对黄铜矿及黄铁矿表面电位的影响 Fig.7 Zeta potential versus pH for chalcopyrite and pyrite with and without locust bean gum |
结果表明:未加刺槐豆胶时黄铜矿及黄铁矿等电点均在pH值4左右, 且随pH值升高矿物表面负电值增加; 加入刺槐豆胶后黄铜矿及黄铁矿表面电位均发生变化, 两种矿物的电位值均向零值移动, 这是由于大分子抑制剂刺槐豆胶不带电, 其在矿物表面的吸附使矿物双电层中的滑移面外移, 导致电位值的数值下降。电位结果也表明, 刺槐豆胶在黄铜矿及黄铁矿表面均发生了吸附作用。
图 8为刺槐豆胶作用于黄铜矿前后的红外光谱图。
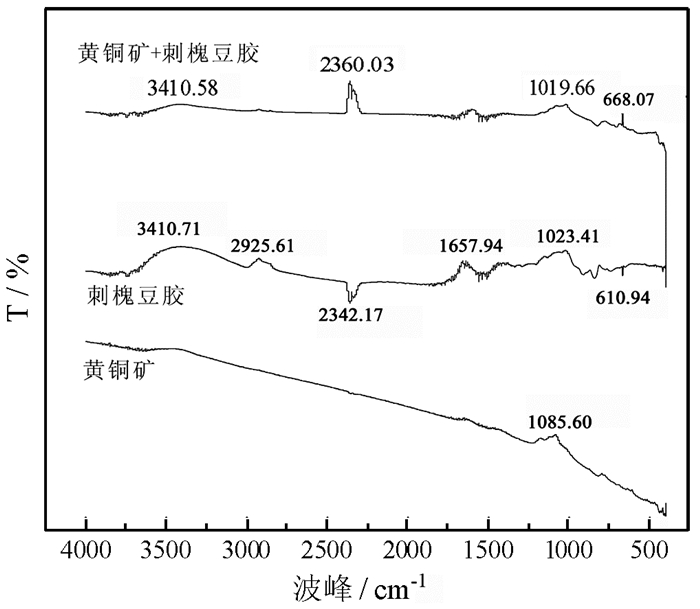 |
| 图 8 刺槐豆胶与黄铜矿作用前后红外光谱 Fig.8 Infrared spectra of chalcopyrite and locust bean gum before and after action |
在3 410.71 cm-1、1 023.41 cm-1处为刺槐豆胶的弯曲振动峰, 在2 342.17 cm-1、1 657.94 cm-1、610.94 cm-1处为刺槐豆胶的伸缩振动峰, 在波长为2 925.61 cm-1处出现了C-H基团的伸缩振动峰。黄铜矿与刺槐豆胶作用后, 在1 085.60 cm-1处的吸收峰强度有所减弱, 在2 925.61 cm-1、2 342.17 cm-1、1 657.94 cm-1、1 023.41 cm-1、610.94 cm-1处出现了新的吸收峰, 表明刺槐豆胶在黄铜矿矿物表面发生的吸附方式为化学吸附。
图 9为黄铁矿与刺槐豆胶作用前后红外光谱图对比。
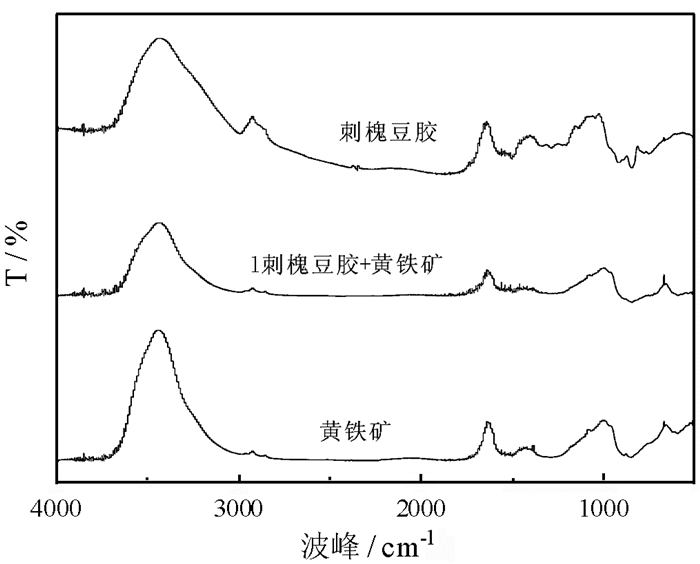 |
| 图 9 黄铁矿与刺槐豆胶作用前后红外光谱 Fig.9 Infrared Spectra of pyrite and locust bean gum before and after action |
由图可知, 与刺槐豆胶作用前后黄铁矿的红外光谱图并无明显差别。图中3 400、2 920 cm-1附近均未出现-OH、-CH2等的特征吸收峰, 由此可以推断刺槐豆胶在黄铁矿表面发生的是物理吸附。
3 结论(1) 黄铜矿及黄铁矿在酸性和弱碱性pH范围内可浮性较好, 不使用抑制剂时较难实现二者的浮选分离; 加入刺槐豆胶后, 在试验所做pH范围内黄铁矿的浮选回收率均较低, 而黄铜矿在酸性及中性pH条件下浮选回收率高, 强碱性pH条件下回收率低。
(2) 在pH为7时使用刺槐豆胶作为抑制剂分选黄铜矿与黄铁矿, 取得了一定的分离效果, 对铜品位为15.58%的混合矿进行浮选分离后, 获得的铜精矿铜品位为21.67%、回收率82.13%。
(3) 通过吸附量试验、Zeta电位测量和红外光谱测试分析其作用机理, 结果表明:刺槐豆胶在黄铜矿及黄铁矿表面均产生吸附作用, 在黄铁矿表面吸附作用更强, 且是通过物理吸附作用在黄铁矿表面。
| [1] |
于雪. 铜锌硫化矿难以分离的可能原因及解决途径[J]. 国外金属矿选矿, 2004(9): 4-8. |
| [2] |
匡敬忠. 铜硫分离中抑制剂的应用[J]. 矿业研究与开发, 2013, 33(5): 51-53. |
| [3] |
于传兵, 刘清高. 难选复杂铜矿石选矿工艺探讨[J]. 有色金属, 2009(4): 19-21. |
| [4] |
余新阳, 周源. 铜硫分离中无机抑制剂的研究[J]. 矿冶工程, 2005, 25(4): 33-35. |
| [5] |
李崇德, 孙传尧. 铜硫浮选分离的研究进展[J]. 国外金属矿选矿, 2000(8): 2-7. |
| [6] |
李宗站, 刘家弟, 王振玉, 等. 国内铜硫浮选分离研究现状[J]. 金属矿山, 2010, 39(7): 12-15. |
| [7] |
詹信顺, 钟宏, 刘广义. 低碱度铜硫分离高效抑制剂的研究[J]. 有色金属(选矿部分), 2009(4): 19-21. |
| [8] |
徐竞, 孙伟, 刘辉, 等. 新型有机抑制剂RC在铜硫矿物浮选分离中的抑制作用[J]. 矿冶工程, 2004, 24(6): 27-30. |
| [9] |
熊道陵, 张辉, 汪杨. 一种新型有机抑制剂的铜硫分离效果[J]. 金属矿山, 2015(6): 59-63. |
| [10] |
刘斌, 周源. 采用有机抑制剂进行无石灰铜硫分离及机理研究[J]. 江西理工大学学报, 2008, 29(3): 24-26. |
| [11] |
Gaisford SE, Harding SE, Mitchell JR. A comparison between the hot and cold water soluble fractions of two locust bean gum samples[J]. Carbohydrate Polymers, 1986, 6(6): 423-442. DOI:10.1016/0144-8617(86)90002-0 |
| [12] |
Pramoda MK, Lin SL. Mixed xanthan gum and locust beam gum therapeutic compositions[J]. US, 1979. |
| [13] |
Chen Y, Liao ML, Boger DV. Rheological characterisation of k-carrageenan/locust bean gum mixtures[J]. Carbohydrate Polymers, 2001, 46(2): 117-124. DOI:10.1016/S0144-8617(00)00293-9 |
| [14] |
Lopes JA, Gonçalves MP, Rao MA. Viscoelastic behaviour of mixtures of locust bean gum and pectin dispersions[J]. Journal of Food Engineering, 1993, 18(3): 211-228. DOI:10.1016/0260-8774(93)90087-Z |
| [15] |
高义霞, 周向军, 王风霞, 等. 海藻酸钠-刺槐豆胶复合凝胶珠吸附孔雀绿[J]. 环境工程学报, 2014, 8(2): 453-459. |
| [16] |
Fernandes PB, Gonçalves MP, Doublier JL. Influence of locust bean gum on the rheological properties of kappa-carrageenan systems in the vicinity of the gel point[J]. Carbohydrate Polymers, 1993, 22(2): 99-106. DOI:10.1016/0144-8617(93)90072-C |
| [17] |
Kaity S, Ghosh A. Carboxymethylation of locust bean gum:application in interpenetrating polymer network microspheres for controlled drug delivery[J]. Industrial & Engineering Chemistry Research, 2013, 52(30): 10033-10045. |
| [18] |
Hoffman J, Lindberg B, Painter T. The distribution of the D-galactose residues in guaran and locust bean gum[J]. Acta Chemica Scandinavica, 1976, 30(4): 365-366. |
| [19] |
Haddarah A, Bassal A, Ismail A. The structural characteristics and rheological properties of lebanese locust bean gum[J]. Journal of Food Engineering, 2014, 120(1): 204-214. |
| [20] |
Vieira MC, Gil AM. A solid state NMR study of locust bean gum galactomannan and konjac glucomannan gels[J]. Carbohydrate Polymers, 2005, 60(4): 439-448. DOI:10.1016/j.carbpol.2005.02.013 |
| [21] |
García-García E, Totosaus A. Low-fat sodium-reduced sausages:Effect of the interaction between locust bean gum, potato starch and k-carrageenan by a mixture design approach[J]. Meat Science, 2008, 78(4): 406-413. DOI:10.1016/j.meatsci.2007.07.003 |
 2018
2018 


