| 三元体系Li+, Cs+//SO42--H2O 298 K稳定相平衡研究 |
2. 中国石油 新疆油田分公司,新疆 克拉玛依 834000;
3. 攀西战略矿产资源综合利用四川省协同创新中心,四川 成都 610059
2. Xinjiang Oilfield Company, PetroChina, Karamay 834000, China;
3. Sichuan Collaborative Innovation Center of Panxi Strategic Mineral Resources Multi-purpose Utilization, Chengdu 610059, China
随着人们对化学制品的需求量越来越大,赖以开采的固体矿产资源不断减少,液态矿产资源(如海水、盐湖卤水、地下卤水等资源)高效开发利用已成为国际资源竞争的主战场[1-2]。
我国盐湖分布众多,人们已从盐湖中开采了大量用于化工、农业、轻工、冶金、建筑和医疗等方面的重要原料,如锂、钾、硼、镁、溴、芒硝、石盐、硝石、石膏和医用淤泥等[3]。众所周知,相平衡研究为液态矿产资源利用与盐分离技术提供指导。因此,针对不同类型的水盐体系开展相平衡研究对综合利用卤水资源具有重要意义[4]。
柴达木盆地盐湖卤水属硫酸盐型卤水[5-10]。其中锂铯离子含量最高可达262 mg/L和0.76 mg/L[11]。目前针对卤水中锂铯提取方法主要有离子交换吸附法、电解法、真空热还原法,但前者回收率低,后两者耗能大成本高,不适宜大规模生产。因此运用相平衡与相分离技术的低耗能高收益特点提取锂铯显得尤为必要。近些年来专家学者针对硫酸盐型水盐体系进行了大量研究[12-21]。但从已有文献来看,已有研究主要集中在Li、Na、K等元素的盐类体系研究,对含Cs体系的研究较少。三元体系Li+, Cs+//SO42--H2O是硫酸盐型卤水到老卤阶段时卤水组成的最基础体系之一,其相平衡数据是老卤中锂、铯资源分离提取不可或缺的基础热力学数据,故本文开展了三元体系Li+, Cs+//SO42--H2O 298 K稳定相平衡研究,其研究结果将有利于完善硫酸盐水盐体系热力学数据,为今后开展含锂、铯的四元、五元复杂相平衡研究提供基础,同时也为工业分离锂、铯资源提供科学依据。
1 试验部分 1.1 试验试剂去离子水pH值为6.6,电导率<1×10-5 S·m-1,试验过程中所用水均为此水。Li2SO4·H2O(成都科龙化工试剂厂,AR),Cs2SO4(江西东鹏新材料有限责任公司,AR),乙二胺四乙酸二钠(成都科龙化工试剂厂,AR),NaOH(成都科龙化工试剂厂,AR),四苯硼钠(成都科龙化工试剂厂,AR),十六烷基三甲基溴化铵(成都科龙化工试剂厂,AR)。
1.2 试验仪器BSA124S型电子天平(Sartorius科学仪器有限公司,精度±0.000 1 g);WYA型阿贝折射仪(上海精密仪器仪表有限公司,精度±0.000 1);HZS-HA型恒温水浴振荡器(哈尔滨市东联电子技术开发有限公司,精度±0.5 K);DX-2700型X-ray粉晶衍射仪(丹东方圆仪器有限公司);iCE-3300型火焰原子吸收光谱仪(赛默飞世尔科技有限公司);UP-Ⅱ-20T型超纯水器(四川优普超纯科技有限公司);常规玻璃仪器等。
1.3 试验方法采用等温溶解平衡法[22]开展稳定相平衡研究。具体做法是向二元体系的饱和盐溶液中梯度加入另一种盐配制溶液(如向Li2SO4饱和液中梯度加入Cs2SO4)于50 mL玻璃瓶中。所配溶液置于恒温水浴振荡器中振荡(温度控制在298±0.5 K)。定期取上层清夜进行密度、折光率和组成分析(取样时应使体系静置至悬浮固体颗粒完全沉淀),以其密度、折光率和组成不变时作为平衡标志。确认体系达到平衡后,取上层清液进行化学成分分析,同时测定液相密度、折光率等物化性质,并取相应固相做固相分析。平衡液相密度采用称量瓶法测定,折光率用阿贝折射仪测定。
1.4 分析方法[23]Li+:结合火焰原子吸收光谱法和差减法。SO42-:EDTA-Ba容量法。Cs+:结合STPB-CTAB返滴定法和原子吸收光谱法。平衡固相分析方法:X-ray粉晶衍射法和Schreinemakers湿渣法[24]。
2 结果与讨论 2.1 三元体系Li+, Cs+//SO42--H2O 298 K稳定相平衡试验研究三元体系Li+, Cs+//SO42--H2O 298 K稳定相平衡数据及其密度、折光率的测定结果见表 1。
| 表 1 三元体系Li+, Cs+//SO42--H2O 298 K溶解度、密度、折光率测定值 Table 1 Measured values of solubility, density and refractive index of the ternary system Li+, Cs+//SO42--H2O at 298 K |
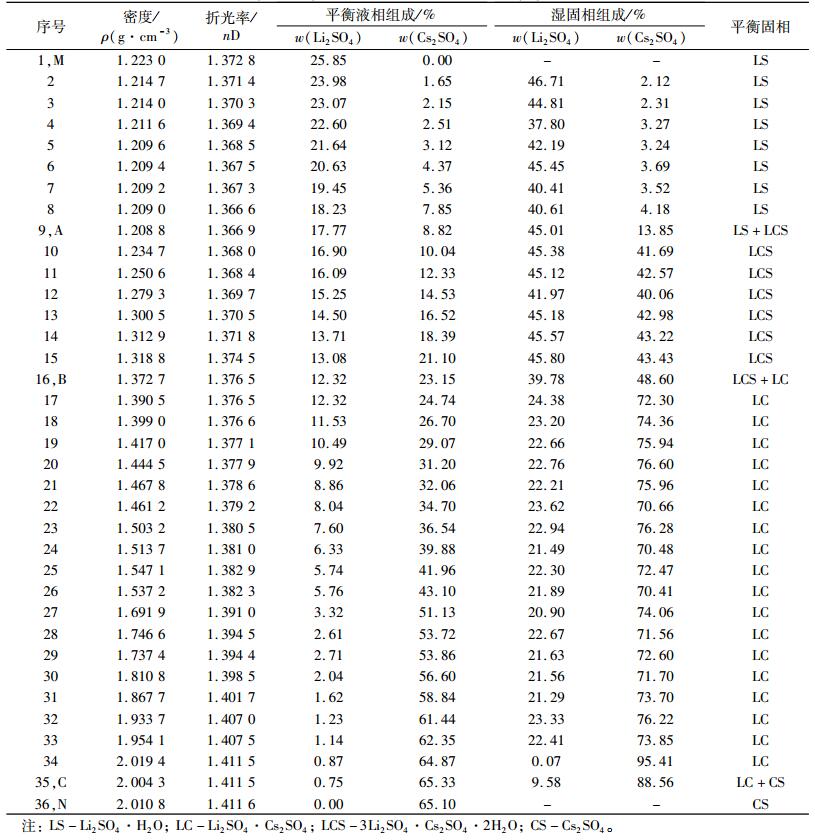 |
根据表 1数据绘制了该三元体系298 K稳定相图,如图 1所示。该三元体系298 K稳定相图有4个结晶区、4条单变量曲线和3个共饱点。3个共饱点(A、B、C)均在水和其共饱和盐对应顶点所构成的三角形内,故均属于相称共饱点。图 2、图 3、图 4分别为共饱点A、B、C处对应的平衡固相X射线粉晶衍射图谱。
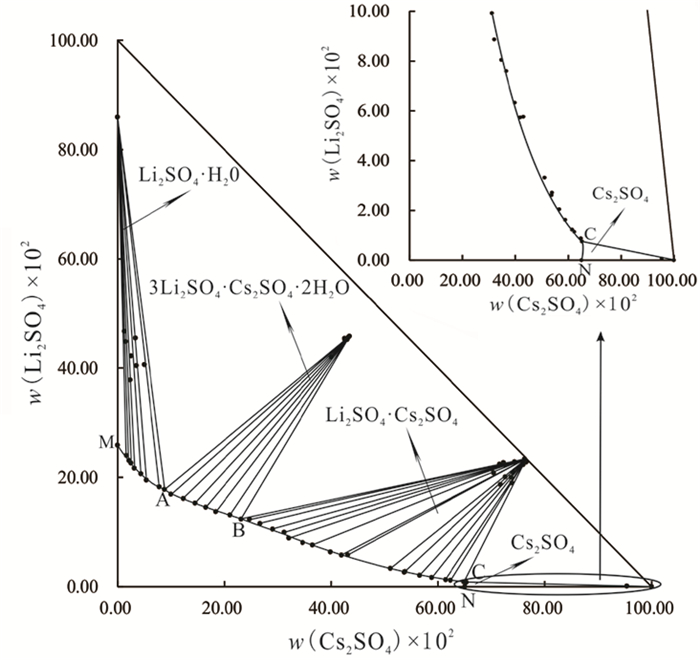 |
| 图 1 三元体系Li+, Cs+//SO42--H2O 298 K稳定相图及局部放大图 Fig.1 Stable phase diagram and its partial enlarged diagram of the ternary system Li+, Cs+//SO42--H2O at 298 K |
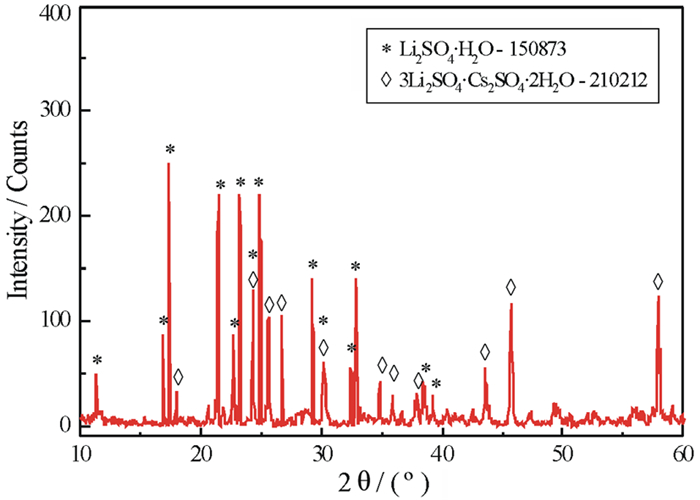 |
| 图 2 共饱点A对应的平衡固相的XRD图 Fig.2 X-ray diffraction patterns of the equilibrated solid phases at invariant point A |
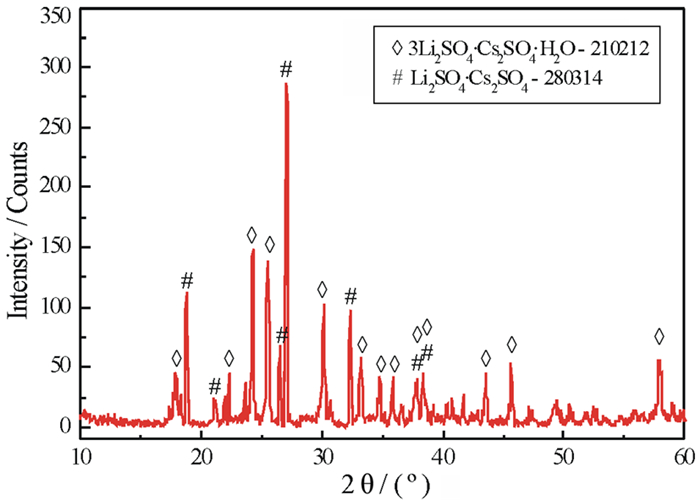 |
| 图 3 共饱点B对应的平衡固相的XRD图 Fig.3 X-ray diffraction patterns of the equilibrated solid phases at invariant point B |
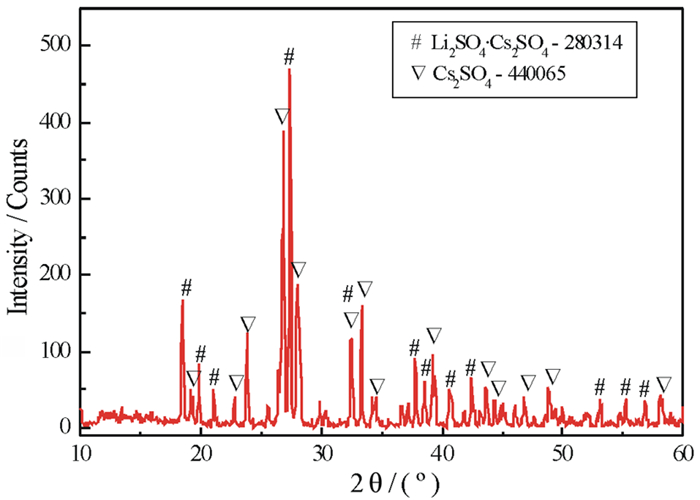 |
| 图 4 共饱点C对应的平衡固相的XRD图 Fig.4 X-ray diffraction patterns of the equilibrated solid phases at invariant point C |
相称共饱点A对应的平衡液相组成为w(Li2SO4)=17.77%,w(Cs2SO4)=8.82%,w(H2O)=73.41%;其平衡固相组成为Li2SO4·H2O+ 3Li2SO4·Cs2SO4·2H2O。相称共饱点B对应的平衡液相组成为w(Li2SO4)=12.32%,w(Cs2SO4)=23.15%,w(H2O)=64.53%;其平衡固相组成为3Li2SO4·Cs2SO4·2H2O+Li2SO4·Cs2SO4。相称共饱点C对应的平衡液相组成为w(Li2SO4)=0.75%,w(Cs2SO4)=65.33%,w(H2O)=33.92%;其平衡固相组成为Li2SO4·Cs2SO4+Cs2SO4。
单变量曲线MA、AB、BC和CN对应的平衡固相分别为Li2SO4·H2O、3Li2SO4·Cs2SO4·2H2O、Li2SO4·Cs2SO4和Cs2SO4。其中,复盐3Li2SO4·Cs2SO4·2H2O和Li2SO4·Cs2SO4为相称复盐。
4个结晶区分别对应Li2SO4·H2O、3Li2SO4·Cs2SO4·2H2O、Li2SO4·Cs2SO4和Cs2SO4。其中Li2SO4·Cs2SO4固相结晶区最大,对应Li2SO4·Cs2SO4的溶解度最小,Cs2SO4固相结晶区最小,对应Cs2SO4的溶解度最大。
2.2 平衡液相物化性质研究由表 1中平衡液相物化性质数据绘制了相应的密度-组成图和折光率-组成图,分别见图 5和图 6。从M点到A点密度和折光率呈减小趋势,从A点到N点逐渐增大。
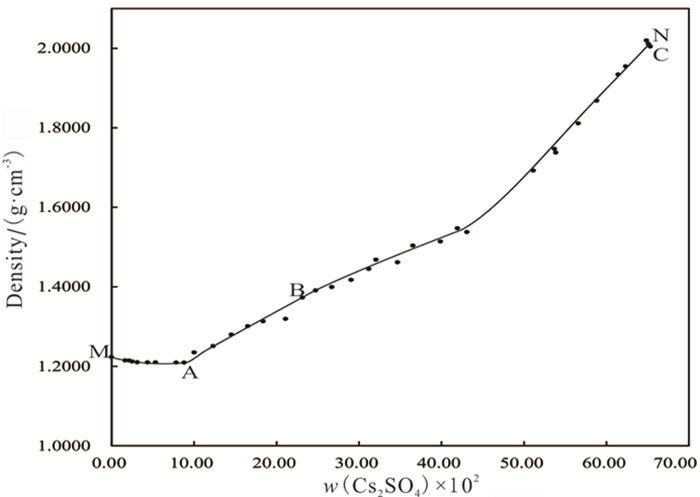 |
| 图 5 三元体系Li+, Cs+//SO42--H2O 298 K平衡液相密度-组成图 Fig.5 Density composition diagram of the equilibrated solution in the ternary system Li+, Cs2+//SO42--H2O at 298 K |
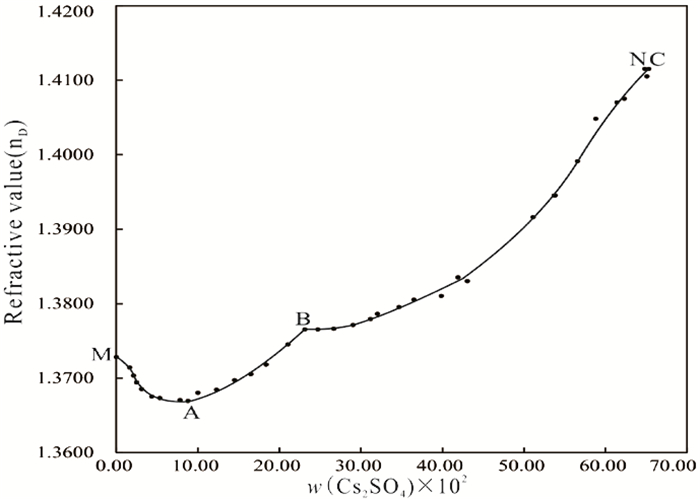 |
| 图 6 三元体系Li+, Cs+//SO42--H2O 298 K平衡液相折光率-组成图 Fig.6 Refractive index composition diagram of the equilibrated solution in the ternary system Li+, Cs2+//SO42--H2O at 298 K |
单变量曲线MA上,平衡液相密度和折光率逐渐减小,可能是由于Cs2SO4的极性大于Li2SO4的极性,当Cs2SO4溶于水中电离出的Cs+就更容易与带有极性的水分子相互结合,而原本与Li+结合的水分子被Cs+夺取而导致锂盐析出。由于Cs2SO4的摩尔质量和溶解度均大于Li2SO4,Cs2SO4的质量分数成了影响平衡液相物化性质的主要因素,故单变量曲线AN上,平衡液相密度和折光率随Cs2SO4的质量分数增大逐渐增大。
3 结论(1) 三元体系Li+, Cs+//SO42--H2O 298 K稳定相图属于复杂共饱型,有复盐生成。整个相图由4个固相结晶区、4条单变量曲线和3个共饱点组成。4个固相结晶区对应单盐Li2SO4·H2O、Cs2SO4和复盐3Li2SO4·Cs2SO4·2H2O、Li2SO4·Cs2SO4。
(2) 体系中形成的复盐3Li2SO4·Cs2SO4·2H2O和Li2SO4·Cs2SO4均为相称复盐;3个共饱点均为相称共饱点。
(3) 平衡液相密度和折光率随Cs2SO4含量增大呈先减小后增大的趋势,在共饱点A处达最小值。
| [1] |
桑世华, 张婷婷, 傅超, 等. 四元体系Li+, K+, Mg2+//B4O72--H2O 273 K相平衡[J]. 化工学报, 2017, 68(9): 3343-3349. |
| [2] |
陆智凭, 国怀专, 孙志伟. 柴达木盆地盐湖矿产开发利用存在的问题与建议[J]. 矿产保护与利用, 2010(5): 11-14. DOI:10.3969/j.issn.1001-0076.2010.05.004 |
| [3] |
郑绵平, 卜令忠. 盐湖资源的合理开发与综合利用[J]. 矿产保护与利用, 2009(1): 17-22. DOI:10.3969/j.issn.1001-0076.2009.01.004 |
| [4] |
Yu X. D., Zeng Y., Mu P. T., et al. Solid-liquid equilibria in the quinary system LiCl-KCl-RbCl-MgCl2-H2O at T=323 K[J]. Fluid phase equilib, 2015, 387: 88-94. DOI:10.1016/j.fluid.2014.12.021 |
| [5] |
樊启顺, 马海州, 谭红兵, 等. 柴达木盆地西部卤水特征及成因探讨[J]. 地球化学, 2007, 36(6): 601-611. DOI:10.3321/j.issn:0379-1726.2007.06.008 |
| [6] |
黄西平. 国内外盐湖(地下)卤水资源综合利用综述[J]. 海洋技术学报, 2002, 21(4): 66-72. |
| [7] |
田向东, 王云生, 侯献华. 柴达木北部新盐带卤水水化学特征研究[J]. 盐科学与化工, 2013, 42(12): 8-12. |
| [8] |
张西营, 马海州, 高东林, 等. 柴达木盆地西台吉乃尔盐湖矿区卤水水化学特征[J]. 盐湖研究, 2007(2): 12-20. DOI:10.3969/j.issn.1008-858X.2007.02.003 |
| [9] |
李廷伟, 谭红兵, 樊启顺. 柴达木盆地西部地下卤水水化学特征及成因分析[J]. 盐湖研究, 2006, 14(4): 26-32. DOI:10.3969/j.issn.1008-858X.2006.04.005 |
| [10] |
韩佳君, 周训, 姜长龙, 等. 柴达木盆地西部地下卤水水化学特征及其起源演化[J]. 现代地质, 2013(6): 1454-1464. DOI:10.3969/j.issn.1000-8527.2013.06.025 |
| [11] |
张彭熹. 柴达木盆地盐湖[M]. 北京: 科学出版社, 1987: 138-139.
|
| [12] |
Zeng Y., Lin X. F., Yu X. D. Study on the solubility of the aqueous quaternary system Li2SO4+Na2SO4+K2SO4+H2O at 273.15 K[J]. J. chem. eng. data, 2012, 57(12): 3672-3676. DOI:10.1021/je300874c |
| [13] |
曾英, 林晓峰, 郑志远. Li+, K+//SO42-, B4O72--H2O交互四元体系273 K介稳相平衡研究[J]. 高校化学工程学报, 2009(1): 7-11. DOI:10.3321/j.issn:1003-9015.2009.01.002 |
| [14] |
Wollmann G., Voigt W. Solid-liquid phase equilibria in the system K+, Mg2+//SO42--H2O at 318 K[J]. Fluid phase equilib, 2010, 291(2): 151-153. DOI:10.1016/j.fluid.2009.12.005 |
| [15] |
Liu Y., Guo Y., Yu X., et al. Solid-liquid metastable phase equilibria in the five-component system (Li+Na+K+Cl+SO4+H2O) at 308.15 K[J]. J. Chem. eng. data, 2014, 59(5): 1685-1691. DOI:10.1021/je500140e |
| [16] |
桑世华, 殷辉安, 曾英, 等. Li+, Na+//SO42-, CO32--H2O交互四元体系288 K介稳相平衡研究[J]. 化学学报, 2006, 64(22): 2247-2253. DOI:10.3321/j.issn:0567-7351.2006.22.007 |
| [17] |
孙柏, 宋彭生. 盐湖卤水体系Li+, Mg2+//Cl-, SO42-, borate-H2O的研究[J]. 盐湖研究, 1994(4): 26-30. |
| [18] |
Sang S. H., Peng J. (Solid+liquid) equilibria in the quinary system Na+, Mg2+, K+SO42-, B4O72--H2O math container loading mathjax at 288 K[J]. Calphad, 2010, 34(1): 64-67. DOI:10.1016/j.calphad.2009.12.001 |
| [19] |
Ye C., Zheng M., Wang Z., et al. Hydrochemical characteristics and sources of brines in the Gasikule salt lake, Northwest Qaidam Basin, China[J]. Geochem. J., 2015, 49(5): 481-494. DOI:10.2343/geochemj.2.0372 |
| [20] |
宋彭生, 董亚萍, 李武. Li+, Na+, K+//Cl-, SO42--H2O五元体系25 ℃相图及其应用[J]. 盐湖研究, 2017, 25(3): 9-17. |
| [21] |
Wang F. Y. Thermodynamic simulation on Rb2SO4-Cs2SO4-MgSO4-H2O system at 25 ℃[J]. Asian J. chem., 2013, 25(13): 7631-7632. DOI:10.14233/ajchem |
| [22] |
牛自得. 水盐体系相图及其应用[M]. 天津: 天津大学出版社, 2002: 172-182.
|
| [23] |
中科院青海盐湖所. 卤水和盐的分析方法[M]. 北京: 科学与技术出版社, 1984: 75-78.
|
| [24] |
Fosbol P., Thomsen K., Stenby E. H. Reverse schreinemakers method for experimental analysis of mixed-solvent electrolyte systems[J]. J. solution chem., 2009, 38(1): 1-14. DOI:10.1007/s10953-008-9353-4 |
 2019
2019



