| 二次铝灰高温焙烧脱氮固氟试验研究 |
2. 中国铝业股份有限公司兰州分公司, 甘肃 兰州 730080
2. Lanzhou branch of aluminum corporation of China LTD, Lanzhou 730050, Gansu, China
二次铝灰(SAD)是一次铝灰回收金属铝后的残渣,通常呈松散的小颗粒或尘粒状,主要由金属铝及其氧化物、氮化铝(AlN)、碳化铝(Al4C3)、其它金属氧化物、无机盐和电解质等组成[1, 2]。由于缺乏低成本、规模化、相对成熟的处理技术,就地填埋和堆积仍是目前二次铝灰的主要处理方法[3]。二次铝灰中AlN在潮湿的环境下易产生具有刺激性气味的氨气,以及溶解在水中易导致氨氮团聚现象是铝灰被列为危险固体废弃物的主要原因之一[4, 5]。二次铝灰中AlN主要以单独针状或大颗粒块状形式存在,也可被α-Al2O3包覆共存,粒径约100~200 μm。一般而言,二次铝灰粒径越小AlN含量越高[6]。AlN有较高的反应活性,除了可与水反应释放出氨气之外,在高温(600~1 300 ℃)下AlN可以氧化生成Al2O3[7]。二次铝灰中可溶出氟化物的浸出是铝灰被列为危险固体废弃物的另一主要原因,二次铝灰的传统处理工艺之一——碱烧结法[8],通过将二次铝灰与碱性物质混合在高温下焙烧反应生成铝酸钠,然后进行溶液浸出、晶种分解和高温煅烧,实现氧化铝的回收[9],但由于该工艺未考虑氟化物的脱除而导致浸出液中氟离子浓度较高。
加入钙盐高温焙烧处理铝灰是抑制氟溶出的最佳途径,中国铝业郑州研究院[10]通过加入氧化钙、回转窑焙烧热处理二次铝灰,处理后二次铝灰中可溶出氟转化率在98%以上,平均可溶氟含量为39.7 mg/L,降低了二次铝灰的浸出毒性。但综观文献,关于焙烧固氟的研究较少,同时也未见焙烧过程中氮化铝转化方面的研究报道。鉴于此,本文对铝灰钙盐高温焙烧脱氮固氟、水洗回收无机盐工艺进行研究,分析焙烧温度和钙盐加入量对铝灰脱氮固氟和减量化的影响,旨在消除二次铝灰中氮化铝和可溶出氟化物的危害,为实现二次铝灰的无害化和减量化提供新思路。
1 试验 1.1 原料与试剂二次铝灰来自中国铝业兰州分公司一合金车间产生的铸造铝灰,铸造铝合金型号为6063,属于铝-镁-硅系列。在熔炼、铸造过程中加入的精炼剂为无机盐,主要成分为氯化钠(NaCl),含有少量的氯化钾(KCl)和六氯乙烷(C2Cl6)。在晶粒细化工艺中加入铝钛硼丝以达到最佳的细化效果。本试验所用试剂均为分析纯。
1.2 铝灰的高温焙烧工艺依次使用破碎机、振筛机、球磨机将二次铝灰处理为粒径小于0.1 mm的均匀颗粒。球磨后的二次铝灰置于105 ℃烘箱中干燥3 h除去水分,采用四分法准确称重50.00 g二次铝灰,分别加入一定量的钙盐,研磨混合,装入刚玉坩埚并置于马弗炉中,在900 ℃~1 300 ℃焙烧4 h,冷却至室温后称重记录。焙烧后的铝灰称为煅后铝灰。焙烧前后铝灰的质量变化通过式(1)进行计算:
| $ {R^*}(\% ) = \frac{{{m_{{\rm{煅后铝灰}}}} - ({m_{{\rm{二次铝灰}}}} + {m_{{\rm{CaC}}{{\rm{l}}_{\rm{2}}}}})}}{{{m_{{\rm{二次铝灰}}}} + {m_{{\rm{CaC}}{{\rm{l}}_{\rm{2}}}}}}} $ | (1) |
将煅后铝灰置于三口烧瓶中,在液固比为5∶1、温度100 ℃、超声30 min的条件下水洗脱除无机盐。水洗后的残渣经液固分离回收无害化、减量化的铝渣,称为水洗铝灰。水洗液经蒸发、结晶回收无机盐。二次铝灰中无机盐回收率r通过式(2)计算:
| $ r(\% ) = \frac{{{m_{{\rm{NaCl - Recovery}}}}}}{{{m_{{\rm{NaCl - 二次铝灰}}}}}} \times 100\% $ | (2) |
焙烧前后铝灰中AlN、Al4C3的含量变化采用Flash EA 1112测定。焙烧前后铝灰与水的反应性通过气体释放量评价,具体为:称取一定量的二次铝灰和煅后铝灰,在液固比为1∶1、加入少量NaOH作催化剂的条件下反应,用排油法测量产生气体体积。焙烧前后铝灰的可溶出氟离子浓度采用GB/T 15555.11—1995《固体废物氟化物的测定离子选择性电极法》测定。
采用激光粒度分析仪分析二次铝灰的粒度分布。采用D/max-2400 X射线衍射仪(XRD)在2θ为10~90°范围内进行扫描,分析二次铝灰、煅后铝灰和回收的无机盐中的主要物相和晶型结构。使用帕纳科-axios X射线荧光光谱仪(XRF)分析二次铝灰的主要元素和含量。采用MettlerTGA/DSC1/1600HT综合热分析仪分析二次铝灰在焙烧过程的质量和可能的成分变化,测试条件:温度为30~1 300 ℃,升温速率为10 ℃/min,空气速率为50 mL/min。
2 结果与讨论 2.1 二次铝灰的组成及成分二次铝灰的粒度分布如图 1a所示。从图 1a可以看出,二次铝灰粒径区间在0.1~700 μm,体积平均粒径为172.1 μm,表面积平均粒径15.784 μm(d50),粒度分布不均匀且颗粒较小。
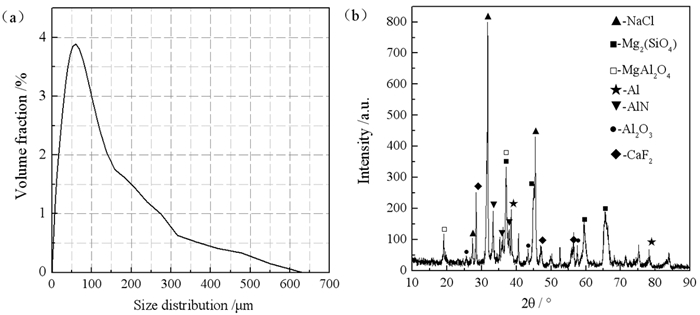 |
| 图 1 (a) 二次铝灰的粒度分布; (b)二次铝灰的XRD谱 Fig.1 (a)Size distribution of SAD; (b)XRD of SAD |
二次铝灰的元素组成及相对含量如表 1所示,从表 1中可以看出二次铝灰中铝、氧、镁为主要元素,其含量分别为33.943%、29.476%、14.209%,其它元素如硅、氟、钙等含量较低。EA分析结果为二次铝灰中C、N元素含量分别为0.85%、2.47%。
| 表 1 二次铝灰元素及含量分析(XRF) Table 1 SAD element and content analysis |

|
二次铝灰的XRD谱如图 1b所示,在图 1b中,33.256°、36.042°、37.971°的衍射峰为氮化铝的特征衍射峰,28.219°、46.866°、55.654°的衍射峰为氟化钙的特征衍射峰,25.54°、35.185°、52.546°和38.4°、44.669°、65.031°的衍射峰分别归属于α-Al2O3和铝单质的特征衍射峰,19.00°和36.846°的衍射峰为尖晶石的特征衍射峰。可见二次铝灰中铝元素主要以铝、氮化铝、刚玉(α-Al2O3)和尖晶石(MgAl2O4)的形式存在;镁元素主要以MgAl2O4和硅酸镁[Mg2(SiO4)]的形式存在。其中,α-Al2O3来源于高温下熔融的铝液和大气中的氧气接触氧化反应,这也是铝液中单质铝损失的主要因素;AlN主要是高温下熔融的铝液和大气中的氮气接触反应产生的;MgAl2O4是镁作为合金元素在重熔过程中氧化的结果;NaCl是铝合金熔炼过程中的精炼剂成分。二次铝灰中游离氟、硅含量低于仪器检测限度,故XRD谱图中难以发现有NaF、SiO2晶相存在。
2.2 高温焙烧脱氟固氮效果 2.2.1 高温焙烧过程热力学计算根据热力学计算方法结合298 K下物质热力学数据,该焙烧体系可能发生的反应方程式为:
| $ {4{\rm{Al}} + 3{{\rm{O}}_2} \to 2{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}} $ | (3) |
| $ {2{\rm{Al}} + {{\rm{N}}_2} \to 2{\rm{AlN}}} $ | (4) |
| $ {4{\rm{Al}}{\rm{N}} + 3{{\rm{O}}_2} \to 2{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 2{{\rm{N}}_2}} $ | (5) |
| $ {2{\rm{Al}}{\rm{N}} + 2{{\rm{O}}_2} \to {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + {{\rm{N}}_2}{\rm{O}}} $ | (6) |
| $ {2{\rm{AlN}} + \frac{5}{2}{{\rm{O}}_2} \to {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 2{{\rm{N}}_2}} $ | (7) |
| $ {2{\rm{AlN}} + \frac{7}{2}{{\rm{O}}_2} \to {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 2{\rm{N}}{{\rm{O}}_2}} $ | (8) |
| $ {2{\rm{AlN}} + 4{{\rm{O}}_2} \to {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + {{\rm{N}}_2}{{\rm{O}}_5}} $ | (9) |
| $ {{\rm{A}}{{\rm{l}}_4}{{\rm{C}}_3} + 6{{\rm{O}}_2} \to 2{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 3{\rm{C}}{{\rm{O}}_2}} $ | (10) |
| $ {{\rm{A}}{{\rm{l}}_4}{{\rm{C}}_3} + \frac{9}{2}{{\rm{O}}_2} \to 2{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} + 3{\rm{CO}}} $ | (11) |
| $ {{\rm{A}}{{\rm{l}}_4}{{\rm{C}}_3} + \frac{7}{2}{{\rm{N}}_2} \to 4{\rm{AlN}} + 3{\rm{CN}}} $ | (12) |
| $ {{\rm{A}}{{\rm{l}}_4}{{\rm{C}}_3} + \frac{7}{2}{{\rm{N}}_2} \to 4{\rm{AlN}} + \frac{3}{2}{{\rm{C}}_2}{\rm{N}}2} $ | (13) |
| $ {2{\rm{NaF}} + {\rm{CaC}}{{\rm{l}}_2} \to {\rm{Ca}}{{\rm{F}}_2} + 2{\rm{NaCl}}} $ | (14) |
不同温度下的反应的焓变(ΔHΘ)和Gibbs自由能(ΔGΘ)计算采用如下公式计算:
| $ \begin{array}{l} {C_p} = {A_1} + {A_2} \times {10^{ - 3}}T + {A_3} \times {10^5}{T^{ - 2}} + \\ {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {\kern 1pt} {A_4} \times {10^{ - 6}}{T^2} + {A_5} \times {10^8}{T^{ - 3}} \end{array} $ | (15) |
| $ {H_i^\varTheta (T) = {\Delta _f}H_i^\varTheta + \int\limits_{298}^T {{C_p}} {\rm{d}}T} $ | (16) |
| $ {\Delta H_i^\varTheta = \sum\nolimits_{{v_i}} {H_i^\varTheta } (T)} $ | (17) |
| $ {S_i^T(t) = S_{i, 298}^\varTheta + \int\limits_0^{298} {{C_p}} {\rm{d}}\ln T + \sum {\frac{{\Delta H_i^t}}{{{T_i}}}} } $ | (18) |
| $ {\Delta {S^\varTheta } = \sum\nolimits_{{v_i}} {S_i^\varTheta } (T)} $ | (19) |
| $ {\Delta {G^\varTheta } = \Delta {H^\varTheta } - T\Delta {S^\varTheta }} $ | (20) |
式中:Cp为等压热容;A1、A2、A3、A4、A5为物质的热容温度系数,由热力学数据手册查出;HiΘ为i物质在温度T下的生成焓;ΔfHiΘ为i物质标准摩尔生成焓;ΔHΘ为化学反应焓变;vi为i物质的化学计量数;SiΘ为i物质在温度T下的熵;为化学反应熵变。
不同反应的反应热焓变、吉布斯自由能随温度的变化如图 2所示。从图 2a中可以看出,只有反应式(12)在温度900~1 400 ℃内ΔH>0,说明Al4C3生成CN的反应是吸热的;Al、AlN、Al4C3的氧化反应均为放热反应,式(10)放热最大,其次为式(3)、式(5);Al、Al4C3与N2的反应均为放热反应,Al与N2的反应放热是高于Al4C3的。从图 2b可以看出,在高温焙烧过程中Al、Al4C3与O2反应的ΔG是一直小于与N2反应的ΔG,说明Al、Al4C3与O2的反应趋势相较与N2的反应趋势更大。Al、AlN、Al4C3的氧化反应在温度900~1 400 ℃内ΔG<0,说明在热力学上均能朝正方向进行,其中AlN的氧化反应生成趋势最大的产物一直为N2;Al4C3的氧化反应生成趋势最大的产物一直为CO2。
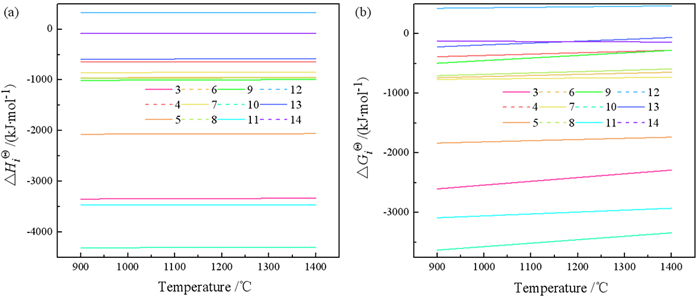 |
| 图 2 焙烧反应的(a)热焓变和(b)Gibbs函数随温度的变化 Fig.2 The change of (a)Enthalpy and(b)Gibbs function of roasting reaction with temperature |
2.2.2 焙烧温度对二次铝灰脱氮效果的影响
焙烧温度对煅后铝灰质量变化的影响如图 3所示。从图 3中可以看出,在900 ℃时煅后铝灰质量较二次铝灰增加了13.29%,这是由于在升温过程中,铝被氧化生成了氧化铝所致。随后,随焙烧温度的升高,煅后铝灰的质量变化呈现减小的趋势,并在1 300 ℃出现最大减重11.91%,这可能是由于NaCl、KCl、NaF等无机盐挥发而造成的。当温度高于1 300 ℃时,煅后铝灰的质量损失会略微减少,减重9.19%。这可由焙烧前后二次铝灰外观形貌的变化(图 4)得到印证,从图 4可以看出,在1 300 ℃下二次铝灰由不规则的灰黑色颗粒(a)烧结成白色的、易破碎块体(b),但在1 400 ℃,煅后铝灰已烧结致密化的坚硬结构(c),产生上述变化的主要原因是由于Al达到熔点熔化,填充了颗粒之间的空隙,进一步阻止了NaCl等无机盐的挥发;AlN在高温下氧化生成氧化铝膜覆盖在表面阻碍了反应的进行。
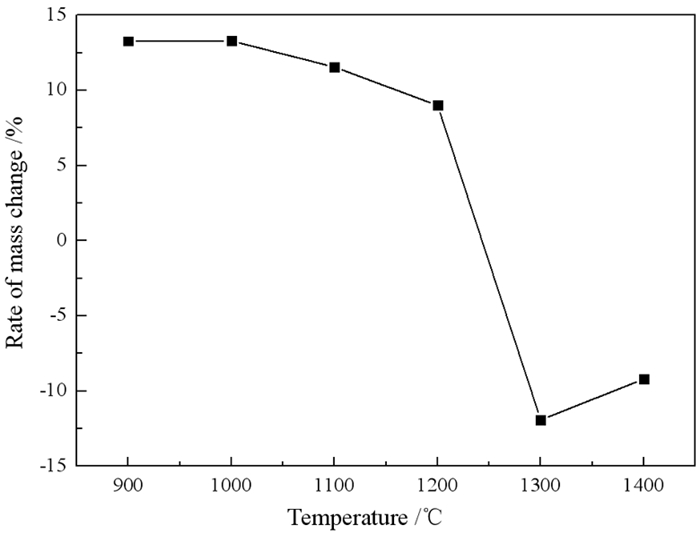 |
| 图 3 焙烧温度对煅后铝灰质量变化率的影响 Fig.3 Influence of roasting temperature on Roasted aluminum dross mass change rate |
 |
| 图 4 (a) 二次铝灰颗粒; (b)1 300 ℃焙烧煅后铝灰颗粒; (c)1 400 ℃焙烧煅后铝灰颗粒样貌 Fig.4 The appearance of(a)SAD particles, (b)Roasted particles at 1 300 ℃; (c)Roasted particles at 1 400 ℃ |
高温焙烧二次铝灰脱氮反应机理如图 5a所示,大气中O2在二次铝灰中AlN表面接触反应生成的α-Al2O3膜覆盖在颗粒表面,生成的N2脱附向大气扩散,生成的氧化铝膜覆盖在颗粒表面阻止反应的进一步发生,直至反应停止。这个过程可以视为未反应核模型,如图 5b所示,反应受扩散机制和反应机制的交替进行[11],反应界面不断向核内延伸,因此过高的温度导致颗粒表面迅速生成氧化铝膜阻止O2与核心接触,反应逐渐停止,同时生成的膜填充了颗粒之间的空隙,阻碍了无机盐的挥发,因此温度高于1 300 ℃时,煅后铝灰的质量减重趋势会略为减小。
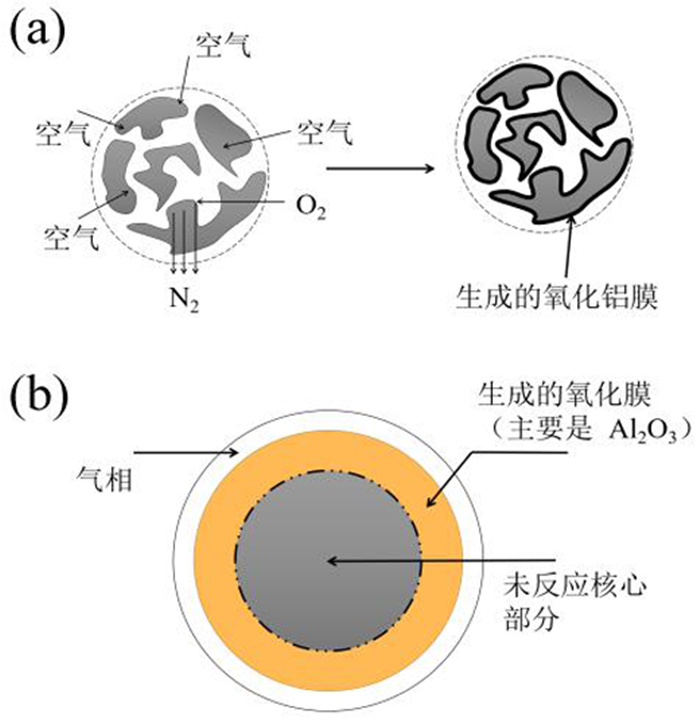 |
| 图 5 (a) 高温焙烧O2和AlN反应机理图; (b)高温焙烧O2和AlN反应模型图 Fig.5 (a)Reaction mechanism diagram of O2 and AlN in high temperature roasting; (b)Model diagram of roasting O2 and AlN reaction |
图 6a为不同温度下煅后铝灰的XRD谱。从图 6a中可以看出,900~1 300 ℃内位于38.4°的Al的特征衍射峰强度完全消失;位于33.256°的AlN特征衍射峰强度逐渐减弱,36.042°的衍射峰消失;25.54°、35.185°、52.546°归属于α-Al2O3的特征衍射峰强度大幅增强,这说明在焙烧过程中AlN,Al转化为α-Al2O3。但在1 400 ℃温度下AlN(33.256°)的特征衍射峰强度是高于1 300 ℃的;α-Al2O3特征衍射峰强度是低于1 300 ℃的,这说明1 400 ℃下AlN的氧化程度低于1 300 ℃,迅速生成的氧化铝膜阻碍了AlN的继续氧化。随着焙烧温度的升高NaCl位于22.736°、31.703°的衍射峰强度明显减弱,表明NaCl在高温下部分挥发;而温度在1 400 ℃时NaCl衍射峰强度均高于1 300 ℃,表明过高的温度下Al的熔化填充了颗粒之间的空隙使得铝灰内部致密化,同时AlN迅速生成的氧化层阻碍了NaCl的挥发。
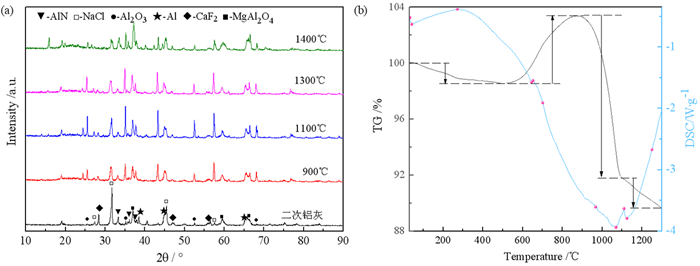 |
| 图 6 (a) 不同温度焙烧后煅后铝灰的XRD谱; (b)二次铝灰的热分析图(TG-DSC) Fig.6 (a)XRD of roasted aluminum dross at different temperatures; (b)Thermal analysis diagram of SAD (TG-DSC) |
二次铝灰高温焙烧过程中的热分析(TG-DSC)结果如图 6b所示,TG曲线显示在30~500 ℃有失重,失重率为1.29%,该过程主要是二次铝灰中结晶水的挥发;500~874 ℃有增重,增重率为4.83%,该过程主要发生氧化反应;温度1 300 ℃时,最终失重14.35%,与前述二次铝灰在1 300 ℃下焙烧后减重11.91%的结果相吻合,主要是无机盐的部分挥发。DSC曲线在42~275 ℃存在一个较大的吸热峰,该温度区间内主要发生了结晶水的挥发;600~650 ℃有一个放热峰,根据热力学计算可知,ΔG(Al的氧化反应)<ΔG(AlN的氧化反应),因此主要是Al的氧化反应;在978~1 110 ℃、1 110~1 235 ℃各存在一个吸热峰,对应的是NaF、NaCl的挥发;在1 050~1 150 ℃存在一个放热峰,对应的是AlN的氧化反应。结合XRD、TG-DSC分析可知Al的氧化主要发生在600~900 ℃,AlN的氧化主要发生在1 100~1 300 ℃。
焙烧温度对铝灰中N、C元素含量的变化如图 7所示,随着焙烧温度的升高,铝灰中N元素逐渐减少,在1 300 ℃时N元素含量达到最少0%;铝灰中C元素随着焙烧温度的升高逐渐减少,在1 400 ℃时含量达到最少0.04%。EA分析结果表明,高温焙烧过程中AlN、Al4C3发生了氧化,进而铝灰中N、C元素含量减少。焙烧温度为1 300 ℃可以实现铝灰脱氮。若焙烧温度高于1 300 ℃,AlN表面生成的氧化膜阻碍反应的进一步进行,因此1 400 ℃煅后铝灰还存在微量N元素。
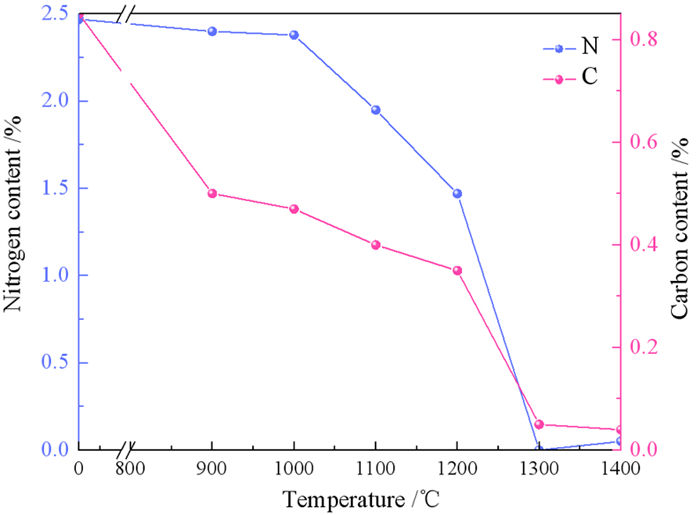 |
| 图 7 焙烧温度对铝灰中N、C元素含量的影响 Fig.7 Effect of roasting temperature on the content of N and C elements in Aluminum dross |
焙烧温度对铝灰反应性的影响如图 8a所示,由于Al、AlN、Al4C3的水解反应是一个自发的放热反应,在反应初期会释放大量热量导致环境温度升高,同时产生的OH-进一步促进水解,因此在10~30 min阶段气体的释放速率最快,反应在60 min后基本达到平衡不再释放出气体。煅后铝灰的反应性随焙烧温度(900~1 300 ℃)的升高逐渐降低,产生气体的速率也逐渐减弱,因此焙烧温度的升高有助于氧化。当温度为1 300 ℃时Al、AlN、Al4C3氧化程度最大,产生的气体量最少,煅后铝灰的反应性最低。当温度为1 400 ℃时,煅后铝灰的内部结块抑制了氧化,产生的气体量较1 300 ℃更多。因此,为了达到二次铝灰除氮的目的,最佳焙烧温度选择1 300 ℃。
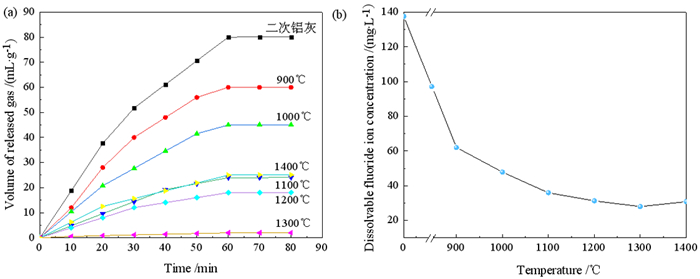 |
| 图 8 (a) 焙烧温度对铝灰反应性和(b)可溶出氟浓度的影响 Fig.8 Influence of roasting temperature on (a)aluminum dross reactivity and (b)soluble fluorine concentration |
焙烧温度对二次铝灰、煅后铝灰中可溶出氟浓度的影响如图 8b所示,可以看出,二次铝灰的可溶出氟浓度为137.55 mg/L,随着焙烧温度的提升,煅后铝灰的可溶出氟离子浓度逐渐降低,从61.99 mg/L(900 ℃)降低到29.93 mg/L(1 300 ℃),这可能是由于可溶出氟化物(NaF)的挥发导致。焙烧温度为1 300 ℃时,煅后铝灰可溶出氟离子浓度最低,为29.93 mg/L。而温度高于1 300 ℃后,煅后铝灰的内部结块抑制了可溶出氟化物的挥发,图 4c中结块表面气孔可以得到印证,因此可溶出氟离子浓度高于1 300 ℃的煅后铝灰。
2.2.3 钙盐对二次铝灰固氟效果的影响为了进一步降低氟离子的溶出,在最佳焙烧温度的条件下研究了CaCl2的加入量对煅后铝灰中可溶出氟离子浓度的影响,如图 9所示,可以看出二次铝灰浸出液中氟离子浓度高达137.55 mg/L,经过焙烧后煅后铝灰的氟离子浓度降低到27.93 mg/L。在加入3%、5%、8%的CaCl2后煅后铝灰中氟离子浓度有明显降低,加入5%的CaCl2后煅后铝灰氟离子最低浓度可达3.02 mg/L。
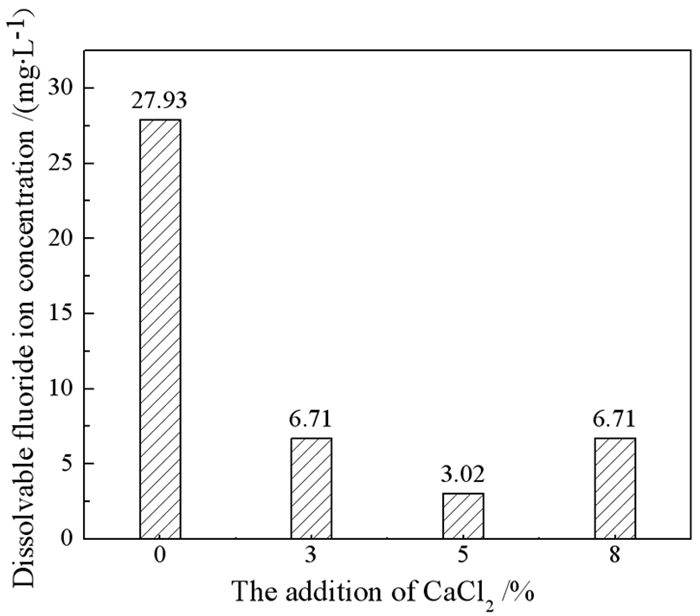 |
| 图 9 CaCl2加入量对二次铝灰可溶出氟浓度的影响 Fig.9 Effect of CaCl2 addition amount on the concentration of soluble fluoride in SAD |
CaCl2的加入量对煅后铝灰质量变化的影响,如图 10a所示,可以看出随着CaCl2加入量的增加,煅后铝灰失重程度先增加后减小。3%的CaCl2加入量煅后铝灰存在最大减重13.44%,主要原因是CaCl2和二次铝灰中氟化钠反应生成了CaF2,未反应的CaCl2、铝灰中NaCl在高温下挥发。加入5%、8%的CaCl2后,煅后铝灰失重程度减小,主要是因为过量的CaCl2未参加反应。考虑到工业中经济性,降低成本节约资源,降低二次铝灰中可溶出氟含量,同时实现二次铝灰的最大减量化,选择加入3%的CaCl2为最佳加料比用以二次铝灰的固氟,此时煅后铝灰可溶出氟离子浓度为6.71 mg/L。
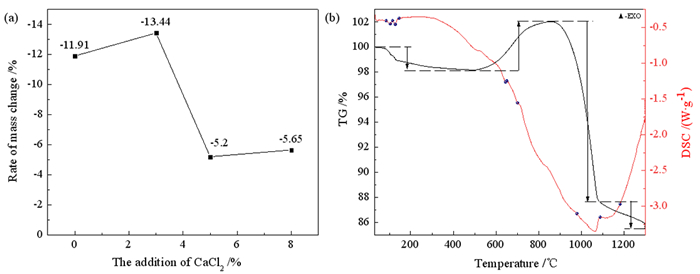 |
| 图 10 (a) CaCl2加入量对煅后铝灰质量变化率的影响; (b)加入3%的CaCl2的二次铝灰热分析图(TG-DSC) Fig.10 (a)Influence of CaCl2 addition on roasted aluminum dross mass change rate; (b)Roasted aluminum dross thermal analysis diagram (TG-DSC) with 3% CaCl2 added |
加入3%的CaCl2的二次铝灰高温焙烧过程中的热分析(TG-DSC)结果如图 10b所示,整个过程与二次铝灰的高温焙烧过程相似,焙烧温度达到1 300 ℃时,最终失重16.61%,与前述加入3%的CaCl2的二次铝灰焙烧减重13.44%结果一致。
加入3%CaCl2、1 300 ℃焙烧后的煅后铝灰经水洗、蒸发浓缩、结晶得到的固体XRD谱如图 11所示,从图 11中可以看出该无机盐主要物相为NaCl,其回收率为84.02%。水洗后残渣主要组分为α-Al2O3。
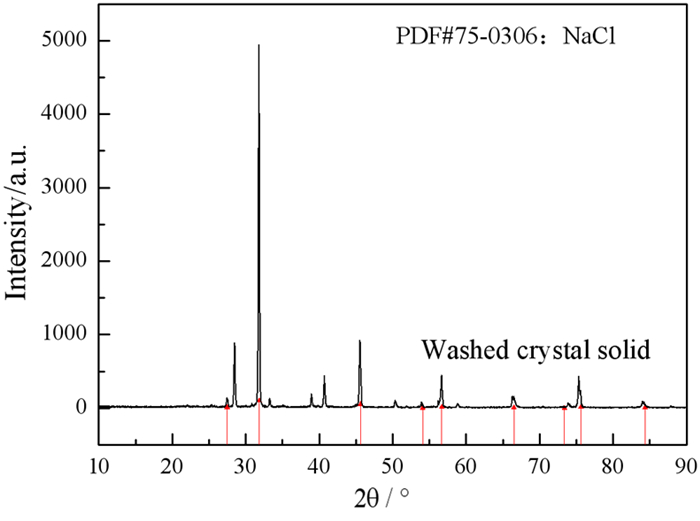 |
| 图 11 水洗结晶固体的XRD谱 Fig.11 XRD of the washed crystal solid |
3 结论
为了脱除二次铝灰中的氮化铝和可溶出氟化物,实现二次铝灰的无害化和减量化,本文采用加入钙盐高温焙烧处理二次铝灰,研究了焙烧温度和加入钙盐的质量对铝灰脱氮固氟效果的影响。结果表明,加入质量分数为3%的CaCl2作为固氟剂、焙烧温度为1 300 ℃、焙烧时间为4 h,在该条件下焙烧后的煅后铝灰氮元素含量降低至0%,气体释放量降低至2 mL/g,可溶出氟离子浓度降低至6.71 mg/L,铝灰减重13.44%。对该条件焙烧后的煅后铝灰进行水洗,回收了剩余的无机盐组分,该组分为NaCl,回收率为84.02%。通过高温焙烧,水洗处理二次铝灰可以实现其氮化物和可溶出氟化物的脱除,最大程度回收无机盐,最终产物为无害化减量化铝灰残渣,其主要成分为α-Al2O3。
| [1] |
SAMSON OLUROPO ADEOSUN, OLATUNDE ISRAEL SEKUNOWO, OMOTAYO OLUWASEYI TAIWO, et al. Physical and mechanical properties of aluminum dross[J]. Advances in Materials, 2014, 3(2): 48-51. |
| [2] |
ABDRAHIM ABDULKADIR, ADESOLA AJAYI, MOHAMED I HASSAN. Evaluating the chemical composition and the molar heat capacities of a white aluminum dross[J]. Energy Procedia, 2015, 75: 2099-2105. DOI:10.1016/j.egypro.2015.07.326 |
| [3] |
MAHINROOSTA MOSTAFA, ALLAHVERDI ALI. Enhanced alumina recovery from secondary aluminum dross for high purity nanostructured γ-alumina powder production: kinetic study[J]. J. Environ Manage, 2018, 212: 278-291. DOI:10.1016/j.jenvman.2018.02.009 |
| [4] |
ARUNABH MESHRAM, KAMALESH KUMAR SINGH. Recovery of valuable products from hazardous aluminum dross: a review[J]. Resources, Conservation & Recycling, 2018, 130: 95-108. |
| [5] |
MIRIAN CHIEKOSHINZATO, RAPHAEL HYPOLITO. Effect of disposal of aluminum recycling waste in soil and water bodies[J]. Environmental Earth Sciences, 2016, 75(7). |
| [6] |
TAKEHITO HIRAKI, TETSUYA NAGASAKA. An easier upgrading process of aluminum dross residue by screening technique[J]. Journal of Material Cycles and Waste Management, 2015, 17(3): 566-573. DOI:10.1007/s10163-014-0283-5 |
| [7] |
邴纯. 铝灰在焙烧中的变化及铝灰返电解槽的试验研究[D]. 沈阳: 东北大学, 2012.
|
| [8] |
张宁燕. 碱法焙烧脱除二次铝灰中的氟、氯元素及铝的回收[J]. 新疆有色金属, 2019, 42(2): 47-49. |
| [9] |
MOSTAFA MAHINROOSTA, ALI ALLAHVERDI. Hazardous aluminum dross characterization and recycling strategies: a critical review[J]. J. Environ Manage, 2018, 223: 452-468. DOI:10.1016/j.jenvman.2018.06.068 |
| [10] |
武正君, 宋良杰. 铝电解过程危险废物的资源化利用技术[J]. 环境科学导刊, 2019, 38(5): 75-78. |
| [11] |
王榕林, 孙加林, 卜景龙, 等. AlN微粉非等温氧化动力学研究[J]. 材料工程, 2011(4): 29-32, 37. |
 2020
2020



