| 重金属离子在改性蛭石表面的竞争吸附及其动力学研究 |
随着我国工业的快速发展和城市化进程加快,越来越多的工业废水和生活污水未经处理就直接排放,导致水环境的重金属污染,重金属废水已成为对环境危害最大的污染物之一。目前,越来越多的处理方法被应用于重金属离子污废水处理工艺,常用的方法有化学净化法、物理净化法和生物净化法,但各有优缺点。自然界普遍存在的天然黏土矿物,具有比表面积大、吸附性能好、储量丰富、处理工艺简单等优点,对污废水中的金属离子具有良好的吸附作用,是目前重金属污废水处理研究的热点[1-2]。
我国蛭石资源丰富,新疆尉犁且干布拉克蛭石矿是我国最大的蛭石矿。蛭石是一种天然的2 : 1型层状硅酸盐黏土矿物,具有很高的阳离子交换容量和吸附性能,可通过离子交换和吸附作用去除水中的重金属离子。研究新型的蛭石净水剂不仅能够降低污水处理成本,而且为蛭石的开发利用开辟了一条新的途径。目前已有蛭石吸附重金属离子方面的相关报道:张莹等[3]在研究中指出,在一定条件下,改性蛭石对汞离子的吸附率最高可达93%;梁洪祥等[4]研究了蛭石对钴离子的吸附作用,他指出在一定的环境下,蛭石对钴离子的吸附率最高可达95%以上;Maria G. da Fonseca等[5]研究了蛭石在溶液中对重金属离子的吸附作用,其研究结果表明,蛭石对不同离子的最佳吸附条件以及达到最大吸附的时间是不同的。本文以改性蛭石为吸附剂,同时研究了Cu2+、Cd2+、Zn2+等重金属离子在蛭石表面的吸附动力学机理以及吸附环境对吸附作用的影响,为蛭石在污废水处理方面提供一些基础数据。
1 试验部分 1.1 仪器与材料TAS-986型原子吸收分光光度计(北京普析通用);GZX-9140MBE数显鼓风干燥箱,上海博讯实业有限公司医疗设备厂;ML-902定时恒温磁力搅拌器,上海浦江分析仪器厂制造;DZKW-S-2电热恒温水浴锅,北京市永光明医疗仪器厂;FA1604电子分析天平,上海天平仪器厂;PHS25A型数值酸度计,上海大中分析仪器厂。
试验所用蛭石产自新疆尉犁,使用前过筛,取20~40目颗粒,粒度为420~840 μm,用蒸馏水洗涤三次,置于烘箱中,在105 ℃温度下烘干,放入干燥器中备用。
CuSO4·5H2O、ZnSO4·7H2O、Cd(NO3)2及其他试剂均为分析纯,水为二次去离子水。Cu2+、Cd2+、Zn2+标准溶液的配制:分别由相应的盐按照常规的方法配制成1 000 mg/L的溶液备用。
1.2 试验方法 1.2.1 蛭石的改性称取一定量备用的蛭石原矿,经900 ℃高温膨胀1 min,用2%的CTMAB溶液在60 ℃水浴中改性搅拌2 h,抽滤后用蒸馏水洗涤3次,置于90 ℃烘箱中烘干,然后将烘箱调温至105 ℃,在此温度下活化2 h,即得到改性的CTMAB-蛭石。经CTMAB改性后的有机蛭石,测得其阳离子交换容量(CEC)为80 mmol/100 g。
1.2.2 蛭石原矿与改性蛭石对金属离子吸附率的比较分别称取0.3 g蛭石原矿和0.3 g改性蛭石于250 mL烧杯中,在相同的条件下,分别加入150 mg/L、pH值为5的重金属溶液50 mL,在室温下搅拌吸附60 min,抽滤、洗涤3次,洗涤液定容至250 mL容量瓶中,用原子吸收法测定洗涤液中重金属离子的浓度,按下式计算重金属离子的吸附率Y(%)和平衡吸附量q(mg/kg):
| $ Y = \left( {{C_0}-C} \right) \times 100\% /{C_0} $ | (1) |
| $ q = \left( {{C_0}-C} \right)V/m $ | (2) |
(1) 式中C0、C分别是吸附前后溶液中重金属离子的浓度(mg·L-1);(2)式中q是平衡吸附量(mg/kg),V是加入的重金属溶液的体积(mL),m是吸附剂的用量(g)。
对所得的试验数据应用二级动力学方程式进行拟合:
| $ C/q = 1/\left( {B \cdot K} \right) + C/B $ | (3) |
式中B是饱和吸附量(mg/kg),C是平衡液中重金属离子浓度(mg/L),K是吸附常数。
1.2.3 进行单因素试验分别考察吸附剂用量、pH值、重金属离子浓度、吸附时间、吸附温度等环境因素对吸附剂吸附率的影响,详见2.2-2.6。
1.2.4 催化剂的表征分别对蛭石改性前后进行了SEM、XRD等表征。
2 结果与分析 2.1 蛭石原矿和改性蛭石吸附率的比较按照1.2.2的试验方法,分别得到了蛭石原矿和改性蛭石对重金属离子的吸附率的变化曲线,结果见图 1。
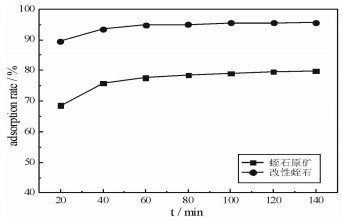 |
| 图 1 蛭石原矿和改性蛭石吸附率的比较 Fig.1 Comparison of adsorption rate of vermiculite and modified vermiculite |
从图 1可以看出,当分别用蛭石原矿和改性蛭石吸附重金属离子时,并在不同时间点取样,测定吸附率。随着吸附时间的增加,蛭石原矿和改性蛭石的吸附率均有所增加,但改性蛭石的吸附率始终高于蛭石原矿,这是因为蛭石原矿经高温膨胀后加大了层间距,又经CTMAB改性后,重金属离子进入层间的概率大大增加,从而实现与层间阳离子交换而被吸附,故改性蛭石吸附率增加;另一方面,根据软硬酸碱理论,由于蛭石表面的单位负电荷较高,使得蛭石晶层表面官能团表现为硬碱,结合软酸Cd2+、Cu2+的能力弱,经CTMAB改性后,层间表面官能团变软,软酸与软碱反应较快速,形成较强键结,与Cd2+、Cu2+的结合能力提高,从而使得改性蛭石吸附率提高。
2.2 改性蛭石用量对吸附率的影响称取0.1、0.2、0.3、0.4和0.5 g改性蛭石分别放入250 mL烧杯中,再分别加入150 mg/L、pH值为5的重金属溶液50 mL,在室温下搅拌吸附60 min,按照1.2.2的方法,抽滤,洗涤,定容,并用原子吸收法测量各烧杯中重金属离子浓度。
由图 2可知,改性蛭石用量在一定的范围内时,重金属溶液中Cu2+、Cd2+、Zn2+的吸附率随着改性蛭石用量的增加而呈现出相似的规律。当改性蛭石用量在0.1~0.5 g时,Cu2+的吸附率从65%增加到90%又降低到86%,Zn2+的吸附率从68%升高到86%又降低到81%,当吸附剂用量为0.3 g时,Cu2+和Zn2+的吸附率均出现峰值;Cd2+的吸附率从70.4%增加到90.4%,当吸附剂用量为0.4 g时,吸附率出现峰值,后随着吸附剂用量增加,吸附率基本保持不变。这是由于当改性蛭石用量增加时,重金属离子的吸附率随着吸附点位的增多而增加。由于溶液中可被吸附的重金属离子的量是一定的,当继续增加改性蛭石用量时,吸附率变化不大,且逐渐趋于平衡[2, 6]。从试验数据得出,当改性蛭石用量为0.3 g时,已经能够满足溶液中重金属离子的吸附,从成本角度出发,试验选择吸附剂用量为0.3 g。
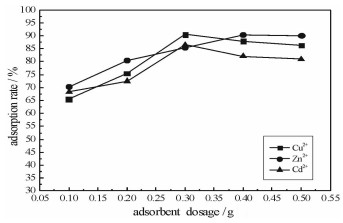 |
| 图 2 吸附剂加入量对重金属离子吸附率(Y)的影响 Fig.2 Effect of adsorbent addition amount on adsorption rate of heavy metal ions |
2.3 pH值对吸附率的影响
称取五份0.3 g改性蛭石于250 mL烧杯中,分别加入pH值为1~8(间隔1个单位pH左右)、浓度为150 mg/L的重金属溶液50 mL,在室温下搅拌吸附60 min后,按照1.2.2的方法,抽滤,洗涤,定容,并用原子吸收法测量各烧杯中重金属离子浓度。
改性蛭石作为吸附剂,其表面电荷在很大程度上取决于溶液的pH值,因此溶液pH值是影响重金属离子吸附率的主要因素。由图 3可以看出,当pH值在1~5的强酸性环境时,随着pH值的增大,Cu2+、Cd2+、Zn2+在改性蛭石表面的吸附率均呈现明显上升趋势,当溶液pH值为5~6的弱酸性环境时,Cu2+、Cd2+、Zn2+在改性蛭石表面的吸附量出现峰值,且基本保持不变。这是由于在溶液的pH值相对较小的情况下,其H+浓度相对较大,H+与重金属离子在蛭石的表层形成竞争吸附,使得重金属离子在改性蛭石表层的吸附率降低;当溶液pH值逐渐增大,一方面,溶液中的H+浓度逐渐降低,使得H+和重金属离子的在改性蛭石表层的竞争吸附能力减弱;另一方面,溶液中的OH-浓度逐渐升高,使得改性蛭石表层与层间的负电荷增多,有利于重金属离子在改性蛭石表面吸附率的提高[7-8]。当溶液pH值大于6,且逐渐升高至中性或弱碱性条件下,溶液开始出现浑浊,这是由于溶液中的重金属离子与OH-发生水解反应,此时水解和吸附作用同时进行,水解产物MOH+(M代表Cu、Cd、Zn)的产生增加了重金属离子的去除率,因此,当应用蛭石吸附重金属离子时,应将溶液pH值控制在5~6。
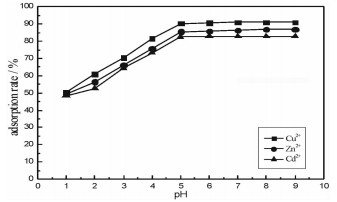 |
| 图 3 pH值对吸附效率的影响 Fig.3 Effect of pH value on adsorption |
2.4 重金属离子初始浓度对吸附量的影响
称取五份0.3 g的改性蛭石于250 mL的烧杯中,分别加入浓度为30、60、90、120、150、180和210 mg/L,pH为5的重金属离子溶液50 mL,在室温下搅拌60 min,按照1.2.2的方法测重金属离子的吸附量。
通过改变重金属离子的初始浓度,研究了重金属离子在改性蛭石表面的吸附量。从图 4可知,初始浓度相同时,改性蛭石对三种金属离子的吸附能力基本相同,随着初始离子浓度的增加,吸附量也逐渐增加。当金属离子的初始浓度从20 mg/L增加到150 mg/L时,吸附剂对Cu2+的吸附量从1 585 mg/kg增加到7 785 mg/kg,对Zn2+的吸附量从1 562 mg/kg增加到7 765 mg/kg,对Cd2+的吸附量从1 558 mg/kg增加到7 208 mg/kg,三种重金属离子的吸附量均有明显增加,这可能是由于随着金属离子浓度的增加,导致溶液本身与矿物表面形成的浓度差越大,使得重金属离子向矿物内部迁移的动力增加,这些重金属离子进入改性蛭石的内部孔道,并被吸附在内壁上,使得大量未经利用的内部吸附点位得到有效利用,因此改性蛭石对三种金属离子的吸附量明显增加,当初始离子浓度为150 mg/L时达到吸附平衡[2, 9],此时改性蛭石对三种金属离子的平衡吸附量顺序为Cu2+>Zn2+>Cd2+。
 |
| 图 4 金属离子初始浓度对吸附量的影响 Fig.4 Effect of original concentration on adsorption |
2.5 吸附时间对吸附效果的影响
称取五份0.3 g的改性蛭石于250 mL的烧杯中,分别加入浓度为150 mg/L、pH值为5的重金属离子溶液50 mL,在室温下搅拌90 min,从第10 min开始,每隔10 min抽样一次,测重金属离子的吸附量。
图 5显示的是改性蛭石对溶液中重金属离子的吸附量随吸附时间变化的情况。从图可知,随着吸附反应时间的延长,改性蛭石对重金属离子的吸附量逐渐增加,且改性蛭石对三种重金属离子吸附量的大小顺序为Cu2+>Zn2+>Cd2+。当吸附反应时间为40 min时,改性蛭石对Cu2+的吸附过程基本达到反应平衡;而对于Zn2+和Cd2+,当吸附反应时间为30 min时,吸附过程就基本达到平衡。当吸附反应达到平衡后,随着反应时间的继续延长,重金属离子的吸附量没有明显增加。总体来说,整个吸附过程可以分为两个阶段,第一阶段是前30 min,为快速反应阶段;第二阶段是30~60 min,为慢速反应阶段,且在该阶段达到反应平衡[10]。综合考虑吸附进行的完全程度和时间成本,本试验选择的吸附时间为60 min。
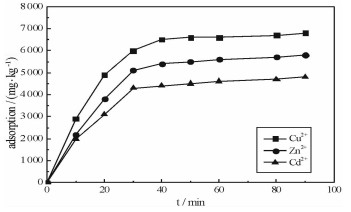 |
| 图 5 反应时间对吸附效果的影响 Fig.5 Effect of contact time on adsorption |
2.6 吸附温度对吸附效果的影响
称取五份0.3 g的改性蛭石于250 mL的烧杯中,分别加入浓度为150 mg/L、pH值为5的重金属离子溶液50 mL,分别在0、10、20、30、40、50、60 ℃下搅拌60 min,按照1.2.2的方法测重金属离子的吸附率。
图 6是吸附反应温度对吸附效果的影响。由图 6可知,在0~60 ℃的温度范围内,随着温度的升高,改性蛭石对重金属离子的吸附率变化不明显,这说明温度不是影响吸附效果的主要因素,同时也证实了试验条件下Cu2+、Zn2+、Cd2+的吸附与反应能量变化无直接关系,且改性蛭石对三种金属离子在相同温度下的吸附率依然是Cu2+>Zn2+>Cd2+。因此,本着节约成本的原则,试验选择室温作为最佳吸附温度。
 |
| 图 6 温度对吸附效果的影响 Fig.6 Effect of temperature on adsorption |
2.7 蛭石改性前后的SEM表征
图 7中的A和B分别是蛭石原矿和负载CTMAB后的照片,从图可以看出,蛭石原矿层间是硅酸盐自身所携带的Na+、Mg2+、Al3+等金属阳离子,由于金属离子体积较小,蛭石的层状结构没有完全被展开,经CTMAB负载后,蛭石的硅酸盐片层间吸附了大量的十六烷基三甲基铵阳离子,且该阳离子体积较大,能够较好的将蛭石的层状结构分散开来,最大限度的增加蛭石的表面积。但是蛭石片层结构吸附的阳离子大部分都只是进入到了层的边缘和表面,并没有进入到蛭石结构深处。这也许是因为蛭石内部层与层之间的相互吸引力较大,所提供的能量尚不能使十六烷基三甲基铵阳离子离子顺利进入到层的中心位置。
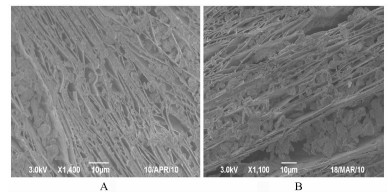 |
| 图 7 蛭石原矿和CTMAB/蛭石的SEM照片 Fig.7 The SEM pattern of vermiculites and CTMAB/vermiculites |
2.8 蛭石改性前后的XRD表征
图 8是蛭石原矿吸附不同负载量CTMAB后的改性蛭石的XRD谱图,图中a、b、c、d分别表示负载量为3%、2%、1%、蛭石原矿。从图可以看出,随着负载量的增加,在衍射角d001为27.50 nm处的蛭石主峰明显变弱,在d001为18.35 nm和45.46 nm处的衍射峰消失,出现了一些新的小峰,整体结构变得比较弥散,也有可能是十六烷基三甲基铵阳离子均匀的分布在载体表面的缘故。
 |
| 图 8 不同负载量的CTMAB/蛭石催化剂的XRD谱图 Fig.8 The XRD pattern of different load quantity of CTMAB/vermiculites |
3 吸附动力学机理初步探讨
当金属离子的浓度一定时,通过改变吸附时间,探讨了金属离子在改性蛭石表面的吸附动力学行为。试验发现,在吸附反应进行的最初10 min内,吸附率即可达到85%以上,在吸附反应进行到30 min时,吸附率达到90%左右,增幅不是很大,说明金属离子在蛭石上的吸附速率开始时较大,接近平衡时吸附速率逐渐降低[11-12]。在金属离子的吸附动力学研究中,二级动力学方程通常被用来拟合试验数据,从而来分析金属离子在吸附剂表面的吸附动力学过程。二级动力学方程的表达式如下:
| $ t/{q_t} = 1/kq_e^2 + \left( {1/{q_e}} \right)t $ | (4) |
式中,qt、qe分别表示t时刻吸附量和平衡吸附量(mg/g),k为吸附速率常数(g·mg-1·min-1)。
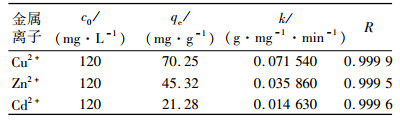
利用t/qt与t作图,分别得到改性蛭石对三种重金属离子的二级动力学方程[13],从方程曲线的斜率可以求出平衡吸附容量qe,从曲线的截距可以求出二级速率常数k。由图可以看出,该二级速率方程较好的描述了改性蛭石对重金属离子的吸附动力学,试验结果能与方程较好吻合。拟合得到的动力学行为参数见表 1,相关系数R达到0.999以上,从拟合结果可以得出,二级动力学模型与重金属离子在改性蛭石表面吸附的试验数据吻合较好,且改性蛭石对三种重金属离子吸附速率大小的顺序为Cu2+>Zn2+>Cd2+,也与试验结果吻合较好,根据截距求出的k值也能表明吸附过程能够在很短的时间内达到平衡,因此,3种重金属离子在改性蛭石上的吸附动力学过程符合二级速率方程。
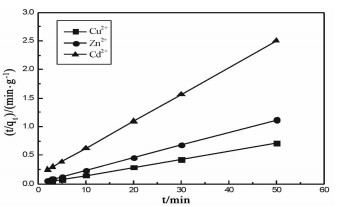 |
| 图 9 蛭石吸附Cu2+、Zn2+、Cd2+的二级动力学模型 Fig.9 Second-order kinetic model for the Cu2+, Zn2+, Cd2+ adsorption on vermiculite |
| 表 1 蛭石吸附Cu2+、Zn2+、Cd2+的二级动力学模型拟合参数 Table 1 Fitting parameters of second-order kinetic model for the Cu2+, Zn2+, Cd2+ adsorption on vermiculite |
 |
蛭石有三种吸附活性中心,分别表述如下:
(1) 结构中的层间阳离子。改性蛭石在被研磨的过程中,存在于晶体结构内部的层间金属阳离子通常被暴露于蛭石表面,使得改性蛭石对金属离子有良好的吸附性和离子交换能力。
(2) Si-O四面体中的O。蛭石内部的Al3+、Fe3+代替了存在于Si-O四面体中的Si4+,导致Si-O四面体中的O2-过剩而带负电,在静电引力的作用下能够对溶液中金属阳离子进行吸附。
(3) 蛭石表层的Si-OH结构。Si-OH结构是由蛭石表层的Si-O-Si结构断键,Si-O-接受一个质子,Si接受一个OH-形成。首先,OH-可与晶体结构中的金属离子发生表面络合反应,对金属阳离子进行吸附。其次,蛭石晶体结构表面有细微的凹坑,且内部有丰富的孔隙,能够形成巨大的表面积,金属离子能够扩散到表面凹坑和孔隙中去,形成物理吸附。
4 结论(1) 蛭石原矿经CTMAB改性后得到有机改性蛭石,优化了蛭石的吸附性能。当吸附剂的用量为0.3 g,pH为5~6,吸附时间60 min,重金属离子浓度120 mg/L,室温条件下,有机蛭石对三种重金属离子的吸附率最高可达93.5%。
(2) 蛭石对重金属的吸附主要是离子交换作用的结果,蛭石对3种重金属离子的吸附顺序为Cu2+> Zn2+> Cd2+,可见吸附行为不仅与蛭石有关,还与金属离子本身有关。
(3) 吸附动力学可用拟二级速率方程来描述,室温下由拟二级速率方程计算得到的平衡吸附量与实测的平衡吸附量吻合甚好,相关系数R达到0.999 9。
(4) 目前研究较多的是对蛭石进行无机盐或有机物改性,改性蛭石吸附能力大大提高,但是改性蛭石经过吸附后,如果处理不当,容易对环境造成二次污染,因此后期的工作应集中在改性蛭石的脱附及回收利用;蛭石作为吸附剂在水处理中的应用目前还处于实验室研究阶段,未见实际工程应用方面的报道,今后应加强这方面的工作。
| [1] |
彭同江, 万朴, 潘兆橹, 等. 新疆尉犁蛭石矿中金云母-蛭石的间层结研究[J]. 岩石矿物学杂志, 1996, 15(3): 250-258. |
| [2] |
谭光群, 李晖, 彭同江. 蛭石对重金属离子吸附作用的研究[J]. 四川大学学报(工程科学版), 2001, 33(5): 58-61. |
| [3] |
张莹, 李洪玲, 肖芙蓉, 等. 改性蛭石对汞离子吸附性能的影响[J]. 石河子大学学报(自然科学版), 2011, 29(5): 613-617. |
| [4] |
梁洪祥, 姚献东. 环境因素对蛭石吸附重金属钴离子的影响及机理[J]. 化学试剂, 2013, 35(6): 551-554. |
| [5] |
Maria G., da Fonseca, Ramon K.S.. Almeida, Luiza N.H. Arakaki, et al. Ver miculite as a useful host for guest cyclic aliphatic amine intercalation, followed by cation adsorption, colloids and surfaces A[J]. Physicochemical and Engineering Aspects, 2006, 280: 1-3, 39. DOI:10.1016/j.colsurfa.2006.01.014 |
| [6] |
陈方明, 陆琦. 非金属矿物材料在废水处理中的应用[J]. 矿产保护与利用, 2004(1): 18-21. |
| [7] |
戴清清, 宋绵新, 张宝述, 等. 溶液pH值对不同粒径蛭石吸附Cu2+、Pb2+的影响[J]. 矿业研究与开发, 2006(3): 56-58. |
| [8] |
吴平霄, 廖宗文, 毛小云. 高表面活性矿物对Zn2+的吸附机理及环境意义[J]. 矿物学报, 2001, 21(3): 335-340. |
| [9] |
方艳, 闵小波, 唐宁, 等. 含锌废水处理技术的研究进展[J]. 工业保护, 2006, 32(7): 5-8. |
| [10] |
李晖, 谭光群, 李瑞. 蛭石对汞的吸附性能研究[J]. 重庆环境科学, 2001, 23(2): 65-67. |
| [11] |
李晖, 谭光群, 彭同江. 蛭石对Cd(Ⅱ)的动态吸附研究[J]. 化学研究与应用, 2000, 12(6): 661-663. |
| [12] |
芦鹏, 吴晓芙, 于旭彪, 等. 固液体系中Cr(Ⅵ)吸附的动态模拟[J]. 中南林业科技大学学报, 2007, 27(1): 118-123. |
| [13] |
于旭彪, 吴晓芙, 芦鹏, 等. 固液体系中蛭石吸附Cu2+动力学研究[J]. 湘潭大学自然科学学报, 2007, 29(2): 85-88. |
 2018
2018 
