| 膨润土纳米片水凝胶的制备及其吸附性能研究 |
随着经济的高速发展,工业废水的排放量不断攀升[1]。含重金属离子的工业废水通过空气、水和土壤对人类的生存环境造成了严重的破坏,并严重威胁人类的身体健康[2-4]。因此,经济、高效的处理重金属离子污染废水已迫在眉睫。目前处理重金属废水较为成熟的方法有化学法、膜分离法、离子交换法、吸附法等[5]。与其他传统废水处理方法相比,吸附法具有操作工艺简单、技术易掌握、对低浓度废水处理效果好等优点,其应用也日益广泛。
膨润土是一种以蒙脱石为主要成分的层状硅酸盐矿物,具有较大的比表面积和孔容、良好的热稳定性和化学稳定性、以及较强的阳离子交换能力。膨润土因具有资源丰富、价格低廉、比表面积大、吸附容量大等特点,被广泛应用于染料和重金属废水处理[6-8]。然而,由于膨润土表面含有亲水硅氧基团,且层间域水合作用会在其表面形成一层水化膜,从而导致其吸附性能降低。
二维纳米吸附材料因具有比表面积大、化学活性强、表面自由能高和吸附容量大等特点,而被认为是一种潜在的高效吸附剂。Peng等人研究发现氧化石墨烯对铅离子表现出了优良的吸附性能,最大饱和吸附量可达790 mg/g[9]。Song等人研究发现MoS2二维纳米片对Cd2+和Hg2+表现出了较强的吸附能力,最大吸附量分别可达477 mg/g和305 mg/g[10, 11]。此外,已有研究发现蒙脱石二维纳米片具有比表面积大、化学活性和电负性强、吸附容量大等特点[12-14]。然而,值得注意的是,由于二维纳米材料尺寸小、分散性好,吸附后固液分离困难是阻碍其广泛应用的瓶颈之一[15]。
水凝胶是在保留了二维纳米材料固有特性的基础上解决二维纳米材料固液分离难题的有效途径之一。水凝胶是一种具有三维网络结构的新型功能材料,具有丰富的亲水性基团、大比表面积、高孔隙率和良好的吸水性等特点,而被广泛应用于工业、生物工程、医药和环保等领域[16]。Wang等人采用一步水热法制备了三聚氰胺改性石墨烯水凝胶,研究发现该3D水凝胶对U(Ⅵ)的最大吸附量可达404.85 mg/g,且脱附再生5次之后U(Ⅵ)的去除率仍可达79.91%,具有良好的循环利用性能[17]。Kang等人采用自组装方法制备了蒙脱石纳米片/壳聚糖水凝胶,研究发现该水凝胶对阳离子有机染料亚甲基蓝的最大吸附量可达530 mg/g[18]。
因此,本研究提出以膨润土为原料,采用机械剥离-离心分离法制备膨润土纳米片,然后以此为原料采用自组装—冷冻干燥法制备膨润土纳米片基水凝胶,并探究所制备水凝胶对铅离子吸附性能。
1 试验 1.1 试验试剂和仪器试验所用的膨润土为钙基膨润土,来自信阳天利膨润土厂,其化学成分为:SiO2 69.26%、Al2O3 18.30%、Fe2O3 2.16%、K2O 2.41%、CaO 1.62%、Na2O 1.06%、烧失量5.19%。本试验研究所用到的主要试剂如表 1,试验仪器如表 2。
| 表 1 试验所用试剂列表 Table 1 Lists of reagents used in the experiments |
 |
| 表 2 试验仪器 Table 2 Lists of instruments and equipments used in the experiments |
 |
1.2 膨润土纳米片基水凝胶的制备
膨润土纳米片悬浊液制备如下:(1)将10 g膨润土粉末缓慢加入到装有200 mL去离子水的烧杯中,以500 r·min-1的转速搅拌20 min;(2)用超声波细胞粉碎仪以40%的功率将混合液超声20 min,得到悬浮液;(3)以1 000 r·min-1的转速将悬浊液离心5 min,取上层液体;(4)接着用高速离心机以10 000 r·min-1的转速离心10 min后,取中间层液体;(5)往液体中加入14 mL去离子水混合均匀,以60 %的功率超声4 min,最后将所得液体放入高速离心机中离心10 min,中间层液体即为膨润土纳米片悬浊液。
膨润土纳米片基水凝胶的制备:(1)量取60 mL去离子水并加热至100 ℃;(2)在500 r·min-1的转速下缓慢加入2 g聚乙烯醇和0.26 g海藻酸钠搅拌2 h;(3)将混合溶液放入80 ℃水浴中,缓慢加入2 g壳聚糖,搅拌6 h,使其完全溶解并冷却至室温;(4)量取40 mL膨润土悬浊液,加入所得溶液中混合均匀;(5)用注射器将混合液滴加至3%氯化钙-饱和硼酸溶液中,交联成3 mm左右的球状凝胶;(6)浸泡12 h后放入冷冻干燥机中干燥24 h后取出,制得膨润土纳米片基水凝胶。
1.3 实验方法及步骤 1.3.1 pH值的影响将质量浓度为50 mg/L的硝酸铅溶液的pH值分别调整为2、3、4、5、5.5,用移液管分别向5个锥形瓶中加入50 mL硝酸铅溶液;随后分别加入0.2 g膨润土水凝胶样品,在温度为25 ℃、转速为150 r·min-1的条件下吸附2 h。在吸附结束后进行取样,取1 mL,用一次性过滤滤头进行过滤,滴入比色管,进行一定倍数的稀释后,用原子吸收分光光度计测量其剩余的铅离子溶液,并计算其吸附量。
1.3.2 吸附时间的影响量取质量浓度为100 mg/L的硝酸铅200 mL,加入到锥形瓶中,称取1.0 g膨润土水凝胶样品加入到锥形瓶中。在温度为25 ℃、转速为150 r/min的条件下,分别在时间为0、5、20、30、75、105、135 min进行取样,对样品进行一定倍数的稀释,用原子吸收分光光度计测量其剩余铅离子浓度,探究吸附时间对吸附量的影响。
1.3.3 吸附浓度的影响配制一系列不同质量浓度的硝酸铅溶液(50、100、200、400、600、1 000 mg/L),分别取50 mL上述溶液于锥形瓶中,放入恒温摇床中。在温度为25 ℃、转速为150 r·min-1的条件下吸附2 h,用5 mL的注射器取1 mL样品于比色管中,在进行一定倍数的稀释后,用原子吸收分光光度计测量其吸附后的铅离子浓度,并计算其吸附量。
吸附量公式(1)如下:
| $ q_{t}=\frac{\left(C_{0}-C_{t}\right) V}{m} $ | (1) |
式中,qt为吸附剂的吸附量,mg/g;C0为吸附剂吸附前的浓度,mg/L;Ct为吸附剂吸附后的剩余浓度,mg/L;V为硝酸铅溶液的体积,L;m为吸附剂的投加量,g。
1.3.4 吸附温度的影响配制50 mg/L的硝酸铅溶液,取50 mL上述溶液于250 mL锥形瓶中,放入恒温摇床中,在转速为150 r·min-1的条件下,在20、30、40 ℃的环境中吸附2 h;用5 mL的注射器取1 mL样品于比色管中,在进行一定倍数的稀释后,用原子吸收分光光度计测量其吸附后的铅离子浓度,并计算其吸附量。
1.4 分析方法(1) XRD表征
将待测量样品进行特定的压片处理,采用X射线衍射仪对样品进行测试。其中辐射源为Cu-Ka X射线(入射光线波长λ=0.154 nm)。仪器扫描角度范围为:5°~60°,步长为0.02°,扫描速率为1°/min。
(2) FT-IR分析
将测量样品研磨成粉状,采用美国赛默飞世尔科技有限公司的Nicolet iS5型傅立叶变换红外光谱仪进行表征分析光谱范围:4 000~400 cm-1,步长为4 cm-1。
(3) SEM分析
将测量样品进行一定的处理,采用德国的Auriga FIB SEM型号的聚焦离子束扫描电镜双数工作站对水凝胶样品进行表征分析。电子束:分辨率:≤1.0 nm@15 kV,≤1.9 nm@1 kV;放大倍率:12×~1000 k×;最低加速电压:≤0.1 kV;离子束:离子束分辨率:≤2.5 nm @30 kV;放大倍率:300×~500 k×;最低加速电压≤1 kV,最高加速电压≥30 kV。
(4) BET测试
称取定量样品利用N2吸附法测定样品的比表面积。凝胶在真空下干燥脱水得到洁净粉末,在-196 ℃下,采用氮气吸附装置(AUTOSORB-I-C,美国Quantachrom公司)进行N2吸附—脱附测定。利用Brunauer-Emmett-Teller(BET)方程计算比表面积,用Barrett-Toyner-Hallenda(BJH)方法测定介孔范围的孔径分布并计算平均孔径、孔体积等。
2 结果与讨论 2.1 膨润土纳米片基水凝胶表征 2.1.1 XRD分析对膨润土和所制备的膨润土纳米片水凝胶采取一定的处理,用XRD衍射仪对其进行分析,如图 3所示。
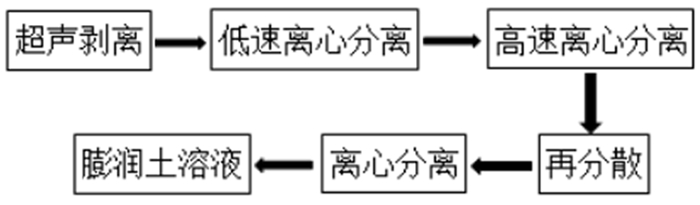 |
| 图 1 膨润土悬浊液制备流程图 Fig.1 Flow chart of the preparation of bentonite suspension liquid |
 |
| 图 2 膨润土纳米片基水凝胶的制备流程图 Fig.2 Flow chart of the preparation process of bentonite nanosheet based hydrogel |
 |
| 图 3 膨润土及其纳米片水凝胶XRD谱图 Fig.3 XRD patterns of bentonite and its nanosheet based hydrogel |
根据布拉格方程(2):
| $ 2 d \sin \theta=n \lambda $ | (2) |
计算出所制备凝胶的结构中的层间距d,其中λ=0.154 nm,得计算结果为d=3.584 nm。
由XRD图谱可知,膨润土的(001)特征峰位于2θ=5.741°附近,计算出d=1.538 nm。膨润土纳米片基水凝胶的(001)特征峰向左偏移且其他特征峰消失,说明膨润土的层间结构遭到破坏,经超声作用后剥离成纳米片结构。凝胶的(001)特征峰位于2θ=2.462°位置处,计算出d=3.584 nm,可知所制备的凝胶属于多孔材料。
2.1.2 红外光谱(FT-IR)分析将凝胶研磨成微细粒粉状,用红外光谱仪对其表面官能团进行分析,所得结果如图 4所示。
 |
| 图 4 膨润土纳米片水凝胶的红外光谱 Fig.4 FT-IR spectrum of bentonite nanosheet based hydrogel |
由图 4可知,样品在3 419 cm-1附近出现了较强的特征峰,该特征峰为-OH的伸缩振动峰,这是由于水被吸附入凝胶中的原因;在2 949 cm-1处出现来自聚乙烯醇或海藻酸钠的C-H伸缩振动峰;在1 635 cm-1处出现特征峰为膨润土的-OH吸收振动峰;在1 427 cm-1处出现了C-H的面内弯曲振动峰;在1 340 cm-1处出现了来自聚乙烯醇的甲基C-H的对称面内弯曲振动峰;在1 035 cm-1出现了C-O的伸缩振动峰。由此可知,膨润土纳米片基水凝胶中保留了膨润土纳米片表面的含氧官能团结构。
2.1.3 形貌分析将膨润土纳米片基水凝胶捏碎,采用扫描电子显微镜(SEM)对其进行形貌分析,其结果如图 5所示。
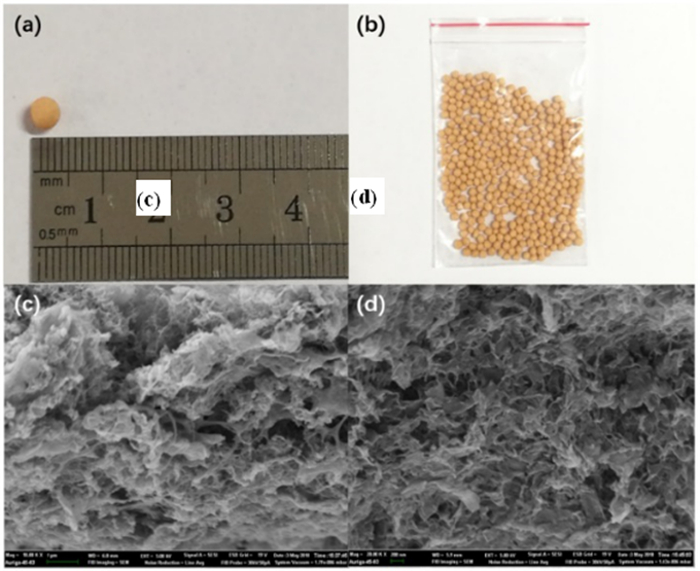 |
| 图 5 膨润土纳米片水凝胶的数码照片(a)和(b),扫描电镜图片(c)和(d) Fig.5 Digital images (a) and (b), and SEM images (c) and (d) of bentonite nanosheet based hydrogel |
由图 5中a和b可知,所制备的凝胶呈均匀的球形,且小球的直径大约为4 mm。由图 5中c和d可知,该凝胶呈片层状结构,且层间具有大量的孔隙,膨润土纳米片均匀地分布在有机试剂形成的骨架网格中。
2.1.4 比表面积测试图 6是膨润土纳米片水凝胶的N2吸脱附等温线。图中吸附等温线是典型的Ⅳ型吸附等温线,具有一个显著的滞后环,属于典型的介孔吸附等温线。这说明该气凝胶内部含有微孔、介孔结构的共存。同时含有微孔及大孔的多层次孔结构材料有利于提升该凝胶的吸附性能。
 |
| 图 6 膨润土纳米片水凝胶的N2吸附-脱附等温线 Fig.6 N2 adsorption-desorption isotherms of bentonite nanosheet based hydrogel |
表 3概括了该凝胶的孔性质。由表可知,该凝胶的比表面积为6.866 5 m2/g,孔体积为0.054 568 cm3/g,平均孔隙直径为31.48 nm。
| 表 3 膨润土纳米片水凝胶的孔性质 Table 3 Pore properties of the bentonite nanosheet based hydrogel |
 |
2.2 膨润土纳米片基水凝胶对铅离子的吸附试验 2.2.1 pH值对凝胶吸附量的影响
pH值对铅离子吸附量的影响主要通过影响铅离子在溶液中的状态和分布以及吸附剂表面功能基团的活性来影响吸附效果。图 7显示了pH值对该凝胶吸附铅离子的影响。
 |
| 图 7 溶液pH值对Pb2+吸附量的影响 Fig.7 Effect of the initial solution pH on the adsorption capacity of Pb2+ |
由图 7可知,当pH值由2.0升高到4.0时,凝胶对铅离子的吸附量由4.96 mg/g增加到9.57 mg/L;当pH值由4.0升高到5.5时,凝胶对铅离子的吸附量下降到8.45 mg/L。产生这种现象的原因是H+和Pb离子之间存在竞争作用。当pH值较低时,溶液中H+浓度较高,H+与膨润土水凝胶中的阳离子的交换概率较高,因此膨润土水凝胶对铅离子的吸附能力较弱。随着pH值的升高,H+的竞争作用减弱,铅离子的容量增加[19]。随着pH值的进一步增大,由于膨润土水凝胶中静电力的存在,铅离子很难置换出凝胶中的阳离子。因此,在一定的范围内,凝胶对铅离子的吸附量先增大后减小。
2.2.2 吸附动力学研究为更好地研究所制备的水凝胶的吸附机理,采用一级动力学模型、二级动力学模型对试验结果进行拟合。
一级动力学模型(3):
| $ q_{t}=q_{e}\left(1-e^{-\alpha_{1} t}\right) $ | (3) |
二级动力学模型(4):
| $ \frac{t}{q_{t}}=\frac{1}{\alpha_{2} q_{e}^{2}}+\frac{t}{q_{e}}=\frac{1}{v_{0}}+\frac{t}{q_{e}} $ | (4) |
上述两式中:qe平衡吸附量,mg/g;qt是t时间的吸附量,mg/g;α1是一级动力学常数,min-1;α2是二级动力学常数,g/(mg·min);v0是初始吸附速率,mg/(g·min);t是吸附时间,min。
由图 8可知,膨润土纳米片基水凝胶对铅离子的吸附量随着吸附时间的增加先迅速上升,之后缓慢增加,最后保持稳定。由于反应开始吸附表面存在大量的吸附位点,所以在0~75 min内吸附速率最大。在100 min左右吸附过程趋于平缓,吸附达到饱和。
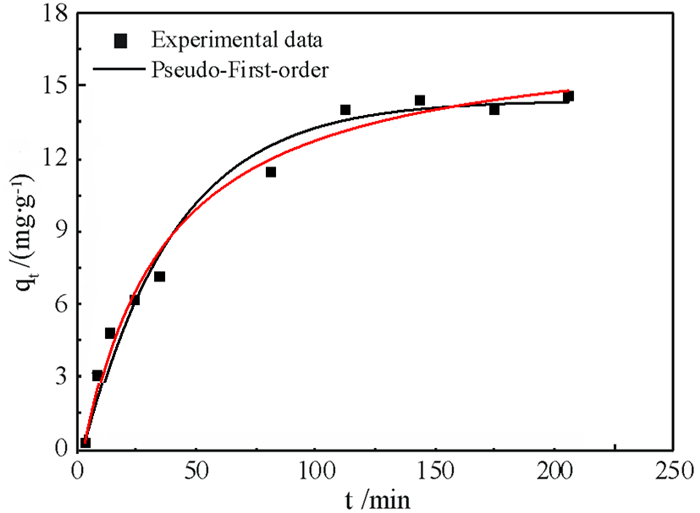 |
| 图 8 凝胶样品吸附铅离子的拟一级、二级动力学拟合曲线 Fig.8 Fitting curves of the pseudo-first- and pseudo -second-order kinetics models for the adsorption of Pb2+ on the bentonite nanosheet based hydrogel |
由表 4可知,与拟一级动力学方程相关性系数相比,膨润土纳米片剂基水凝胶的拟二级动力学相关性系数更高,且拟合出的平衡吸附量qe为16.37 mg/g,与试验测得的吸附量接近。因此,该凝胶对铅离子的吸附过程更好地符合拟二级动力学方程。
| 表 4 凝胶吸附铅离子拟一级和拟二级吸附动力学参数 Table 4 Kinetic parameters of the pseudo-first- and pseudo-second-order adsorption forthe adsorption of Pb2+ on the bentonite nanosheet based hydrogel |
 |
2.2.3 吸附等温线研究
朗格缪尔吸附模型的规律可用朗格缪尔吸附等温式(5)来进行概括:
| $ q_{t}=q_{m} \cdot \frac{b \cdot C}{1+b \cdot C} $ | (5) |
式中:qt是t时刻的吸附量,mg/g;qm是平衡吸附量,mg/g;b是吸附平衡常数,mg/L;C是吸附后铅离子溶液浓度,mg/L。
弗伦德里希经验公式有一点假设:假设吸附过程属于多分子层的吸附。弗伦德里希大量实验的结果进行了归纳,得到以下的经验公式(6):
| $ q=k \cdot C^{1 / n} $ | (6) |
其中:qt是t时刻的吸附量,mg/g;C是吸附后的铅离子浓度,mg/L;k吸附容量,mg/g,n是弗伦德里希平衡参数,表示吸附强度。
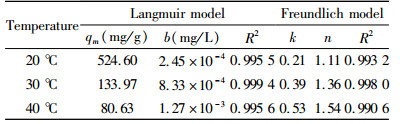
由图 9~图 11和表 5可知,三种温度下Langmuir模型的相关系数R2都大于Freundlich模型的,表明该凝胶对铅离子的吸附等温线过程符合Langmuir模型。Langmuir常数为正值,说明该吸附反应在20、30、40 ℃下都是自发进行的。此外,在Freundlich模型中,1/n都在0~1之间,说明该凝胶吸附铅离子过程比较容易进行。
 |
| 图 9 20 ℃时凝胶样品对铅离子的Langmuir和Freundlich等温吸附线性拟合 Fig.9 Fitting of Langmuir and Freundlich isotherms for Pb2+ on the bentonite nanosheet based hydrogel at 20℃ |
 |
| 图 10 30 ℃时凝胶样品对铅离子的Langmuir和Freundlich等温吸附线性拟合 Fig.10 Fitting of Langmuir and Freundlich isotherms for Pb2+ on the bentonite nanosheet based hydrogel at 30 ℃ |
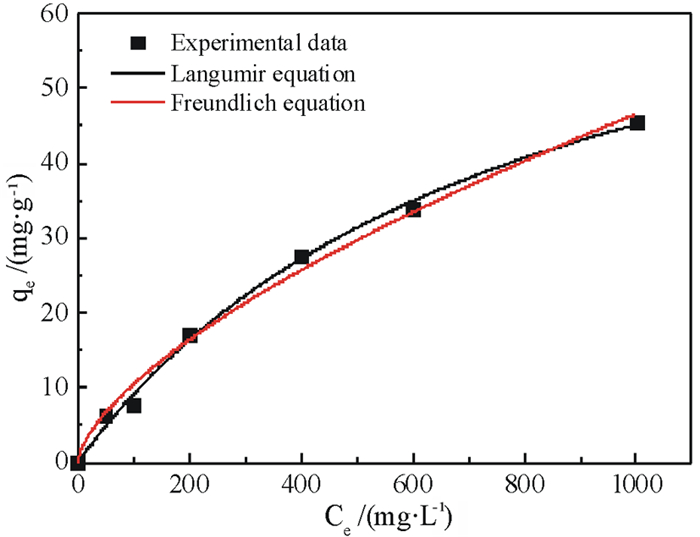 |
| 图 11 40℃时凝胶样品对铅离子的Langmuir和Freundlich等温吸附线性拟合 Fig.11 Fitting of Langmuir and Freundlich isotherms for Pb2+ on the bentonite nanosheet based hydrogel at 40 ℃ |
| 表 5 凝胶对铅离子吸附等温线模型常数及相关参数 Table 5 Adsorption isotherm model constants and related parameters of Pb2+ by the bentonite nanosheet based hydrogel |
 |
2.2.4 温度对吸附量的影响
按照化学平衡理论,对于一个化学反应来说,温度对反应的影响是不可忽略的。对于放热反应,降低温度有利于反应的进行,而吸热反应恰恰相反。通过吸附量公式计算出吸附量q与浓度C的关系如图 12所示。
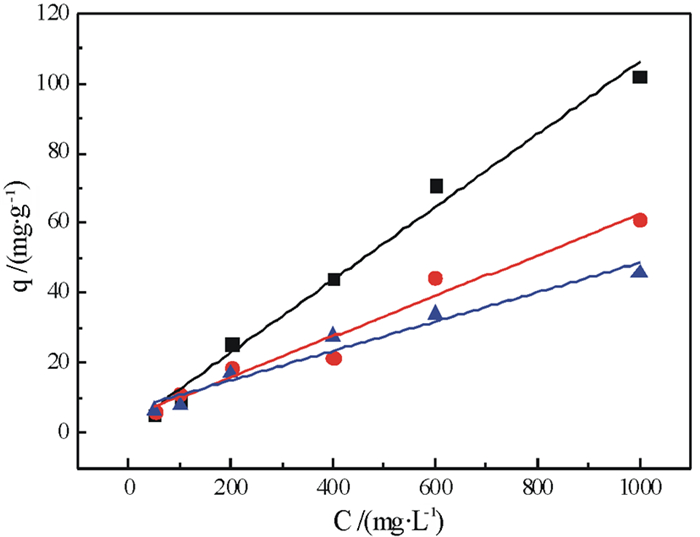 |
| 图 12 温度对膨润土纳米片基水凝胶Pb2+吸附量的影响 Fig.12 Effect of temperature on the adsorption of Pb2+ by the bentonite nanosheet based hydrogel |
由图 12可知,随着温度的增加,膨润土纳米片基水凝胶对铅离子的吸附量降低,可能是由于该吸附过程除了化学吸附外还存在物理吸附,当温度升高时,已被吸附的Pb2+又从凝胶表面脱落下来,导致吸附量降低[20]。对比不同温度下的吸附等温线,发现温度对膨润土水凝胶对铅离子的吸附有较大的影响,温度越低,膨润土纳米片基水凝胶对铅离子的吸附量越大。这说明该凝胶吸附Pb2+是放热反应,提高反应温度不利于吸附反应的进行。
3 结论(1) 经过超声剥离和离心分离获得膨润土纳米片能形成均匀的纳米片基水凝胶,并且所制备的膨润土水凝胶属于微孔和介孔共存材料。通过分析可知膨润土水凝胶中保留了膨润土纳米片表面的含氧官能团结构。
(2) 由吸附试验结果可知,膨润土纳米片基水凝胶吸附铅离子的最佳pH值范围为4~5,吸附过程较好的符合拟二级动力学方程和Langmuir等温吸附模型,且吸附过程比较容易进行。
(3) 温度对膨润土水凝胶对铅离子的吸附量有较大的影响。随着温度的升高,膨润土纳米片基水凝胶对铅离子的吸附量不断降低,说明该吸附过程为放热反应。
| [1] |
沈永昌.中国经济增长与环境污染关系的实证研究[D].蚌埠, 安徽财经大学, 2015.
|
| [2] |
Liu L, Li Y, Liu X, Zhou Z, et al. Chelating stability of an amphoteric chelating polymer flocculant with Cu(Ⅱ), Pb(Ⅱ), Cd(Ⅱ), and Ni(Ⅱ)[J]. Spectrochimica acta. Part A, Molecular and biomolecular spectroscopy, 2014(118): 765-75. |
| [3] |
O'Connell D W, Birkinshaw C, O'Dwyer T F. Heavy metal adsorbents prepared from the modification of cellulose:a review[J]. Bioresource technology, 2008, 99: 6709-24. DOI:10.1016/j.biortech.2008.01.036 |
| [4] |
刘金燕, 刘立华, 薛建荣, 等. 重金属废水吸附处理的研究进展[J]. 环境化学, 2018(37): 2016-2024. |
| [5] |
邵利芬, 杨玉杰, 姚曙光, 等. 含铜电镀废水处理技术研究进展[J]. 工业用水与废水, 2007(3): 13-15, 39. DOI:10.3969/j.issn.1009-2455.2007.03.004 |
| [6] |
王端鑫. 有机膨润土在废水处理中的应用及其进展[J]. 资源节约与环保, 2014(2): 128. |
| [7] |
余丽秀, 邵晨, 朱进, 等. 膨润土开发利用水平评估影响因素探讨[J]. 矿产保护与利用, 2018, 218(6): 26-29, 36. |
| [8] |
郑水林, 孙志明. 非金属矿物材料[M]. 化学工业出版社, 2007.
|
| [9] |
Peng W, Li H, Liu Y, et al. Comparison of Pb(Ⅱ) adsorption onto graphene oxide prepared from natural graphites:Diagramming the Pb(Ⅱ) adsorption sites[J]. Applied surface science, 2016(364): 620-627. |
| [10] |
Wang Q, Yang L, Jia F, et al. Removal of Cd (Ⅱ) from water by using nano-scale molybdenum disulphide sheets as adsorbents[J]. Journal of molecular liquids, 2018, 263: 526-533. DOI:10.1016/j.molliq.2018.04.149 |
| [11] |
Jia F, Wang Q, Wu J, et al. Two-dimensional molybdenum disulfide as a superb adsorbent for removing Hg2+ from water[J]. ACS sustainable chemistry & engineering, 2017(5): 7410-7419. |
| [12] |
Zhang X, Yi H, Bai H Y, et al. Correlation of montmorillonite exfoliation with interlayer cations in the preparation of two-dimensional nanosheets[J]. Rsc Advances, 2017(7): 41471-41478. |
| [13] |
Zhou W J, Guan W J, Lu C. Natural montmorillonite nanosheet colloid-catalyzed hydrogen peroxide ultra-weak chemiluminescence[J]. Rsc advances, 2014(4): 15377-15380. |
| [14] |
Otsu K, Suzuki S, Miyayama M. Anisotropy in lithium ion conduction in laminated thin films of montmorillonite nanosheets[J]. Semiconductor science and technology, 2014(29): 064011. |
| [15] |
Cui L, Wang Y, Gao L, et al. EDTA functionalized magnetic graphene oxide for removal of Pb(Ⅱ), Hg(Ⅱ) and Cu(Ⅱ) in water treatment: Adsorption mechanism and separation property[J]. Chemical engineering journal, 2015, 281: 1-10. DOI:10.1016/j.cej.2015.06.043 |
| [16] |
吴宁梅.新型水凝胶的制备及其对重金属的吸附研究[D].南京, 南京大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10284-1013191634.htm
|
| [17] |
Wang X, Li R, Liu J, et al. Melamine modified graphene hydrogels for the removal of uranium(Ⅵ) from aqueous solution[J]. New journal of chemistry, 2017(41): 10899-10907. |
| [18] |
Kang S C, Zhao Y L, Wang W, et al. Removal of methylene blue from water with montmorillonite nanosheets/chitosan hydrogels as adsorbent[J]. Applied surface science, 2018, 448: 203-211. DOI:10.1016/j.apsusc.2018.04.037 |
| [19] |
李玉洁, 李雨佳, 李红芬, 等. 膨润土负载壳聚糖对水中Cu(Ⅱ)的吸附特性研究[J]. 矿产保护与利用, 2019(39): 84-89. |
| [20] |
邓林.镁铝水滑石基复合材料吸附去除水中铬(Ⅵ)、磷酸盐的研究[D].长沙: 湖南大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10532-1015734180.htm
|
 2019
2019



