| 含铊锌烟灰的选择性浸出研究 |
铊是典型的稀有分散元素,在光导纤维、辐射闪烁器、光学透镜、辐射屏蔽材料、催化剂和超导材料等方面具有潜在应用价值。但由于铊对环境和人体的较大危害性,使得对含铊物料的无害化和资源化处置技术的开发迫在眉睫[1-2]。自然界中铊主要以微量元素形式伴生于方铅矿、黄铁矿、闪锌矿等矿物中[3-4],并伴随着铅锌的冶炼最终主要富集于烟灰中,存在形态包括Tl2O、Tl2SO4、Tl2S,同时烟灰中还含有较高的铅锌。经济高效分离铊和铅锌既可实现铊的集中处置,也可使脱铊后烟灰返回系统进一步回收铅锌,从而提高资源利用率[5-8]。
目前含铊烟灰的回收以湿法工艺为主,包括浸出和分离两个步骤,其中分离包括置换法、萃取法、氯化沉铊法、硫化沉铊法、结晶法等[9-11]。而无论采用哪种分离回收工艺,浸出是必经步骤,主要有水浸、酸性浸出和碱性浸出法。邵传兵等[12]采用高锰酸钾氧化浸出铅冶炼含铊烟尘,获得了92%以上的铊浸出率;林文军等[13]针对高氟氯含铊烟尘,采用碱洗法脱除氟氯铊,经两段碱洗铊的脱除率可达80%左右;成林等[14]研究了碱性氧化—酸浸法从方铅矿中脱铊,获得了83%以上的脱铊率。
为高效经济地从含锌烟尘中脱除铊,本文系统研究比较了水浸、酸浸、碱浸三种工艺从烟灰中选择性浸出铊,以找出铊和锌分离的适宜工艺,并通过硫化沉淀、硫酸浸出和锌板置换制备海绵铊,为含铊烟灰的资源化回收提供完整方案。
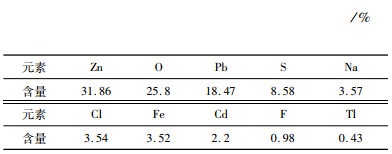
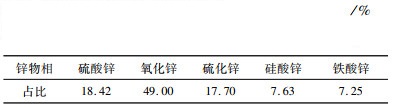
1 试验部分 1.1 试验原料试验所用烟灰取自铅锌渣处理后得到的锌烟灰,其主要成分、SEM和XRD分析分别如表 1、表 2和图 1所示,其中Zn和Tl含量分别为31.86%和0.43%,锌的物相中氧化锌占比为49.00%;XRD检测出的主要物相为硫酸铅和氧化锌,而经EDS能谱比对可以得出颗粒中有针状氧化锌、致密硫酸铅、细小硫酸锌颗粒及含氯、铁、锌、铁的复杂物相颗粒。试验所用试剂包括硫酸、氢氧化钠、硫化钠、锌板和蒸馏水,均为分析纯。
| 表 1 锌烟灰中元素含量 Table 1 Chemical composition of zinc ash |
|
| 表 2 锌烟灰中锌的物相组成形式 Table 2 Chemical phase composition of Zn in Zn -bearing ash |
|
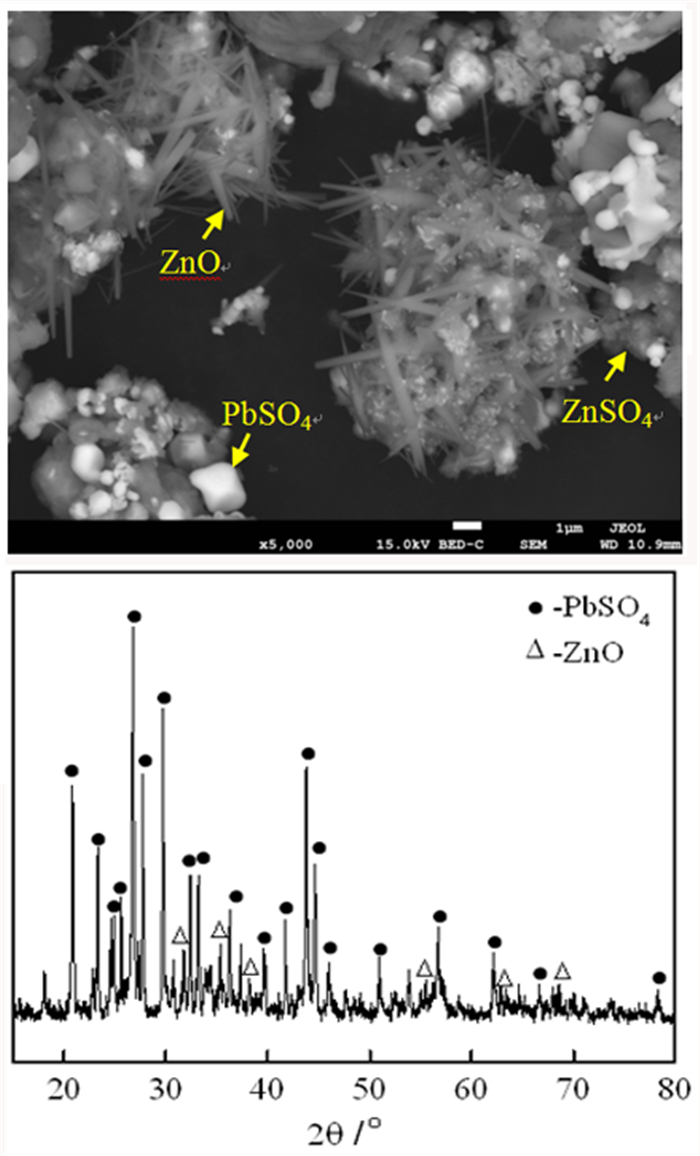 |
| 图 1 锌烟灰的SEM(a)和XRD谱(b) Fig.1 SEM image and XRD pattern of the Zinc ash |
1.2 试验方法
本文以实现锌烟灰中铊的选择性浸出分离为目的,通过对比水浸、酸浸和碱浸等不同浸出体系的浸出效果,确定实现锌铊分离的选择性浸出工艺;在此基础上,以浸出液为原料,通过硫化沉铊实现铊从浸出液中的富集分离,并进一步进行硫酸浸出和锌板置换,最终得到海绵铊,具体过程如下:
(1) 烟灰浸出:试验在磁力恒温水浴锅中进行,每次分别称量一定量蒸馏水、H2SO4、NaOH于1 000 mL烧杯中,并置于水浴锅中升温至设定温度后加入烟灰反应2 h,反应结束后进行真空抽滤分离滤渣和滤液,滤渣烘干取样进行XRD分析,量取滤液体积并分析铊锌含量,根据溶液中铊锌含量计算铊和锌的浸出率。
(2) 海绵铊制备:取1 000 mL浸出液倒入烧杯中,在搅拌条件下加入一定量硫化钠,反应结束后过滤得到滤液和硫化渣,硫化渣烘干后取样分析;取40 g硫化渣加入烧杯中,倒入硫酸,进行浸出反应2 h后过滤得到酸浸液和酸浸渣,液、渣分别取样分析;酸浸液进一步加入锌板进行置换反应,反应结束后剥离分离得到置换后液和海绵铊,分别取样分析。
1.3 试验原理在浸出过程中发生的主要反应如下:
| $ {\rm{T}}{{\rm{l}}_2}{\rm{O}} + {{\rm{H}}_2}{\rm{O}} = 2{\rm{TlOH}} $ | (1) |
| $ {\rm{T}}{{\rm{l}}_2}{\rm{O}} + {{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4} = {\rm{T}}{{\rm{l}}_2}{\rm{S}}{{\rm{O}}_4} + {{\rm{H}}_2}{\rm{O}} $ | (2) |
| $ {\rm{ZnO}} + {{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4} = {\rm{ZnS}}{{\rm{O}}_4} + {{\rm{H}}_2}{\rm{O}} $ | (3) |
| $ {\rm{ZnS}} + {\rm{ F}}{{\rm{e}}_2}{\left( {{\rm{S}}{{\rm{O}}_4}} \right)_3}\; = {\rm{ZnS}}{{\rm{O}}_4} + 2{\rm{FeS}}{{\rm{O}}_4} + {{\rm{S}}^0} $ | (4) |
| $ {\rm{PbO}} + {{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4} = {\rm{PbS}}{{\rm{O}}_4} + {{\rm{H}}_2}{\rm{O}} $ | (5) |
| $ {\rm{T}}{{\rm{l}}_2}{\rm{S}} + 2{\rm{NaOH}} = 2{\rm{TlOH}} + {\rm{N}}{{\rm{a}}_2}{\rm{S}} $ | (6) |
| $ {\rm{ZnO}} + 2{\rm{NaOH}} = {\rm{N}}{{\rm{a}}_2}{\rm{Zn}}{{\rm{O}}_2} + {{\rm{H}}_2}{\rm{O}} $ | (7) |
| $ {\rm{ZnS}}{{\rm{O}}_4} + 2{\rm{NaOH}} = {\rm{Zn}}{\left( {{\rm{OH}}} \right)_2} + {\rm{N}}{{\rm{a}}_2}{\rm{S}}{{\rm{O}}_4} $ | (8) |
图 2为锌和铊不同浓度下的E-pH图[15-16],可以看出铊和锌在酸性和碱性溶液中均存在可溶区和不溶区,而Zn在pH 6~12.3的范围内可以形成Zn(OH)2沉淀,此后转变成可溶的Zn(OH)42-离子;而Tl+在pH 0~13的范围内均可溶,且溶解度较大,在pH≥13后形成TlOH沉淀。因此本文分别考察了水浸、酸浸、碱浸对铊和锌浸出效果的影响,从而找出合适的工艺条件,以实现铊和锌的选择性浸出。
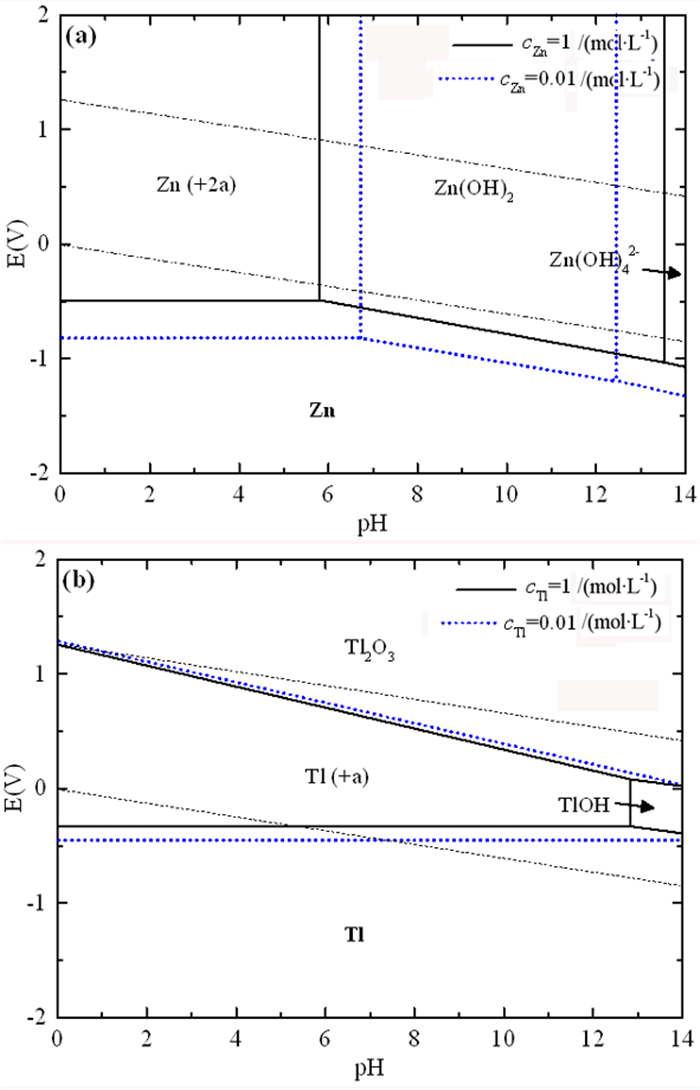 |
| 图 2 锌(a)和铊(b)不同浓度下的电位-pH图 Fig.2 E-pH diagram of the Zn and Tl at different concentration |
在海绵铊的制备过程中发生的主要反应如下,包括Tl在内的重金属离子首先与S2-形成硫化物沉淀而与溶液分离,其后采用硫酸浸出硫化渣得到硫酸盐,最后用锌板置换出铊,从而实现金属铊的生产。
| $ 2{\rm{T}}{{\rm{l}}^ + } + {{\rm{S}}^{2 - }} = {\rm{T}}{{\rm{l}}_2}{\rm{S}} \downarrow $ | (9) |
| $ {\rm{C}}{{\rm{d}}^{2 + }} + {{\rm{S}}^{2 - }} = {\rm{CdS}} \downarrow $ | (10) |
| $ {\rm{P}}{{\rm{b}}^{2 + }} + {{\rm{S}}^{2 - }} = {\rm{PbS}} \downarrow $ | (11) |
| $ {\rm{Z}}{{\rm{n}}^{2 + }} + {{\rm{S}}^{2 - }} = {\rm{ZnS}} \downarrow $ | (12) |
| $ {\rm{T}}{{\rm{l}}_2}{\rm{S}} + {{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4} = {\rm{T}}{{\rm{l}}_2}{\rm{S}}{{\rm{O}}_4} + {{\rm{H}}_2}{\rm{S}} $ | (13) |
| $ {\rm{CdS}} + {{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4} = {\rm{CdS}}{{\rm{O}}_4} + {{\rm{H}}_2}{\rm{S}} $ | (14) |
| $ {\rm{T}}{{\rm{l}}_2}{\rm{S}}{{\rm{O}}_4} + {\rm{Zn}} = {\rm{ZnS}}{{\rm{O}}_4} + 2{\rm{Tl}} $ | (15) |
| $ {\rm{CdS}}{{\rm{O}}_4} + {\rm{Zn}} = {\rm{ZnS}}{{\rm{O}}_4} + {\rm{Cd}} $ | (16) |
固定液固比5:1、反应时间2 h的条件下,改变反应温度,考察反应温度对锌、铊浸出率的影响,结果如图 3所示。从图 3可以看出,温度对烟灰中锌的溶解量影响不大,锌浸出率维持在20%;铊的溶解量随着温度的升高而增加,至70 ℃后铊浸出率维持在78%左右。根据锌物相分析可知,烟灰中硫酸锌物相占总锌的比例约为18.42%,因此水浸时溶解的只是这部分的锌。铊在水中以TlOH形式溶解,其溶解度大,在30 ℃和90 ℃时可达49.9 g和126.1 g[17],因此烟灰中原以氧化物形式存在的铊均可被浸出。可见水浸对铊有一定的效果,但选择性并不好。
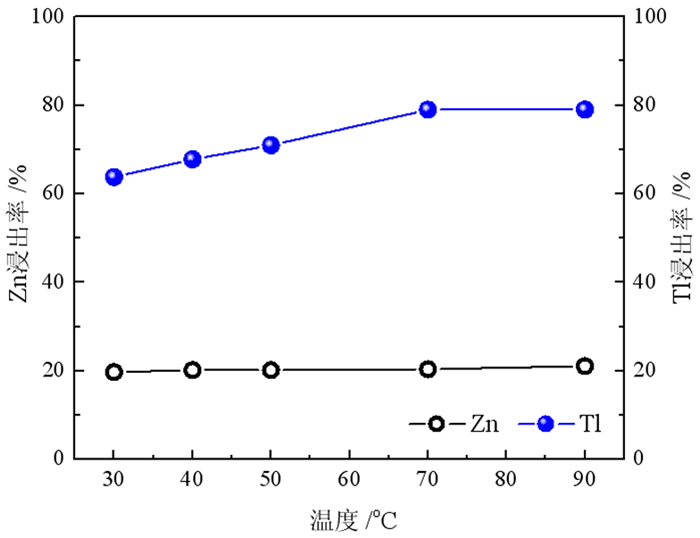 |
| 图 3 水浸温度对锌和铊浸出率的影响 Fig.3 Effect of water leaching temperature on leaching rate of Zn and Tl |
2.2 锌烟灰酸浸 2.2.1 起始硫酸浓度对锌烟灰酸浸的影响
固定反应温度50 ℃、液固比5:1、反应时间2 h,考察起始硫酸浓度对烟灰中锌、铊浸出率的影响,结果如图 4所示。从图 4可以看出,随着硫酸浓度的提高铊的浸出率提升不明显,从10 g·L-1的73%缓慢提高至40 g·L-1的81%,此后几乎不再提高。而锌的浸出率随着硫酸浓度的提高快速提高,从10 g·L-1的20%提高至40 g·L-1的87%,因此为实现选择性浸出,宜将硫酸质量浓度控制在40 g·L-1以下。
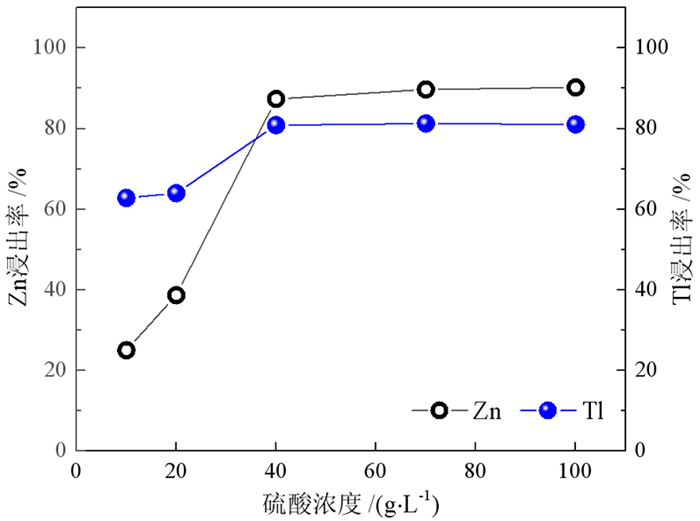 |
| 图 4 硫酸浓度对锌和铊浸出率的影响 Fig.4 Effect of H2SO4 concentration on leaching rate of Zn and Tl |
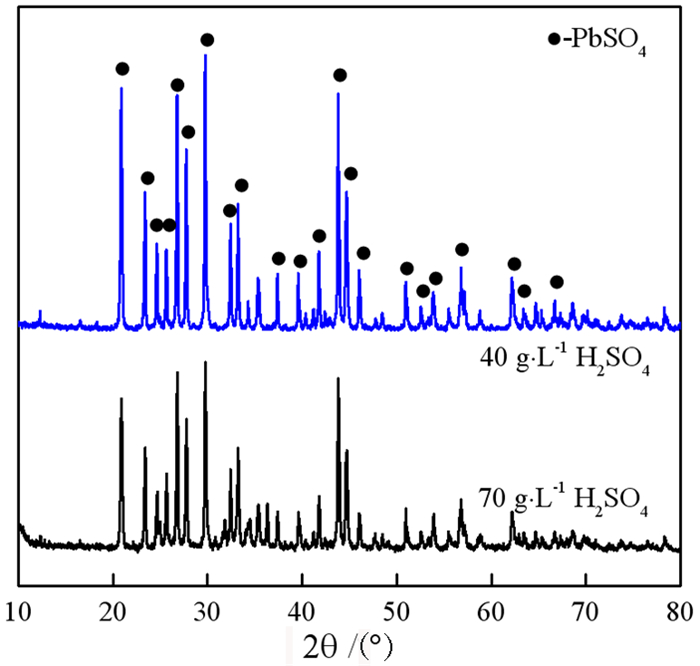 |
| 图 5 不同硫酸浓度下浸出渣的XRD谱 Fig.5 XRD patterns of the leaching residue at different H2SO4 concentration |
进一步对酸浸渣进行了XRD表征,从图中可以看出在起始H2SO4质量浓度分别为40 g·L-1和70 g·L-1的浸出渣主要成分均为PbSO4,对比原料的XRD结果可知ZnO被大量浸出,剩下硫酸铅物相,所以酸浸对锌和铅的分离效果良好。
2.2.2 温度对锌烟灰酸浸的影响固定起始硫酸质量浓度40 g·L-1、液固比5:1、反应时间2 h,考察浸出温度对锌、铊浸出率的影响,结果如图 6所示。可以看出,铊浸出率随温度提高先升高后基本保持不变,当温度大于50 ℃时,铊浸出率高于80%。Tl2SO4在30 ℃和90 ℃时的溶解度分别为6.16 g、14.2 g,因此提高温度有利于铊的浸出。锌浸出率随酸浸温度提高而升高缓慢,在90 ℃时锌浸出率达90%以上,高温提高了难浸锌物相硫化锌和铁酸锌的浸出率。可见,酸性浸出对铊、锌的浸出率都比较高,选择性不好。
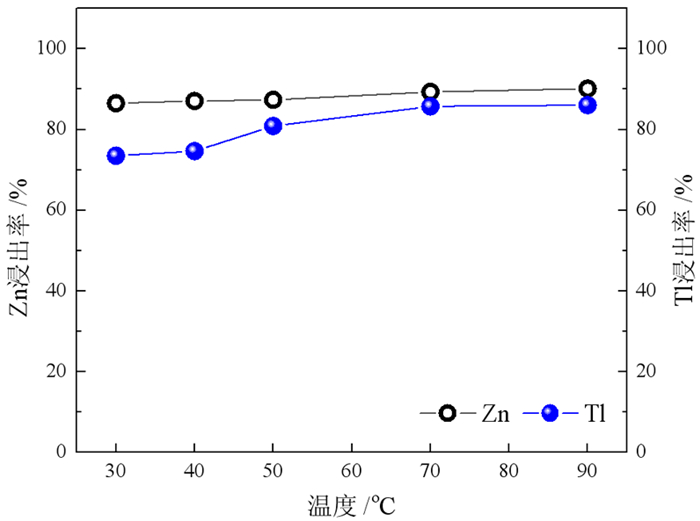 |
| 图 6 硫酸浸出温度对锌和铊浸出率的影响 Fig.6 Effect of H2SO4 leaching temperature on leaching rate of Zn and Tl |
2.3 锌烟灰碱浸 2.3.1 NaOH浓度对锌烟灰碱浸的影响
固定反应温度50 ℃、反应时间2 h,改变NaOH浓度,考察碱度对锌、铊浸出的影响,结果如图 7所示,浸出渣的XRD表征如图 8所示。可以看出,铊浸出率随NaOH浓度增大先提高后基本保持不变,从NaOH质量浓度10 g·L-1时的64%提高至40 g·L-1时的91%,并进一步提高至48 g·L-1时的92%。而锌的浸出率先减小后增加。对比XRD图可知,低碱度时溶液中游离的锌离子形成氢氧化锌沉淀进入渣中,导致溶液中锌离子浓度和浸出率降低,在40 g·L-1和48 g·L-1时锌的浸出率分别为0.99%和1.01%;随着NaOH浓度升高,氢氧化锌或氧化锌发生反应(7)转变为ZnO22-又重新进入溶液中,因此锌的浸出率又有所提高。因此,从铊锌选择性浸出分离和NaOH消耗出发,选择40 g/L NaOH浓度作为后续试验条件。
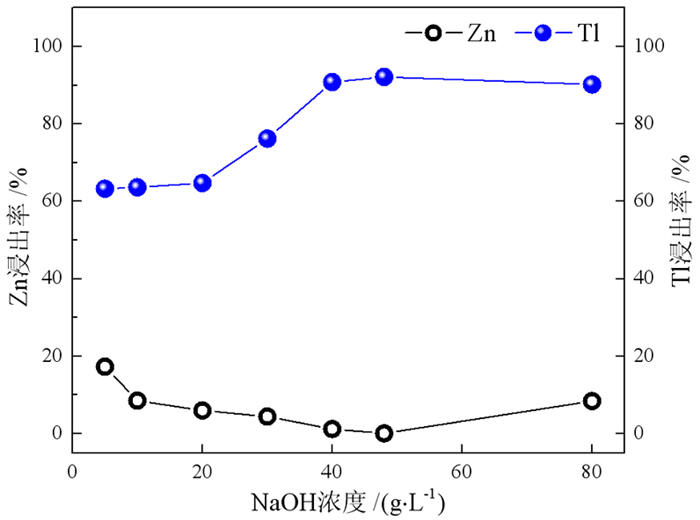 |
| 图 7 NaOH浓度对锌和铊浸出率的影响 Fig.7 Effect of NaOHconcentraton on leaching rate of Zn and Tl |
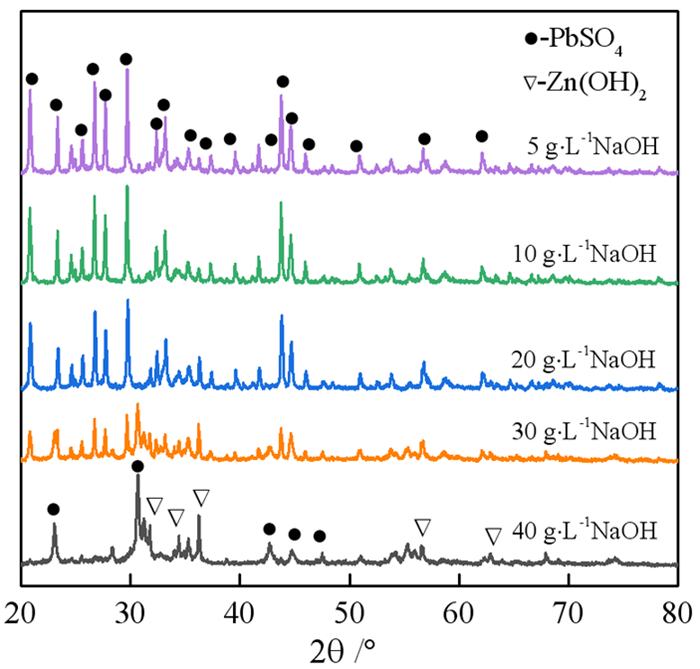 |
| 图 8 不同NaOH浓度下浸出渣的XRD谱 Fig.8 XRD patterns of the leaching residue at different NaOH concentration |
从图 9浸出渣的SEM结果可以看出,浸出渣的形貌变化不大,针棒状颗粒2仍然是以氧化锌为主要成分,原来结晶良好、结构致密的硫酸铅颗粒仍明显存在,但其中硫的摩尔含量低于铅,可能是部分硫酸铅发生了脱硫转化。而从颗粒1成分推测其更接近于锌的氧化物或氢氧化物,说明原硫酸锌物相消失,这与XRD分析结果一致。
 |
| 图 9 40 g·L-1NaOH时浸出渣的SEM图 Fig.9 SEM images of leaching residue at 40 g·L-1 NaOH |
2.3.2 温度对锌烟灰碱浸的影响
固定NaOH质量浓度40 g·L-1、反应时间2 h,改变碱浸温度,得出碱浸温度对锌、铊浸出率的影响如图 10所示。可以看出,铊浸出率随温度提高先升高后不变,当温度大于50 ℃时,铊浸出率大于90%;而锌的浸出率一直维持在较低的水平,处于1%左右,并随碱浸温度升高而略微上升,此时大部分游离锌以Zn(OH)2的形式沉淀,因此在高于50 ℃的条件下可实现铊的最大限度浸出和锌的抑制浸出。
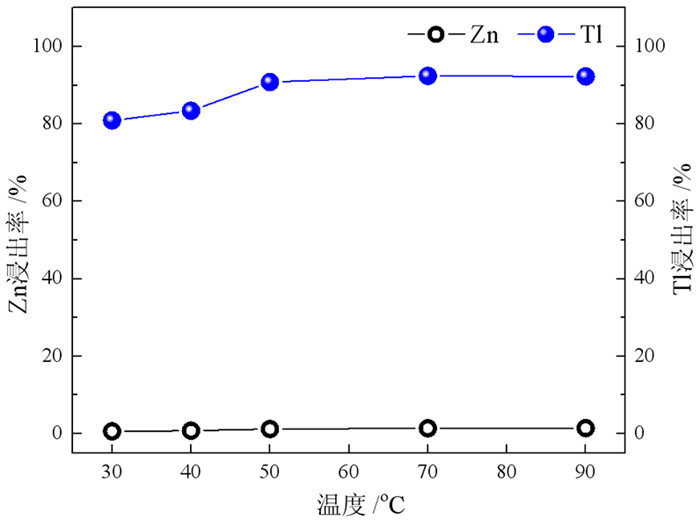 |
| 图 10 NaOH浸出时温度对锌和铊浸出率的影响 Fig.10 Effect of NaOH leaching temperature on leaching rate of Zn and Tl |
综上可见,水浸时铊的浸出率最高可达80%,而锌的浸出率也达20%,考虑到烟灰中锌含量远远高于铊,所以浸出液中锌含量也高于铊,会在硫化过程中大量生成硫化锌,这不利于后续的提铊过程;在酸浸烟灰过程中虽然铊的浸出率有所增加,但锌的浸出率也大幅提高,所以浸出选择性不好;而在碱性浸出时,可以得到高的铊浸出率,而同时锌的浸出率可控制在1%以下,浸出选择性较好,因此选定碱性浸出为含铊烟锌灰的处理工艺,弱碱性的溶液环境也有利于硫化沉铊的进行。
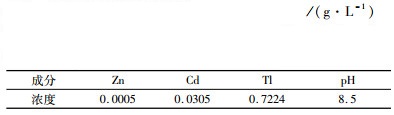
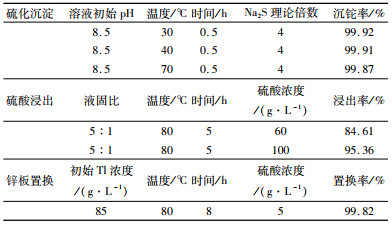
2.4 海绵铊的制备本试验以烟灰碱浸后液为原料制备海绵铊,其主要成分如表 3所示,其中含Tl 0.722 4 g/L、Cd 0.030 5 g/L,经硫化沉淀、硫酸浸出、锌板置换后制得海绵铊。各步骤操作条件及结果如表 4所示。由表 4可以看出,硫化沉淀的初始pH为8.5,为碱性浸出后液的碱度,因此减少了进一步调pH的酸碱消耗,反应温度为30 ℃、Na2S为理论量4倍、搅拌反应0.5 h,平均沉铊率达99.90%;而随着温度升高到70 ℃,沉铊率有下降趋势,因为高温会增加硫化铊溶解度,并促进S2-的水解反应,从而不利于沉铊反应的进行。
| 表 3 选择性碱浸出后液成分 Table 3 Solution composition of the lixivium after selective alkaline leaching |
|
| 表 4 金属铊制备过程条件及结果 Table 4 Process conditions and results of the metallic Tl preparation |
|
其后对硫化渣进行了硫酸浸出,固定液固比5:1、温度80 ℃、时间5 h,在硫酸质量浓度为60 g·L-1时铊的浸出率达84.61%,而当硫酸质量浓度提高到100 g·L-1时,铊浸出率达95.36%,可见在浸出过程中硫酸浓度对铊浸出率影响较大。最后,对浸出液进行了锌板置换,在温度为80 ℃、初始硫酸质量浓度100 g·L-1、初始铊质量浓度85 g·L-1时,反应8 h后铊置换率为99.82%,说明锌板置换铊进行充分。
海绵铊制备过程中硫化渣及浸出渣的XRD如图 11所示。由XRD结果可知,硫化渣中的铊主要以硫化亚铊、氯化亚铊的形式存在,此外还有少量硫酸亚铁等杂质,说明碱性浸出具有良好的选择性,得到了品位达73%的硫化铊渣。酸浸渣中主要成分为硫单质,而未浸出的铊则以氯化亚铊的形式留存渣中,这是因为原烟灰中含氯较高,在碱浸时一部分氯进入溶液与铊结合成氯化铊,并随溶液温度降低而析出进入硫化渣中,其难以被稀硫酸所浸出。
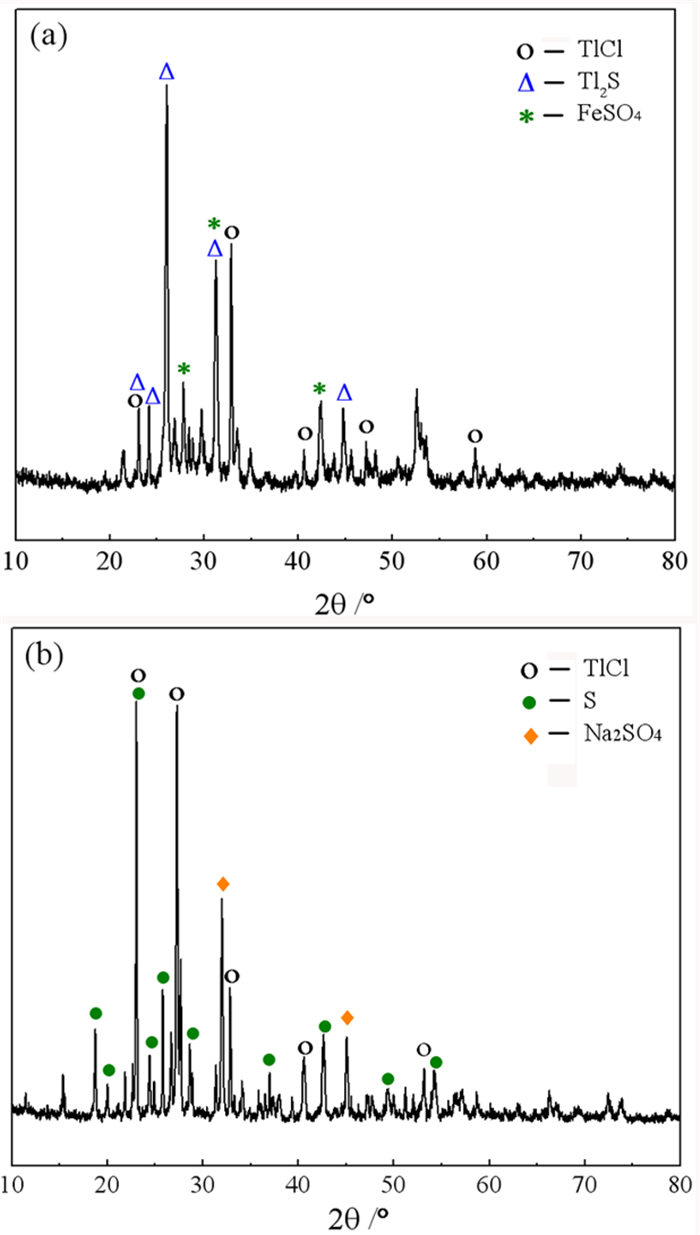 |
| 图 11 硫化渣(a)和酸浸渣(b)的XRD Fig.11 XRD pattern and the sulfide and acidic leachingresidue |
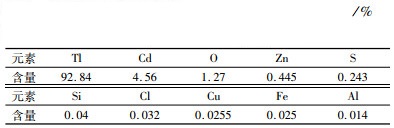
浸出液锌板置换后得到海绵铊,表 5是所得海绵铊的XRF分析结果。由表 5可知海绵铊中的纯度达92.84%,主要杂质为Cd和Zn,含镉较高原因是由于沉铊反应中硫化钠与浸出液中的镉离子生成硫化镉沉淀进入硫化亚铊中,从而被一道浸出和置换进入海绵铊;而锌含量较高是由置换过程中从锌板上刮落所致,该海绵铊经火法或电解精炼后可得精铊产品。
| 表 5 海绵铊元素含量分析 Table 5 Chemical composition of the spongy Tl |
|
3 结论
考察了水浸、酸浸和碱浸工艺对含铊锌烟灰的选择性浸出效果,并进行了金属铊的制备。得出在水浸温度为70 ℃以上时铊浸出率可达78%,酸浸时在硫酸质量浓度40 g/L、酸浸温度70 ℃的条件下铊和锌浸出率分别为79%和85%,水浸和酸浸的选择性均不佳;碱浸时在NaOH为40 g·L-1、温度70 ℃的条件下,铊和锌的浸出率分别为91%和1%左右,具有良好的选择浸出性。所得碱浸后液经硫化沉淀—硫酸浸出—锌板置换后获得海绵铊产品,沉铊率、铊浸出率和置换率分别为99.92%、95.36%和99.82%,所得海绵铊纯度为92.84%,含锌仅为0.45%,起到了良好的锌铊分离效果。新工艺提供了一种含铊烟灰除去和资源化铊的方法,具有高选择性和高富集率的优势。
| [1] |
GALVAN-ARZATE S, SANTAMARIA A. Thallium toxicity[J]. Toxicology Letters, 1998, 99(1): 1-13. DOI:10.1016/S0378-4274(98)00126-X |
| [2] |
BELZILE N, CHEN Y W. Thallium in the environment: acritical review focused on natural waters, soils, sedi-ments and airborne particles[J]. Applied Geochemis-try, 2017, 84: 218-243. DOI:10.1016/j.apgeochem.2017.06.013 |
| [3] |
谭欣, 王中明, 肖巧斌, 等. 银铅无碱混选工艺分选含银低品位铅锌硫化矿石[J]. 矿产保护与利用, 2021(2): 89-98. |
| [4] |
敖顺福. 典型铅锌选矿厂废水零排放工艺对比分析[J]. 矿产保护与利用, 2021(1): 38-44. |
| [5] |
李凯旋, 冷成彪, 任志, 等. 铅锌矿伴生的稀散元素研究进展[J]. 矿物学报, 2021, 41(3): 225-233. |
| [6] |
GENCHI GIUSEPPE, CAROCCI ALESSIA, LAURIA GRAZIANTONIO, et al. Thallium use, toxicity, and detoxification therapy: an overview[J]. Applied Sciences, 2021, 11(18): 1-15. |
| [7] |
陈玲玲, 韩俊伟, 覃文庆, 等. 铅锌冶炼渣综合利用研究进展[J]. 矿产保护与利用, 2021(3): 49-54. |
| [8] |
陈永亨, 谢文彪, 吴颖娟, 等. 中国含铊资源开发与铊环境污染[J]. 深圳大学学报, 2001(1): 57-63. DOI:10.3969/j.issn.1000-2618.2001.01.013 |
| [9] |
林文军, 刘一宁, 赵为上, 等. 氧化锌烟灰的综合回收方法: CN101818254A[P]. 2010-09-01.
|
| [10] |
王雷. 含锌烟灰回收锌的工艺研究[J]. 烧结球团, 2020, 45(3): 67-71. |
| [11] |
徐素鹏, 李晓乐, 汤长青, 等. 用铅锌烟灰和氯碱厂副产盐酸制备纳米氧化锌的清洁工艺[J]. 无机盐工业, 2017, 49(11): 50-53. |
| [12] |
邵传兵, 鲁兴武, 马爱军, 等. 萃取法从含铊烟尘中综合回收稀散金属的研究[J]. 有色金属(冶炼部分), 2014, 4(10): 57-58+63. DOI:10.3969/j.issn.1007-7545.2014.10.014 |
| [13] |
林文军, 王文军, 刘一宁, 等. 综合回收含镉铟高氯氧化锌的试验研究[J]. 湖南有色金属, 2016, 32(5): 24-26+33. DOI:10.3969/j.issn.1003-5540.2016.05.007 |
| [14] |
成林, 田学达, 张小云, 等. 浮选方铅矿精矿中铊的脱除工艺[J]. 中国有色金属学报, 2018, 28(2): 425-433. |
| [15] |
HAIYIN XU, YUANLING LUO, PING WANG, et al. Removal of thallium in water/wastewater: A review[J]. Water Research, 2019, 165: 114981. DOI:10.1016/j.watres.2019.114981 |
| [16] |
YING HUANG, DIYUN CHEN, LINGJUN KONG, et al. Aqueous two-phase systems (polyethylene glycol + ammonia sulfate) for thallium extraction: Optimization of extraction efficiency, structural characterization, and mechanism exploration[J]. Separation and Purification Technology, 2020, 235: 115740. DOI:10.1016/j.seppur.2019.115740 |
| [17] |
周令治, 陈少纯. 稀散金属提取冶金[M]. 北京: 冶金工程出版社, 2008: 109-110.
|
 2021
2021

