| 高磷鲕状赤铁矿深度还原过程中磷灰石还原热力学研究 |
我国鲕状赤铁矿资源丰富,仅在鄂西的探明储量达37.2亿t[1]。该矿具有铁品位低(35%~50%),铁矿物结晶粒度微细且与石英、鲕绿泥石等矿物共生,磷含量高(0.4%~1.8%)等特点[2-3]。采用传统选矿工艺处理鲕状赤铁矿,存在着铁精矿中铁品位低和磷含量偏高的问题。
采用深度还原—磁选技术处理高磷鲕状赤铁矿,可获得铁品位、回收率和金属化率均大于90%的还原铁粉[4]。在此基础上,还原过程中磷的走向得到了相关科研工作者的关注。针对还原过程中磷元素的走向,目前存在着"深度还原—脱磷"和"深度还原—富磷"两种方案[5-6]。围绕"深度还原—脱磷"工艺开展的研究结果表明,在添加大量脱磷剂的条件下,可以阻止磷元素向金属相迁移。而控制还原条件使磷向金属相迁移,经过高磷金属相脱磷,实现磷、铁资源的综合利用也不失为一种可选择工艺。
基于此,本文在热力学分析的基础上,通过模拟计算和试验研究,考察了高磷鲕状赤铁矿中磷灰石的还原行为,以期为"深度还原—脱磷"和"深度还原—富磷"工艺的选择提供参考。
1 试验原料及方法 1.1 试验原料试验用高磷鲕状赤铁矿取自湖北官店,矿石的化学成分分析结果如表 1所示。
| 表 1 高磷鲕状赤铁矿化学成分分析结果 /% Table 1 Chemical compositions of high phosphorus-containing oolitic hematite ore |
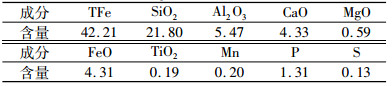 |
由表 1可见,原矿铁品位为42.21%,矿石中有害元素磷含量为1.31%。杂质成分主要为SiO2 21.80%,Al2O3 5.47%和CaO 4.33%,其它杂质元素含量均较低。
为查明高磷鲕状赤铁矿中矿物的存在形式,对其进了XRD分析,结果如图 1所示。由图 1可以看出,矿石中的铁矿物主要为赤铁矿,主要脉石矿物为石英、鲕绿泥石等,磷主要以磷灰石的形式存在。
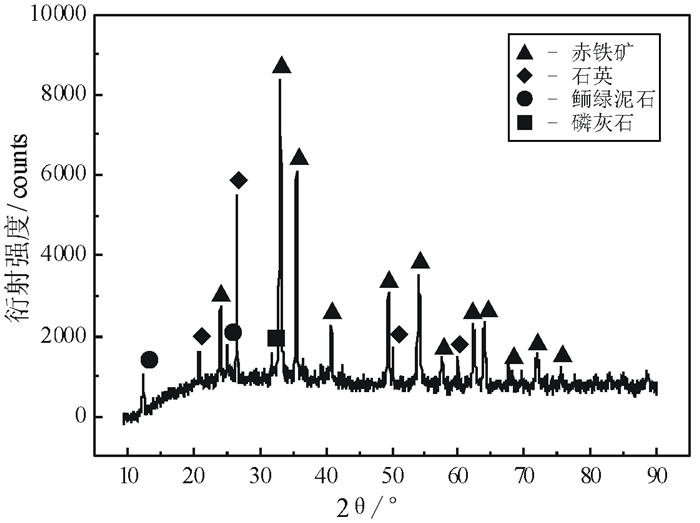 |
| 图 1 高磷鲕状赤铁矿的XRD图谱 Fig.1 XRD spectrum of high phosphorus-containing oolitic hematite ore |
试验所用还原剂为煤粉,其工业分析结果如表 2所示。由表 2可见,煤粉固定碳含量为67.83%;挥发分和灰分含量分别为18.56%和12.09%;磷的含量较低,仅为0.004%。
| 表 2 煤粉工业分析结果 /% Table 2 Proximate compositions of coal |
 |
1.2 试验方法
高磷鲕状赤铁矿深度还原试验在轨道箱式炉中进行。将原矿和按C/O摩尔比(煤粉中固定碳与矿石中铁键合氧的摩尔比)分别为1.0、1.5、2.0或2.5配入的煤粉混匀后装入100 mL的刚玉坩埚中。在混合物料的表面覆盖一薄层煤粉,以保持坩埚内的还原气氛。当炉膛温度升至设定温度(1 473、1 498、1 523或1 548 K)时,将坩埚放入炉膛内,到指定时间取出坩埚进行水淬处理。水淬后得到的还原物料磨细至-0.074 mm粒级含量占85%,取出15 g有代表性的磨矿产品,用XCSG-Φ50型磁选管在磁场强度为107 kA/m的条件下进行磁选。未被还原的磷灰石作为非磁性矿物,将进入磁选尾矿中,故将磁选尾矿(脉石相)称重后化验P2O5含量。磷灰石的还原程度以P2O5的还原度表示,如式(1)所示:
| $ \alpha = 1 - \frac{{m \times {\gamma _s} \times {w_{{{\rm{P}}_2}{{\rm{O}}_5}}}}}{{{m_{{{\rm{P}}_2}{{\rm{O}}_5}}}}} \times 100 $ | (1) |
式中:α—P2O5还原度,%;wP2O5—磁选尾矿中P2O5的含量,%;γS—磁选尾矿与磁选给矿的质量比;m—还原产品的质量,g;mP2O5—每次试验用高磷鲕状赤铁矿中P2O5的质量,g。
2 结果与讨论 2.1 磷灰石还原热力学分析高磷鲕状赤铁矿中磷主要以磷灰石Ca5(PO4)3(F, Cl, OH)形态存在,即Ca3(PO4)2和CaF2、CaCl2及Ca(OH)2形成的复盐。因此在进行热力学计算时,反应物中的磷矿物均以Ca3(PO4)2表示。Matinde等[7]的研究结果显示,当还原温度高于1 273 K时,磷灰石还原得到的还原产物主要以P2的形式存在,因此产生的磷均按P2计算。此外,高磷鲕状赤铁矿作为复杂的矿物体系,在深度还原过程中,磷灰石的还原必然受到SiO2和Al2O3等成分的影响[8]。故依据纯物质热化学数据手册[9],对Ca3(PO4)2、Ca3(PO4)2-SiO2、Ca3(PO4)2-Al2O3和Ca3(PO4)2-SiO2-Al2O3体系最易于发生反应的吉布斯自由能变(ΔrGmθ)进行计算,反应如式(2)~(5)所示。
| $ \begin{array}{l} \;\;\;\;{\rm{C}}{{\rm{a}}_3}{\left( {{\rm{P}}{{\rm{O}}_4}} \right)_2}( {\rm{s}} ) + 5{\rm{C}}\left( {\rm{s}} \right) = \\ 3{\rm{CaO}}\left( {\rm{s}} \right) + 5{\rm{CO}}\left( {\rm{g}} \right) + {{\rm{P}}_2}\left( {\rm{g}} \right) \end{array} $ | (2) |
| $ \begin{array}{l} {\Delta _r}G_{m, 2}^{\rm{ \mathtt{θ} }} = \left[{1732900-994.91\left( {{\rm{T}}/{\rm{K}}} \right)} \right]{\rm{J}} \cdot {\rm{mo}}{{\rm{l}}^{ - 1}}\\ \;\;\;\;\;\;{\rm{C}}{{\rm{a}}_3}{\left( {{\rm{P}}{{\rm{O}}_4}} \right)_{2\left( {\rm{s}} \right)}} + 5{{\rm{C}}_{\left( {\rm{s}} \right)}} + 3{\rm{Si}}{{\rm{O}}_{2\left( {\rm{s}} \right)}} = \\ \;\;\;\;\;\;3{\left( {{\rm{CaO}} \cdot {\rm{Si}}{{\rm{O}}_2}} \right)_{\left( {\rm{s}} \right)}} + 5{\rm{C}}{{\rm{O}}_{\left( {\rm{g}} \right)}} + {{\rm{P}}_{2\left( {\rm{g}} \right)}} \end{array} $ | (3) |
| $ \begin{array}{l} {\Delta _r}G_{m, 3}^{\rm{ \mathtt{θ} }} = \left[{1471960-1002.15\left( {{\rm{T}}/{\rm{K}}} \right)} \right]{\rm{J}} \cdot {\rm{mo}}{{\rm{l}}^{ - 1}}\\ \;\;\;\;\;\;{\rm{C}}{{\rm{a}}_3}{\left( {{\rm{P}}{{\rm{O}}_4}} \right)_{2\left( {\rm{s}} \right)}} + 5{{\rm{C}}_{\left( {\rm{s}} \right)}} + 6{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_{3\left( {\rm{s}} \right)}} = \\ \;\;\;\;\;\;3{\left( {{\rm{CaO}} \cdot 2{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}} \right)_{\left( {\rm{s}} \right)}} + 5{\rm{C}}{{\rm{O}}_{\left( {\rm{g}} \right)}} + {{\rm{P}}_{2\left( {\rm{g}} \right)}} \end{array} $ | (4) |
| $ \begin{array}{l} {\Delta _r}G_{m, 4}^{\rm{ \mathtt{θ} }} = \left[{1582720-1067.74\left( {{\rm{T}}/{\rm{K}}} \right)} \right]{\rm{J}} \cdot {\rm{mo}}{{\rm{l}}^{ - 1}}\\ \;\;\;\;\;\;{\rm{C}}{{\rm{a}}_3}{\left( {{\rm{P}}{{\rm{O}}_4}} \right)_{2\left( {\rm{s}} \right)}} + 5{{\rm{C}}_{\left( {\rm{s}} \right)}} + 6{\rm{Si}}{{\rm{O}}_{2\left( {\rm{s}} \right)}} + 3{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_{3\left( {\rm{s}} \right)}} = \\ \;\;\;\;\;\;3{\left( {{\rm{CaO}} \cdot {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3} \cdot 2{\rm{Si}}{{\rm{O}}_2}} \right)_{\left( {\rm{s}} \right)}} + 5{\rm{C}}{{\rm{O}}_{\left( {\rm{g}} \right)}} + {{\rm{P}}_{2\left( {\rm{g}} \right)}} \end{array} $ | (5) |
| $ {\Delta _r}G_{m, 5}^{\rm{ \mathtt{θ} }} = \left[{1445100-1072.06\left( {{\rm{T}}/{\rm{K}}} \right)} \right]{\rm{J}} \cdot {\rm{mo}}{{\rm{l}}^{ - 1}} $ |
由式(2)~(5)可知,标准状态下,Ca3(PO4)2被碳直接还原的起始温度在1 741 K以上;在SiO2或Al2O3参与反应时,反应温度最低可分别降为1 468 K和1 482 K;当SiO2和Al2O3同时参加反应时,反应温度最低可降至1 373 K以下。上述分析显示,在1 473~1 578 K温度区间,即预定的高磷鲕状赤铁矿深度还原的温度范围内,Ca3(PO4)2有条件发生还原反应。反应趋势最大的是Ca3(PO4)2-SiO2-Al2O3体系被碳还原生成CaO·Al2O3·2SiO2和P2的反应,其次为Ca3(PO4)2-SiO2体系被碳还原生成CaO·SiO2和P2的反应。
2.2 磷灰石还原的模拟计算采用HSC Chemistry 6.0软件对高磷鲕状赤铁矿深度还原过程中反应平衡时Ca3(PO4)2的还原度进行模拟计算。由于深度还原试验是依据煤粉中固定碳含量铁和氧化物中的氧含量,按一定的C/O摩尔比计算煤粉的配入量,因此平衡相模拟过程中考虑了铁氧化物还原消耗还原剂的影响。还原温度介于1 073~1 573 K、C/O为0.5~2.5之间时,Ca3(PO4)2、Ca3(PO4)2-SiO2、Ca3(PO4)2-Al2O3和Ca3(PO4)2-SiO2-Al2O3体系中Ca3(PO4)2还原度的变化如图 2所示。
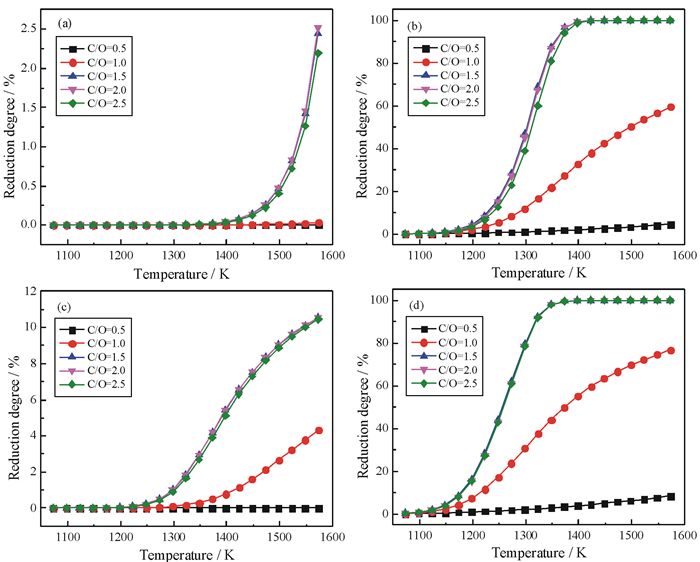 |
| 图 2 Ca3(PO4)2还原度的模拟计算 Fig.2 Analog computation for the reduction degree of Ca3(PO4)2 (a) Ca3(PO4)2;(b) Ca3(PO4)2-SiO2体系;(c) Ca3(PO4)2-Al2O3体系;(d) Ca3(PO4)2-SiO2-Al2O3体系 |
2.2.1 还原温度对模拟结果的影响
由图 2(a)可以看出,模拟温度为1 373 K时,Ca3(PO4)2开始发生还原反应;随着还原温度的升高,Ca3(PO4)2的还原度逐渐增大,但增加幅度很小,至1 573 K时,Ca3(PO4)2的还原度最高仅为2.51%。图 2(b)表明Ca3(PO4)2-SiO2体系中Ca3(PO4)2的起始还原温度为1 148 K,且升高温度导致Ca3(PO4)2的还原度快速增大,当温度高于1 423 K时,Ca3(PO4)2可完全还原。对于Ca3(PO4)2-Al2O3体系(图 2(c)),模拟温度为1 223 K时,Ca3(PO4)2开始发生还原反应,随着还原温度升至1 573 K,Ca3(PO4)2的还原度最高可达10.55%。图 2(d)显示Ca3(PO4)2-SiO2-Al2O3体系中Ca3(PO4)2的还原度的变化趋势与Ca3(PO4)2-SiO2体系类似,自1 123 K起Ca3(PO4)2开始发生还原反应,至1 373 K及以上时,可反应完全。
整体而言,对于四个体系,升高还原温度均有利于增大Ca3(PO4)2的还原度,只是增加幅度有所差别。此外,模拟结果显示四个体系的起始反应温度均低于标准状态下热力学分析得到的Ca3(PO4)2还原反应的起始温度。这可能是因为,模拟过程将P2分压计算在内导致的。
2.2.2 杂质成分对模拟结果的影响为方便对比各杂质成分对Ca3(PO4)2还原的影响,将C/O摩尔比为1.0时,Ca3(PO4)2、Ca3(PO4)2-SiO2、Ca3(PO4)2-Al2O3和Ca3(PO4)2-SiO2-Al2O3体系中Ca3(PO4)2的还原度随温度的变化归纳为图 3。
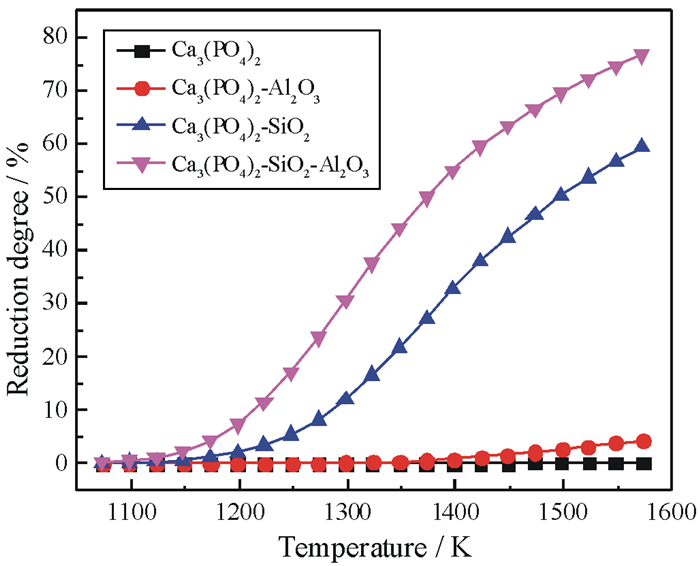 |
| 图 3 SiO2、Al2O3和SiO2-Al2O3对Ca3(PO4)2还原度的影响 Fig.3 Effect of SiO2, Al2O3 and SiO2-Al2O3 on the reduction degree of Ca3(PO4)2 |
由图 3可见,三种成分提高Ca3(PO4)2还原度的能力表现为SiO2-Al2O3 > SiO2 > Al2O3。例如,还原温度为1 523 K时,Ca3(PO4)2、Ca3(PO4)2-Al2O3、Ca3(PO4)2-SiO2和Ca3(PO4)2-SiO2-Al2O3体系中Ca3(PO4)2的还原度分别为0.01%、3.22%、53.63%和72.25%。该模拟结果与热力学分析得到的规律一致。
2.2.3 C/O摩尔比对模拟结果的影响考虑到高磷鲕状赤铁矿石中同时存在着SiO2和Al2O3杂质,为了尽可能接近实际情况,以Ca3(PO4)2-SiO2-Al2O3体系为模拟对象,考察了C/O摩尔比对Ca3(PO4)2还原度的影响,结果如图 4所示。
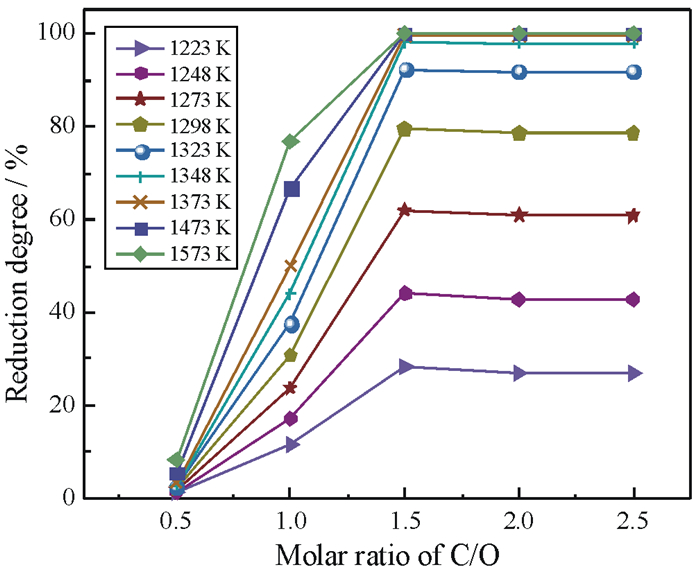 |
| 图 4 C/O摩尔比对Ca3(PO4)2还原度的影响 Fig.4 Effect of C/O molar ratio on the reduction degree of Ca3(PO4)2 |
由图 4可见,随着C/O摩尔比由0.5增大到1.5,Ca3(PO4)2的还原度显著提高。继续增大C/O摩尔比,Ca3(PO4)2的还原度变化不大。以1 323 K为例,当C/O摩尔比由0.5增大到1.5时,Ca3(PO4)2的还原度由2.48%增加至92%,进一步增加C/O摩尔比至2.5,Ca3(PO4)2的还原度并无明显变化。
上述模拟计算结果显示,若想实现磷灰石的充分还原,应保证还原温度高于1 373 K、C/O摩尔比大于1.5。当然,HSC Chemistry 6.0模拟软件不是万能的,缺点在于其只包含了热力学计算而没有考虑动力学因素,以及把反应物质都简化成理想的体系,这就使计算结果与实际情况有误差。因此,有必要对磷灰石的还原行为进行试验研究。
2.3 磷灰石还原试验研究 2.3.1 还原温度对磷灰石还原度的影响在C/O摩尔比1.5、还原时间50 min和还原温度1 473~1 548 K条件下,对高磷鲕状赤铁矿进行深度还原试验。依据式(1),还原温度对磷灰石还原度的影响如图 5所示。
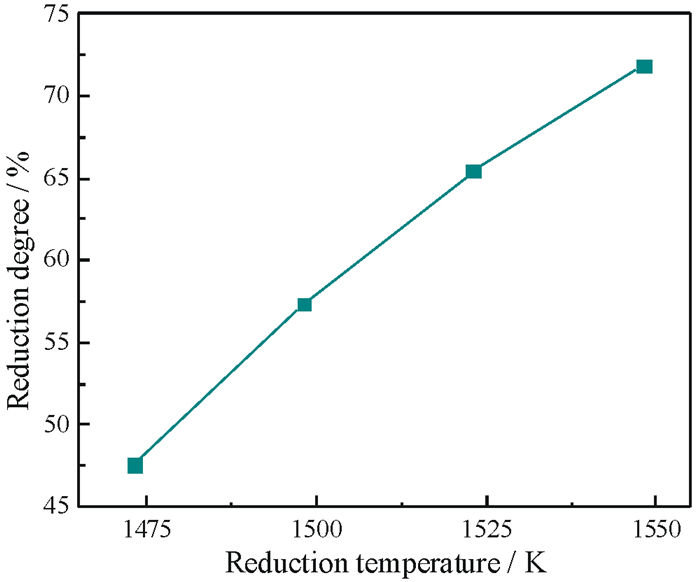 |
| 图 5 还原温度对磷灰石还原度的影响 Fig.5 Effect of reduction temperature on the reduction degree of apatite |
由图 5可见,当还原温度由1 473 K升高到1 548 K,磷灰石的还原度由47.55%增加到71.89%;其中,还原温度由1 473 K增加到1 498 K时,磷灰石还原度增加幅度最大,达9.79%。这是因为磷灰石的还原反应是吸热反应,升高温度有利于反应的正向进行。
2.3.2 还原时间对磷灰石还原度的影响固定还原温度1 548 K、C/O摩尔比1.5,深度还原过程中磷灰石的还原度随还原时间的变化曲线如图 6所示。
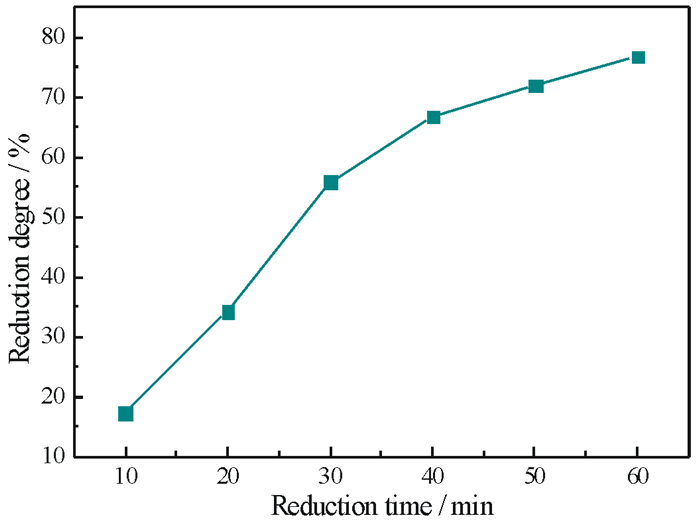 |
| 图 6 还原时间对磷灰石还原度的影响 Fig.6 Effect of reduction time on the reduction degree of apatite |
由图 6可知,延长还原时间有利于提高磷灰石的还原度,特别是还原时间由10 min延长到40 min时,磷灰石的还原度由17.22%增加到66.69%;进一步延长还原至60 min,磷灰石的还原度增加至76.72%,增加幅度有所变缓。可见,为了使磷灰石达到较高的还原度,必须保证足够的还原时间。
2.3.3 C/O摩尔比对磷灰石还原度的影响在还原温度1 548 K、还原时间50 min的条件下,考察了C/O摩尔比对磷灰石还原度的影响,结果如图 7所示。
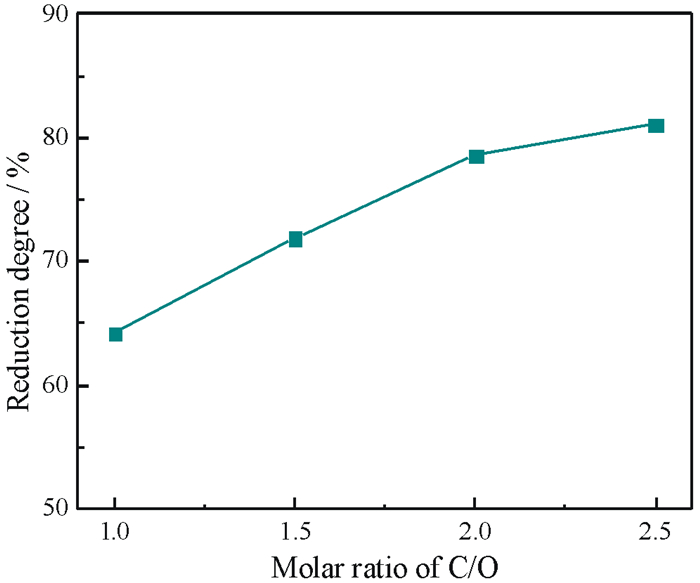 |
| 图 7 C/O摩尔比对磷灰石还原度的影响 Fig.7 Effect of C/O molar ratio on the reduction degree of apatite |
由图 7可以看出,随着C/O摩尔比的增大,磷灰石的还原度呈增加趋势,尤其是C/O摩尔比低于2.0时,磷灰石还原度的增加幅度最为明显。C/O摩尔比由1.0增大到2.0时,磷灰石的还原度由64.16%增加到78.57%,增加幅度为14.41%。继续增大C/O摩尔比至2.5时,磷灰石的还原度为81.06%,增加幅度仅为2.49%。这是因为煤粉作为磷灰石的还原剂,在一定范围内增大C/O摩尔比(即增加还原剂的用量)有利于增加磷灰石与还原剂的接触面积,进而促进反应的进行。而过量的还原剂对增加磷灰石还原度的效果不再明显。
整体而言,磷灰石还原试验确定的不同还原条件下磷灰石的还原度在数值上与模拟计算的结果存在着一定的差别,但与模拟结果显示的升高还原温度、增加C/O摩尔比有利于提高磷灰石的还原度这一趋势是相符的。这表明,模拟计算对磷灰石还原试验具有一定的指导意义,有利于减少试验的工作量。
3 结论(1) 磷灰石还原反应的热力学分析表明,高磷鲕状赤铁矿作为复杂的反应体系,在预定的深度还原温度范围内,矿石中的磷灰石能够发生还原反应。反应趋势最大的是Ca3(PO4)2-SiO2-Al2O3-C反应生成CaO·Al2O3·2SiO2和P2,其次为Ca3(PO4)2-SiO2-C反应生成CaO·SiO2和P2。
(2) 模拟计算结果表明:升高还原温度、增大C/O摩尔有利于增加磷灰石的还原度。杂质成分参与反应同样可以促进磷灰石的还原,三种成分提高Ca3(PO4)2还原度的能力表现为SiO2-Al2O3 > SiO2 > Al2O3。
(3) 磷灰石还原试验确定还原条件显著影响磷灰石的还原度。升高还原温度、增大C/O摩尔比和延长还原时间均有利于增加磷灰石的还原度。在还原温度1 548 K、还原时间50 min、C/O摩尔比2.0的条件下,磷灰石的还原度达到78.57%。模拟计算对磷灰石还原的趋势有一定的预测作用。
| [1] |
Sun Y. S., Han Y. X., Gao P., et al. Distribution behavior of phosphorus in the coal-based reduction of high-phosphorus-content oolitic iron ore[J]. Int. J. Min. Met. Mater., 2014, 21(4): 331-338. DOI:10.1007/s12613-014-0913-x |
| [2] |
Wu J., Wen Z. J., Cen M. J.. Development of technologies for high phosphorus oolitic hematite utilization[J]. Steel Res. Int., 2011, 82(5): 494-500. DOI:10.1002/srin.201100040 |
| [3] |
李英堂, 马驰, 卞孝东, 等. 鄂西高磷鲕状赤铁矿工艺矿物学研究[J]. 矿产保护与利用, 2010(4): 33-37. |
| [4] |
Li K. Q., Ni W., Zhu M., et al. Iron extraction from oolitic iron ore by a deep reduction process[J]. J. Iron Steel Res. Int., 2011, 18: 9-13. DOI:10.1016/S1006-706X(11)60096-4 |
| [5] |
杨大伟, 孙体昌, 杨慧芬, 等. 鄂西高磷鲕状赤铁矿直接还原焙烧同步脱磷机理[J]. 北京科技大学学报, 2010, 32(8): 968-974. |
| [6] |
李国峰, 高鹏, 韩跃新, 等. 高磷鲕状赤铁矿深度还原过程中磷的迁移行为[J]. 金属矿山, 2017(2): 43-47. |
| [7] |
MatindeE., SasakiY., HinoM., 等. Phosphorus gasification from Sewage Sludge during carbothermic reduction[J]. ISIJ Int., 2008, 48(7): 912-917. |
| [8] |
Jacob K., Reynolds D.. Reduction of tricalcium phosphate by carbon:effect of silica and alumina on the reaction[J]. Ind. Eng. Chem. Res., 1928, 20(11): 1204-1210. DOI:10.1021/ie50227a027 |
| [9] |
伊赫桑·巴伦. 纯物质热化学数据手册[M]. 程乃良, 牛四通, 徐桂英, 译. 北京: 科学出版社, 2001.
|
 2018
2018 
