| 偕胺肟螯合树脂中钒的解吸和沉淀回收制备钒酸钡 |
2. 上海交通大学 核科学与技术学院,上海 200240;
3. 广西有色金属及特色材料加工重点试验室,广西 南宁 530004
2. School of Nuclear Science and Engineering, Shanghai Jiao Tong University, Shanghai 200240, China;
3. Guangxi Key Laboratory of Processing for Non-ferrous Metal and Featured Materials, Nanning 530004, China
铝土矿中常伴生镓、钒、钪等稀散元素。在用拜耳法处理铝土矿后,80%~85%的镓、30%的钒进入拜耳母液中[1, 2]。因此,世界上约有90%的镓从拜耳法生产氧化铝的种分母液中提取,在氧化铝生产过程的循环碱性母液中镓、钒得到富集[3]。目前从氧化铝生产循环母液中回收镓的主要方法是采用偕胺肟螯合树脂吸附回收,该树脂选择性强不吸附铝,但对溶液中的钒离子发生共吸附[4-6]。吸附在树脂上的镓可用无机酸(盐酸、硫酸、硝酸)淋洗洗脱得到富镓溶液[7],但树脂上的钒离子难以解吸,势必导致树脂重复使用时对镓的吸附能力下降, 降低树脂寿命。因此,综合回收钒不仅降低钒在富集过程中对树脂的影响,提高树脂的寿命,还可以增加钒的相关产品的附加值。我国提钒的工艺技术水平仍较低,废弃物较多,环境污染较为严重;其次伴生矿或元素利用较低,钒资源综合利用程度较低[8]。目前市场上主要用沉淀法综合回收钒,但反应温度高(90 ℃),回收率低(45.34%)[9]。为此,以吸钒后的偕胺肟螯合树脂为研究对象,研究树脂中钒的解吸方法,并针对解吸液中的钒离子进行沉淀回收制备钒酸钡产品,为镓、钒的分离及回收工艺研究提供更简便、环保、综合利用率更高的技术方法,并且综合回收的钒酸钡产品可作为可调谐激光晶体的基质材料和特种陶瓷基体材料[10-13]。
1 试验原液、药剂及方法 1.1 试验原液及药剂试验所用溶液为模拟配制工业生产氧化铝循环母液,根据其中钒离子浓度配制模拟溶液,得到钒浓度为200 μg/mL、氢氧化钠浓度为1 mol/L的溶液。取室温下吸附钒的树脂为试验研究对象,试验所用树脂为含水量为45%的偕胺肟螯合树脂,其功能基团为氨基和肟基。氢氧化钠、氨水、盐酸、硫酸、硝酸、氧化钡、氧化钙等为分析纯试剂。
1.2 试验方法钒的解吸及沉淀均为静态试验,将一定量树脂与解吸液或沉淀药剂放在离心管中在一定的条件下进行解吸与沉淀。计算相应的解吸率及沉淀率。采用电感耦合等离子体原子发射光谱仪(ICP-AES: Shimadzu, ICPS-7510)测定反应后经过预处理的溶液中离子浓度。采用傅里叶变换红外光谱(FT-IR, Bruker Vertex 70)对树脂表面官能团进行了表征,其表征方法为样品以1:100的比例与溴化钾混合,进一步充分研磨并压制成薄片,在波长400~4 000 cm-1范围内收集红外光谱。
2 试验结果及讨论 2.1 解吸剂种类的影响为探究不同解吸剂在不用浓度及不同温度下对钒离子解吸效果的影响,试验采用不同的碱性及酸性解吸剂[氢氧化钠(NaOH)、氨水(NH3·H2O)、盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)]对吸附钒的树脂进行4组解吸试验,解吸时间均为60 min。第1组解吸剂浓度均为1.5 mol/L,解吸温度为25 ℃;第2组解吸剂浓度均为10 mol/L,解吸温度为25 ℃;第3组解吸剂浓度均为1.5 mol/L,解吸温度为60 ℃;第4组解吸剂浓度均为10 mol/L,解吸温度为60 ℃。解吸试验结果如图 1所示,解吸后树脂的红外谱图如图 2所示。
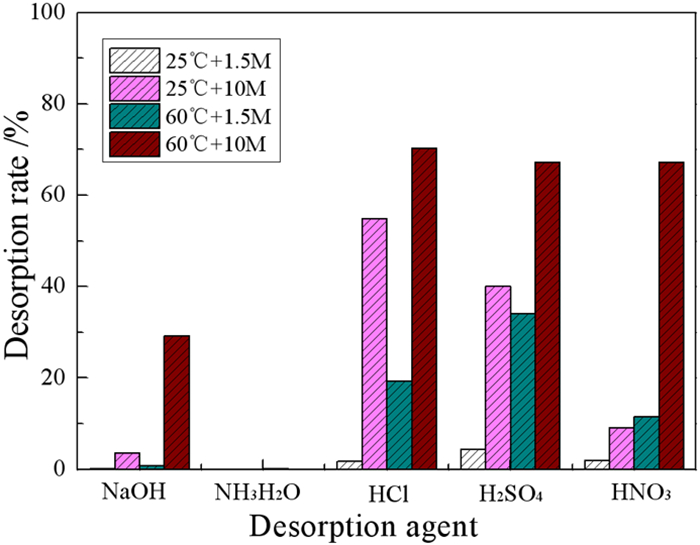 |
| 图 1 解吸剂种类对钒解吸率的影响 Fig.1 Effect of desorption agent on desorption rate of V |
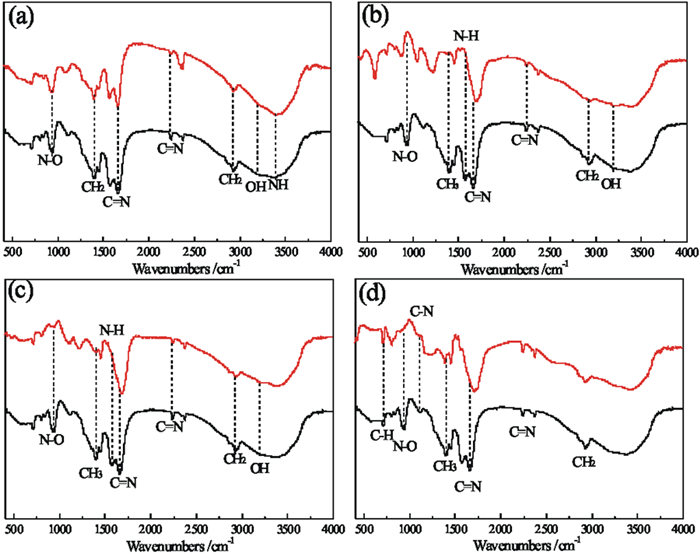 |
| 图 2 树脂傅里叶红外光谱图:(a)NaOH、(b)HCl、(c)H2SO4、(d)HNO3 Fig.2 FT-IR of resin: (a) NaOH, (b) HCl, (c) H2SO4, (d) HNO3 —before adsorption (a)—after elution by 10 mol/L NaoH (b)—after elution by 10 mol/L HCl (c)—after elution by 10 mol/L HNO3 (d)—after elution by 10 mol/L H2SO4 |
由图 1中可以看出:低浓度的解吸剂对钒离子的解吸率非常低;高浓度酸性解吸剂在60 ℃时对钒离子的解吸效果显著提高,其中盐酸解吸率达到60.77%,硫酸解吸率达到70.44%,硝酸解吸率达到67.22%;10 mol/L氢氧化钠在温度为60 ℃下对钒离子有一定的解吸效果,解吸率为29%;氨水对钒离子的解吸率几乎为零。不同的解吸剂随着浓度的增大以及反应温度的提高,其解吸率都逐渐增大。
根据文献资料[6]可知,偕胺肟螯合树脂起吸附作用的活性基团为C=NOH和C-NH2。从图 2(a)可看出树脂经氢氧化钠解吸后无明显特征峰变化,说明树脂中钒离子得到有效解吸且树脂未被破坏;从图 2(b)可以看出处在590 cm-1处出现新的峰,原本分别处于945 cm-1和1 119 cm-1的N-O和C=N峰发生了严重偏移并在1 218 cm-1处生成了新的峰,此外处于1 401 cm-1和1 565 cm-1处的CH3和NH峰消失,说明树脂遭到了破坏;从图 2(c)可以看出处于937 cm-1的N-O峰和处于1 401 cm-1的CH3被削弱,在1 218 cm-1处生成了新的峰,处于1 565 cm-1处的NH峰已经消失;从图 2(d)可以看出处于721 cm-1处的CH峰得到加强,分别处于945 cm-1和1 119 cm-1的N-O和C-N峰消失,处于1 401 cm-1的CH3偏移并被削弱,其相临峰得到加强。由此说明,10 mol/L强酸溶液会破坏树脂官能团,降低树脂寿命。因此选择了对钒有一定解吸能力却又不破坏树脂结构的氢氧化钠作为解吸剂。
2.2 氢氧化钠浓度的影响为探究不用浓度的氢氧化钠对钒离子解吸效果的影响。制备12 mol/L的氢氧化钠溶液,将其稀释为试验所需的不同浓度的解吸液。试验中解吸时间为1 h,解吸温度为50 ℃,振动速率为160 r/min。氢氧化钠浓度的影响试验结果如图 3所示。
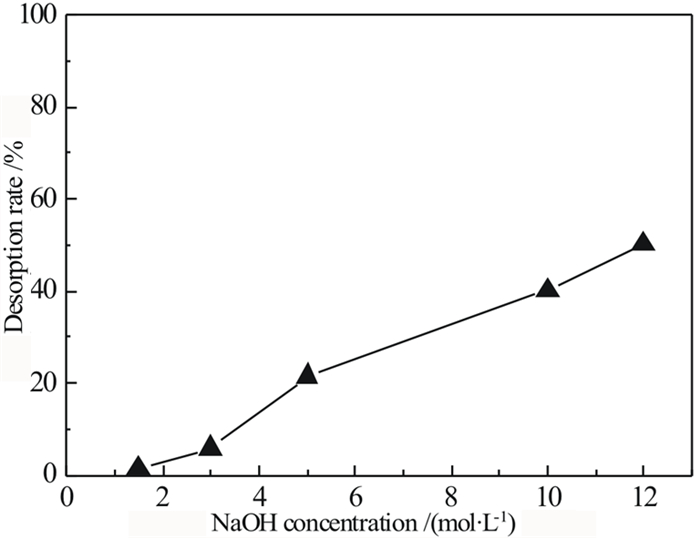 |
| 图 3 NaOH浓度对钒解吸率的影响 Fig.3 Effect of NaOH concentration on desorption rate of V |
从图 3可知,随着氢氧化钠浓度的增大,钒的解吸率明显的增大,这可能是因为解吸反应需要OH-的参与,说明氢氧化钠对钒有较好的解吸效果。由于氢氧化钠溶解度的影响,试验配制氢氧化钠溶液最高浓度为12 mol/L。因此选择使用浓度为12 mol/L的氢氧化钠溶液继续下一步试验。
2.3 解吸温度的影响为探究不同的解吸温度对钒离子解吸效果的影响,选取氢氧化钠为解吸剂,控制解吸时间1 h,振动速率为160 r/min,改变不同解吸温度。试验结果如图 4所示。
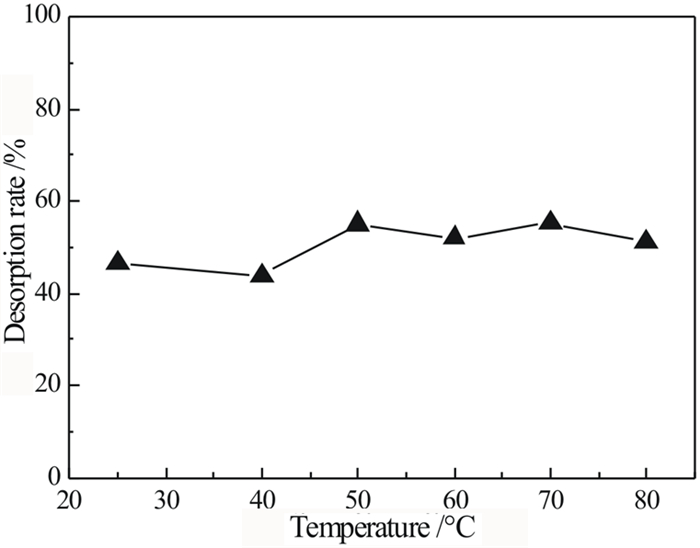 |
| 图 4 解吸温度对钒解吸率的影响 Fig.4 Effect of temperature on desorption rate of V |
从图 4中可以得知,升高反应温度,钒的解吸率逐渐增大,当温度达到50 ℃时,继续升高温度对钒解吸率的影响较小,在温度为50 ℃的时候,钒的解吸率最高,即50 ℃为氢氧化钠从偕胺肟螯合树脂中解吸钒的最佳温度,因此选择50 ℃作为最佳温度条件继续之后试验。
2.4 解吸时间的影响研究了解吸时间对钒解吸效果的影响。选取浓度为12 mol/L氢氧化钠为解吸剂,解吸温度为50 ℃,振动速率为160 r/min,解吸时间的影响试验结果如图 5所示。
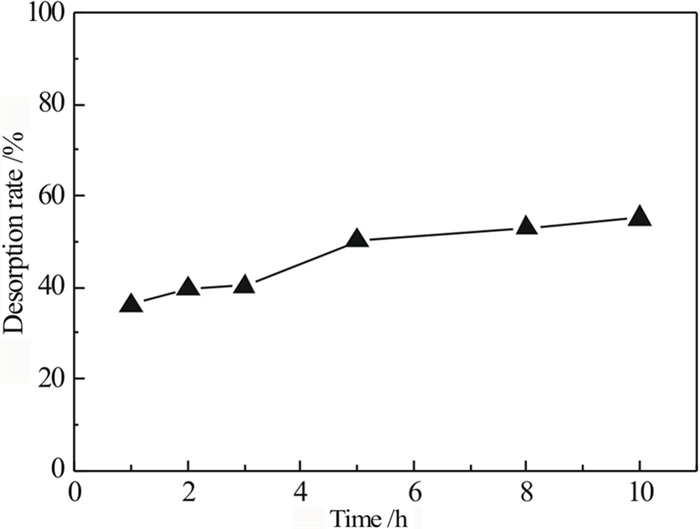 |
| 图 5 解吸时间对钒解吸率的影响 Fig.5 Effect of time on desorption rate of V |
由图 5可看出,钒的解吸率随着解吸时间的增加而缓步提高,当解吸时间达到5 h解吸基本达到平衡。由此可知为提高钒的回收率,可适当增加解吸时间。由之前的工作可知树脂经多次解吸,解吸液中钒离子会逐渐累积,当解吸次数达到5次时,溶液中钒离子浓度不在增加,且随着解吸次数增加,钒解吸率降低[14]。
3 钒的沉淀试验 3.1 钒的沉淀剂种类的影响沉淀剂种类试验以氨水(NH3·H2O)、氯化铵(NH4Cl)、氧化钡(BaO)和氧化钙(CaO)为沉淀剂对含钒溶液进行沉淀试验,沉淀时间均为40 min,K=3(K值为所加沉淀剂与溶液中五氧化二钒的质量比),沉淀温度为室温。试验结果如图 6所示。
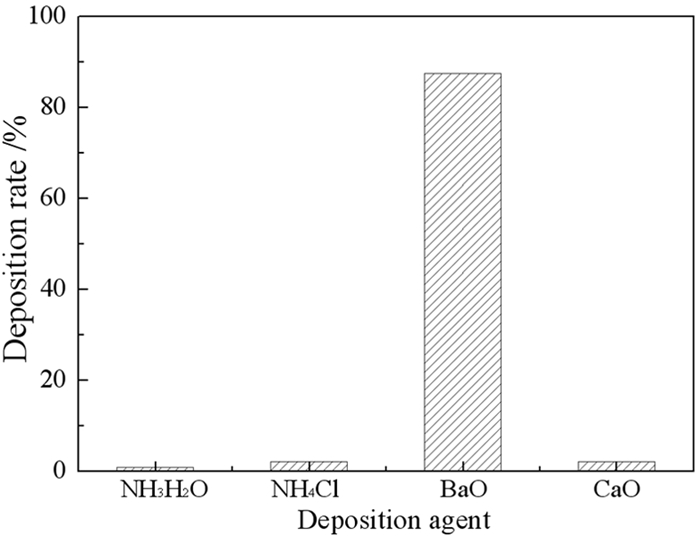 |
| 图 6 沉淀剂种类对沉淀率的影响 Fig.6 Effect of deposition agent on deposition rate of V |
由图 6可知,用氧化钡作为沉淀剂沉钒,其沉淀率可达87.48%,沉淀效果远远优于其他三种沉淀剂,因此选择氧化钡作为沉淀剂继续试验。
3.2 NaOH浓度对沉淀的影响选取氧化钡(BaO)为沉淀剂,沉淀时间为40 min,K=3,沉淀温度为室温,考察溶液中氢氧化钠浓度的影响,试验结果如图 7所示,不同氢氧化钠浓度沉淀产物的扫描电镜和沉淀产物物相如图 8和图 9所示。
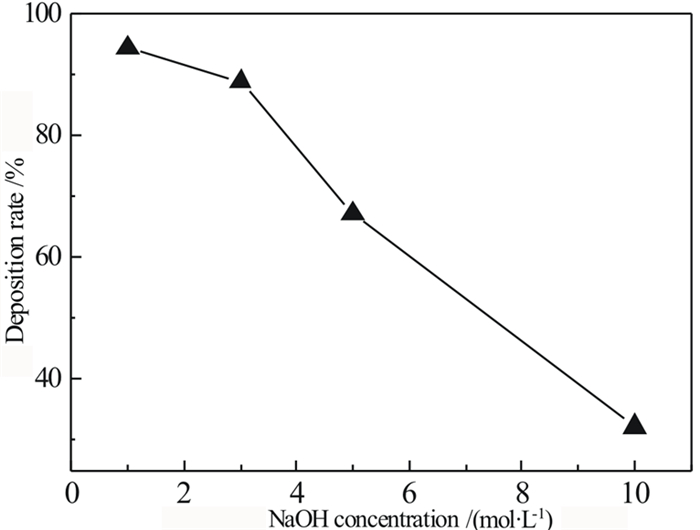 |
| 图 7 氢氧化钠浓度对钒沉淀影响 Fig.7 Effect of NaOH concentration on deposition rate of V |
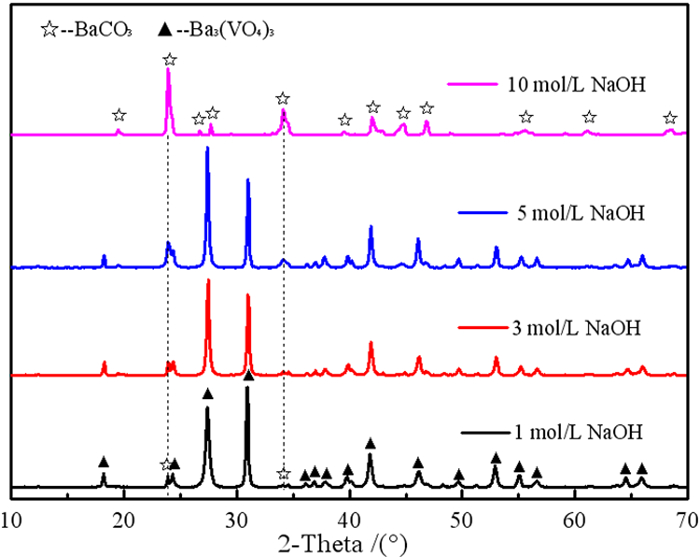 |
| 图 8 NaOH浓度对BaO沉淀钒物相(XRD)的影响 Fig.8 Effect of NaOH concentration on the phase of BaO precipitated V |
 |
| 图 9 钒酸钡电镜图:(a)1 mol/L NaOH,(b)3 mol/L NaOH,(c)5 mol/L NaOH,(d)10 mol/L NaOH Fig.9 SEM image of Ba3(VO4)2: (a)1 mol/L NaOH, (b)3 mol/L NaOH, (c)5 mol/L NaOH, (d)10 mol/L NaOH |
如图 7可知,随着溶液NaOH浓度的增大,钒的沉淀率逐渐减小。当溶液NaOH浓度为1 mol/L时,钒的沉淀率为94.42%,当NaOH浓度为10 mol/L时降到32.4%。当NaOH浓度越高,对树脂中钒解吸率越高,这可能是因为高浓度溶液中NaOH对钒的结合能力强,只有少数的钒与氧化钡产生沉淀。图 8中XRD图谱可知,当NaOH浓度为1 mol/L时沉淀物主要Ba3(VO4)2且其纯度最高,优于其他方法合成的产物[10, 11],无次晶相Ba2V2O7的出现;随着NaOH浓度的增加,沉淀率降低,沉淀中Ba3(VO4)2的含量逐渐减小,出现BaCO3特征峰,当溶液NaOH浓度达到10 mol/L时,沉淀主要以BaCO3的形式存在。由图 9电镜图可知,当溶液中NaOH浓度1 mol/L、3 mol/L、5 mol/L时产生的沉淀主要以Ba3(VO4)2为主,而Ba3(VO4)2的形貌以片状形式存在。当溶液中NaOH浓度为10 mol/L时,沉淀物主要以条状形式存在,显示了沉淀物BaCO3的条状结构。
3.3 沉淀温度的影响选取氧化钡为沉淀剂,K=3,沉淀时间为40 min,溶液中氢氧化钠溶液浓度为1 mol/L, 沉淀温度的影响试验结果如图 10所示。
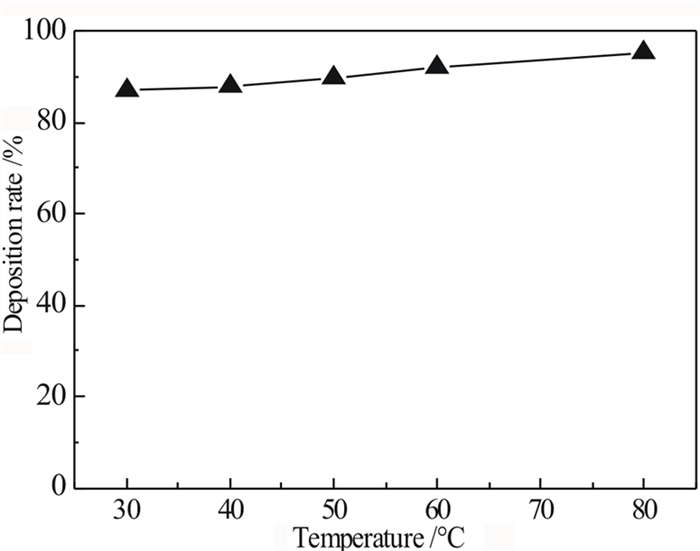 |
| 图 10 沉淀温度对V沉淀率的影响 Fig.10 Effect of deposition temperature on deposition rate of V |
由图 10可以看出温度不显著,随着温度的升高BaO对钒离子的沉淀率缓慢增加。因此为得到更高的钒的沉淀回收率,可适当提高沉淀温度。从成本上综合考虑,采用室温条件较为合适,因此,后续试验温度设定为室温。
3.4 K值对沉淀的影响选取氧化钡(BaO)为沉淀剂,沉淀时间为40 min,沉淀温度为室温,溶液中NaOH溶液浓度为1 mol/L,考察K值对钒沉淀的影响,试验结果如图 11所示。
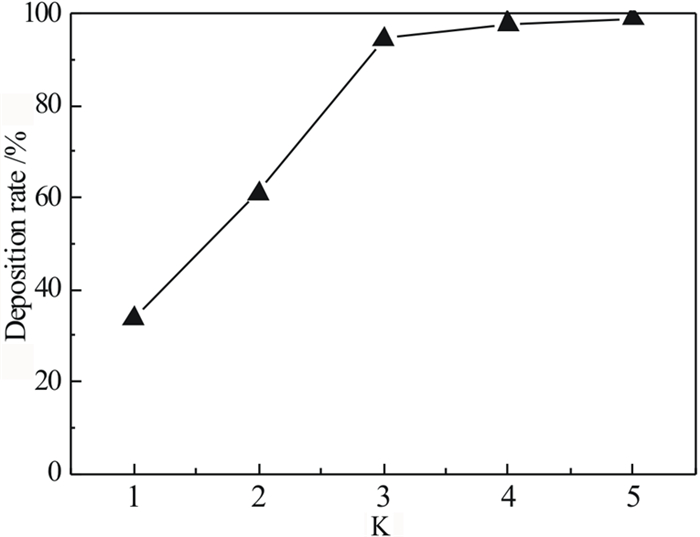 |
| 图 11 K值对V沉淀率的影响 Fig.11 Effect of K on deposition rate of V |
从图 11可以看出当K值小于3时,钒的沉淀率随K值的增加呈线性增长,当K值大于3时,沉淀率几乎保持不变,由此可判定当K值为3时,沉淀已达到临界点,为降低沉淀成本,选择K=3为BaO的最佳用量。
3.5 沉淀时间的影响选取氧化钡为沉淀,K=3,沉淀温度为室温,溶液中氢氧化钠溶液浓度为1 mol/L, 沉淀时间的影响试验结果如图 12所示。
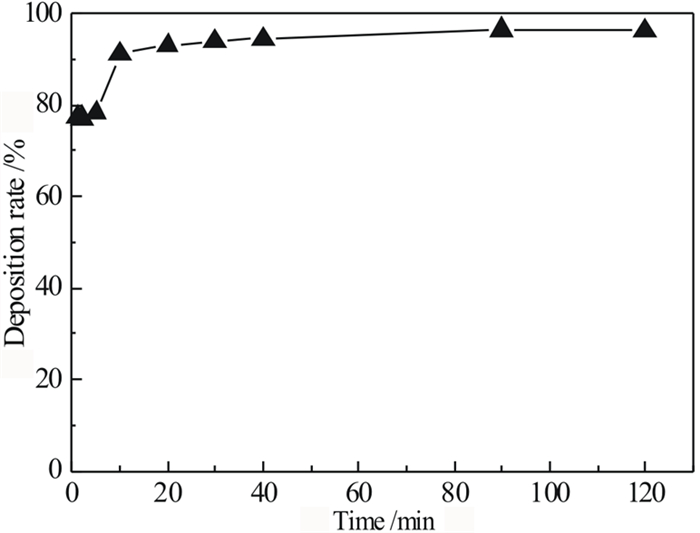 |
| 图 12 沉淀时间对钒沉淀率的影响 Fig.12 Effect of deposition time on deposition rate of V |
从图 12可知用BaO沉钒速率快,随着时间的推移其沉淀率越来越高,直到沉淀时间到达40 min,40 min后其沉淀率趋于稳定,由此可推断当沉淀时间到达40 min时,沉淀达到平衡。
4 结论(1) 用氢氧化钠作为解吸剂将钒从树脂中解吸是可行的,氢氧化钠浓度为12 mol/L时,其在50 ℃解吸10 h,解吸率达到55.78%;10 mol/L强酸溶液对钒的解吸率高达60~70%,但强酸会破坏树脂结构。
(2) 以BaO为沉淀剂,随着溶液中NaOH浓度的增加其沉淀率逐渐降低且沉淀产物中Ba3(VO4)2含量逐渐减少,BaCO3含量逐渐增大。溶液中NaOH浓度为1 mol/L时产物Ba3(VO4)2纯度最高。
(3) 在强碱性条件下,用氨水、氯化铵和氧化钙沉淀钒,沉淀率极低,而氧化钡能够迅速与碱液中的钒离子反应且沉淀效果显著;在最佳钒的沉淀条件(K=3,反应温度25 ℃,NaOH浓度为1 mol/L,沉淀时间为40 min)下,沉淀率可达94.42%。
| [1] |
翟秀静, 吕子剑. 镓冶金[M]. 北京: 冶金工业出版社, 2010.
|
| [2] |
赵汀, 秦鹏珍, 王安建, 等. 镓矿资源需求趋势分析与中国镓产业发展思考[J]. 地球学报, 2017, 38(1): 77-84. |
| [3] |
赵秦生, 李中军. 钒冶金[M]. 长沙: 中南大学出版社, 2010.
|
| [4] |
段国义.富集-电解法回收氧化铝循环母液中镓的电流效率及杂质影响问题研究[D].北京: 北京化工大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10010-1016322246.htm
|
| [5] |
BAUTISTA R. G.. Processing to obtain high-purity gallium[J]. JOM, 2003, 55(3): 23-26. DOI:10.1007/s11837-003-0155-2 |
| [6] |
ZHAO Z, LI X H, CHAI Y Q, et al. Adsorption performances and mechanisms of amidoxime resin toward gallium(Ⅲ) and vanadium(V) from bayer liquor[J]. ACS Sustainable Chemistry & Engineering, 2015, 4(1): 53-59. |
| [7] |
郑琦, 韦悦周, 何春林, 等. 广西某铝母液中镓钒铝的偕胺肟螯合树脂吸附与解吸试验[J]. 金属矿山, 2019, V48(3): 111-115. |
| [8] |
李延芬, 刘叶凤, 罗浩, 等. 提钒技术研究进展[J]. 化工进展, 2016, 35(S1): 223-229. |
| [9] |
陈肖虎, 陈颖, 甘蔓, 等. 沉淀法从拜耳法铝酸钠溶液中分离钒[J]. 过程工程学报, 2010, 10(S1): 142-145. |
| [10] |
熊巍, 林树坤, 谢勇平. 液相法合成Ba3(VO4)2晶体原料[J]. 福州大学学报(自然科学版), 2003, 31(5): 618-621. DOI:10.3969/j.issn.1000-2243.2003.05.026 |
| [11] |
周振泽, 张德, 徐建梅, 等. Ba3(VO4)2合成过程的研究[J]. 材料工程, 2009(11): 20-22. DOI:10.3969/j.issn.1001-4381.2009.11.005 |
| [12] |
ZHANG Z, ZHU H, LI Y, et al. Low temperature sintering and dielectric properties of Ba3(VO4)2 microwave ceramics using CO2O3 additives[J]. Journal of Materials Science:Materials in Electronics, 2017, 28(24): 18474-18479. DOI:10.1007/s10854-017-7794-5 |
| [13] |
KHATRI P, BEHERA B, SRINIVAS V, et al. Structural and dielectric properties of Ba3V2O8 ceramics[J]. Current Applied Physics, 2009, 9(2): 515-519. DOI:10.1016/j.cap.2008.05.002 |
| [14] |
蒙杰杰, 何春林, 李杰, 等. 拜耳循环母液镓吸附-萃取富集试验[J]. 矿产保护与利用, 2020(1): 110-117. |
 2020
2020


