| 典型金属离子对闪锌矿浮选行为的影响及作用机制的研究进展 |
2. 昆明理工大学 国土资源与工程学院,云南 昆明 650093;
3. 攀钢集团矿业有限公司,四川 攀枝花 617000
2. Faculty of Land Resource Engineering, Kunming University of Science and Technology, Kunming 650093, China;
3. Panzhihua Iron and Steel Group Mining Co. Ltd., Panzhihua 617000, China
闪锌矿是锌金属最重要的来源之一,90%左右的锌产量来源于闪锌矿,其化学式为ZnS, 属于等轴晶系[1]。闪锌矿通常与方铅矿、黄铁矿、黄铜矿等矿物共伴生,浮选是分离多金属矿物最有效的方法,它是一个涉及到固、液、气三相的复杂过程。矿浆化学环境对闪锌矿的浮选行为具有显著影响,某些金属离子对其浮选有活化作用,而某些金属离子对其浮选有抑制作用,且某些金属离子在不同条件下对闪锌矿的浮选行为的影响也不尽相同。如Ca2+对于无金属离子活化的闪锌矿的浮选,具有活化作用,对于经过铜活化后的闪锌矿的浮选,Ca2+的存在对闪锌矿浮选是有抑制作用的;再如,Pb2+在酸性或弱碱性矿浆中存在时,对闪锌矿具有活化作用,但当矿浆碱性较强时,表面会生成大量Pb(OH)2胶体,反而对闪锌矿有抑制作用[2, 3]。
各种金属离子在闪锌矿表面的作用机制已经成为研究热点,这些研究对了解闪锌矿的浮选机制起到了十分重要的作用,但是长期以来,大部分研究者都是研究某种金属离子对闪锌矿浮选的影响及其作用机理[2, 4-5],而没有去系统性总结,为此,本文归纳总结了铜、铅、铁、钙、镁、锌等对闪锌矿浮选影响较为明显的典型金属离子的作用机制的研究进展,并对金属离子在闪锌矿表面的作用机制的研究方向进行展望,为以后对金属离子与闪锌矿表面作用机制的研究提供参考和依据。
1 金属离子的来源 1.1 矿物学因素 1.1.1 晶格杂质由于成矿环境和条件的影响,硫化矿中通常都会含有晶格杂质,这些晶格杂质以金属离子最为常见,而闪锌矿中的金属离子杂质以铁、锰、镉、铟、镓、汞、锗、铜、锡、锑、铋等为主,在浮选中这些金属离子杂质的存在是不可避免的,且无法消除,必定会对浮选产生一定的影响,其铁晶格杂质是Fe3+的重要来源[6-8]。
1.1.2 矿物溶解有用矿物及脉石矿物溶解也会产生许多离子,闪锌矿浮选时,方铅矿溶解产生的Pb2+是Pb2+的重要来源。Basilio[9]研究了闪锌矿在方铅矿存在时的浮选,结果表明方铅矿存在时闪锌矿表面的Pb2+明显增加,促进了闪锌矿的浮选。黄福根等[10]研究发现,由于方铅矿溶解释放Pb2+的活化作用,导致闪锌矿在方铅矿浮选时的后期显示出相当大的可浮性,使铅锌分离困难。
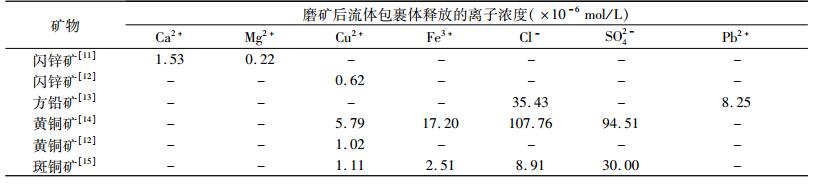
1.1.3 流体包裹体释放在矿物形成的过程中,由于各种因素的影响,使正在形成(或形成后)的矿物产生各种晶格缺陷,被矿物圈闭于这些缺陷中而保留、保存下来的介质称为流体包裹体。有用矿物和脉石矿物中含有大量流体包裹体,它们的破裂会释放出各种各样的金属离子,这些离子对闪锌矿浮选也具有很大的影响。表 1是各种矿物中流体包裹体所释放的各成分的浓度。
| 表 1 流体包裹体释放的离子的浓度 Table 1 The ion concentration of fluid inclusion releasing |
 |
1.2 闪锌矿浮选的矿浆环境 1.2.1 浮选药剂
浮选药剂是矿浆中Cu2+、Ca2+、Zn2+的重要来源,CuSO4和ZnSO4作为闪锌矿最常用的活化剂和抑制剂,为浮选矿浆带来大量的Cu2+和Zn2+,它们能够改变闪锌矿的可浮性。CaO作为闪锌矿浮选的pH调整剂,在水中会产生大量的Ca2+,这些Ca2+同样能改变闪锌矿的可浮性。
1.2.2 水质研究表明,水质中所含的Ca2+、Mg2+等金属离子对浮选具有明显的影响。孙昊等[16]研究了水质对十二酸浮选分离菱镁矿与白云石的影响,结果表明,按不同比例将离去子水与自来水混合,然后用于浮选菱镁矿与白云石,随着自来水所占混合水百分含量的增加,菱镁矿的回收率明显下降;其中Ca2+和Mg2+对菱镁矿的浮选有抑制作用,且抑制作用的强弱与十二酸的浓度有关。Ikumapayi等[17]研究发现,利用工业用水浮选闪锌矿纯矿物时,其回收率高于使用去离子水浮选。
1.2.3 磨矿介质作为最常用的磨矿介质,钢球介质和铁介质会释放出大量的Fe3+和Fe2+,这也是闪锌矿浮选时Fe3+、Fe2+重要的来源,对后续的浮选具有很大的影响[18, 19]。Grano等[19]研究了钢球介质和陶瓷介质对黄铜矿、黄铁矿微细粒浮选的影响,研究表明,相比于钢球介质,陶瓷介质能减少铁在矿物表面的污染,有利于提高黄铜矿、黄铁矿微细粒浮选的回收率。
2 矿浆中离子的作用 2.1 Cu2+对闪锌矿浮选行为的影响闪锌矿在酸性介质中很容易被浮选,但在碱性溶液中需要加入活化剂才能获得较好的浮选效果[20]。近几十年来,CuSO4作为闪锌矿的活化剂被广泛使用[21-24]。在浮选矿浆中,Cu2+和铜的氢氧化物是铜的主要存在形式,Cu2+在能够与ZnS直接发生置换反应从而取代Zn2+, 使闪锌矿表面可浮性增加;而铜的氢氧化物首先吸附在闪锌矿表面,然后转变为稳定性更强的CuS,使闪锌矿表面可浮性增加。
2.1.1 Cu2+的活化作用Cu2+活化机理一直是研究的热点,通常认为Cu2+活化闪锌矿的机理是Cu2+与ZnS发生了取代反应,即Cu2+取代了闪锌矿表面的Zn2+,其取代后使闪锌矿表面生成了铜的硫化物,且减少了闪锌矿表面的过度氧化[25-29]。一般情况下硫化矿表面疏水性较弱,需要加入黄药增强其疏水性,其作用原理为硫化矿表面的金属离子与黄药会生成金属黄原酸盐,具有疏水基团的金属黄原酸盐使其可浮性增强。相比于黄药与Cu2+生成的黄原酸铜,黄原酸锌溶解度积负对数比较小,稳定性不如黄原酸铜,故表面含CuS薄膜的闪锌矿对黄药的吸附更容易发生[30-32]。
早期的研究者认为铜活化闪锌矿机理是Cu2+与闪锌矿表面的ZnS发生简单的取代反应,即Cu2+是按1 : 1的比例取代闪锌矿中的Zn2+[31]。其活化机理可以表示为:
| $ {\rm{ZnS)ZnS + C}}{{\rm{u}}^{{\rm{2 + }}}} \to {\rm{ZnS)CuS + Z}}{{\rm{n}}^{{\rm{2 + }}}} $ | (1) |
之所以Cu2+能够取代ZnS中的Zn2+,是因为Cu2+与Zn2+离子半径十分相近,且CuS的溶度积比ZnS的溶度积小[31]。
然而铜活化闪锌矿机理一直存在争议,Cu2+取代Zn2+后,表面形成的ZnS处于亚稳态,闪锌矿表面会发生氧化,Cu2+会被还原为Cu+[25, 27, 29]。Frinkelstein等[26]提出在溶液中铜的主要存在形式为Cu2+时,活化闪锌矿的机理可以表示为:
| $ y{\rm{ZnS}} + x{\rm{C}}{{\rm{u}}^{{\rm{2 + }}}} = (y - x){\rm{ZnS}}\cdot x{\rm{C}}{{\rm{u}}^{\rm{ + }}}{{\rm{S}}^{\rm{ - }}} + x{\rm{Z}}{{\rm{n}}^{{\rm{2 + }}}} $ | (2) |
Gerson[27]指出当闪锌矿表面的覆盖层低于两层分子时,无论在酸性pH条件下,还是在碱性pH条件下,Cu2+在闪锌矿表面的作用都是以1 : 1的比例取代闪锌矿中的Zn2+。但是随着闪锌矿表面的氧化,表面的Cu2+会被还原为Cu+。而研究也发现,铜活化后的闪锌矿表面不仅Cu2+会被还原为Cu+,而且S2-也会被氧化为S-[26]。Ejtemaei等[29]利用Cryo-XPS研究发现,在闪锌矿晶格中存在Cu2+取代Zn2+的现象,随着矿物表面的氧化,闪锌矿表面的Cu2+被还原为Cu+,S2-会被氧化为S-,在表面形成了分子层。其具体转化可用图 1表示[2, 26, 29]。
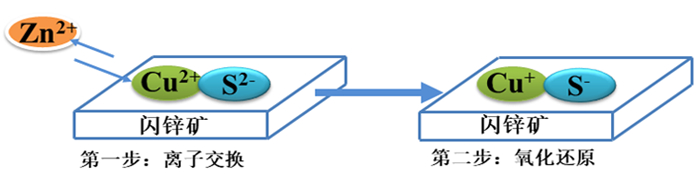 |
| 图 1 铜在闪锌矿表面取代和氧化模型 Fig.1 Substitution and oxidation models of copper on sphalerite surface |
随着进一步研究,发现铜取代后闪锌矿表面的氧化并不是纯粹的将Cu2+还原为Cu+、S2-氧化为S-,氧化后还会有许多其他价态的铜硫化合物生成。Boulton等[33]通过XPS和TOF-SIMS分别对闪锌矿和黄铜矿浮选的精矿和尾矿表面进行分析,结果表明,在闪锌矿和黄铁矿表面都存在疏水性更强的Cu2S和黄药捕收剂,而且它们的浓度在闪锌矿上较大。Kartio[4]分别对有无空气时,闪锌矿在pH值为9、CuSO4浓度为1×10-4 mol/L的溶液中活化处理30 min后做光谱分析,结果表明,没有空气时,S0和S-的强度比为1.4 : 1,从而推测出闪锌矿表明含有Cu2S5,同理发现了有空气时闪锌矿表面含有Cu2S6。顾帼华等[28]通过热力学分析和电化学测试研究闪锌矿在常见的弱碱性至碱性浮选体系CuSO4活化闪锌矿的电化学机理,结果表明,加入CuSO4后,闪锌矿表面主要存在Cu2S和CuS的一系列氧化行为,氧化的结果使得闪锌矿表面可能存在Cu2S,Cu1.96S,Cu1.74~1.82S,Cu1.75S,Cu1.60S,Cu1.40S,Cu1.12S,CuS等一系列铜的硫化物。
上述结果表明,Cu2+活化闪锌矿首先是Cu2+与ZnS发生取代反应生成,形成的只是处于亚稳态,当氧化时间足够时,闪锌矿表面会形成许多不同氧化程度的铜硫化合物,这些铜硫化合物与捕收剂的作用能力更强从而使闪锌矿具有更强的疏水性。
2.1.2 Cu(OH)2的活化与Cu2+一样,氢氧化铜对闪锌矿也有活化作用。闪锌矿在碱性条件下加入Cu2+活化浮选时,溶液中首先会生成Cu(OH)2胶体[26, 27, 34]。生成的Cu(OH)2胶体覆盖在闪锌矿表面[32]。其反应过程可表示为[26]:
| $ \begin{align} & y\text{ZnS}+x\text{C}{{\text{u}}^{\text{2+}}}+2x\left( \text{O}{{\text{H}}^{\text{-}}} \right)\rightleftharpoons \\ & y\text{ZnS}+x\text{Cu}{{\left( \text{OH} \right)}_{2}}\rightleftharpoons y\text{ZnS}\cdot x\text{Cu}{{\left( \text{OH} \right)}_{\text{2}}} \\ \end{align} $ | (3) |
随着Cu(OH)2胶体覆盖在闪锌矿表面,Cu(OH)2会转变为稳定性更强的CuS,其转变过程可以表示为:
| $ \begin{align} & y\text{ZnS}\cdot x\text{Cu}{{\left( \text{O}{{\text{H}}^{\text{-}}} \right)}_{2}}\rightleftharpoons \\ & (y-x)\left( \text{ZnS} \right)\cdot x\text{C}{{\text{u}}^{\text{2+}}}{{\text{S}}^{\text{2-}}}\cdot x\text{Zn}{{\left( \text{OH} \right)}_{2}}\rightleftharpoons \\ & (y-x)\left( \text{ZnS} \right)\cdot x\text{C}{{\text{u}}^{\text{2+}}}{{\text{S}}^{\text{2-}}}+x\text{Zn}{{\left( \text{OH} \right)}_{\text{2}}}\text{ }\!\!~\!\!\text{ } \\ \end{align} $ | (4) |
Liu等[35]用量子化学模拟了Cu(OH)2在闪锌矿表面的作用过程,结果表明在闪锌矿表面的S与Cu(OH)2分子之间存在着剧烈的相互作用,Cu(OH)2中的OH-趋向于和闪锌矿表面的Zn2+相互作用,而Cu(OH)2中的Cu2+则趋向于和闪锌矿表面的S原子相互作用,由于OH-与Cu2+运动路径的方向不同,导致了Cu-OH键的断裂。Liu等利用计算机模拟很好的解释了Cu(OH)2在闪锌矿表面的作用过程,并且证实了在碱性条件下闪锌矿表面生成了CuS和Zn(OH)2。与Cu2+活化闪锌矿形成的Cu2+S2-一样,其也同样处于亚稳态,最终也有可能被氧化为不同氧化程度的铜硫化合物。
2.2 Pb2+对闪锌矿浮选行为的影响闪锌矿浮选时,Pb2+的存在在很多情况下都是难以避免的,且这些难免的Pb2+对闪锌矿浮选的影响是不可忽略的[9]。
2.2.1 Pb2+的活化早期一度认为Pb2+活化闪锌矿的机理和Cu2+的活化机理一样,都是简单的取代反应[36, 37],即:
| $ \text{ZnS)ZnS+P}{{\text{b}}^{\text{2+}}}\rightleftharpoons \text{ZnS)PbS+Z}{{\text{n}}^{\text{2+}}} $ | (5) |
但此活化机理与很多研究结果相违背[5, 38-40]。与Cu2+通过取代闪锌矿表面Zn2+来活化闪锌矿不同,由于铅的范德华半径(2.02 Å)远大于锌的范德华半径(1.39 Å),假如Pb2+以取代形式活化闪锌矿,闪锌矿表面会发现很明显的驰豫现象[5, 40]。Morey等[41]研究发现,被Pb2+活化后的闪锌矿伏安循环曲线并未出现PbS的氧化峰,加入黄药后也未出现明显的电流峰,然而在加入黄药后方铅矿(PbS)表面出现了氧化形成黄原酸铅的氧化峰,此现象说明了在闪锌矿表面并未形成PbS组分,因此认为闪锌矿表面并未发生Pb2+取代ZnS中Zn2+的反应。Sarvaramini等[37]利用XPS和量子化学模拟研究了Pb2+在闪锌矿表面的取代,结果表明,铅取代后的闪锌矿表面的Pb-S键长为2.73 Å,远大于Zn-S(2.28 Å)的键长,单个Pb2+在闪锌矿表面的取代时,取代能达到了+440 kJ/mol,当闪锌矿表面第一层Zn2+全部被Pb2+取代时,取代能更是达到了+518.4 kJ/mol,其结果说明在闪锌矿表面Pb2+取代Zn2+是很难发生的。
在酸性及弱碱性浮选环境中存在的Pb2+对闪锌矿具有活化作用,其活化作用的方式存在以下两种观点:一种观点认为Pb2+活化闪锌矿表明形成了氧化铅物质,Pb2+通过与O2的作用在闪锌矿表面形成了Zn-O-Pb键,从而实现了吸附。Steele等[40]研究表明,Pb2+不会因为在闪锌矿表面上形成Zn-Pb和Pb-S键而吸附,但是PbO和Pb2+在闪锌矿表面会因为形成Zn-O-Pb键而实现吸附。Patirick等[39]认为,虽然在pH=5.5或更低条件下,Pb2+是溶液中铅主要的组成物质,但它的水解产物Pb(OH)+却更容易吸附到闪锌矿表面,而Pb(OH)+的存在促进了Pb2+通过氧气附着到表面,而且在闪锌矿表面存在S-O键和Pb-O键。另一种观点认为Pb2+直接与闪锌矿表面的Zn2+和S2-作用,从而吸附在闪锌矿表面,图 2为Sarvaramini等[5]研究了五种最有可能的吸附方式,得出的Pb2+在闪锌矿表面最为稳定的吸附方式可用图 2表示。
 |
| 图 2 Pb2+在闪锌矿表面的吸附 Fig.2 Pb2+ absorption on sphalerite surface |
2.2.2 Pb(OH)2的抑制作用
碱性条件下,Pb2+在矿浆中会和OH-生成Pb(OH)2胶体,在强碱性条件下,Pb(OH)2会将闪锌矿表面覆盖[5, 42]。相比于Pb2+单独存在时,Pb(OH)2和Pb2+都存在时铅对闪锌矿的活化作用相对来说更弱,Pb(OH)2会使铅的活化效果降低,当pH超过零电点时,铅的存在对闪锌矿具有抑制作用[5, 38]。Sui等[43]研究表明,当矿浆pH值小于7时,Pb2+活化闪锌矿效果显著,pH值超过10时,疏水的Pb(OH)2成为闪锌矿表面的主要成分,Pb(OH)2在表面的覆盖致使Pb2+的活化效果降低, 当矿浆pH值达到11时,添加Pb2+对闪锌矿几乎没有活化作用。
研究发现Pb(OH)2在闪锌矿表面的吸附是通过Pb(OH)2中的Pb2+和ZnS中的S2-形成共价键、Pb(OH)2中的一个氧原子和ZnS中的Zn2+形成共价键来实现的,而Pb(OH)2中的另一个氧原子则和另一个相邻的Pb(OH)2分子中的氢原子形成共价键,当黄药在覆盖了Pb(OH)2分子的闪锌矿表面吸附时,吸附能为-307 kJ/mol,远大于黄药在有Pb2+吸附的闪锌矿表面(-655.9 kJ/mol)上吸附的吸附能,甚至比黄药在无铅作用的闪锌矿表面(-370 kJ/mol)上吸附的吸附能还大,说明Pb2+在闪锌矿表面的吸附对其闪锌矿浮选具有活化作用,Pb(OH)2在闪锌矿表面的吸附对闪锌矿浮选有抑制作用[5]。
2.3 铁对闪锌矿浮选行为的影响闪锌矿浮选时,铁对其的影响主要来自两个方面:一为矿浆环境中的Fe3+和Fe2+等离子,二为闪锌矿晶体中混入的铁晶格杂质。矿浆溶液中铁主要以氢氧化物沉淀存在,其中Fe2+以Fe(OH)2的形式对闪锌矿起活化作用,铁晶格杂质能够改变闪锌矿的界面化学性质,从而影响闪锌矿浮选。对于矿浆中的Fe2+和Fe3+在闪锌矿浮选时的作用以及作用方式,当前的研究较少。
2.3.1 Fe3+和Fe2+的影响适当的碱性pH条件下,Fe(OH)2能够活化闪锌矿[44]。Zhang等[44]提出当pH值在8~11范围时,闪锌矿在含有Fe2+的矿浆中浮选会比较容易,但闪锌矿的浮选不受矿浆中的Fe3+的影响,Zeta电位测试也表明,pH值在8~11时,对比黄药在有和无Fe3+作用的闪锌矿作用时,添加Fe3+对闪锌矿表面电位没有明显影响,但对比黄药与经过Fe2+和没有经过Fe2+作用的闪锌矿表面作用时,加入的Fe2+使闪锌矿表面的电位降低明显,在pH>2.5,溶液中的Fe3+会生成Fe(OH)3沉淀,导致Fe3+对闪锌矿浮选没有影响,用黄药捕收闪锌矿,矿浆中能够活化闪锌矿的只有Fe2+,且认为Fe2+活化闪锌矿的机理可用以下方式表示:
(ⅰ)首先Fe(OH)+吸附在闪锌矿表面:
| $ \text{F}{{\text{e}}^{\text{2+}}}\text{+}{{\text{H}}_{\text{2}}}\text{O=FeO}{{\text{H}}^{\text{+}}}\text{+}{{\text{H}}^{\text{+}}} $ | (6) |
(ⅱ)吸附在闪锌矿表面的Fe(OH)+氧化生成Fe(OH)2+或者Fe(OH)2+:
| $ \begin{align} & \text{ZnS)Fe}{{\left( \text{OH} \right)}^{\text{+}}}+\frac{1}{4}{{\text{O}}_{\text{2}}}\text{+}\frac{1}{2}{{\text{H}}_{\text{2}}}\text{O}= \\ & \text{ZnS)Fe}{{\left( \text{OH} \right)}^{\text{2+}}}\text{+O}{{\text{H}}^{\text{-}}} \\ \end{align} $ | (7) |
或
| $ \text{ZnS)FeO}{{\text{H}}^{\text{+}}}+\frac{1}{4}{{\text{O}}_{\text{2}}}\text{+}\frac{\text{1}}{\text{2}}{{\text{H}}_{\text{2}}}\text{O}=\text{ZnS(Fe}\left( \text{OH} \right)_{2}^{+} $ | (8) |
(ⅲ)吸附在闪锌矿表面的Fe(OH)2+和黄药(X-)作用生成Fe(OH)2X或者Fe(OH)2X:
| $ \text{ZnS)Fe}{{\left( \text{OH} \right)}^{2+}}+\text{2}{{\text{X}}^{\text{-}}}\text{=ZnS)Fe}\left( \text{OH} \right){{\text{X}}_{2}} $ | (9) |
或
| $ \text{ZnS)Fe}{{\left( \text{OH} \right)}^{\text{+}}}_{\text{2}}\text{+}{{\text{X}}^{\text{-}}}\text{=ZnS)Fe}{{\left( \text{OH} \right)}_{\text{2}}}\text{X }\!\!~\!\!\text{ } $ | (10) |
晶格杂质中的Fe3+会降低闪锌矿的可浮性,使其浮选效果降低。
相对于闪锌矿来说,铁闪锌矿(Zn, Fe)S的浮选性能较差,闪锌矿晶格上的锌原子被Fe3+取代,使其化合价和电荷状态失去平衡,并会使部分Zn2+变为Zn+,降低了空穴浓度、增加了电子密度,使闪锌矿从p型半导体变为n型半导体,影响其界面电化学反应。由于电子密度增加,铁闪锌矿形成了对黄原酸根离子较强的排斥作用,不利于捕收剂的吸附,因此,铁闪锌矿的可浮性比闪锌矿的可浮性差,另外闪锌矿中铁杂质的存在会使Cu2+在闪锌矿晶格中的取代速度变慢,尽管长时间活化作用下,铁的存在使闪锌矿上Cu2+取代量有所增加,但因为Fe3+存在于闪锌矿表层分子之中,使表层分子中Cu2+含量反而减少,铁杂质对黄药在闪锌矿上吸附的排斥作用,导致了黄药在闪锌矿表面的吸附减少而减弱了闪锌矿的浮选效果[8, 45-48]。
Chen等[49]研究发现,闪锌矿中的铁杂质能够促进CN-在闪锌矿表面的吸附,其促进作用主要因为CN-中的C容易和杂质Fe3+发生相互作用。Liu和Solecki等[48, 50]研究发现铁杂质的存在使铁闪锌矿对Cu2+的吸附作用得到加强,但对丁基黄药在铜活化闪锌矿表面的吸附却有减弱作用,TOF-SIMS测试结果表明,闪锌矿表层的Zn2+已经全部被Cu2+取代,而铁闪锌矿表层的Zn2+全部被取代,但Fe3+却还存在于表层分子层之中。Szczypa[51]利用合成的闪锌矿(铁含量最高达40%)研究发现,铁含量的增加降低闪锌矿表面的氧化强度,导致乙基黄药在闪锌矿表面的吸附减少。
2.4 Ca2+、Mg2+、Zn2+的影响浮选用水大部分都是来自于矿山附近的溪流、水库、地下水,对于未处理的选矿回水,其中含有大量的Ca2+和Mg2+,调节矿浆pH所用的调整剂大多是生石灰,产生的Ca2+数量更是巨大,这些Ca2+和Mg2+会对矿物的浮选行为产生很大的影响[2, 17, 52-54]。因此,研究Ca2+和Mg2+在选矿过程中对闪锌矿浮选影响的作用是必要的,它能为降低Ca2+和Mg2+对闪锌矿的浮选不利影响提供理论依据,提高生产效益。
2.4.1 Ca2+和Mg2+的影响Ca2+和Mg2+对闪锌矿浮选的影响主要观点为:
(1) 当无Cu2+存在时,Ca2+能够促进闪锌矿表面和黄药的作用,有利于闪锌矿的浮选。Dávila-Pulido等[3]发现pH值在7~11之间时,黄药在“钙活化闪锌矿”表面的吸附与Ca2+在闪锌矿表面的吸附成正比,对闪锌矿的浮选有促进作用,在碱性较弱时(pH=7~9),Ca2+可以增加闪锌矿的浮选回收率,而当pH值升高到10~11之间时,Ca2+会形成Ca(OH)2沉淀,并覆盖在闪锌矿表面,使矿物表面疏水性减弱,闪锌矿回收率降低。
(2) 有Cu2+存在时,通常认为Ca2+和Mg2+会抑制铜活化闪锌矿表面与黄药的作用。接触角测量表明,Ca2+的存在会使铜活化闪锌矿表面的疏水性减弱[3, 55]。但Ca2+和Mg2+抑制作用的机理并没有形成共识[55, 56]。一种观点认为减少Cu2+在闪锌矿表面的取代是Ca2+和Mg2+降低Cu2+活化闪锌矿效果的主要途径,Ca2+和Mg2+的添加使铜活化闪锌矿表面的铜含量下降,它们与铜活化的闪锌矿表面的作用是一样的,即铜活化闪锌矿表面存在的铜硫化物减少。另一种观点认为Ca2+和Mg2+影响黄药与铜活化闪锌矿表面作用的主要是因为在闪锌矿表面形成了钙镁的氢氧化物,因为钙镁氢氧化物的增加,导致了表面Cu(OH)2的减少,而且Ca(OH)2和Mg(OH)2导致铜活化闪锌矿表面与黄药的作用减弱[56]。而且Ca2+和Mg2+作用过程也有所不同。随着pH值的增加Mg2+使闪锌矿的回收率急剧下降,而Ca2+相比于Mg2+下降速率却慢的多,Mg2+形成Mg(OH)2沉淀所需的pH比Ca2+小的多,在pH值大于10时,Mg2+就形成了Mg(OH)2沉淀覆盖在闪锌矿表面,而Ca2+在pH值为10~12时,首先形成的是CaOH+,pH值在12以上时才形成Ca(OH)2沉淀覆盖在表面[56, 57]。
2.4.2 Zn2+的抑制作用Zn2+在碱性条件下会生成Zn(OH)2胶体吸附在闪锌矿表面,阻碍闪锌矿表面和捕收剂的作用[6, 31]。
硫酸锌首先在水中解离:
| $ \text{ZnS}{{\text{O}}_{\text{4}}}\text{+2}{{\text{H}}_{\text{2}}}\text{O=Zn}{{\left( \text{OH} \right)}_{\text{2}}}\text{+2}{{\text{H}}^{\text{+}}}\text{+SO}_{4}^{2-} $ | (11) |
而在碱性介质中则生成HZnO2-和ZnO22-胶体:
| $ \text{Zn}{{\left( \text{OH} \right)}_{\text{2}}}\text{+O}{{\text{H}}^{\text{-}}}\text{=HZnO}_{2}^{-}\text{+}{{\text{H}}_{\text{2}}}\text{O} $ | (12) |
| $ \text{Zn}{{\left( \text{OH} \right)}_{\text{2}}}\text{+2O}{{\text{H}}^{\text{-}}}\text{=ZnO}_{\text{2}}^{\text{2-}}\text{+2}{{\text{H}}_{\text{2}}}\text{O} $ | (13) |
由于硫酸锌单独使用时,其抑制效果并不是很好,因此很多时候都是和氰化物、硫化钠、亚硫酸盐等配合使用[6]。Liu等研究了硫酸锌和二甲基二硫代氨基甲酸钠联合使用时抑制闪锌矿的效果,结果表明其对闪锌矿抑制效果明显,能够抑制铜活化后的闪锌矿,而对黄铜矿只有微弱的抑制作用[58]。
3 结论金属离子对闪锌矿的浮选有着重要的影响,大量研究表明,在不同的环境下,金属离子对闪锌矿的浮选的影响不尽相同。
(1) Cu2+作为闪锌矿最常用的活化剂,无论是以Cu2+形式存在还是以氢氧化物形式存在,对闪锌矿都能起活化作用。
(2) Pb2+在闪锌矿的浮选过程中不会在闪锌矿表面发生取代,Pb2+以吸附形式作用在闪锌矿表面,对闪锌矿具有活化作用,当矿浆pH为碱性,Pb2+会以氢氧化铅的形式存在,氢氧化铅的吸附会对闪锌矿的浮选有抑制作用。
(3) Ca2+在无铜活化时对闪锌矿有活化作用,但Ca2+对铜活化后的闪锌矿具有抑制作用,Mg2+与Ca2+具有相似的作用机制,但是它们形成相似效果的矿浆环境有所不同。而对Zn2+的抑制作用是以在闪锌矿表面形成氢氧化物的形式实现的。
(4) 铁的离子价态不同,其对闪锌矿的浮选的影响也不同。铁的离子价态不同,其对闪锌矿的浮选的影响也不同,溶液中Fe2+能够活化闪锌矿,Fe3+对闪锌矿的浮选没有明显影响。而以晶格缺陷存在于闪锌矿晶格中的铁而言,主要对闪锌矿的半导体类型、晶格参数、界面电化学等产生影响,从而影响其可浮性。
单一的金属离子对闪锌矿的影响在环境不同时作用差别很大,因此,对于矿浆环境差别很大的整个浮选流程来说,金属离子与其它活化抑制剂组合使用能使获得更佳的效果,且能较为明显得节约生产成本,因此金属离子的组合活化剂或抑制剂的研究是一个重要的研究方向。现阶段而言,各种金属离子在闪锌矿浮选时产生的影响比较明确,然而它们的具体作用方式、作用的具体物质组成尚需要进行深入地探索,这些探索对金属离子的使用及降低浮选时金属离子的不利影响具有重要意义。
| [1] |
刘建.闪锌矿表面原子构型及铜吸附活化浮选理论研究[D].昆明: 昆明理工大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10674-1015641661.htm
|
| [2] |
Kirjavainen V, Schreithofer N, Heiskanen K. Effect of calcium and thiosulfate ions on flotation selectivity of nickel-copper ores[J]. Minerals engineering, 2002, 15(1): 1-5. |
| [3] |
Dávila-Pulido G, Uribe-Salas A, álvarez-Silva M, et al. The role of calcium in xanthate adsorption onto sphalerite[J]. Minerals engineering, 2015, 71: 113-119. DOI:10.1016/j.mineng.2014.09.004 |
| [4] |
Kartio I J, Basilio C I, Yoon R H. An XPS study of sphalerite activation by copper[J]. Langmuir, 1998, 14(18): 5274-5278. DOI:10.1021/la970440c |
| [5] |
Sarvaramini A, Larachi F, Hart B. Collector attachment to lead-activated sphalerite-experiments and DFT study on pH and solvent effects[J]. Applied surface science, 2016, 367: 459-472. DOI:10.1016/j.apsusc.2016.01.213 |
| [6] |
胡熙庚. 有色金属硫化矿选矿[M]. 北京: 冶金工业出版社, 1987.
|
| [7] |
Huston D L, Sie S H, Suter G F, et al. Trace elements in sulfide minerals from eastern Australian volcanic-hosted massive sulfide deposits; Part Ⅰ, proton microprobe analyses of pyrite, chalcopyrite, and sphalerite, and Part Ⅱ, selenium levels in pyrite; comparison with delta 34 S values and implications for the source of sulfur in volcanogenic hydrothermal systems[J]. Economic geology, 1995, 90(5): 1167-1196. DOI:10.2113/gsecongeo.90.5.1167 |
| [8] |
陈建华, 曾小钦, 陈晔, 等. 含空位和杂质缺陷的闪锌矿电子结构的第一性原理计算[J]. 中国有色金属学报, 2010, 20(4): 765-71. |
| [9] |
Basilio C I, Kartio I J, Yoon R H. Lead activation of sphalerite during galena flotation[J]. Minerals engineering, 1996, 9(8): 870-879. |
| [10] |
黄福根, 肖鹂. 方铅矿浮选时闪放的铅活化[J]. 国外选矿快报, 1997(16): 7-12. |
| [11] |
Liu J, Wen S, Wu D, et al. Determination of the concentrations of calcium and magnesium released from fluid inclusions of sphalerite and quartz[J]. Minerals engineering, 2013, 45(3): 41-43. |
| [12] |
Deng J, Mao Y, Wen S, et al. New influence factor inducing difficulty in selective flotation separation of Cu-Zn mixed sulfide minerals[J]. International journal of minerals, metallurgy, and materials, 2015, 22(2): 111-115. DOI:10.1007/s12613-015-1050-x |
| [13] |
Bai S, Wen S, Xian Y, et al. New source of unavoidable ions in galena flotation pulp: components released from fluid inclusions[J]. Minerals engineering, 2013, 45: 94-99. DOI:10.1016/j.mineng.2013.02.001 |
| [14] |
Deng J, Wen S, Xian Y, et al. New discovery of unavoidable ions source in chalcopyrite flotation pulp: fluid inclusions[J]. Minerals engineering, 2013, 42: 22-8. DOI:10.1016/j.mineng.2012.10.010 |
| [15] |
Deng J, Wen S, Wu D, et al. Existence and release of fluid inclusions in bornite and its associated quartz and calcite[J]. International journal of minerals metallurgy & materials, 2013, 20(9): 815-822. |
| [16] |
孙昊, 孙体昌, 朱阳戈, 等. 水质对十二酸浮选分离菱镁矿与白云石的影响研究[J]. 有色金属(选矿部分), 2017(5): 89-92. DOI:10.3969/j.issn.1671-9492.2017.05.020 |
| [17] |
Ikumapayi F, Makitalo M, Johansson B, et al. Recycling process water in sulphide flotation: effect of calcium and sulphate on sphalerite recovery[J]. Minerals engineering, 2012, 29(4): 45-64. |
| [18] |
钟素姣.磨矿对方铅矿和闪锌矿浮选行为的影响研究[D].长沙: 中南大学, 2006. http://d.wanfangdata.com.cn/Thesis/Y997676
|
| [19] |
Grano S. The critical importance of the grinding environment on fine particle recovery in flotation[J]. Minerals engineering, 2009, 22(4): 386-394. DOI:10.1016/j.mineng.2008.10.008 |
| [20] |
黄凌云. 闪锌矿晶体结构性质及其铜活化作用[J]. 矿产保护与利用, 2018(3): 26-30. |
| [21] |
Sun S, Liu R, Song W. An electrochemical investigation on collectorless flotation of sphalerite in presence of Cu2+ ions[J]. Trans. nonferrous met. soc. China, 2000, 10(S1): 56-60. |
| [22] |
Ravitz S F, Wall W A. The adsorption of copper sulfate by sphalerite and its relation to flotation[J]. J. phys. chem., 2002, 38(1): 13-18. |
| [23] |
李宁.铜锌硫化矿浮选分离研究[D].长沙: 中南大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10533-1012477129.htm
|
| [24] |
聂光华, 李帅, 邱盛华. 某铁闪锌矿浮选试验研究[J]. 矿冶工程, 2012, 32(4): 44-47. DOI:10.3969/j.issn.0253-6099.2012.04.012 |
| [25] |
Buckley A N, Woods R, Wouterlood H J. An XPS investigation of the surface of natural sphalerites under flotation-related conditions[J]. International journal of mineral processing, 1989, 26(1-2): 29-49. DOI:10.1016/0301-7516(89)90041-0 |
| [26] |
Finkelstein N P. The activation of sulphide minerals for flotation: a review[J]. International journal of mineral processing, 1997, 52(2-3): 81-120. DOI:10.1016/S0301-7516(97)00067-7 |
| [27] |
Gerson A R, Lange A G, Prince K E, et al. The mechanism of copper activation of sphalerite[J]. Applied surface science, 1999, 137(1-4): 207-223. DOI:10.1016/S0169-4332(98)00499-1 |
| [28] |
Gu G, Wang D, Liu R. Electrochemical mechanisms on cupric sulphate activating sphalerite[J]. Journal of central south university of technology, 1999, 30(4): 374-377. |
| [29] |
Ejtemaei M, Nguyen A V. Characterisation of sphalerite and pyrite surfaces activated by copper sulphate[J]. Minerals engineering, 2017, 100: 223-232. DOI:10.1016/j.mineng.2016.11.005 |
| [30] |
Laskowski J S, Liu Q, Zhan Y. Sphalerite activation: flotation and electrokinetic studies[J]. Minerals engineering, 1997, 10(8): 787-802. DOI:10.1016/S0892-6875(97)00057-5 |
| [31] |
谢广元, 张明旭, 边炳鑫. 选矿学[M]. 徐州: 中国矿业大学出版社, 2001.
|
| [32] |
Chandra A P, Gerson A R. A review of the fundamental studies of the copper activation mechanisms for selective flotation of the sulfide minerals, sphalerite and pyrite[J]. Adv colloid interface sci, 2009, 145(1): 97-110. |
| [33] |
Boulton A B, Fornasiero D, Ralston J. Characterisation of sphalerite and pyrite flotation samples by XPS and ToF-SIMS[J]. International journal of mineral processing, 2003, 65(1): 205-219. |
| [34] |
Ralston O C, King C R, Tartaron F X. Copper sulfate as flotation activator for sphalerite[J]. Trans. AIME, 1930, 87: 389-400. |
| [35] |
Liu J, Zeng Y, Luo D, et al. Ab initio molecule dynamic simulation of Cu(OH)2 interaction with sphalerite (1 : 1 : 0) surface[J]. Minerals engineering, 2018, 122: 176-178. DOI:10.1016/j.mineng.2018.04.003 |
| [36] |
Fuerstenau D W, Metzger P H. Activation of sphalerite with lead ions in the presence of zinc salts[J]. Minerals engineering, 1960, 217: 119-123. |
| [37] |
Popov S R, Vuini D R, Kaanik J V. Floatability and adsorption of ethyl xanthate on sphalerite in an alkaline medium in the presence of dissolved lead ions[J]. International journal of mineral processing, 1989, 27(3-4): 205-219. DOI:10.1016/0301-7516(89)90065-3 |
| [38] |
Trahar W J, Senior G D, Heyes G W, et al. The activation of sphalerite by lead a flotation perspective[J]. International journal of mineral processing, 1997, 49(3-4): 121-148. DOI:10.1016/S0301-7516(96)00041-5 |
| [39] |
Pattrick R A D, Charnock J M, England K E R, et al. Lead sorption on the surface of ZnS with relevance to flotation: a fluorescence reflexafs study[J]. Minerals engineering, 1998, 11(11): 1025-33. DOI:10.1016/S0892-6875(98)00090-9 |
| [40] |
Steele H M, Wright K, Hillier I H. A quantum-mechanical study of the (110) surface of sphalerite (ZnS) and its interaction with Pb2+ species[J]. Physics and chemistry of minerals, 2003, 30(2): 69-75. DOI:10.1007/s00269-002-0296-9 |
| [41] |
Morey M S, Grano S R, Ralston J, et al. The electrochemistry of Pb Ⅱ activated sphalerite in relation to flotation[J]. Minerals engineering, 2001, 14(9): 1009-1017. DOI:10.1016/S0892-6875(01)00108-X |
| [42] |
Rashchi F, Sui C, Finch J A. Sphalerite activation and surface Pb ion concentration[J]. International journal of mineral processing, 2002, 67(1): 43-58. |
| [43] |
Sui C, Lee D, Casuge A, et al. Comparison of the activation of sphalerite by copper and lead[J]. Minerals engineering, 1999, 16(3): 53-61. |
| [44] |
Zhang Q, Rao S R, Finch J A. Flotation of sphalerite in the presence of iron ions[J]. Colloids & surfaces, 1992, 66(2): 81-89. |
| [45] |
童雄, 周庆华, 何剑, 等.铁闪锌矿的选矿研究概况[J]. 2006(6): 8-12.
|
| [46] |
Chen Y, Chen J, Guo J. A DFT study on the effect of lattice impurities on the electronic structures and floatability of sphalerite[J]. Minerals engineering, 2010, 23(14): 1120-1130. DOI:10.1016/j.mineng.2010.07.005 |
| [47] |
Ye C, Chen J, Lan L, et al. The influence of the impurities on the flotation behaviors of synthetic ZnS[J]. Minerals engineering, 2012, 27-28(1): 65-71. |
| [48] |
Liu J, Wang Y, Luo D, et al. Comparative study on the copper activation and xanthate adsorption on sphalerite and marmatite surfaces[J]. Applied surface science, 2018, 439: 263-271. DOI:10.1016/j.apsusc.2018.01.032 |
| [49] |
Chen Y, Chen J. The first-principle study of the effect of lattice impurity on adsorption of CN- on sphalerite surface[J]. Minerals engineering, 2010, 23(9): 676-684. DOI:10.1016/j.mineng.2010.04.002 |
| [50] |
SoleckiJ, 詹德俊. 铜离子对不同铁含量混合闪锌矿的活化作用[J]. 国外金属矿选矿, 1982(1): 19-22. |
| [51] |
Szczypa J, Solecki J, Komosa A. Effect of surface oxidation and iron contents on xanthate ions adsorption of synthetic sphalerites[J]. International journal of mineral processing, 1980, 7(2): 151-157. DOI:10.1016/0301-7516(80)90007-1 |
| [52] |
Scott J L, Smith R W. Calcium ion effects in amine flotation of quartz and magnetite[J]. Minerals engineering, 1993, 6(12): 1245-1255. DOI:10.1016/0892-6875(93)90102-S |
| [53] |
Liu Q, Zhang Y. Effect of calcium ions and citric acid on the flotation separation of chalcopyrite from galena using dextrin[J]. Minerals engineering, 2000, 13(13): 1405-1416. DOI:10.1016/S0892-6875(00)00122-9 |
| [54] |
Zhang W, Honaker R Q, Groppo J G. Flotation of monazite in the presence of calcite part Ⅰ: calcium ion effects on the adsorption of hydroxamic acid[J]. Minerals engineering, 2017, 100: 40-48. DOI:10.1016/j.mineng.2016.09.020 |
| [55] |
Ejtemaei M, Plackowski C, Nguyen A V. The effect of calcium, magnesium, and sulphate ions on the surface properties of copper activated sphalerite[J]. Minerals engineering, 2016, 89: 42-51. DOI:10.1016/j.mineng.2016.01.005 |
| [56] |
Lascelles D, Finch J A, Sui C. Depressant action of Ca and Mg on flotation of Cu activated sphalerite[J]. Canadian metallurgical quarterly, 2013, 42(2): 133-140. |
| [57] |
孙伟, 胡岳华, 邱冠周, 等. 闪锌矿(110)表面离子吸附的动力学模拟[J]. 中国有色金属学报, 2002, 12(1): 187-190. DOI:10.3321/j.issn:1004-0609.2002.01.037 |
| [58] |
Liu J, Wang Y, Luo D, et al. Use of ZnSO4, and SDD mixture as sphalerite depressant in copper flotation[J]. Minerals engineering, 2018, 121: 31-38. DOI:10.1016/j.mineng.2018.03.003 |
 2019
2019



