| 三元体系Rb+, Mg2+//SO42--H2O 298 K稳定相平衡研究 |
2. 攀西战略矿产资源综合利用四川省协同创新中心,四川 成都 610059;
3. 硫酸盐型盐湖资源综合利用青海省重点实验室,青海 格尔木 816000
2. Sichuan Collaborative Innovation Center of Panxi Strategic Mineral Resources Multipurpose Utilization, Chengdu 610059, China;
3. Qinghai Key Laboratory of Sulfate Salt Lakes Multipurpose Utilization, Golmud 816000, China
铷是一种重要的稀有碱金属,广泛地应用于国防、航空航天、基因工程、生物化学、能源、医药、环境科学等众多领域[1-4],被称为“空间时代金属”[5]。全球铷的总储量(不包括海水中的铷)约有1 077万t,其中92%以上(约1 000万t)存在于盐湖中[6]。由于盐湖卤水中多种碱(土)金属元素处于共存状态,离子间相互作用关系复杂,使得铷的提取分离困难。含铷体系相平衡与相图的研究可为盐湖卤水中铷的分离提取工艺制定提供科学依据。
从已有文献来看,目前有关含铷体系的相图研究主要集中在氯化物体系[8-11]和硼酸盐体系[12-15],而铷的硫酸体系鲜有报道[16-18]。本文开展了三元体系Rb+, Mg2+//SO42- - H2O 298 K稳定相平衡研究,探讨铷、镁硫酸盐共存时的盐类析出规律,为硫酸盐型卤水中铷、镁的提取分离提供基础热力学数据。
1 试验部分 1.1 试验试剂试验用水均为去离子水(pH=6.6,电导率 < 1 × 10-4 S·m-1);MgSO4·7H2O(AR,成都市科龙化工试剂厂);Rb2SO4(AR,江西东鹏新材料有限责任公司)。
1.2 仪器和设备恒温水浴振荡器(HZS - HA型,哈尔滨市东联电子技术开发有限公司);电子分析天平(BSA124S型,Sartorius科学仪器(北京)有限公司);阿贝折射仪(WYA型,上海精密仪器仪表有限公司);X-ray衍射仪(DX-2700型,丹东方圆仪器有限公司)。
1.3 试验方法该三元体系的相平衡研究采用等温溶解法。以298 K温度下单盐的溶解度数据为基础,按照一定梯度向其中一种盐的饱和溶液中加入另一种盐,配制试液于100 mL蓝玻瓶中。蓝玻瓶置于恒温水浴振荡器中,控制温度为298±0.5 K,充分振荡。定期取上层清液测定组分含量,当组分含量不变时体系达到平衡,静置。分别取液相和湿渣分析其化学组成,同时测定平衡液相的密度。平衡固相的组成用Schreinemakers湿渣法[19]确定,并且采用X - ray粉晶衍射法进行固相鉴定。
1.4 平衡液相及湿固相组成分析测定方法[20]Mg2+:EDTA容量法;
Rb+:四苯硼钠(STPB)-季胺盐(CTAB)返滴定法;
SO42-:BaCl2容量法。
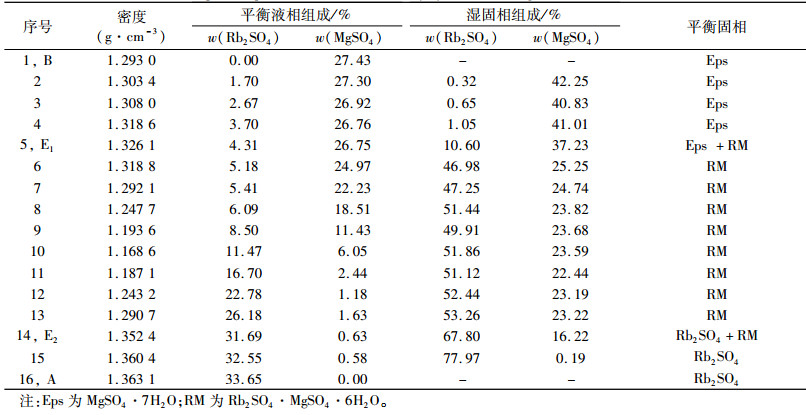
2 结果与讨论 2.1 三元体系Rb+, Mg2+//SO42- - H2O 298 K稳定相平衡试验结果试验测定的三元体系Rb+, Mg2+//SO42- - H2O 298 K下的平衡液相及湿固相组成、平衡液相的密度列于表 1,其中w(M)为M的质量分数,M为Rb2SO4或MgSO4。由表 1数据绘制了三元体系Rb+, Mg2+//SO42- - H2O 298 K的稳定相图及其局部放大图,见图 1。
| 表 1 三元体系Rb+, Mg2+//SO42- - H2O 298 K稳定相平衡数据 Table 1 Stable phase equilibrium data of the ternary system Rb+, Mg2+//SO42- - H2O at 298 K |
 |
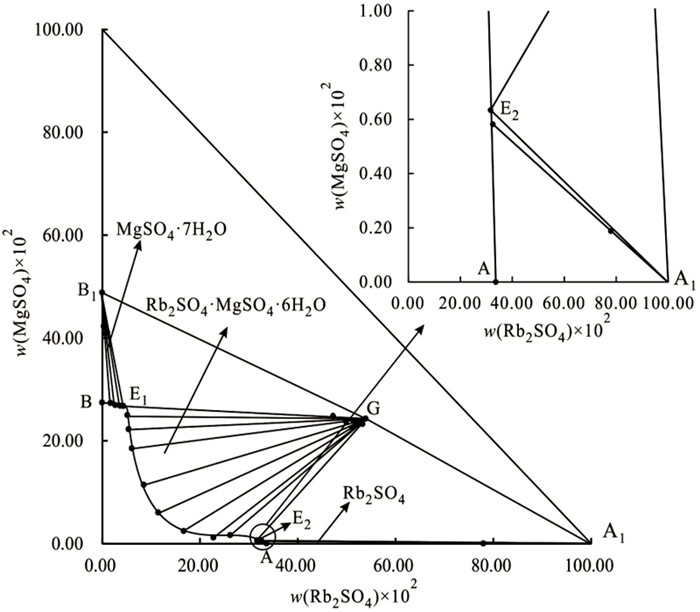 |
| 图 1 三元体系Rb+, Mg2+//SO42- - H2O 298 K稳定相图及其局部放大图 Fig.1 Stable phase diagram and partial enlarged drawing of the ternary system Rb+, Mg2+//SO42- - H2O at 298 K |
三元体系Rb+, Mg2+//SO42- - H2O在298 K时有复盐Rb2SO4·MgSO4·6H2O生成,是一个复杂体系。该体系稳定相图由2个三元共饱点(E1,E2),3条单变量曲线(E1B,E1E2,E2A)以及3个结晶区组成。3个结晶区分别对应于单盐MgSO4·7H2O、Rb2SO4和复盐Rb2SO4·MgSO4·6H2O的结晶区,结晶区大小依次为Rb2SO4·MgSO4·6H2O>MgSO4·7H2O>Rb2SO4。
共饱点E1,E2均为相称共饱点,它们对应的平衡固相盐的X射线粉晶衍射谱图分别见图 2和图 3。结果表明,共饱点E1处对应的平衡固相为MgSO4·7H2O + Rb2SO4·MgSO4·6H2O,液相组成为w(Rb2SO4)=4.31%,w(MgSO4)=26.75%;共饱点E2处对应的平衡固相为Rb2SO4 + Rb2SO4·MgSO4·6H2O,液相组成为w(Rb2SO4)=31.69%,w(MgSO4)=0.63%。
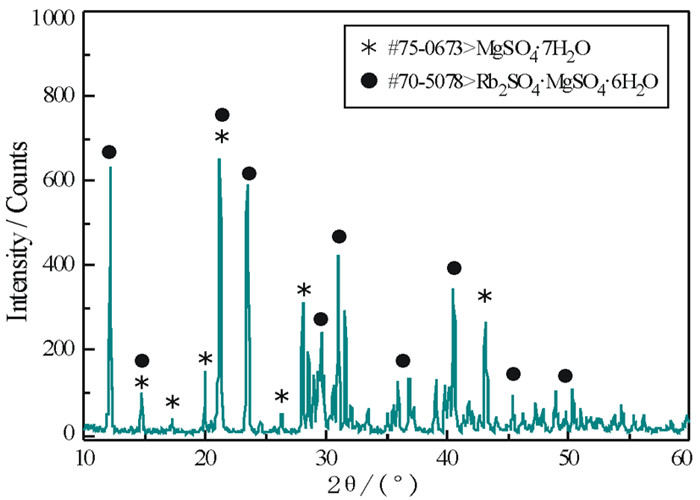 |
| 图 2 共饱点E1对应的平衡固相盐XRD图 Fig.2 XRD patterns of the solid phases corresponding to the invariant point E1 |
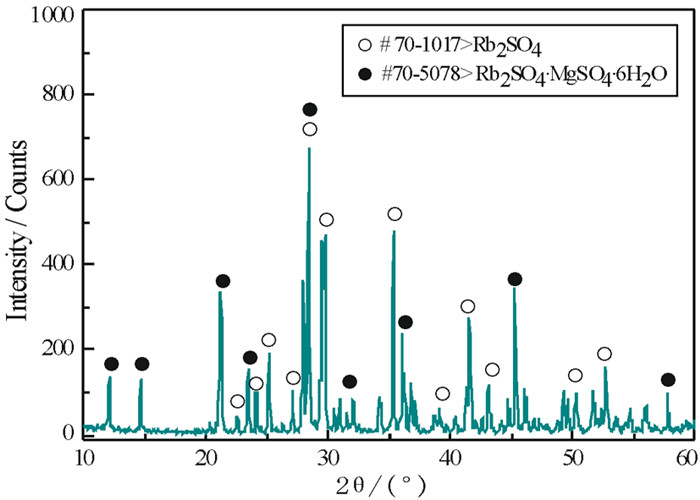 |
| 图 3 共饱点E2对应的平衡固相盐XRD图 Fig.3 XRD patterns of the solid phases corresponding to the invariant point E2 |
2.2 平衡液相密度的测定结果及计算
以w(Rb2SO4)为横坐标、密度为纵坐标,绘制了三元体系Rb+, Mg2+//SO42- - H2O 298 K密度-组成图,见图 4。由图 4可以看出,在单变量曲线BE1上,平衡溶液的密度随Rb2SO4质量分数的增大而增大。在单变量曲线E1E2上,随着Rb2SO4质量分数的增大,密度呈先减小后增大的趋势。E1点到密度最低点,MgSO4质量分数的降幅远大于Rb2SO4质量分数的增幅,MgSO4是影响平衡溶液密度变化的主要因素,因此溶液密度随MgSO4质量分数的减小而减小;同理,从密度最低点至E2点,Rb2SO4的质量分数的增幅大于MgSO4的质量分数的降幅,Rb2SO4是影响平衡溶液密度变化的主要因素,因此密度随Rb2SO4质量分数的增大而增大。在单变量曲线E2A上,平衡溶液的密度随Rb2SO4质量分数的增大而减小。
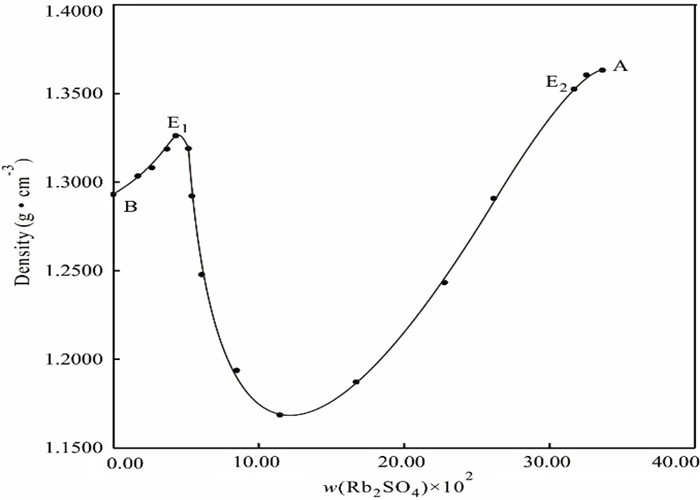 |
| 图 4 三元体系Rb+, Mg2+//SO42- - H2O 298 K密度-组成图 Fig.4 Density vs composition diagram of the ternary system Rb+, Mg2+//SO42- - H2O at 298 K |
基于溶液密度模型[21],用经验方程式(式1)计算了该三元体系平衡液相的密度ρn:
| $ \ln \frac{{{\rho _n}}}{{{\rho _0}}} = \sum {A_i} \times {w_i} $ | (1) |
其中,ρ0为相应温度下蒸馏水的密度,g/cm3,298 K时ρ0等于0.997 07 g/cm3;Ai为相应温度下体系中组分i的不变常数,在298 K时,Rb2SO4和MgSO4的不变常数分别为0.009 293和0.009 475;wi为组分i在平衡液相中的质量分数,%。
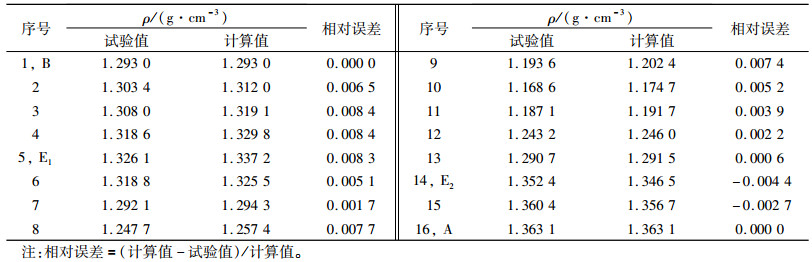
将平衡液相密度的计算值和试验值进行比较,结果列于表 2。对比发现,该三元体系平衡溶液密度的试验值和计算值吻合较好,相对误差均小于1%。
| 表 2 三元体系Rb+, Mg2+//SO42- - H2O 298 K密度的计算值和试验值的比较 Table 2 Comparison of the calculated and experimental values of density in the ternary system Rb+, Mg2+//SO42- - H2O at 298 K |
 |
3 结论
(1) 三元体系Rb+, Mg2+//SO42- - H2O在298 K时为复杂体系,有复盐Rb2SO4·MgSO4·6H2O生成。
(2) 三元体系Rb+, Mg2+//SO42- - H2O 298 K时的稳定相图由2个三元共饱点、3条单变量曲线和3个结晶区构成。3个结晶区的大小依次为:Rb2SO4·MgSO4·6H2O > MgSO4·7H2O > Rb2SO4。2个共饱点均为相称共饱点。
(3) 采用经验方程式对该体系平衡液相的密度进行了计算,计算值与试验值吻合良好,相对误差均小于1%。
| [1] |
Slobodin B V, Ishchenko A V, Samigullina R F, et al. Preparation and luminescent properties of rubidium and cesium vanadates[J]. Inorganic materials, 2014, 50(2): 179-183. DOI:10.1134/S0020168514020150 |
| [2] |
郭宁, 赵武壮, 任卫峰, 等. 铷铯行业开辟新纪元[J]. 中国有色金属, 2013(15): 44-45. |
| [3] |
刘昊, 刘亮明. 铷和铯的应用前景及其制约因素[J]. 南方国土资源, 2015(11): 31-33. DOI:10.3969/j.issn.1672-321X.2015.11.011 |
| [4] |
闫明, 钟辉, 张艳. 卤水中分离提取铷、铯的研究进展[J]. 盐湖研究, 2006, 14(3): 67-72. DOI:10.3969/j.issn.1008-858X.2006.03.013 |
| [5] |
陈尚清, 石健, 史振, 等. 溶剂萃取法从卤水中提取铷、铯研究进展[J]. 盐业与化工, 2017, 46(6): 45-49. |
| [6] |
冯光熙. 无机化学丛书:第一卷, 稀有气体、氢、碱金属[M]. 北京: 科学出版社, 2011.
|
| [7] |
牛自得, 程芳琴. 水盐体系相图及其应用[M]. 天津: 天津大学出版社, 2002.
|
| [8] |
陈杰, 曾英, 程兴龙, 等. 四元含锂铷氯化物水盐体系298.2 K介稳相平衡研究[J]. 四川大学学报(自然科学版), 2018, 3(579): 584. |
| [9] |
刘舟, 曾英, 于旭东. 三元体系Rb+//Cl-, Borate-H2O 348 K稳定相平衡研究[J]. 稀有金属, 2013, 37(1): 104-107. |
| [10] |
Zeng Y, Xie G, Wang C, et al. Stable phase equilibrium in the aqueous quaternary system Rb+, Mg2+//Cl-, borate-H2O at 323 K[J]. Journal of chemical & engineering data, 2016, 61(7): 2419-2425. |
| [11] |
Yin Q, Mu P, Tan Q, et al. Phase equilibria for the aqueous reciprocal quaternary system Rb+, Mg2+//Cl-, borate-H2O at 348 K[J]. Journal of chemical & engineering data, 2014, 59(7): 2235-2241. |
| [12] |
Li H, Liu L, Yu X, et al. The phase diagram and physicochemical properties of the quaternary system Li+, Rb+, Mg2+//borate-H2O at 348 K[J]. Russian journal of physical chemistry A, 2015, 89(9): 1572-1577. DOI:10.1134/S0036024415090149 |
| [13] |
Yan F, Yu X, Yin Q, et al. The solubilities and physicochemical properties of the aqueous quaternary system Li+, K+, Rb+//borate-H2O at 348 K[J]. Journal of chemical & engineering data, 2013, 59(59): 110-115. |
| [14] |
Duan X, Zeng Y, Luo J, et al. Stable phase equilibrium of aqueous quaternary system Li+, Rb+, Mg2+//borate-H2O at 298.2 K[J]. Journal of chemical engineering of Japan, 2017, 40(7): 470-475. |
| [15] |
Yu X, Zeng Y, Guo S, et al. Stable phase equilibrium and phase diagram of the quinary system Li+, K+, Rb+, Mg2+//borate-H2O at T=348.15K[J]. Journal of chemical & engineering data, 2016, 61(3): 1246-1253. |
| [16] |
F. Wang and B. Hu.Solubility prediction of RbCl-Rb2SO4-H2O system at 25℃ using pitzer ion-interaction model[J]. Russ. j. inorg. chem., 2010, 55(3): 441-443.
|
| [17] |
Kalinkin A M, Vasin S K, Antropova O V. Solubility diagram of (lithium sulfate + sodium sulfate + rubidium sulfate)(aq) at the temperature 29815 K[J]. J. chem. thermodyn., 1994, 26(1): 91-100. DOI:10.1006/jcht.1994.1024 |
| [18] |
Wang F Y. Thermodynamic simulation on Rb2SO4-CS2SO4-MgSO4-H2O system at 25℃[J]. Asian j. chem., 2013, 25(13): 7631-7632. DOI:10.14233/ajchem |
| [19] |
宋彭生. 湿渣法在水盐体系相平衡研究中的应用[J]. 盐湖研究, 1991(1): 15-23. |
| [20] |
中国科学院青海盐湖研究所分析室. 卤水和盐的分析方法[M]. 北京: 科学出版社, 1988.
|
| [21] |
房春晖. 一个预测盐湖卤水密度的新的理论模型:盐湖化学基础理论研究之一[J]. 盐湖研究, 1990(2): 15-20. |
 2019
2019



