| t-BAMBP从萃铯余液中分离提取铷的工艺研究 |
2. 稀土稀有稀散矿产勘查及综合利用重点实验室,湖北 武汉 430034
2. Rare Mineral Exploration and Utilization Key Laboratory, Wuhan 430034, China
铷是一种非常活泼的稀有碱金属,不仅在传统的电子器件、催化剂及特种玻璃等领域应用广泛,而且在新能源、航空航天等高科技领域显示出极大的应用前景[1-3]。铷作为分散元素,至今仍未发现单纯的铷矿,而是以伴生状态赋存于锂云母、铯榴石、铯锂云母、光卤石、钾长石、盐湖卤水、地热水及海水中[4-5]。由于没有独立的铷矿可以直接利用,从浸出液和卤水中回收是获取铷的主要方式。从溶液中分离提纯铷的关键是去除其中性质极为相似的锂、钾、钠元素[6]。
目前,溶剂萃取是从低含量铷溶液中分离富集铷的主要工业方法,常用的萃取剂为4-叔丁基-2-(α-甲苄基)苯酚(t-BAMBP)。t-BAMBP是一种弱酸性取代苯酚萃取剂,已工业化生产,萃取性能优异,价格较便宜,被广泛用于铷、铯、钾的分离研究[7-10]。通城铷矿为一大型稀有金属矿,Rb2O品位为0.05%,Cs2O品位为0.021%,铷主要赋存在云母和长石中。对该矿采用“氯化焙烧—浸出”工艺提取铷,得到低含量的铷铯浸出液。该浸出液采用t-BAMBP+二甲苯体系进行萃铯洗铷试验,铯96.82%在有机相中,铷88.27%留在水相中,铷铯得到了较好的分离。本次试验溶液为萃铯洗铷之后的萃余液,该溶液铷含量低,钾钠含量较高,碱度(OH-)高,铷与钾钠分离难度大。本次试验以t-BAMBP+二甲苯的萃取体系,对萃铯余液中的铷进行萃取分离研究。
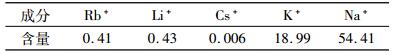
1 试验 1.1 原料、试剂及仪器原料取自通城铷矿萃铯余液,主要化学成分见表 1。
| 表 1 萃铯余液主要成分 /(g·L-1) Table 1 Main content of cesium raffinate |
 |
试剂:t-BAMBP(纯度大于90%,北京瑞乐康分离科技有限公司);二甲苯(纯度大于99%,天津天力化学试剂有限公司);氢氧化钠(分析纯,国药集团化学试剂有限公司)。
仪器:250 mL梨形分液漏斗、康氏振荡器。
1.2 试验原理t-BAMBP是一种弱酸性取代苯酚萃取剂,在碱性条件下苯酚上的羟基解离出H+与被萃取碱金属离子M+以离子形式进行交换,生成疏水性酚酸盐,元素M+进入有机相。由于萃取剂t-BAMBP对碱金属离子的萃取难易程度不同,从而实现铷与其他伴生离子的萃取分离。t-BAMBP萃取碱金属的先后顺序依次为铯、铷、钾、钠,其反应为[11-12]:
| $ {\rm{M}}_{{\rm{(a)}}}^{\rm{ + }}{\rm{ + }}n{\rm{RO}}{{\rm{H}}_{{\rm{(o)}}}}{\rm{ = }}{\left[ {{\rm{MOR}} \cdot \left( {n{\rm{ - 1}}} \right){\rm{ROH}}} \right]_{{\rm{(o)}}}}{\rm{ + H}}_{{\rm{(a)}}}^{\rm{ + }} $ | (1) |
试验方法:设置好萃取条件,将萃取有机相和被萃水相置于250 mL分液漏斗中,在振荡器上振荡一定时间,取出静置直至完全分层;待两相分层完全后分相,分析萃余水相中金属离子浓度,用差减法求出有机相中金属离子浓度。金属离子的萃取率和分离系数计算公式分别为[13]:
| $ E = 100\% - \frac{{{C_a}{V_a}}}{{CV}} \times 100\% $ | (2) |
| $ {\beta _{A/B}} = \frac{{{{[{C_A}]}_0}/{{[{C_A}]}_a}}}{{{{[{C_B}]}_0}/{{[{C_B}]}_a}}} $ | (3) |
其中:Ca-水相中金属离子平衡总浓度,g/L;C0-有机相中金属离子平衡总浓度,g/L;C-萃原液中金属离子浓度,g/L。Va-平衡后金属离子的水相体积,L;V-萃原液体积,L。
2 结果与讨论 2.1 料液碱度对萃取效果的影响t-BAMBP为弱酸性萃取剂,萃取分离铷、钾需在碱性介质中进行[14]。用NaOH调节料液碱度(OH-),研究料液碱度对铷钾萃取率和分离系数的影响。有机相中t-BAMBP的体积分数为30%,萃取相比为VO/VA=3/1,萃取时间为3 min。料液碱度试验结果如图 1所示。
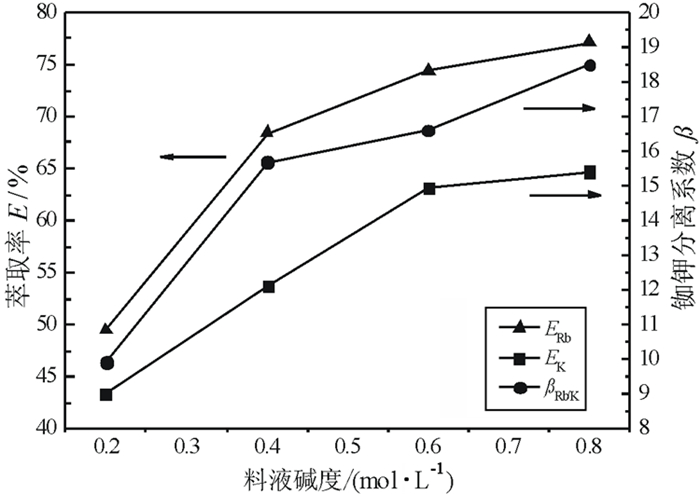 |
| 图 1 料液碱度对铷钾萃取效果的影响 Fig.1 Influence of feed alkalinity on rubidium and potassium extraction |
从图 1可以看出, 料液碱度对铷、钾的萃取率有显著的影响,随着料液碱度的提高,铷、钾的萃取率先快速上升,后逐渐趋于平缓。铷的萃取率随着料液碱度的提高而迅速上升; 当料液碱度C(OH-)>0.4 mol/L后,铷的萃取率逐渐趋于稳定。钾的萃取率随着料液碱度的增加而迅速提高; 当料液碱度C(OH-)>0.6 mol/L后,钾的萃取率逐渐趋于平缓。铷钾分离系数随着料液碱度的提高而迅速上升,当料液碱度C(OH-)>0.4 mol/L后,铷钾分离系数逐渐趋于平缓。因此,从铷钾的分离效果并结合提高料液碱度所需的成本,选择料液碱度为0.4 mol/L。
2.2 萃取剂浓度对萃取效果的影响料液碱度为0.4 mol/L,萃取相比为VO/VA=3 : 1,萃取时间为3 min,考察t-BAMBP+二甲苯体系中萃取剂浓度对铷、钾萃取效果的影响。萃取剂浓度试验结果如图 2所示。
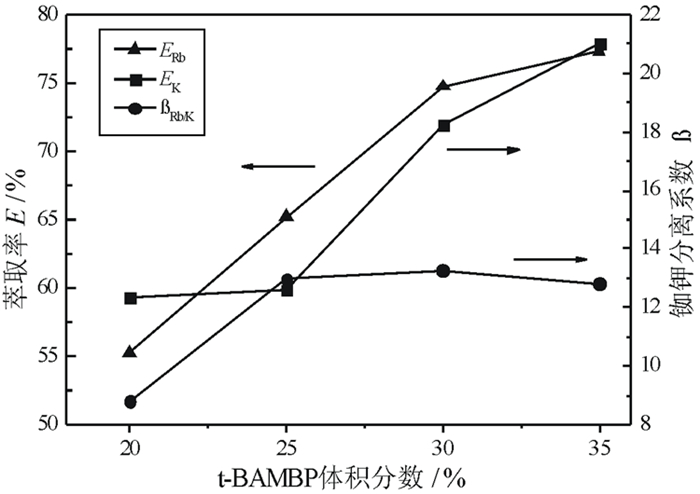 |
| 图 2 萃取剂浓度对铷钾萃取效果的影响 Fig.2 Influence of extractant concentration on rubidium and potassium extraction |
从图 2可以看出, 萃取剂浓度对铷、钾的萃取率有显著的影响,随着有机相中t-BAMBP体积分数的增大,铷、钾的萃取率迅速提高;当t-BAMBP体积分数大于30%,继续增加萃取剂浓度,铷、钾的萃取率增大趋势趋于平缓。铷钾的分离系数随着萃取剂浓度的增加迅速增大,当t-BAMBP体积分数大于25%后,铷钾的分离系数增大趋于平缓,而后有小幅度下降。因此,考虑铷、钾的萃取分离效果和萃取剂成本,选择有机相中t-BAMBP体积分数为30%。
2.3 萃取时间对萃取效果的影响调节分液漏斗的振荡时间,考察萃取反应时间对铷钾分离效果的影响。t-BAMBP体积分数为30%,料液碱度为0.4 mol/L,萃取相比为VO/VA=3 : 1。萃取时间试验结果如图 3所示。
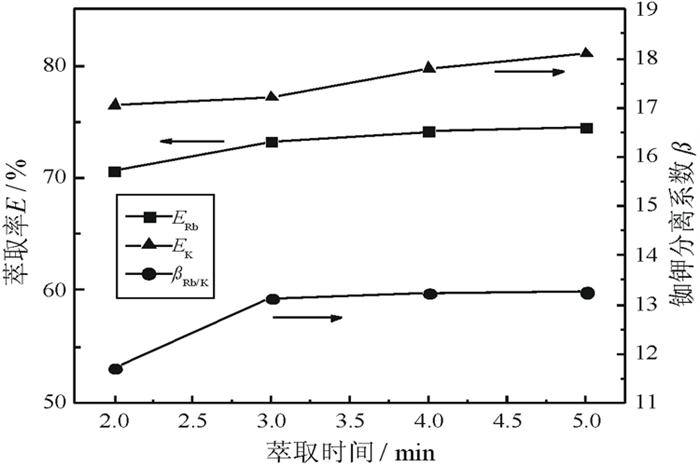 |
| 图 3 萃取时间对铷钾萃取效果的影响 Fig.3 Influence of extraction time on rubidium and potassium extraction |
从图 3可以看出, 萃取时间对铷、钾的萃取率影响较小,随着萃取时间的增加,铷、钾的萃取率先小幅增加,后逐渐趋于平缓。当萃取时间小于3 min时,铷钾分离系数增加明显,当萃取时间超过3 min后,铷钾分离系数不再增加。因此,考虑铷钾分离效果和萃取成本,选择萃取时间为3 min。
2.4 萃取相比对萃取效果的影响控制有机相和水相的体积,得到不同的萃取相比,考察萃取相比的变化对铷钾萃取效果的影响。t-BAMBP体积分数为30%,料液碱度为0.4 mol/L,常温下萃取3 min。萃取相比试验结果如图 4所示。
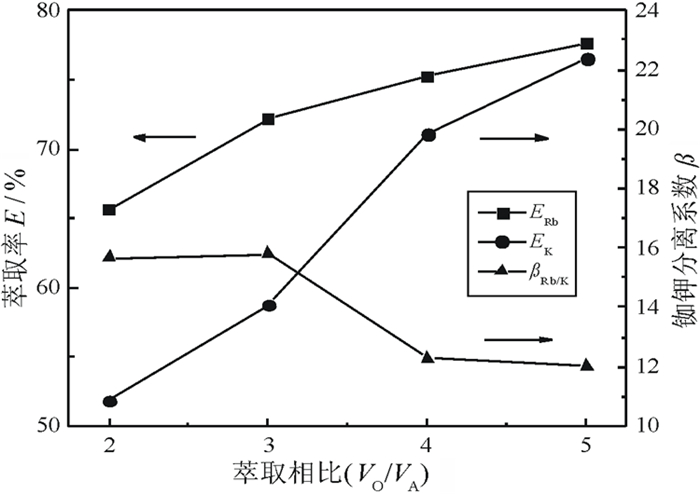 |
| 图 4 萃取相比对铷钾萃取效果的影响 Fig.4 Influence of phase ration on rubidium and potassium extraction |
从图 4可看出, 萃取相比对铷、钾的萃取率有显著的影响,随着萃取相比的增大,铷、钾的萃取率都是逐渐增加。当萃取相比VO/VA>3时,铷的萃取率增加趋缓;而此时,钾的萃取率有较大的增长趋势。当萃取相比VO/VA>4时,钾的萃取率增加趋势变得平缓。铷钾分离系数随着萃取相比的增加逐渐减小,当萃取相比VO/VA>3时,铷钾分离系数降低明显。当萃取相比VO/VA=3时,有机相有较高的萃铷能力,且钾的萃取率较低,铷钾分离系数较大。因此,选择萃取相比为VO/VA=3。
2.5 多级分馏萃取模拟试验在料液碱度为0.4 mol/L、有机相中t-BAMBP体积分数为30%、萃取相比VO/VA=3 : 1、洗涤液为0.1 mol/L NaOH溶液、洗涤相比VO’/VA’=4 : 1、常温萃取3 min的条件下,对料液进行四级萃取四级洗涤萃取模拟试验,试验萃铷余液中Rb+的浓度为12.6 mg/L,Rb的萃取率为94.6%。
| 表 2 铷萃余液主要成分 /(g·L-1) Table 2 Main content of rubidium raffinate |
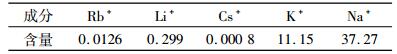 |
以1 mol/L盐酸溶液为反萃剂,对含铷有机相进行3级逆流反萃,有机相与水相的相比为5 : 1,单级反萃取时间为5 min,逆流反萃试验结果见表 3。
| 表 3 逆流反萃试验结果 /(mg·L-1) Table 3 Test results of rubidium counter-current extraction |
 |
铷有机相用1 mol/L盐酸反萃,在相比VO/VA=5 : 1时,经三级逆流反萃,反萃率为91.04%。
由于萃铯余液中钾钠含量较高,经过一轮萃取反萃试验后,还有少量的钾钠残留在反萃液中,使铷的纯度降低。铷反萃液进行新一轮的萃取反萃试验,可进一步提高反萃液中铷的浓度,降低杂质离子含量,提高铷盐的纯度。
3 结论(1) 在料液碱度为0.4 mol/L、有机相中t-BAMBP体积分数为30%、萃取相比VO/VA=3 : 1、洗涤相比VO’/VA’=4 : 1、常温萃取3 min的条件下,对含铷萃铯余液进行四级萃取四级洗涤萃取模拟试验,Rb的萃取率达94.6%。
(2) 铷有机相用1 mol/L盐酸反萃,在相比VO/VA=5 : 1时,经三级逆流反萃,反萃率为91.04%,铷钾得到了较好的分离。
(3) t-BAMBP+二甲苯体系对低浓度含铷萃铯余液有较好的萃取分离提铷效果。铷反萃液进行新一轮的萃取反萃试验,可进一步提高反萃液中铷的浓度,降低杂质离子含量,为得到高纯度铷盐提供了技术依据。
| [1] |
曹冬梅, 张雨山, 高春娟, 等. 提铷技术研究进展[J]. 盐业与化工, 2011, 40(5): 44-47. |
| [2] |
廖元双, 杨大锦. 铷的资源和应用及提取技术现状[J]. 云南冶金, 2012, 41(4): 27-30. DOI:10.3969/j.issn.1006-0308.2012.04.007 |
| [3] |
黄东方, 郑红, 宝阿敏, 等. t-BAMBP/磺化煤油萃取体系从盐湖卤水中萃取铷的动力学研究[J]. 盐湖研究, 2017, 25(1): 49-56. |
| [4] |
曹耀华, 高照国, 王守敬, 等. 从某难选铷矿石中提取铷[J]. 金属矿山, 2011, 5(12): 83-87. |
| [5] |
刘丹.花岗岩黑云母中铷的提取工艺研究[D].长春: 吉林大学, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10183-1014270798.htm
|
| [6] |
Jiawei Wang, Dehua Che, Wei Qin. Extraction of rubidium by t-bambp in cyclohexane[J]. Chinese journal of chemical engineering, 2015, 23(7): 1110-1113. DOI:10.1016/j.cjche.2015.04.005 |
| [7] |
王威, 曹耀华, 高照国, 等. 铷、铯分离提取技术研究进展[J]. 矿产保护与利用, 2013(4): 54-58. DOI:10.3969/j.issn.1001-0076.2013.04.014 |
| [8] |
蒋颖, 胡启阳, 李新海, 等. 合成副产物对t-BAMBP萃取铷铯的影响[J]. 稀有金属, 2015, 39(4): 343-349. |
| [9] |
杨少华, 赖晓晖, 王君, 等. t-BAMBP萃取分离高钾钠卤水中的铷工艺研究[J]. 有色金属科学与工程, 2015, 6(5): 17-21. |
| [10] |
尤志刚, 王舒娅, 李波, 等. t-BAMBP萃取微量铷的基础研究[J]. 化学试剂, 2015, 37(2): 161-164. |
| [11] |
Zheng li, Yoko Pranolo, Zhaowu Zhu, et al. Solvent extraction of cesium and rubidium from brine solutions using 4-tert-butyl-2-(α-methylbenzyl)-phenol[J]. Hydrometallurgy, 2017, 171: 1-7. DOI:10.1016/j.hydromet.2017.03.007 |
| [12] |
LIU Shiming, LIU Hehui, HUANG Yunning, et al. Solvent extraction of rubidium and cesium from salt lake brine with t-bambp-kerosene solution[J]. Transactions of nonferrous metals society of China, 2015, 25(1): 329-334. DOI:10.1016/S1003-6326(15)63608-1 |
| [13] |
黄礼煌. 化学选矿:第2版[M]. 北京: 冶金工业出版社, 2012: 156.
|
| [14] |
杨锦瑜, 古映莹, 钟世安, 等. 以t-BAMBP萃取分离铷钾的研究[J]. 有色金属, 2008, 60(2): 55-58. |
 2018
2018 
