| 氟化钙在磷酸铵-氨水溶液中的溶解行为研究 |
2. 崇义章源钨业有限公司,江西 赣州 341000
2. Chongyi Zhangyuan Tungsten Co., Ltd, Ganzhou 341000, China
目前,白钨矿已成为我国钨冶炼工业的主要原料[1-4].目前,我国大多数钨冶炼企业采用氢氧化钠分解-强碱性阴离子树脂交换-蒸发结晶工艺处理白钨矿制备仲钨酸铵[5-7].由于白钨矿氢氧化钠浸出液中WO3浓度较高([WO3]≈300g/L), 为了满足获得较高的树脂吸附容量,需要把浸出液中WO3浓度稀释至20g/L左右(约稀释15倍),从而在离子交换过程中产生了大量含钠盐的碱性废水[8].我国钨冶炼企业年排放废水2400万m3,其中含烧碱4.16×105t、氨氮3.16×105t,冶炼废水排放造成严重的环境污染[9, 10].2008年国家环保部发布规定钨冶炼为一类元素排放废水,要求实现零排放.
鉴于此,国内钨冶炼科技工作者对白钨冶炼进行了科技攻关,获得了多项喜人的科研成果.赵中伟等[11]采用磷酸-硫酸混酸分解白钨矿,钨以磷钨杂多酸进入浸出液,经结晶磷钨杂多酸分离钨后返回白钨矿浸出工序,从而实现了冶炼废水的循环利用.张贵清等[12]采用碳酸根型季铵盐萃取剂从白钨矿苏打浸出液中萃取钨,含有碳酸根的萃余液返回浸出工序,实现了白钨矿高压浸出和碱性萃取2个工序内部水的循环利用.李小斌等[13]将钨矿物原料和矿化剂氟化钙配料后进行焙烧,焙砂经碳酸铵溶液浸出得到粗钨酸铵溶液,经除杂后蒸发结晶制得仲钨酸铵(APT)产品, 蒸发结晶过程产生的结晶母液、氨气和二氧化碳气体可返回至焙砂浸出工序,冶炼过程无废水排放.
江西理工大学[14]发明了“铵盐体系白钨绿色冶炼工艺”,采用磷酸铵-氨水-氟化钙协同高压分解白钨矿生成氟磷酸钙沉淀(见反应方程式1),并一步制得粗钨酸铵溶液,经净化除杂后,蒸发结晶得到APT产品,结晶母液和氨尾气返回白钨浸出过程,实现了白钨冶炼废水零排放.
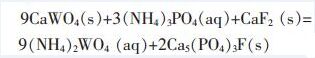
|
(1) |
白钨浸出过程中,氟化钙作为唯一的氟源,其先在溶液中反应释放出游离的氟离子,再与磷酸根离子一起与白钨发生化学反应(见反应方程式2),生成钨酸铵和氟磷酸钙沉淀,因此,氟化钙的溶解与白钨的浸出效果密切相关.

|
(2) |
白钨浸出实验中也发现,氟化钙的用量对白钨浸出率影响很大.为此,重点研究了氟化钙在磷酸铵-氨水混合溶液中的溶解行为,考察磷酸铵用量、氨水用量、温度、液固比等工艺参数对氟化钙浸出率的影响,以期为白钨的浸出优化提供指导.
1 实验 1.1 化学试剂本实验所采用的氟化钙、磷酸铵、氨水和测定氟浓度所需的分析试剂均为分析纯,所用水为去离子水.
1.2 实验方法将预先配置成不同浓度的磷酸铵和氨水混合溶液加入高压釜中,然后再加入一定量的氟化钙,升温至预设温度,开始计时.当反应一定的时间后,取样分析浸出液中氟离子浓度,从而计算出氟化钙的浸出率.另外,对不同反应时间的浸出渣进行XRD分析.
本研究采用氟离子选择性电极测定浸出液中的氟离子浓度.
2 结果与讨论 2.1 磷酸铵用量对氟化钙浸出率的影响实验条件:氟化钙重量为5g,氨水浓度为3mol/L,浸出温度为180℃,液固比为50∶1,搅拌速率450r/min,保温时间为180min,磷酸铵用量分别为理论量的5、10、15、20、25、30倍.氟化钙浸出率曲线如图 1所示.
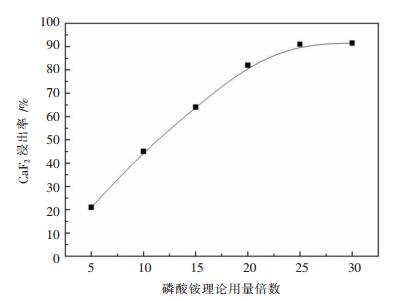 |
| 图 1 磷酸钠用量对氟化钙浸出率影响 |
从图 1可知,磷酸钠用量对氟化钙浸出率的影响非常大.当磷酸铵用量从理论量的5倍上升至25倍时,氟化钙浸出率由21%上升到91%,继续增加磷酸铵用量氟化钙浸出率变化不大.本实验采用了较大的液固比(50∶1),这主要是考虑到白钨浸出过程中氟化钙理论摩尔量仅为白钨理论摩尔量的1/9,而白钨浸出过程液固比约为3∶1,因此,浸出液质量相比于氟化钙质量比值很大.在高液固比(50∶1)条件下,当磷酸铵用量为理论量5倍时,溶液中磷浓度较低(仅约为32g/L),从而氟化钙浸出率较低;当磷酸铵用量增大至理论量20倍时,溶液中磷浓度高达119g/L,因此,氟化钙浸出率急剧上升.由此可见,增大磷酸铵浓度有利于氟化钙的溶出.
2.2 氨水浓度对氟化钙浸出率的影响实验条件:氟化钙重量为5g,磷酸铵用量为理论量的25倍,浸出温度为180℃,液固比为50∶1,搅拌速率450r/min,保温时间为180min,氨水浓度为0~7mol/L倍.氟化钙浸出率曲线如图 2所示.
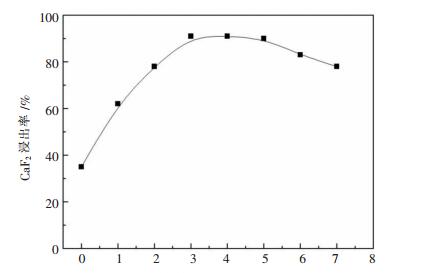 |
| 图 2 氨水浓度对氟化钙浸出率影响 |
由图 2可知,氨水浓度对氟化钙浸出率也具有重要的影响.与磷酸铵用量对氟化钙浸出作用规律不同,当氨水浓度从0增大至4mol/L时,氟化钙浸出率由35.2%上升至91.4%,当氨水浓度进一步增大至7mol/L时,氟化钙浸出率反而下降至78.2%.氨水在浸出过程中主要用于维持一定的pH值,使得溶液中的磷以PO43-形态存在,从而有利于氟化钙的分解.众所周知,磷在溶液中的存在形态与pH密切相关.当氨水浓度较低时(小于1mol/L),溶液pH偏低,磷可能主要以H2PO4-和HPO42-存在,因此,氟化钙的浸出率较低.但当氨水浓度过高时(>5mol/L),氨水对磷酸铵表现出明显的溶析效应[15],即氨水浓度过高会使得磷酸铵从溶液中结晶析出,使得溶液中磷浓度降低,因此,氟化钙浸出率也随之下降.由此可见,氨水浓度过低或过高均不利于氟化钙的浸出,较为合适的氨水浓度为3~5mol/L.
2.3 温度对氟化钙浸出率的影响实验条件:氟化钙重量为5g,磷酸铵用量为理论量的25倍,氨水浓度为3mol/L,液固比为50∶1,搅拌速率450r/min,保温时间为180min,浸出温度分别为120℃、140℃、160℃、180℃、200℃.氟化钙浸出率曲线如图 3所示.
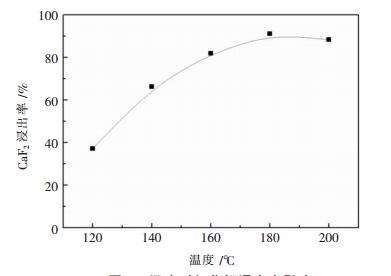 |
| 图 3 温度对氟化钙浸出率的影响 |
由图 3可知,氟化钙浸出率受温度影响很大.当温度由120℃上升至180℃时,氟化钙浸出率由37.1%上升至91.1%,但当温度继续上升至200℃时,氟化钙浸出率略微下降至88.3%.在一定程度上,升高温度有利于氟化钙的浸出.但当温度过高(>180℃)时,氨气会大量挥发进入气相,从而使溶液中的氨浓度下降,不利于氟化钙的浸出,另一方面,浸出液中的氟也易以HF挥发进入气相中,也会使得测定出的氟化钙浸出率下降.因而,有利于氟化钙浸出的温度为180℃.
2.4 保温时间对氟化钙浸出率的影响实验条件:氟化钙重量为5g,磷酸铵用量为理论量的25倍,氨水浓度为3mol/L,液固比为50∶1,搅拌速率450r/min,浸出温度为180℃,保温时间分别为30min、60min、120min、180min、240min.氟化钙浸出率曲线如图 4所示.
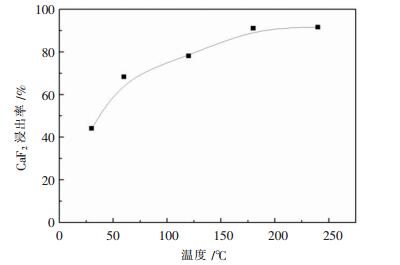 |
| 图 4 温度对氟化钙浸出率的影响 |
由图 4可知,随着浸出时间的延长,氟化钙浸出率逐渐增大.但当保温时间达到180min时,保温时间增大,氟化钙浸出率基本保持不变.从图 5和图 6也可以看出,对比保温时间30min和180min浸出渣的XRD图,浸出时间增大,反应物氟化钙的衍射峰减弱,而产物氟磷酸钙的衍射峰增强,表明氟化钙逐渐与磷酸铵逐渐反应生成氟磷酸钙.因此,较为合适的保温时间为180min.
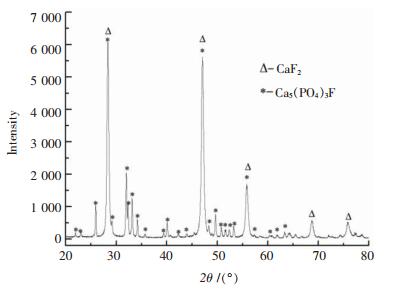 |
| 图 5 保温时间30分钟浸出渣的XRD谱 |
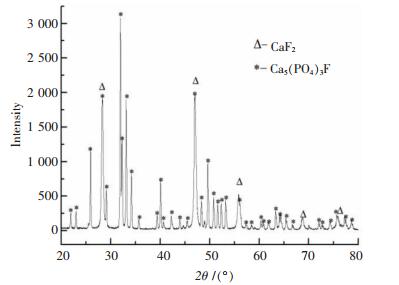 |
| 图 6 保温时间180分钟浸出渣的XRD谱 |
实验条件:氟化钙重量为5g,磷酸铵用量为理论量的25倍,氨水浓度为3mol/L,搅拌速率450r/min,浸出温度为180℃,保温时间为180min,液固比分别为30∶1、40∶1、50∶1、60∶1、70∶1,氟化钙浸出率曲线如图 7所示.
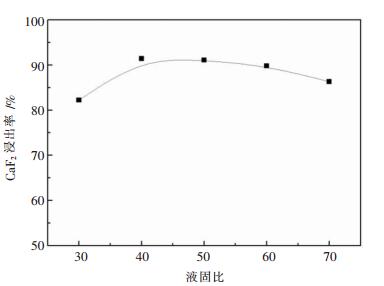 |
| 图 7 温度对氟化钙浸出率的影响 |
从图 7可以看出,氟化钙浸出率随液固比增大,呈现出先增大后减小的规律.由液固比由30∶1增大至50∶1时,氟化钙浸出率由82.2%上升至91.1%;继续增大液固比至70∶1时,浸出率则下降至86.3%.当液固比相对较小(30∶1)时,磷酸铵用量为定值,因而,磷酸铵浓度相对较高,由于氨水对磷酸铵具有溶析效应,会使得磷酸铵从溶液中结晶析出,相当于降低了磷酸铵用量,因此,氟化钙浸出率偏低.当液固比过大(70∶1)时,溶液中磷酸铵浓度下降,因而也使得氟化钙浸出率下降.综合考虑,较为适合的液固比为40∶1~50∶1.
3 结论本研究考察了氟化钙在磷酸铵和氨水混合溶液中的溶出规律.磷酸铵用量、氨水浓度和反应温度对氟化钙的浸出率影响非常显著.当磷酸铵用量为理论量的25倍、氨水浓度为3mol/L、温度为180℃、液固比为50∶1以及保温时间为180min时,氟化钙浸出率达到91.1%.浸出渣的XRD分析表明,反应产物为氟磷酸钙.
| [1] |
赵中伟, 李江涛, 陈星宇, 等. 我国白钨矿钨冶炼技术现状及发展[J]. 有色金属科学与工程, 2013, 4(5): 12-14. |
| [2] |
夏庆霖, 汪新庆, 刘壮壮, 等. 中国钨矿成矿地质特征与资源潜力分析[J]. 地学前缘, 2018, 25(3): 50-57. |
| [3] |
YANG X S. Beneficiation studies of tungsten ores-A review[J]. Minerals Engineering, 2018, 125: 111-119. DOI:10.1016/j.mineng.2018.06.001 |
| [4] |
GAO Y S, GAO Z Y, SUN W, et al. Selective flotation of scheelite from calcite: A novel reagent scheme[J]. International Journal of Mineral Processing, 2016, 154: 10-15. DOI:10.1016/j.minpro.2016.06.010 |
| [5] |
CHEN M, LI Z, LI X W, et al. Mechanochemically extracting tungsten through caustic processing of scheelite by controlling calcium dissolution[J]. International Journal of Refractory Metals and Hard Materials, 2016, 58: 211-215. DOI:10.1016/j.ijrmhm.2016.04.005 |
| [6] |
HUO G H, PENG C, SONG Q, et al. Tungsten removal from molybdate solutions using ion exchange[J]. Hydrometallurgy, 2014, 147/148: 217-222. DOI:10.1016/j.hydromet.2014.05.015 |
| [7] |
李停停, 钟祥熙, 张威, 等. 白钨矿浸出工艺现状及发展趋势[J]. 金属矿山,, 2017, 10:-128-133. |
| [8] |
ZHAO Z W, HU F, HU Y J, et al. Adsorption behaviour of WO42- onto 201×7 resin in highly concentrated tungstate solutions[J]. International Journal of Refractory Metals and Hard Materials, 2010, 28(5): 633-637. DOI:10.1016/j.ijrmhm.2010.04.005 |
| [9] |
万林生, 邓登飞, 赵立夫, 等. 钨绿色冶炼工艺研究方向和技术进展[J]. 有色金属科学与工程, 2013, 4(5): 15-18. |
| [10] |
何利华, 赵中伟, 杨金洪. 新一代绿色钨冶金工艺—白钨硫磷混酸协同分解技术[J]. 中国钨业, 2017, 32(3): 49-52. |
| [11] |
LI J T, ZHAO Z W. Kinetics of scheelite concentrate digestion with sulfuric acid in the presence of phosphoric acid[J]. Hydrometallurgy, 2016, 163: 55-60. DOI:10.1016/j.hydromet.2016.03.009 |
| [12] |
ZHANG G Q, GUAN W J, XIAO L S, et al. A novel process for tungsten hydrometallurgy based on direct solvent extraction in alkaline medium[J]. Hydrometallurgy, 2016, 165: 233-237. DOI:10.1016/j.hydromet.2016.04.001 |
| [13] |
LI X B, XU X M, ZHOU Q S, et al. Thermodynamic and XRD analysis of reaction behaviors of gangue minerals in roasting mixture of scheelite and calcium carbonate for Ca3WO6 preparation[J]. International Journal of Refractory Metals and Hard Materials, 2016, 60: 82-91. DOI:10.1016/j.ijrmhm.2016.07.007 |
| [14] |
WAN L S, YANG L, CHEN Y M, et al. Synthesis of scheelite with wolframite and calcium carbonate by a direct solid-state synthesis route[J]. International Journal of Refractory Metals and Hard Materials, 2015, 48: 301-304. DOI:10.1016/j.ijrmhm.2014.09.023 |
| [15] |
杨亮, 万林生, 舒柳飞. (NH4)3PO4-NH3·H2O-H2O 体系中磷酸铵溶解度[J]. 有色金属科学与工程, 2016, 7(2): 39-42. |
 2019, Vol. 39
2019, Vol. 39


