| 精炼渣钙铝比对铈处理钢中夹杂物的影响 |
低合金高强钢(HSLA)广泛应用于桥梁、核电、军工、风电和压力容器等领域[1-2],因此,对低合金高强钢的冲击韧性和疲劳强度的要求越来越高,冲击韧性和疲劳强度受非金属夹杂物成分、形状和尺寸的影响显著[3]。在铝镇静钢中,常见的夹杂物为Al2O3和MgO·Al2O3尖晶石夹杂物。该类夹杂物通常呈棱角状,硬度高,在钢中容易产生裂纹缺陷,因此,生产过程中应尽量避免出现此类夹杂物[4-6]。有学者研究了钙对氧化铝和镁铝尖晶石夹杂物的改性,并建立了不同的氧化铝夹杂物改性模型[7-9]。
在钢中添加稀土元素的作用(脱氧、脱硫、夹杂物改性和微合金化等)已受到广泛关注[10-12]。近年来,改善焊接性能的稀土氧化物冶金技术已成为研究的热点课题[13]。但在相关研究中,对稀土加入后氧化物夹杂物的演变过程研究较多[14-17],而有关精炼渣对钢中稀土夹杂物影响的研究较少,且这些研究均倾向于研究渣中添加稀土氧化物后对渣物理化学性质和钢中夹杂物的影响[18-19]。
本研究采用不同组分的精炼渣处理添加稀土Ce的低合金钢,通过实验室管式炉渣钢平衡实验,研究了精炼过程中不同时刻钢中O含量、夹杂物尺寸、数量、类型的变化,对夹杂物的演变规律进行了深入分析。
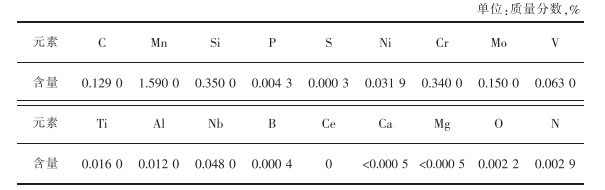
1 实验方法 1.1 实验原料实验所用钢的化学成分如表 1所列。
|
|
表 1 实验钢化学成分 |
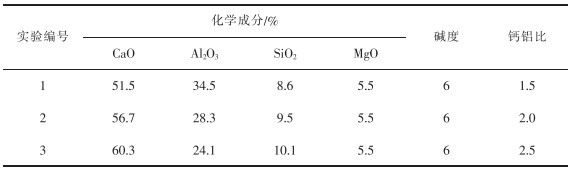
实验所用的精炼渣样均由各成分的分析纯配制而成,混匀后在马弗炉中进行预熔,使其成分均匀,进行渣钢平衡实验时可快速熔化。精炼渣成分如表 2所列。
|
|
表 2 精炼渣化学成分 |
将实验分为3组:1号(钙铝比为1.5)、2号(钙铝比为2.0)、3号(钙铝比为2.5)。将装有500 g钢样的氧化镁坩埚(60 mm×120 mm)置于管式炉中,在氩气保护气氛(2 L/min)下升温。当温度达到1 600 ℃时保持恒温,待钢样完全熔化后(约20 min),将100 g预熔后的块状渣样置于氧化镁坩埚中。渣样熔化后,向钢液中加入1.5 g的10% Ce-Fe合金,并开始计时。分别在3、6、9、20、40、60、120 min时,用石英管取钢样进行水冷。
1.3 实验分析方法钢中O含量(质量分数,下同)采用红外吸收光谱法(EMGA-830)测定。钢中Ce含量(质量分数,下同)采用电感耦合等离子发射光谱法(ICP-AES)测定。所取钢样经切割、机械研磨、抛光后,利用MLA250型扫描电子显微镜(SEM)和能谱分析仪(EDS)对钢中夹杂物进行分析。使用AZtecSteel夹杂物自动分析系统分析在尺寸在(0,1)μm、[1,2)μm、[2,3)μm、[3,4)μm、[4,5)μm、[5,10)μm范围内的夹杂物分布情况、平均尺寸和数密度等。
2 结果与讨论 2.1 钢中成分变化实验钢中的O含量随反应时间的变化规律如图 1所示。3组实验钢中的O含量均随着钢渣反应的进行而逐渐降低,这与文献[20]中结论稀土具有良好的脱氧效果相一致。2号实验钢终点O含量为7.8×10-6,低于1号和3号实验钢的1.1×10-5。当钙铝比由1.5增大至2.0时,终点O含量降低;当钙铝比由2.0增大至2.5时,终点O含量升高。3组实验钢中的O含量均在反应前9 min内大幅度下降,之后下降较为平缓。在整个过程中,2号实验钢中O含量始终低于1号和3号。从控制低合金钢中O含量的角度来看,2号实验钢效果优于1号和3号。钢中S含量均为3×10-6。
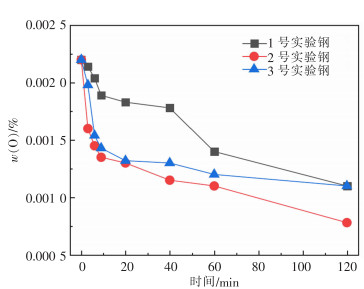 |
| 图 1 钢中O含量随反应时间的变化规律 |
图 2所示为钢中Ce含量随反应时间的变化规律。由图 2可以看出,3组实验初始Ce含量都较高。这是因为在实验室管式炉实验时无法进行底吹搅拌,取样时间也较短(加入稀土后3 min取初始样),稀土分布不均匀,使取样点附近Ce含量过高。在反应进行至3~6 min时,钢中Ce含量急剧下降,降至50%。主要是因为钢液成分更均匀化及稀土夹杂物被熔渣吸附。钙铝比越大,熔渣黏度越小,对稀土夹杂物的吸收能力越强。因此,3号实验钢终点Ce含量最低。反应进行9 min后,3组实验钢中Ce含量的下降速率较为平缓,终点Ce含量相差不大,约为6×10-5。
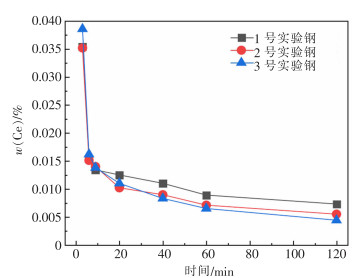 |
| 图 2 钢中Ce含量随反应时间的变化规律 |
未添加稀土元素的钢中典型夹杂物元素分布情况如图 3所示。通过SEM-EDS测定S含量的变化情况,未添加稀土时钢中的氧化物夹杂物主要为Al2O3,还有少量的MnS。其中Al2O3夹杂物可单独存在,因钢中S含量较低,MnS夹杂物数量较少,且在凝固过程中析出,包裹在Al2O3夹杂物的周围,以Al2O3-MnS复合夹杂物形式存在。
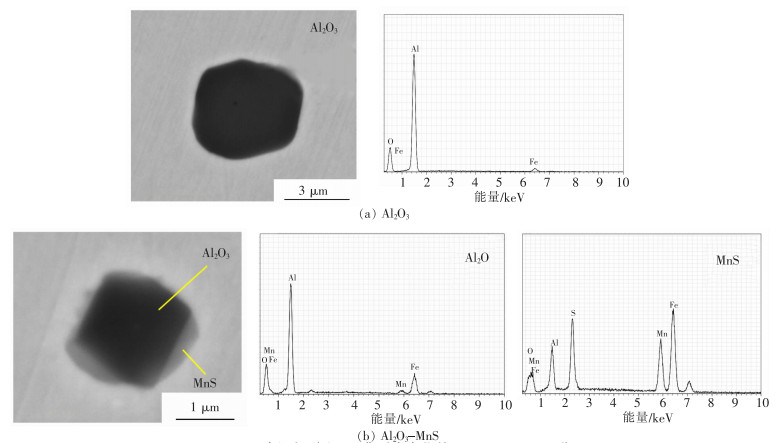 |
| 图 3 未添加稀土Ce典型夹杂物的SEM及EDS图谱 |
添加稀土Ce后钢中典型夹杂物元素分布情况如图 4所示。根据SEM-EDS检测结果可知,在反应进行3 min时,钢中的Al2O3夹杂物已被快速且完全改性为稀土夹杂物。其中绝大多数夹杂物为Ce2O3,同时,还存在少量的Ce2O2S夹杂物和被Ce2O3包裹的CeAlO3夹杂物。由图 5可知。当反应进行至40 min时,1号和3号实验钢中除Ce2O3和Ce2O2S夹杂物外,还存在CeAlO3夹杂物与被CeAlO3包裹的Ce2O3夹杂物,而2号实验钢则在反应进行至60 min时出现此类夹杂物。
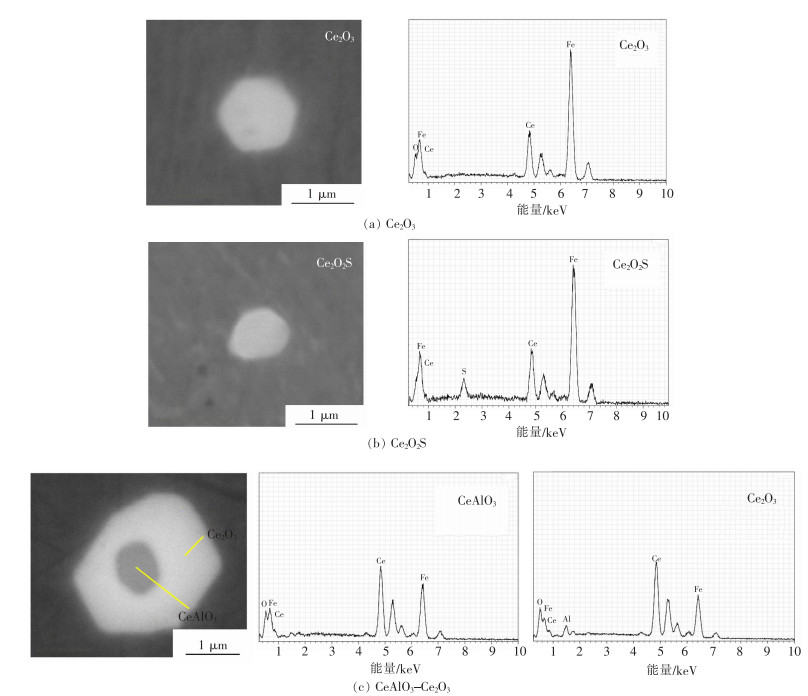 |
| 图 4 添加稀土Ce后,实验钢40 min前(2号实验钢60 min前)典型夹杂物的SEM及EDS图谱 |
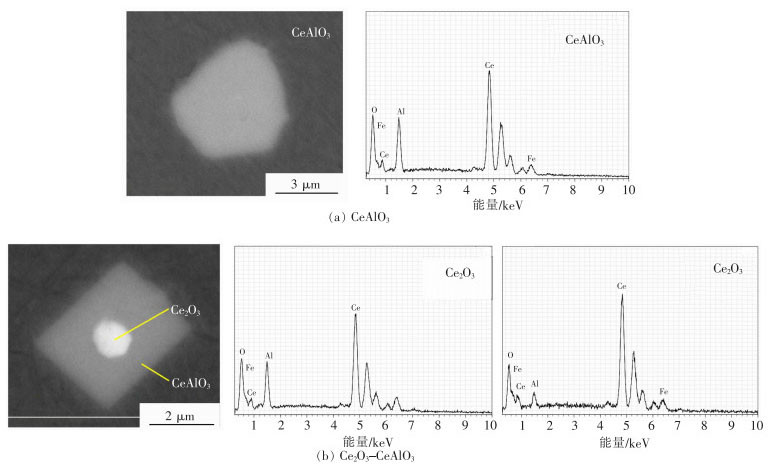 |
| 图 5 添加稀土Ce后,实验钢40 min时(2号实验钢60 min时)典型夹杂物的SEM及EDS图谱 |
根据AZtecSteel的分析结果,3组实验钢中夹杂物尺寸在(0,1)μm、[1,2)μm、[2,3)μm、[3,4)μm、[4,5)μm、[5,10)μm范围内的分布情况如图 6所示。随着反应的进行,3组实验钢中小于2 μm的夹杂物占比显著增加,在反应为3 min时达到最大,而大于2 μm,尤其大于3 μm的夹杂物所占比例明显降低,其中2号实验钢中小于2 μm的夹杂物所占比例最大,为94%,大于2 μm的夹杂物所占比例最小,为6%。夹杂物的平均尺寸随着稀土Ce的加入而减小,在反应进行至3 min时最小,其中2号实验钢的平均尺寸最小,为1.21 μm,如图 7所示。夹杂物数密度随着稀土Ce的加入而增大,在反应进行至3 min时达到最大,2号实验钢的数密度最小,为163 mm-2,如图 8所示。稀土夹杂物的加入可深度脱氧,减小夹杂物尺寸、增大夹杂物数密度,这与文献[20]的报道一致。在反应进行至3 min后,3组实验钢中尺寸小于2 μm的夹杂物比例随反应时间延长而逐渐降低,大于2 μm的夹杂物所占比例逐渐增加,夹杂物平均尺寸随反应时间延长逐渐增大,而夹杂物数密度随反应时间延长逐渐减小。
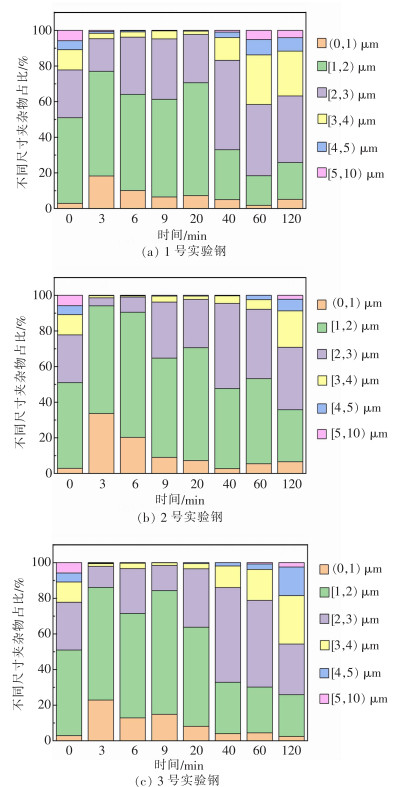 |
| 图 6 3组实验不同时刻钢中氧化物夹杂的尺寸分布 |
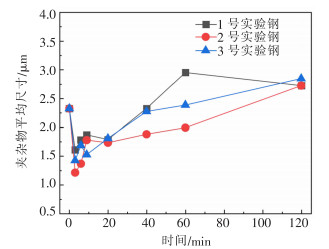 |
| 图 7 钢中氧化物夹杂的平均尺寸随反应时间的变化 |
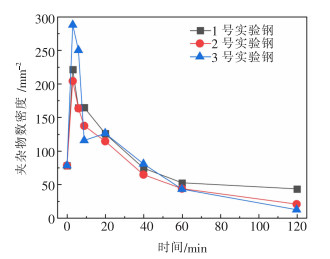 |
| 图 8 钢中氧化物夹杂的数密度随反应时间的变化 |
为了研究稀土夹杂物在钢液中的转变情况,利用FactSage 8.0热力学软件的Phase Diagram模块计算得到在1 600 ℃下Ce-Al-O-S-C-Si-Mn-Fe体系中的稳定相图,如图 9所示。当O含量一定时,随着Ce含量的增加,钢中夹杂物的转变顺序为Al2O3→CeAlO3→Ce2O3或Ce2O2S。文献[20-22]报道了Ce对Al2O3和MgO·Al2O3夹杂物的改性机理和夹杂物演变过程。用未反应核模型解释Ce与Al2O3和MgO·Al2O3夹杂物的改性过程,主要表现为钢中出现了外层被Ce-Al-O或Ce-O-S包裹的Al2O3类复合夹杂物。
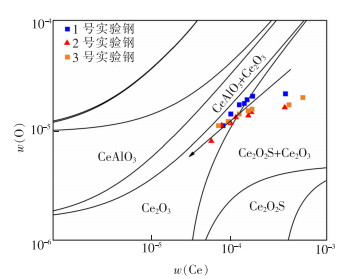 |
| 图 9 1 600 ℃下Ce-Al-O-S-C-Si-Mn-Fe体系中的稀土夹杂物稳定相图(除O和Ce之外的元素含量与原料钢中含量相同) |
此外,将3组实验钢在不同的反应时间内进行取样,将测得的O含量与Ce含量标记在图 9中。在1 600 ℃时,加入稀土Ce后3组实验钢初始成分均位于Ce2O3+Ce2O2S区域,说明钢液中此时会生成Ce2O3和Ce2O2S夹杂物,未生成CeAlO3夹杂物,这与图 4中观察到的Ce2O3和Ce2O2S夹杂物一致,而图 4中被Ce2O3包裹的CeAlO3夹杂物为尚未被Ce完全改性的非平稳态过度物。由前文可知,随着实验的进行,3组实验钢的O含量和Ce含量均随反应时间延长而逐渐降低,实验钢所在区域逐渐由Ce2O3+Ce2O2S区域转移到Ce2O3区域,但未到达CeAlO3+Ce2O3区域,说明此时钢液中的Ce2O2S夹杂物转变为Ce2O3夹杂物,但仍未生成CeAlO3夹杂物。然而,由图 5可知,1号和3号实验钢在反应进行40 min(2号钢60 min)后出现了CeAlO3夹杂物,此时热力学计算结果与SEM、EDS的检测结果不符。
由于在石英管中取样时,水冷前石英管中的钢样已开始凝固,通过SEM、EDS检测到的夹杂物可能不是1 600 ℃下钢样中的夹杂物。因此,利用FactSage 8.0热力学软件的Equilib模块计算得到1号钢反应进行120 min时的平衡凝固过程,如图 10所示。实验钢在1 480 ℃左右时开始凝固。在1 600 ℃时,钢液中夹杂物均为Ce2O3。在约1 430 ℃时,钢液中Ce2O3夹杂物含量开始下降,生成Ce2O2S夹杂物,其含量随着温度的降低而逐渐增加。在1 380 ℃左右时,钢液中开始析出CeAlO3夹杂物,直至1 300 ℃左右时趋于稳定。从该平衡凝固过程可以发现,Ce2O3在凝固前就已生成,随着反应温度的下降,在凝固过程中逐渐转变为Ce2O2S和CeAlO3夹杂物。此外,也计算了1号和3号钢在40 min(2号钢60 min)后的试样的平衡凝固过程,与图 10趋势大致相同。由此解释了各组实验钢在实验后期出现CeAlO3夹杂物的现象。
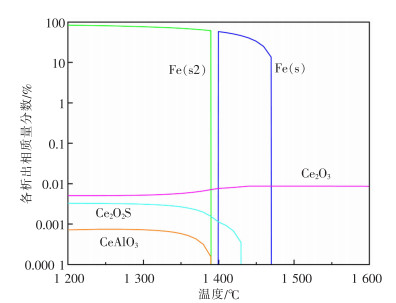 |
| 图 10 1号钢120 min试样的平衡凝固过程 |
通过以上实验数据和热力学计算结果,初步分析了钢中夹杂物的转变过程。由前文分析可知,夹杂物转变主要经历两个阶段:阶段Ⅰ(Al2O3→Ce2O3或Ce2O2S)和阶段Ⅱ(Ce2O3→CeAlO3),夹杂物的演化过程如图 11所示。
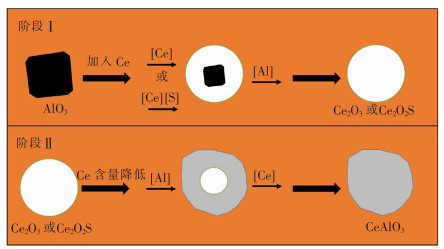 |
| 图 11 钢中夹杂物演化过程 |
阶段Ⅰ:夹杂物由Al2O3转变为Ce2O3或Ce2O2S的演化过程如下。
1)1 600 ℃时,最初钢液中形成的夹杂物为Al2O3。
2)加入稀土Ce后,Ce原子扩散到Al2O3/钢液界面,在Al2O3/钢液界面形成Ce3+,如式(1)所列。

|
(1) |
3)Ce3+逐渐向内扩散到未反应核Al2O3的表面。
4)在Al2O3表面,Ce3+与Al2O3通过反应式(2)—式(4),在Al2O3夹杂物周围形成了一层薄薄的CeAlO3、Ce2O3或Ce2O2S层,如图 11所示。
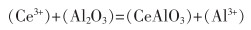
|
(2) |
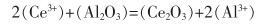
|
(3) |
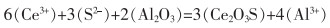
|
(4) |
5)形成CeAlO3层时,Ce3+与形成的CeAlO3层继续反应,反应如式(5)所列。
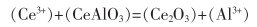
|
(5) |
6)在Al2O3/钢液界面发生反应如式(6)所列,反应生成的[Al]扩散进入至钢液。
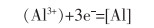
|
(6) |
7)Ce3+通过新形成的层扩散到内部,并继续与未反应的中心Al2O3夹杂物发生反应,生成新的Ce2O3或Ce2O2S。不断形成的Ce2O3或Ce2O2S使夹杂物外层开始变厚,从而导致Ce和Al的扩散阻力不断增加,反应速度越来越慢。最后,所有夹杂物均转变为稀土夹杂物,如反应式(7)、式(8)所列。稀土夹杂物Ce2O3或Ce2O2S分布均匀,呈球形,有助于提高材料的抗疲劳和耐腐蚀性能。
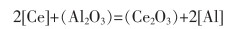
|
(7) |

|
(8) |
阶段Ⅱ:夹杂物由Ce2O3转变为CeAlO3的演化过程如下。
1)随着反应的进行,钢中的稀土Ce含量大幅度下降后,钢液中Al原子扩散到Ce2O3/钢液界面,在Ce2O3/钢液界面形成Al3+,反应如式(9)所列。
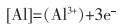
|
(9) |
2)Al3+逐渐向内扩散到未反应核Ce2O3的表面。
3)在Ce2O3表面,Ce3+与Ce2O3通过反应式(10),在Ce2O3夹杂物周围形成了一层薄薄的CeAlO3层,如图 11所示。
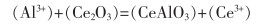
|
(10) |
4)在Al2O3/钢液界面发生式(11)反应,之后反应产生的[Ce]扩散进入钢液。
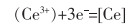
|
(11) |
5)Al3+通过新形成的层扩散到内部,并继续与未反应的中心Ce2O3夹杂物反应,生成新的CeAlO3夹杂物。不断形成的CeAlO3使外层开始变厚,反应速度不断减缓,直至Ce2O3夹杂物全部转变为CeAlO3夹杂物,反应如式(12)所列。
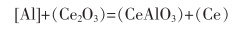
|
(12) |
1)稀土Ce添加初期(t≤3 min),钢中夹杂物的平均尺寸与1~3 μm的夹杂物占比显著减小,但夹杂物的数密度增加。随着反应的进行,钢中夹杂物的平均尺寸与1~3 μm夹杂物的占比逐渐增大,夹杂物的数密度则逐渐减小。
2)2号实验钢(钙铝比为2.0)可获得更低的氧含量(7.8×10-6),同时,在稀土Ce加入初期(t≤3 min)获得的稀土夹杂平均尺寸最小(1.21 μm)。综合考虑脱氧率和夹杂物尺寸变化规律,实际生产中采用2号实验渣精炼,添加稀土处理时间低于9 min,可获得良好的洁净度和小尺寸夹杂物。
3)不同钙铝比精炼渣处理的钢中稀土夹杂物类型和形貌相同,夹杂物转变时间不同,稀土夹杂物主要为Ce2O3和CeAlO3,同时还有少量的Ce2O2S。钢中加入稀土Ce后,夹杂物的转变路径为Al2O3→CeAlO3→ Ce2O3或Ce2O2S。随着精炼时间延长,钢中O含量与Ce含量逐渐下降,钢中开始生成部分CeAlO3夹杂物。
| [1] |
JINDAL S, CHHIBBER R, MEHTA N P. Issues in welding of HSLA steels[J]. Advanced Materials Research, 2011, 365: 44-49. DOI:10.4028/www.scientific.net/AMR.365.44 |
| [2] |
CHEN X Z, HUANG Y M, LEI Y C. Microstructure and properties of 700 MPa grade HSLA steel during high temperature deformation[J]. Journal of Alloys and Compounds, 2015, 631: 225-231. DOI:10.1016/j.jallcom.2015.01.093 |
| [3] |
CHEN X Z, HUANG Y M, LEI Y C. Microstructure and properties of 700 MPa grade HSLA steel during high temperature deformation[J]. Journal of Alloys and Compounds, 2015, 631: 225-231. DOI:10.1016/j.jallcom.2015.01.093 |
| [4] |
PARK J H, TODOROKI H. Control of MgO·Al2O3 spinel inclusions in stainless steels[J]. ISIJ International, 2010, 50(10): 1333-1346. DOI:10.2355/isijinternational.50.1333 |
| [5] |
WANG H, LI J, SHI C B, et al. Evolution of All2O3 inclusions by magnesium treatment in H13 hot work Die steel[J]. Ironmaking & Steelmaking, 2017, 44(2): 128-133. |
| [6] |
HU Y, CHEN W Q, WAN C J, et al. Effect of deoxidation process on inclusion and fatigue performance of spring steel for automobile suspension[J]. Metallurgical and Materials Transactions B, 2018, 49(2): 569-580. DOI:10.1007/s11663-018-1187-x |
| [7] |
SHI C B, YU W T, WANG H, et al. Simultaneous modification of alumina and MgO·Al2O3 inclusions by calcium treatment during electroslag remelting of stainless tool steel[J]. Metallurgical and Materials Transactions B, 2017, 48(1): 146-161. DOI:10.1007/s11663-016-0771-1 |
| [8] |
HIGUCHI Y, NUMATA M, FUKAGAWA S, et al. Inclusion modification by calcium treatment[J]. ISIJ International, 1996, 36(Sl): S151-S154. |
| [9] |
TABATABAEI Y, COLEY K S, IRONS G A, et al. A kinetic model for modification of MgAl2O4 spinel inclusions during calcium treatment in the ladle furnace[J]. Metallurgical and Materials Transactions B, 2018, 49(5): 2744-2756. DOI:10.1007/s11663-018-1354-0 |
| [10] |
李春红, 杨宇鹏, 曾小华, 等. 稀土钇元素对H13模具钢组织及性能影响[J]. 江西冶金, 2021, 41(4): 7-12. |
| [11] |
PAN F, ZHANG J, CHEN H L, et al. Effects of rare earth metals on steel microstructures[J]. Materials (Basel, Switzerland), 2016, 9(6): 417. DOI:10.3390/ma9060417 |
| [12] |
王龙妹. 稀土在低合金及合金钢中的应用[M]. 北京: 冶金工业出版社, 2016.
|
| [13] |
SONG M M, SONG B, XIN W B, et al. Effects of rare earth addition on microstructure of C-Mn steel[J]. Ironmaking & Steelmaking, 2015, 42(8): 594-599. |
| [14] |
GENG R M, LI J, SHI C B. Evolution of calcium aluminate inclusions by cerium treatment in Al-killed steel during ruhrstahl-heraeus refining process[J]. Steel Research International, 2020, 91(9): 2000117. DOI:10.1002/srin.202000117 |
| [15] |
杨晓红, 吴鹏飞, 吴铖川, 等. 特殊钢中稀土变质夹杂物行为研究[J]. 中国稀土学报, 2010, 28(5): 612-618. |
| [16] |
鲍道华, 黄宇, 成国光, 等. Ce含量对H13钢中稀土夹杂物析出行为的影响[J]. 钢铁研究学报, 2021, 33(8): 792-800. |
| [17] |
LI X, WANG L Z, YANG S F, et al. Effect of slag composition on the cleanliness of drill rod steel[J]. Ironmaking & Steelmaking, 2019, 46(5): 416-423. |
| [18] |
YANG X H, LONG H, CHENG G G, et al. Effect of refining slag containing Ce2O3 on steel cleanliness[J]. Journal of Rare Earths, 2011, 29(11): 1079-1083. |
| [19] |
WANG X J, LIU Y, LI G Q, et al. Effect of Ce2O3 on the fluoride vaporization of CaF2-CaO-Al2O3-(Ce2O3) slag used for vacuum electroslag remelting[J]. Vacuum, 2021, 185: 109997. |
| [20] |
LI H, YU Y C, REN X, et al. Evolution of Al2O3 inclusions by cerium treatment in low carbon high manganese steel[J]. Journal of Iron and Steel Research, International, 2017, 24(9): 925-934. |
| [21] |
TORKAMANI H, RAYGAN S, MATEO C, et al. The influence of La and Ce addition on inclusion modification in cast niobium microalloyed steels[J]. Metals, 2017, 7(9): 377. |
| [22] |
YU Z, LIU C J. Modification mechanism of spinel inclusions in medium manganese steel with rare earth treatment[J]. Metals, 2019, 9(7): 804. |
 2023, Vol. 43
2023, Vol. 43