| 冶金粉尘铟碳热还原热力学分析及铟元素迁移路径 |
2. 河北博泰环保科技有限公司,河北 唐山 063611
2. Hebei Botai Environmental Protection Technology Co., Ltd., Tangshan 063611, Hebei, China
高炉瓦斯灰来源于高炉布袋除尘灰,其化学成分较复杂,主要为铁及未燃烧的焦粉和煤粉,此外,还含有铅、锌、铋、铟、镉、锡等金属及碱金属氧化物。高炉炼铁每生产1 t铁水将产生15~25 kg高炉烟尘[1],按我国2020年全年高炉生铁产量为8.88亿吨计算,高炉烟尘高达2 000万吨左右。其中30%~40%为瓦斯灰,60%~70%为重力尘。高炉瓦斯灰中铟的品位一般只有0.01%~0.02%,若能有效回收其中的铟元素,则通过处理高炉瓦斯灰生产的粗铟可达800 t左右。因此,选择合理的生产工艺对高炉瓦斯灰进行回收处理,具有一定的经济和社会价值。
高炉瓦斯灰堆放或填埋处理不仅会污染环境,还会造成资源浪费。作为生产烧结矿原料,存在降低烧结料层的透气性、影响烧结指标及高炉顺行的弊端[2]。目前,湿法工艺存在单元流程多、成本高、生产效率低的问题[3]。火法工艺能实现不易挥发组分(铁、碳、钙、硅、镁等)和挥发组分(锌、铅、钾、钠、铟、铋、镉、锡)的有效分离,且分离效率较高,能满足大规模处理的需要。目前,火法工艺主要有回转窑工艺、富氧竖炉(OxyCup)工艺和转底炉工艺。回转窑工艺的优点有:工艺脱锌率较高,一般能达到90%以上,钢铁尘泥利用自带碳,无需添加燃料或添加较少燃料即可直接入窑,运行成本低,工艺成熟、投资低、运行简单等[4]。目前,已有众多学者研究了关于回转窑内锌铅钾钠还原挥发行为[5-7],铟作为稀缺资源,与其他稀散金属元素一样也已引起了广泛关注。本文研究高炉瓦斯灰处理全流程中铟含量及转变行为,掌握了铟的迁移路径,为回转窑工艺优化提供基础数据。
目前,关于铟元素在热力学上的分析还鲜有报道,火法处理瓦斯灰时铟的挥发率低,相关铟在工艺流程中迁移的研究尚未见报道[8-10]。本文为探究回转窑工艺还原过程中In2O3的分解行为,通过热力学计算,研究气体还原和固体碳还原In2O3的热力学过程和分解特征,通过对In-C-O体系进行热力学计算和分析,推测碳热还原过程中In的转变形式和还原分离条件,为还原回收铟提供依据。并作出铟在全流程及其化合物在粉尘中迁移的猜想,为未来工业化应用提供重要参考。
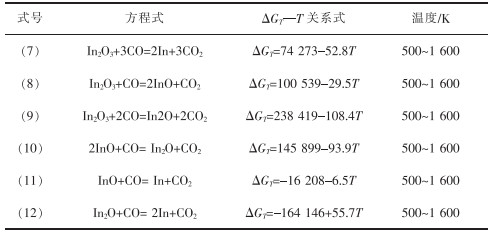
1 含铟粉尘碳热还原过程的热力学分析 1.1 In2O3与碳反应的热力学分析铟的氧化物以多种形式存在,主要有In2O3、In2O和InO,In2O3直接与C反应的化学方程式如表 1所列[11]。根据表 1数据绘制In2O3碳热还原反应吉布斯自由能(ΔGT)与温度(T)的关系曲线,结果如图 1所示[12]。
|
|
表 1 In2O3碳热还原反应及ΔGT—T关系 |
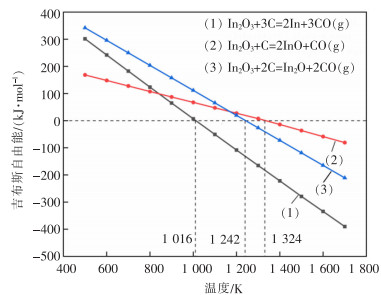 |
| 图 1 式(1)—式(3)的吉布斯自由能随温度的变化 |
标准状态下,反应式(1)—式(3)吉布斯自由能随着温度升高而逐渐降低,在反应温度超过1 016、1 242、1 324 K时,ΔGT<0,反应开始进行。说明In2O3可以被还原为In、In2O、InO,还原难度依次增加,In、In2O、InO开始生成的温度分别为1 016、1 242、1 324 K,可见In2O3最容易被还原为单质In,其次是In2O和InO。InO和In2O会进一步被还原和转化。
1.2 铟的低价氧化物与碳反应的热力学分析由1.1节可知,In2O3与C发生反应可能生成铟的低价氧化物In2O、InO,铟的低价氧化物与碳可能发生的反应如表 2所列。根据表 2数据绘制铟的低价氧化物碳热还原反应ΔGT—T关系曲线,结果如图 2所示。
|
|
表 2 In2O、InO碳热还原反应及ΔGT—T关系 |
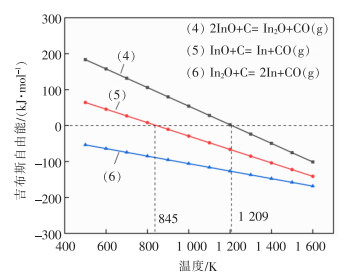 |
| 图 2 式(4)—式(6)的吉布斯自由能随温度的变化 |
由图 2可以看出,InO转化为In2O的温度为1 209 K;反应式(6)发生的吉布斯自由能(ΔGT)在500~1 600 K的温度范围内始终小于0,说明C容易将In2O还原为单质In;InO被还原为In的温度为845 K。反应式(4)直线始终在反应式(5)的上方,说明只有少量的InO转化为In2O,大部分InO直接被还原为单质In。
1.3 系统压强对In2O3碳热还原过程的影响图 3所示为反应In2O3+3C=2In+3CO(g)在不同压强下的ΔGT—T变化曲线。由图 3可以看出,In2O3与C反应的ΔGT值随着T的升高而降低,且在同一温度、不同压强条件下,ΔGT值变化明显。在CO压强分别为106、105、104、103、102、10、1 Pa时,反应开始的最低温度分别为1 049、1 014、981、951、922、895、869 K。说明在真空条件下In2O3与C容易发生反应,且随着压强的减小,反应所需的温度也随之降低。
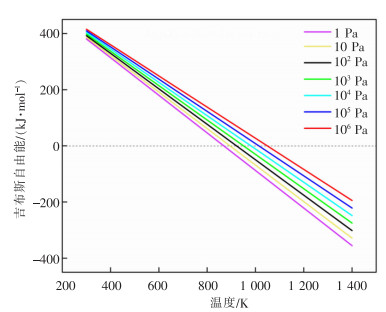 |
| 图 3 不同压强下C与In2O3反应的吉布斯自由能随温度的变化 |
In2O3在CO气氛下分解遵循逐级转变的原则,铟氧化物与CO的反应方程式如表 3所列。由表 3数据绘制铟氧化物与CO发生还原反应的ΔGT—T关系曲线,结果如图 4、图 5所示。
|
|
表 3 CO气氛下铟氧化物还原反应及ΔGT—T关 |
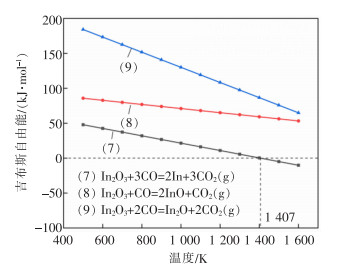 |
| 图 4 式(7)—式(9)的吉布斯自由能随温度的变化 |
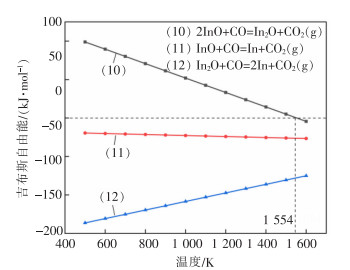 |
| 图 5 式(10)—式(12)的吉布斯自由能随温度的变化 |
由图 4可以看出,In2O3被CO还原生成In的最低温度为1 407 K,同时反应式(8)和式(9)的吉布斯自由能始终大于0,因此,在实验条件下,In2O3不会被CO还原为InO和In2O;由图 5可以看出,反应式(10)的吉布斯自由能小于0,说明InO可与CO反应生成In2O,反应开始的最低温度为1 554 K;InO和In2O被CO还原为单质In的反应式(11)和式(12)吉布斯自由能在实验温度范围内恒小于0,说明反应都可能发生,且反应式(12)与式(11)相比,反应的吉布斯自由能更低,说明该反应更容易发生。
利用反应式(7)—式(12)数据绘制出CO还原铟氧化物的温度与CO分压的关系曲线,结果如图 6所示。反应式(12)的曲线趋近于0,微量的CO即可使In2O还原。而反应式(8)和式(9)的曲线趋近于100,证明In2O3即使在高浓度的CO气氛条件下,依然不会被还原生成InO和In2O。CO分压只需10%左右,反应式(11)就能顺利进行。反应式(7)和式(10)曲线表明,随着温度升高,反应平衡所需的CO分压减小,曲线位于图的中上部,在温度为1 407 K条件下,还原反应所需的CO分压为53%。因此,In2O3即使在高浓度CO气氛下也很难被还原为单质In,而InO和In2O却易被还原生成单质In,In2O3在高温(1 407 K)高浓度的CO气氛下几乎不会生成InO和In2O。此结果与热力学分析吻合。
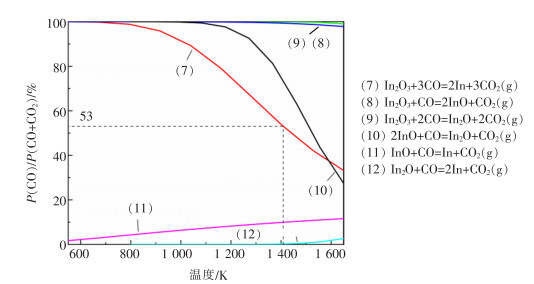 |
| 图 6 铟氧化物在CO气氛下还原温度与CO分压关系 |
铟的3种氧化物中铟有3种价态+1、+2、+3,因此,在高温条件下,In2O与InO可能发生歧化反应,发生的歧化反应方程式如表 4所列。由表 4数据绘制铟氧化物发生歧化反应的ΔGT—T关系曲线,结果如图 7所示。
|
|
表 4 铟氧化物歧化反应及ΔGT—T关系 |
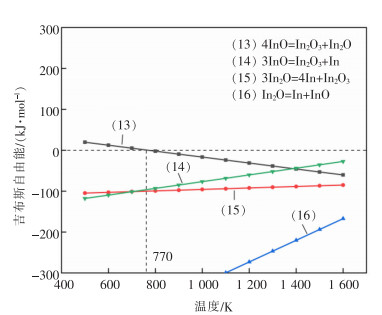 |
| 图 7 式(13)—式(16)的吉布斯自由能随温度的变化 |
由反应式(14)可知,在温度大于770 K时,InO将转化为In2O3和In;其余的反应式(13)、式(15)、式(16)在500~1 700 K时ΔGT<0,说明反应均会发生,证明了InO与In2O在温度超过770 K时不能稳定存在,最终转化为单质In和In2O3存在于残留物和烟气中。
1.6 铟硫化物的氧化反应含铟冶金粉尘可能存在铟的硫化物,在高温下,铟的硫化物能与氧气发生反应生成In2O3或In。由表 5数据绘制铟硫化物氧化反应的ΔGT—T关系曲线,结果如图 8所示。
|
|
表 5 铟硫化物氧化反应ΔGT—T关系 |
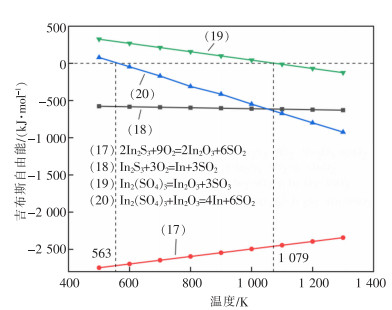 |
| 图 8 式(17)—式(20)的吉布斯自由能随温度的变化 |
反应式(17)和式(18)在温度为500~1 300 K时吉布斯自由能始终小于0,说明In2S3容易与氧气发生反应生成In2O3和In,且反应式(17)始终在反应式(18)下方,说明In2S3更容易被氧化生成In2O3。反应式(19)在温度超过1 079 K时,ΔGT<0,反应开始发生,In2(SO4)3离解生成In2O3和SO3。反应式(20)在温度超过563 K时,ΔGT<0,In2(SO4)3与In2S3反应生成In和SO2。
2 铟元素迁移分析 2.1 铟元素在全流程中的迁移与富集铟在铁矿石中的含量为4×10-6~4×10-5 [13~15],在矿石烧结过程中,绝大部分铟留存在烧结块中,极小部分进入烧结尘。高炉炼铁时,铟随气流被带入高炉煤气,在对高炉煤气干法或湿法除尘净化过程中,铟与锌、锡、铅、铋、镉等其他有价元素一起被富集于高炉瓦斯灰中,其品位为0.01%~0.02%,此时铟含量与铁矿石相比高出近50倍。高炉瓦斯灰与焦粉(或粉煤)按一定的比例混合后加入回转窑,窑内反应段的温度为1 100~1 200 ℃,窑尾烟气温度为650~750 ℃,瓦斯灰中的铟等有价金属被还原后挥发,经除尘系统收集后得到次氧化锌[16]。通过火法富集,铟在次氧化锌粉尘中被富集(含量为0.05%~0.10%),同时,瓦斯灰中的其他有价元素锌、锡、铅、铋、镉等也不同程度被富集。次氧化锌粉尘中铟含量比瓦斯灰中的含量高5倍。后序通过对次氧化锌粉尘进行脱氟氯及多段浸出后,得到含铟的浸出渣和含锌的浸出液。再对浸出渣进行多级萃取、加入铝片置换及熔铸,得到In含量大于99.5%的粗铟,利用真空蒸馏炉除杂和常规的电解精炼,可将铟提纯到In含量为99.993%~99.999%的高纯铟[17]。铟在全流程中的迁移与富集如图 9所示。
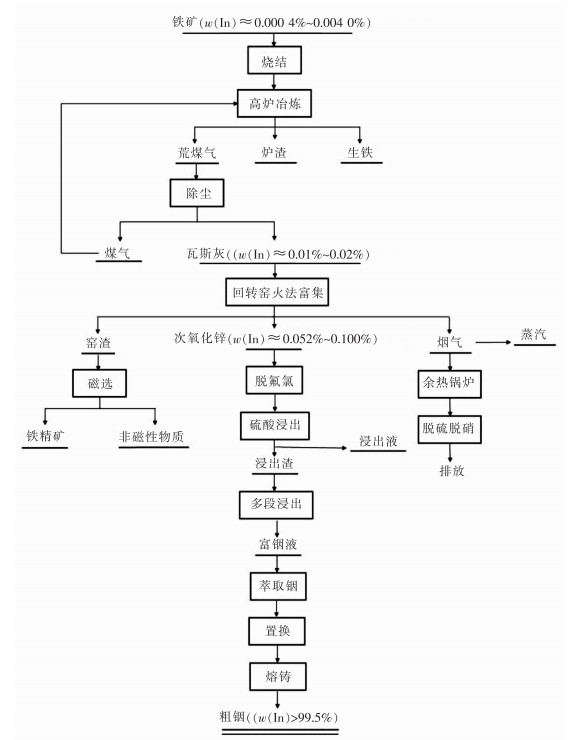 |
| 图 9 铟在全流程中的迁移与富集 |
为了解粉尘中铟化合物的迁移路径,应先了解铟化合物的相关特性。铟各类化合物的蒸汽压如图 10所示[18]。温度高于850 ℃时焙烧氢氧化物、碳酸盐、硝酸盐、硫酸盐等均可获得In2O3,单质In和In2O3的蒸汽压很小,且In2O3还原生成的InO难挥发,虽然In、InO和In2O3均不易挥发,但却易被窑内的蒸汽流带入收尘系统,同时,In和InO在烟气中被氧化为In2O3。InCl3蒸汽压较大,易挥发,在148~440 ℃时开始升华,在焙烧过程中由固态汽化后在二次粉尘中冷却,在流程中是简单的物理变化过程。
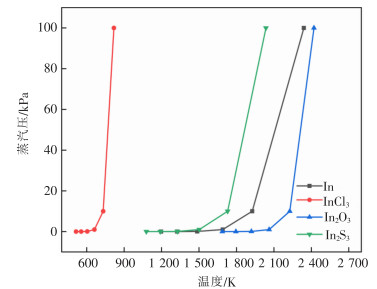 |
| 图 10 铟及其主要化合物的饱和蒸汽压与温度关系 |
铟的硫化物In2S3在225 ℃开始被氧化,反应式为:In2S3+O2=2InS+SO2,产物InS在温度达到400 ℃后氧化速度激增,反应式为:4InS+7O2=2In2O3+4SO2。在温度为225~460 ℃之间的氧化产物为铟的氧化产物MeO与MeS的混合物,在温度为380 ℃左右时,进行的主要反应是生成In2(SO4)3的氧化过程: In2S3+6O2= In2(SO4)3,当温度超过540 ℃时,主要产物为In2S3,同时发生In2(SO4)3的离解及相关的交互反应[19]。当温度高于900 ℃时,温度对氧化反应的影响逐步消失,反应为:2In2S3+9O2=2In2O3+6SO2、In2S3+3O2=2In+3SO2、In2(SO4)3=In2O3+3SO3和In2(SO4)3+In2S3=4In+6SO2,随着铟的氧化及相关的交互反应进行,In2S3焙烧的最后产物为In2O3,最终富集在二次粉尘中[20]。
图 11所示为粉尘中铟元素在全流程中物相转变的假设分析,铟的氧化物In2O3在高温下先后被还原生成In2O、In、InO,产物铟难挥发,1 200 ℃时的蒸汽压仅为106.66 Pa,产物InO也不易挥发,而产物In2O在高于800 ℃时便显著挥发。因挥发尘中的大部分铟以In2O3的形态存在,故可认为,在高温下部分铟被还原为单质In和InO,随蒸汽流进入烟气,在烟气中被氧化生成In2O3;部分铟被还原为In2O而挥发进入烟气,在烟气中亦被氧化成In2O3。
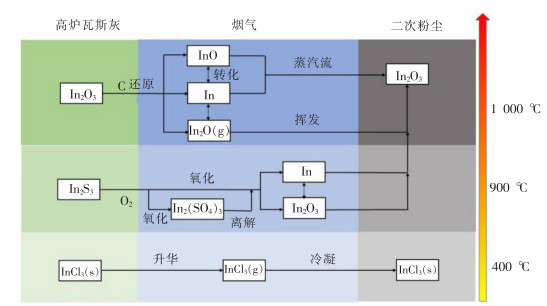 |
| 图 11 铟在流程中物相转变 |
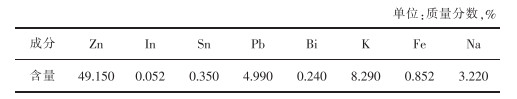
试验选取回转窑收集的二次粉尘,成分如表 6所列,选择高纯石墨为还原剂,将石墨粉和二次粉尘以1∶4(m/m)的比例混合,在管式竖炉中达到实验温度后,放入管式竖炉中恒温40 min,收集残留物进行化学分析,计算铟的挥发率,结果如图 12所示。900 ℃时铟的挥发率为48.17%,950 ℃时为94.08%,1 000 ℃时达到98.94%。由此可以看出,当温度超过950 ℃,铟显著挥发,这与前文热力学计算分析相吻合。对挥发物进行X射线衍射(XRD)分析,结果如图 13所示。由图 13可知,挥发物中的In以In2O3和InCl3的形式存在,与铟在全流程中物相转变的推测相符。
|
|
表 6 二次粉尘成分及含量 |
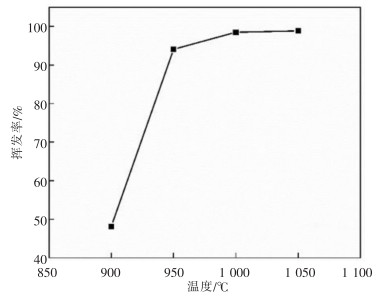 |
| 图 12 还原温度对铟挥发率的影响 |
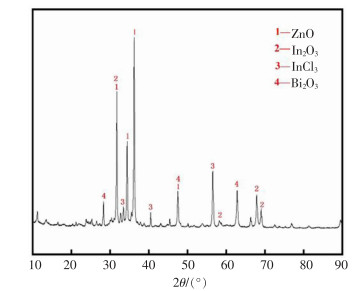 |
| 图 13 挥发物的XRD衍射图谱 |
1)含铟粉尘碳热还原过程中In2O3被依次还原为In、In2O、InO,反应开始的温度分别为1 016、1 242、1 324 K;C将In2O和InO还原为单质In, 当温度超过845 K时,InO被还原为In;InO转变为In2O的开始温度为1 209 K;In2O3与C的还原反应随着总压的减小,反应所需的温度也随之降低。
2)In2O3在CO气氛条件下,不会被还原生成InO和In2O;当温度达到1 408 K时,In2O3被还原为单质In反应所需的CO分压为0.53 Pa;CO容易将InO和In2O还原为单质In;In2O和InO在温度超过770 K时,便不会稳定存在,In2O和InO发生歧化反应生成In2O3和In。
3)在高炉→回转窑→湿法处理的工艺流程中,铟不断迁移与富集。从铁矿石到瓦斯灰,铟含量增加了约50倍;铟在回转窑内发生碳热还原反应后挥发进入二次烟尘,铟的含量增加了约5倍,最终二次烟尘通过湿法处理分离提取后得到粗铟,完成对铟的回收利用。含铟冶金粉尘中铟的主要存在形式为In2O3、InCl3、In2S3。In2O3在还原过程中会生成In、In2O和InO,在温度高于800 ℃时In2O显著挥发,金属铟和InO虽难挥发,却易被窑内的蒸汽流带入收尘系统,三者在烟气中均被氧化为In2O3;InCl3在温度为144 ℃时开始升华后被收尘装置收集在二次粉尘中。当温度超过900 ℃,In2S3发生氧化和离解反应生成In2O3,最后进入二次粉尘中;二次粉尘中In主要以In2O3形式存在。
| [1] |
王树楷. 瓦斯灰回收有色金属及再资源化(续)[J]. 资源再生, 2009(11): 52-53. |
| [2] |
佘雪峰, 薛庆国, 王静松, 等. 钢铁厂含锌粉尘综合利用及相关处理工艺比较[J]. 炼铁, 2010, 29(4): 56-62. DOI:10.3969/j.issn.1001-1471.2010.04.016 |
| [3] |
尚海霞, 李海铭, 魏汝飞, 等. 钢铁尘泥的利用技术现状及展望[J]. 钢铁, 2019, 54(3): 9-17. |
| [4] |
王静松, 李岩, 冯怀萱, 等. 钢铁产业集聚区难处理尘泥处理与全量资源化利用进展[J]. 工程科学学报, 2021, 43(12): 1737-1749. DOI:10.3321/j.issn.1001-053X.2021.12.bjkjdxxb202112014 |
| [5] |
王子宏, 阮志勇, 墙蔷, 等. 钢厂含锌尘泥锌铁火法分离研究[J]. 烧结球团, 2021, 46(5): 86-92. |
| [6] |
庞建明, 郭培民, 赵沛. 回转窑处理含锌、铅高炉灰新技术实践[J]. 中国有色冶金, 2013, 42(3): 19-24. DOI:10.3969/j.issn.1672-6103.2013.03.005 |
| [7] |
李敦华. 火法富集-湿法分离工艺从固废资源中回收锌及其他有价金属的探究[J]. 中国有色冶金, 2020, 49(1): 8-12. DOI:10.3969/j.issn.1672-6103.2020.01.003 |
| [8] |
郭志娟, 宋云涛, 徐仁廷, 等. 云南个旧锡多金属矿集区稀散元素铟的分布富集特征[J]. 现代地质, 2020, 34(5): 908-916. |
| [9] |
罗虹霖, 刘维, 覃文庆, 等. 氧化锌烟尘中铟的挥发富集[J]. 中国有色金属学报, 2014, 24(11): 2892-2899. |
| [10] |
高文成, 温建康, 付政, 等. 还原焙烧—磁选分步回收针铁矿渣中的锌铟铁[J]. 有色金属(冶炼部分), 2022(2): 1-7. |
| [11] |
谢富春, 尹周澜, 丁治英, 等. 常压碳热还原含铟渣中三氧化二铟的动力学[J]. 中国有色金属学报, 2016, 26(6): 1350-1355. |
| [12] |
叶大伦. 实用无机物热力学数据手册[M]. 北京: 冶金工业出版社, 1981.
|
| [13] |
陈立卿, 廖璐, 李红立. 某含铟锌铁多金属矿的选矿试验研究[J]. 矿产保护与利用, 2015(2): 33-36. |
| [14] |
何名飞, 卜浩, 高玉德, 等. 铁闪锌矿中稀有金属铟的高效提取应用研究[J]. 有色金属(选矿部分), 2021(6): 102-106. |
| [15] |
ZHU D Q, YANG C C, PAN J, et al. New pyrometallurgical route for separation and recovery of Fe, Zn, In, Ga and S from jarosite residues[J]. Journal of Cleaner Production, 2018, 205: 781-788. |
| [16] |
童晓忠, 马黎阳, 李永华, 等. 高炉瓦斯灰中有价金属回收及无害化处理技术[J]. 中国金属通报, 2016(4): 35-37. |
| [17] |
朱耀平. 高炉瓦斯灰中铟锌铋的回收实践[J]. 有色金属(冶炼部分), 2009(6): 14-16. |
| [18] |
GREEN D W, PERRY R H. Perry's chemical engineers' handbook[M]. Eighth Edition. New York: McGraw-Hill.
|
| [19] |
王树楷. 铟冶金[M]. 北京: 冶金工业出版社, 2006.
|
| [20] |
(俄)FEDOROVP I, (俄)AKCHURIN, PIFEDOROV, 著. 张启运, 徐克敏编译. 铟化学手册[M]. 北京: 北京大学出版社, 2005.
|
 2023, Vol. 43
2023, Vol. 43