| 自养硝化颗粒污泥吸附铅离子机理研究 |
工业生产过程中产生大量含重金属废水,若处理不当会对渔业、农业、人体健康等构成严重威胁。其中,Pb2+是生产生活中典型的重金属污染物之一,可通过食物链累积直接或间接危害人类健康[1]。目前,含铅废水的治理技术包括化学法、物理法及生化法。化学法和物理法常适用于中高浓度重金属废水治理,具有成本较高、对低浓度废水处理效果差和易产生二次污染等缺点。相比之下,生化法因具有廉价、原料易得等优点备受研究者的关注[2-3]。生化法主要是利用细菌、真菌、藻类等微生物吸附去除水中的重金属离子[4]。然而,目前主流的活性污泥法普遍存在吸附容量小、泥水分离困难等不足[5]。因此,研发高效生物吸附剂具有较好的工程意义。
好氧颗粒污泥(Aerobic Granular Sludge,AGS)是微生物自凝聚形成的颗粒状生物聚集体,已被研究证实具备成为生物吸附剂的潜力,具有结构致密、沉降性能良好、高耐毒性等优点[6-7]。Xu等发现AGS对Zn2+的吸附容量为180 mg/g[8];Sun等发现AGS对Cr(Ⅳ)的吸附容量为348.125 mg/g[9];姚磊等发现当初始浓度为50 mg/L时,AGS对Pb2+的吸附最大容量约为44.3 mg/g[10];刘名等发现干燥后的硝化AGS对Pb2+的最大吸附容量为79.58 mg/g,且证实-OH、-NH、C=O、C=C、C-OH和C-OC等活性基团参与了对Pb2+的吸附[11];李姝等则认为钙化AGS吸附Pb2+的过程中羧基和胺基为主要吸附官能团[12];张江水等提取AGS中的胞外聚合物吸附Pb2+,发现胞外聚合物中的-COOH、-NH2和-OH在吸附过程中起关键作用[13]。综上所述,AGS对一些金属离子有较好的吸附效果,且作为Pb2+的吸附剂也是可行的。
自养硝化颗粒污泥(Autotrophic Nitrifying Granular Sludge, ANGS)一般在无机高氨氮废水中驯化而成,相比于传统的AGS,颗粒内富集大量的自养硝化细菌,不易发生污泥膨胀,具有较好的污泥稳定性[14-15]。张斌超等发现ANGS对Cu2+有一定的吸附能力,最大吸附容量为15.02 mg/g[16]。但是,目前有关ANGS吸附Pb2+的研究却鲜有报道,对其吸附效果及机理的研究亦十分匮乏。因此,本文利用ANGS吸附初始浓度为100~500 mg/L的Pb2+,通过吸附等温线和吸附动力学模型求解ANGS对Pb2+的吸附容量及吸附速率,并利用SEM-EDS、FTIR、XPS及XRD分析检测手段探索其对Pb2+的机理,旨在为重金属废水的高效治理提供技术支持。
1 材料与方法 1.1 ANGS来源ANGS取自运行中的序批式反应器(Sequencing Batch Reactor,SBR),粒径在0.60~2.36 mm之间,悬浮物固体浓度/挥发性悬浮物固体浓度(MLVSS/MLSS)在0.69~0.77之间,污泥容积指数(SVI)及SV30/SV5(污泥沉降比,SV)分别稳定在21~23 mL/g及0.9~1之间,胞外聚合物(EPS)在13.13~25.04 mg/g之间,蛋白质/多糖(PN/PS)比值稳定在0.29左右。高通量测序表明ANGS内部优势菌群分别为:Nitrosomonas(51.15%)、Comamonas(7.33%)、Dokdonella(5.74%)、Chiayiivirga(2.94%)等。其中,Nitrosomonas是常见的好氧氨氧化菌[17],Comamonas是常见的具有硝化反硝化能力的菌属[18],Dokdonella是常见的反硝化菌[19],Chiayiivirga是具有有机物降解能力的菌属[20]。
1.2 吸附等温线ANGS吸附对不同浓度Pb2+的反应条件为:pH=3(2%稀HNO3调节),混合液悬浮污泥(MLSS)为6 062 mg/L,转速160 r/min,时间2.5 h,在气浴摇床(HNY-1102C,China)上进行,Pb2+浓度用等离子体发射光谱仪(PerkinElmer Avio 200-ICP-OES)测量,其他数据如初始离子浓度等在拟合数据表中说明。对吸附后的结果数据进行Langmuir吸附模型(1)拟合,旨在进一步阐释吸附剂表面与吸附质之间的关系。
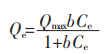
|
(1) |
其中,Qe为单位质量污泥的吸附量,mg/g;b为Langmuir常数;Ce为吸附平衡时水相中的Pb2+浓度,mg/L;Qmax为污泥最大吸附容量,mg/g。
1.3 吸附动力学为检验Pb2+在ANGS上的吸附动力学,采用Lagergren拟一级动力学(式(2))和拟二级动力学(式(3))线性方程式拟合试验数据。
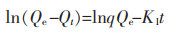
|
(2) |

|
(3) |
其中,Qt为相应时间点吸附量,mg/g;Qe为达到吸附平衡时的吸附量,mg/g;t为吸附时间,min;K1为一级动力学速率常数,min-1;K2为二级动力学常数,g/(mg·min)。
1.4 表征手段采用SEM(美国FEI公司MLA650F)观察吸附前后ANGS的微观形貌变化,同时连用EDS(BRUKER,QUANTAX,Germany)分析吸附前后颗粒表面元素变化。采用FTIR(Thermo Nicolet 6700,USA)观察吸附前后ANGS内官能团变化,其中检测波数范围为4 000~400 cm-1,分辨率4 cm-1。采用XPS(ThermoFischer,EscaLabXi+,USA)表面元素与化学位移进行定性分析,其中测试通能全谱为100 eV,窄谱为20 eV,步长0.05 eV,最后以C1s结合能为284.80 eV的能量标准进行荷电校正。用X射线衍射(XRD)(DX-2700,中国昊远仪器有限公司)在Cu-Kα辐射下检测样品相,扫描速率为4.8 °/min,步长为0.02°。FTIR、XPS、XRD分析的样品处理流程如下:ANGS用去离子水洗涤3次,在冷冻干燥机中冷冻,在-50 ℃的冷井中放置8 h,真空处理24 h,在干燥机中保存备用。
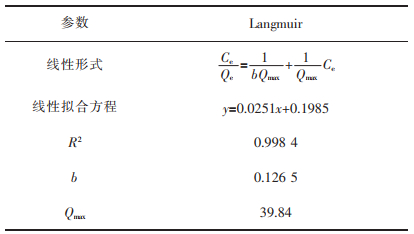
2 结果与讨论 2.1 吸附热力学Langmuir方程是描述物质吸附过程最常用的单分子吸附模型[21-22]。将表 1所列试验数据进行拟合,拟合过程如图 1所示,所得参数如表 2所列。Langmuir方程的R2为0.998 4,显然Langmuir方程可高度拟合ANGS对Pb2+的吸附过程,即吸附过程属于单分子层吸附,对吸附过程起主导作用的是ANGS中的某些官能团发生化学反应或静电吸附作用;Langmuir拟合最大吸附量Qmax为39.84 mg/g。姚磊等拟合出AGS对Pb2+的吸附容量约为44.3 mg/g[10];刘名等的干硝化颗粒污泥对Pb2+的最大吸附容量为79.58 mg/g[11];Huang等磁化改性的AGS活性炭对Pb2+的最大吸附容量可达127.0 mg/g[23],而本研究的吸附容量相对偏小,推测主要是菌群结构的差异导致。与异养AGS相比,ANGS中的自养菌EPS的分泌量明显降低,而EPS对生物吸附容量的大小起着至关重要的作用,本试验所用的硝化颗粒污泥未经驯化与预处理也是影响吸附容量大小的重要原因。
|
|
表 1 吸附热力学拟合数据 |
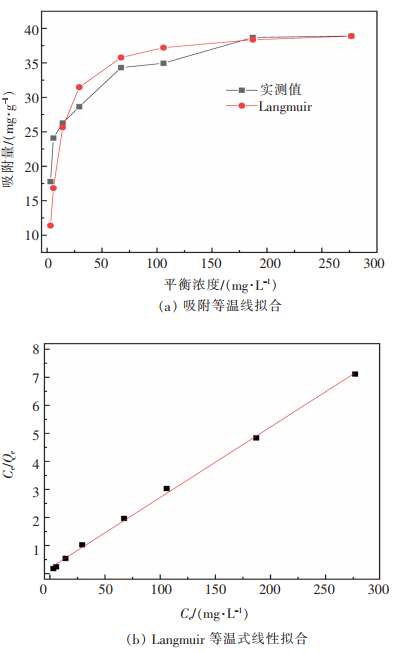 |
| 图 1 Langmuir吸附等温线拟合 |
|
|
表 2 吸附热力学模型参数 |
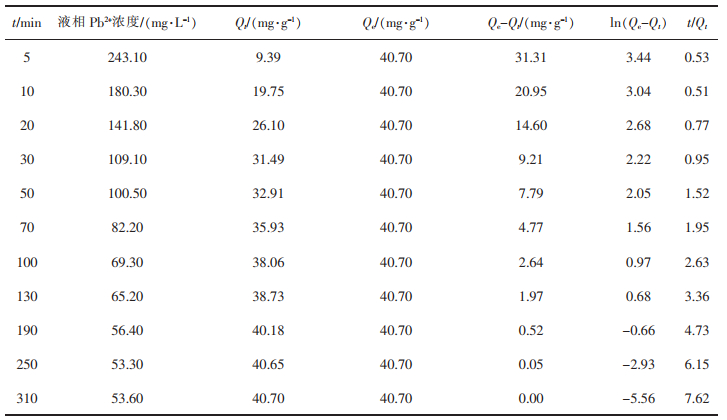
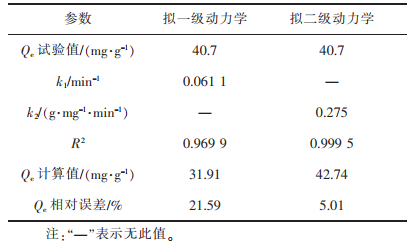
吸附动力学是研究吸附平衡前吸附质在固、液两相之间的分配规律,可反映吸附剂吸附目标物时吸附速率的快慢。本研究采用准一级动力学和准二级动力学模型研究ANGS对Pb2+的吸附过程,Pb2+初始浓度为300 mg/L,MLSS为6 000 mg/L,平衡吸附浓度(Qe)为40.70 mg/L,其他拟合数据如表 3所列,拟合结果及拟合动力学模型参数分别见图 2和表 4。由表 3可以看出,虽然拟一级动力学与拟二级动力学的线性相关系数均在0.95以上,但拟一级动力学模型计算的平衡吸附量与实测值相对误差较大(21.59%),即拟一级动力学模型不能准确描述ANGS对Pb2+的吸附过程。而拟二级动力学模型计算出的平衡吸附量则更接近于试验测量值(误差为5.01%),这表明ANGS对Pb2+吸附过程中的控制步骤为化学吸附,符合传统生物吸附剂的吸附原理[24-25]。
|
|
表 3 吸附动力学拟合数据 |
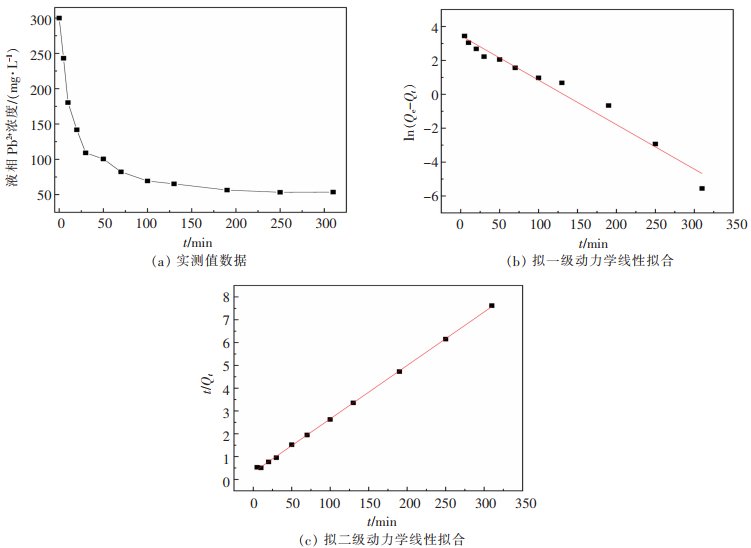 |
| 图 2 ANGS吸附Pb2+的动力学拟合 |
|
|
表 4 吸附动力学模型参数 |
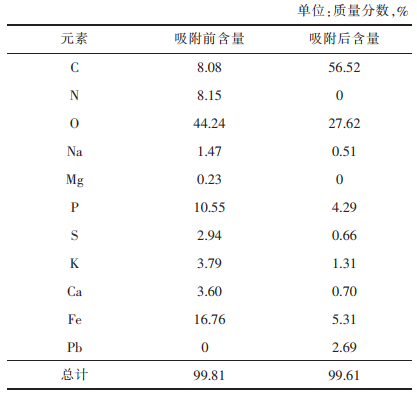
吸附前后ANGS污泥形态变化如图 3所示,ANGS吸附Pb2+前颜色为棕色,吸附后的颗粒污泥颜色明显变浅(略发白),显微镜下观察颗粒污泥依旧保持原有结构,未解体。扫描电镜(SEM)观察到吸附前后ANGS结构依旧致密,微生物(球菌与杆菌)之间紧密结合,即吸附过程并不会损害颗粒污泥结构。总而言之,ANGS对Pb2+具有较强的耐受性,吸附Pb2+不影响其结构稳定性。EDS表征的元素组成如表 5所列,吸附前后的Na、Mg、P、K、Ca、Fe等元素含量均不同程度下降,而Pb元素含量出现了明显上升,表明吸附过程中Pb2+取代原本K+、Ca2+、Na+、Mg2+所占据的吸附位点,故可推断出ANGS吸附Pb2+反应机理包含离子交换反应,这与其他研究者的结论一致[26-27]。
 |
| 图 3 吸附前后ANGS污泥形态变化 |
|
|
表 5 吸附前后污泥表面元素变化 |
吸附前后的ANGS的傅里叶红外光谱结果如图 4所示,3 438.35 cm-1处峰的存在代表了O-H/N-H拉伸[28],在2 927.71 cm-1处峰的存在代表C-H拉伸[29],吸附后这两处特征峰强度减弱,这可能是因O-H/N-H中的H与Pb发生交换反应生成表面羟基络合物引起。1 644.46 cm-1处峰的存在代表蛋白质中C=O/C-N(酰胺I)拉伸,1 544.20 cm-1处峰的存在代表蛋白质中的C=O/C-H弯曲,1 386.34 cm-1处峰代表-COOH上的C=O的伸缩式振动,1 245.15 cm-1处的峰则归因于-COOH或酯的C=O的变形式振动,这些基团中的O具有双电子空位,易与缺乏电子的金属离子进行配位[30],吸附后这些峰的强度改变或偏移,一般是与Pb2+发生络合。1 052.52 cm-1处的强峰则代表磷酸基团上P-O的振动[31],吸附后特征峰强度减弱,结合XRD表征发现,颗粒内存在Pb3(PO4)2和Pb5(PO4)3OH,说明磷酸基团的确参与了对Pb2+的捕捉吸附。因此,ANGS表面存在大量的活性基团(羟基、羧基、氨基、羰基、磷酸基团等),在ANGS吸附Pb2+的过程中,易与Pb2+发生络合或离子交换反应。
 |
| 图 4 ANGS吸附前后FTIR光谱变化 |
ANGS的XPS全谱分析如图 5(a)所示,吸附后的ANGS中出现明显的Pb特征峰(138.85、143.70 eV),被认为是-COO-Pb和-O-Pb络合物[23],证明了ANGS与Pb2+发生了吸附反应。图 5(b)显示了O1s上存在O-H和C-O-C/C-O-H[32],而吸附后O-H的峰面积增大,C-O-C/C-O-H的峰面积减少,可能是C-O-H中的C-O键断裂和H+与Pb2+交换而引发-OH增多。从图 5(c)可知,ANGS的C1s高分辨率光谱在284.81、286.35、288.10 eV出现了3个强峰,分别对应C-C/C-H、C-O-C/C-O-H/C-N和O-C=O官能团[33],图 5(d)中位于399.82 eV处的特征峰可归因于-NH-、-NH2特征峰[34]。吸附后C-C/C-H特征峰面积减小,由于C-C比C-H更加稳定,引起此变化的原因可能是C-H键断裂,结合C-O-C/C-O-H/C-N、O-C=O和-NH-/-NH2峰面积增大的现象,推测C-H断裂后,-C又重新组成了C-O-C/C-O-H/C-N、O-C=O,而-H与-N-组成了-NH-/-NH2,Pb2+在此过程中易与活跃的官能团发生络合反应,有利于ANGS对Pb2+的吸附。
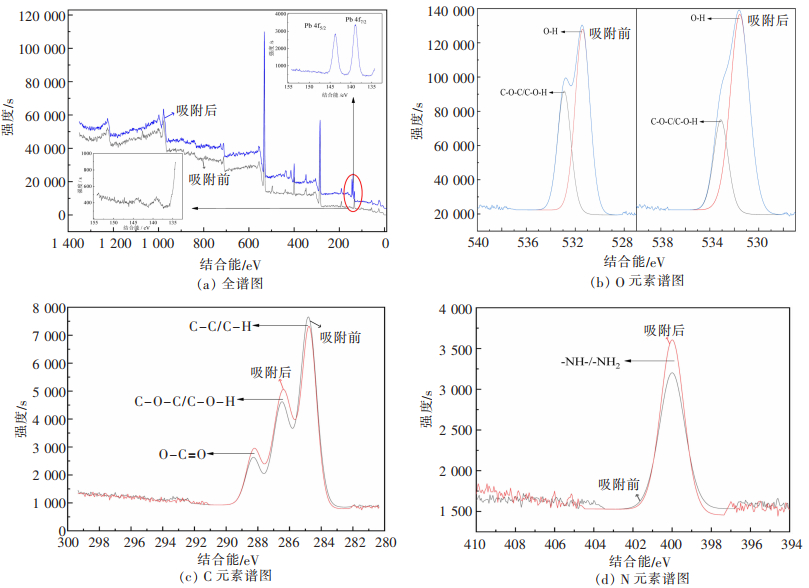 |
| 图 5 ANGS吸附前后XPS光谱变化 |
ANGS吸附前后物相的XRD变化如图 6所示。吸附前后ANGS的衍射峰位置基本相同,而吸附后的ANGS在30.00°~30.40°之间有明显的特征衍射峰。用Jade6.0对其晶相进行分析,与Pb有关的晶相出现在30.136°、30.215°和30.250°,对应的晶体有PbS、Pb(OH)2、Pb3(PO4)2、Pb5(PO4)3OH、PbCO3等[35],这与FTIR和XRD的分析结论一致,即络合物沉淀是ANGS吸附Pb2+的机理之一。颗粒污泥中也常存在硫酸盐还原菌和聚磷菌[36-37],推测是S2-和PO43-与ANGS中的Pb2+发生反应,其产物以晶体形式分布在ANGS中。
 |
| 图 6 吸附前后ANGS的物相变化 |
1)Langmuir与拟二级动力学能较好地描述实际吸附过程,Langmuir拟合出最大吸附量(Qmax)为39.84 mg/g,这与拟二级动力学拟合出的Qmax绝对误差仅为6.8%(R2=0.995),ANGS对Pb2+的吸附主要为表面均匀的单层化学吸附,吸附过程中的控制步骤为化学吸附。
2)ANGS吸附Pb2+的机理包括:Pb2+与ANGS表面的K+、Ca2+、Na+、Mg2+发生离子交换;Pb2+与ANGS表面的O-H、C=O、C-O-H、O-C=O和-NH-等官能团发生化学反应(表面络合);Pb2+与ANGS中带负电的官能团发生静电吸引;Pb2+与ANGS中的阴离子(如CO32-、OH-、PO43-和S2-等)形成无机微沉淀。
| [1] |
FU F L, WANG Q. Removal of heavy metal ions from wastewaters: a review[J]. Journal of Environmental Management, 2011, 92(3): 407-418. DOI:10.1016/j.jenvman.2010.11.011 |
| [2] |
王建龙, 陈灿. 生物吸附法去除重金属离子的研究进展[J]. 环境科学学报, 2010, 30(4): 673-701. |
| [3] |
LIU Y, LAM M C, FANG H H. Adsorption of heavy metals by EPS of activated sludge[J]. Water Science and Technology, 2001, 43(6): 59-66. DOI:10.2166/wst.2001.0340 |
| [4] |
MARKOU G, MITROGIANNIS D, ÇELEKLI A, et al. Biosorption of Cu2+ and Ni2+ by arthrospira platensis with different biochemical compositions[J]. Chemical Engineering Journal, 2015, 259: 806-813. DOI:10.1016/j.cej.2014.08.037 |
| [5] |
LAURENT J, CASELLAS M, DAGOT C. Heavy metals biosorption on disintegrated activated sludge: Description of a new equilibrium model[J]. Chemical Engineering Journal, 2010, 164(1): 63-69. DOI:10.1016/j.cej.2010.08.023 |
| [6] |
WANG Q, DU G C, CHEN J. Aerobic granular sludge cultivated under the selective pressure as a driving force[J]. Process Biochemistry, 2004, 39(5): 557-563. DOI:10.1016/S0032-9592(03)00128-6 |
| [7] |
LIU L L, WANG Z P, YAO J, et al. Investigation on the formation and kinetics of glucose-fed aerobic granular sludge[J]. Enzyme and Microbial Technology, 2005, 36(5/6): 712-716. |
| [8] |
XU H, TAY J H, FOO S K, et al. Removal of dissolved copper(Ⅱ) and zinc(Ⅱ) by aerobic granular sludge[J]. Water Science and Technology, 2004, 50(9): 155-160. DOI:10.2166/wst.2004.0559 |
| [9] |
SUN X F, LIU C Y, MA Y, et al. Enhanced Cu(Ⅱ) and Cr(Ⅵ) biosorption capacity on poly(ethylenimine) grafted aerobic granular sludge[J]. Colloids and Surfaces B: Biointerfaces, 2011, 82(2): 456-462. DOI:10.1016/j.colsurfb.2010.10.002 |
| [10] |
姚磊, 叶正芳, 王中友, 等. 好氧颗粒污泥对Pb2+的吸附特性研究[J]. 科学通报, 2007, 52(20): 2434-2438. DOI:10.3321/j.issn:0023-074x.2007.20.016 |
| [11] |
刘名, 唐朝春, 衷诚, 等. 干硝化好氧颗粒污泥对Pb2+的吸附特性与机理[J]. 环境科学研究, 2015, 28(12): 1923-1930. |
| [12] |
李姝, 胡学伟, NGUYEN DINH T, 等. 干燥好氧颗粒污泥对重金属的吸附研究[J]. 工业水处理, 2013, 33(10): 40-43. |
| [13] |
张江水, 刘文, 孙卫玲, 等. 胞外聚合物对Pb2+和Cd2+吸附行为研究[J]. 北京大学学报(自然科学版), 2013, 49(3): 514-522. |
| [14] |
NANCHARAIAH Y V, KIRAN KUMAR REDDY G. Aerobic granular sludge technology: Mechanisms of granulation and biotechnological applications[J]. Bioresource Technology, 2018, 247: 1128-1143. DOI:10.1016/j.biortech.2017.09.131 |
| [15] |
WANG H Y, SONG Q, WANG J, et al. Simultaneous nitrification, denitrification and phosphorus removal in an aerobic granular sludge sequencing batch reactor with high dissolved oxygen: Effects of carbon to nitrogen ratios[J]. Science of the Total Environment, 2018, 642: 1145-1152. DOI:10.1016/j.scitotenv.2018.06.081 |
| [16] |
张斌超, 曾敏静, 张立楠, 等. 自养硝化颗粒污泥吸附铜离子性能及吸附等温线[J]. 化工进展, 2020, 39(4): 1583-1590. |
| [17] |
XIA J T, YE L, REN H Q, et al. Microbial community structure and function in aerobic granular sludge[J]. Applied Microbiology and Biotechnology, 2018, 102(9): 3967-3979. DOI:10.1007/s00253-018-8905-9 |
| [18] |
FRA-VÁZQUEZ A, MORALES N, FIGUEROA M, et al. Bacterial community dynamics in long-term operation of a pilot plant using aerobic granular sludge to treat pig slurry[J]. Biotechnology Progress, 2016, 32(5): 1212-1221. DOI:10.1002/btpr.2314 |
| [19] |
PALMA T L, DONALDBEN M N, COSTA M C, et al. Putative role of flavobacterium, dokdonella and methylophilus strains in paracetamol biodegradation[J]. Water, Air, & Soil Pollution, 2018, 229(6): 1-23. |
| [20] |
RODRIGUEZ-SANCHEZ A, LEYVA-DIAZ J C, GONZALEZ-MARTINEZ A, et al. Linkage of microbial kinetics and bacterial community structure of MBR and hybrid MBBR-MBR systems to treat salinity-amended urban wastewater[J]. Biotechnology Progress, 2017, 33(6): 1483-1495. DOI:10.1002/btpr.2513 |
| [21] |
MALAKOOTIAN M, MANSOORIAN H J, YARIA R. Removal of reactive dyes from aqueous solutions by a non-conventional and low cost agricultural waste: adsorption on ash of Aloe Vera plant[J]. Iranian Journal of Health, Safety and Environment, 2014, 1(3): 117-125. |
| [22] |
DAVIS C W, DI TORO D M. Modeling nonlinear adsorption to carbon with a single chemical parameter: a lognormal Langmuir isotherm[J]. Environmental Science & Technology, 2015, 49(13): 7810-7817. |
| [23] |
HUANG X, WEI D, ZHANG X W, et al. Synthesis of amino-functionalized magnetic aerobic granular sludge-biochar for Pb(Ⅱ) removal: Adsorption performance and mechanism studies[J]. Science of the Total Environment, 2019, 685: 681-689. DOI:10.1016/j.scitotenv.2019.05.429 |
| [24] |
HUANG D L, LI B, OU J, et al. Megamerger of biosorbents and catalytic technologies for the removal of heavy metals from wastewater: Preparation, final disposal, mechanism and influencing factors[J]. Journal of Environmental Management, 2020, 261: 109879. DOI:10.1016/j.jenvman.2019.109879 |
| [25] |
XU S Z, XING Y H, LIU S, et al. Characterization of Cd2+ biosorption by Pseudomonas sp.strain 375, a novel biosorbent isolated from soil polluted with heavy metals in Southern China[J]. Chemosphere, 2020, 240: 124893. DOI:10.1016/j.chemosphere.2019.124893 |
| [26] |
WANG X H, SONG R H, TENG S X, et al. Characteristics and mechanisms of Cu(Ⅱ) biosorption by disintegrated aerobic granules[J]. Journal of Hazardous Materials, 2010, 179(1/2/3): 431-437. |
| [27] |
WANG L, WAN C L, ZHANG Y, et al. Mechanism of enhanced Sb(V) removal from aqueous solution using chemically modified aerobic granules[J]. Journal of Hazardous Materials, 2015, 284: 43-49. DOI:10.1016/j.jhazmat.2014.10.041 |
| [28] |
WU D, HU L H, WANG Y G, et al. EDTA modified β-cyclodextrin/chitosan for rapid removal of Pb(Ⅱ) and acid red from aqueous solution[J]. Journal of Colloid and Interface Science, 2018, 523: 56-64. DOI:10.1016/j.jcis.2018.03.080 |
| [29] |
YAO L, YE Z F, TONG M P, et al. Removal of Cr3+ from aqueous solution by biosorption with aerobic granules[J]. Journal of Hazardous Materials, 2009, 165(1/2/3): 250-255. |
| [30] |
KOSASIH A N, FEBRIANTO J, SUNARSO J, et al. Sequestering of Cu(Ⅱ) from aqueous solution using cassava peel (Manihot esculenta)[J]. Journal of Hazardous Materials, 2010, 180(1/2/3): 366-374. |
| [31] |
VAN HULLEBUSCH E D, PEERBOLTE A, ZANDVOORT M H, et al. Sorption of cobalt and nickel on anaerobic granular sludges: isotherms and sequential extraction[J]. Chemosphere, 2005, 58(4): 493-505. DOI:10.1016/j.chemosphere.2004.09.017 |
| [32] |
LIU W, ZHANG J S, JIN Y J, et al. Adsorption of Pb(Ⅱ), Cd(Ⅱ) and Zn(Ⅱ) by extracellular polymeric substances extracted from aerobic granular sludge: Efficiency of protein[J]. Journal of Environmental Chemical Engineering, 2015, 3(2): 1223-1232. DOI:10.1016/j.jece.2015.04.009 |
| [33] |
ZHAO J J, NIU Y Z, REN B, et al. Synthesis of Schiff base functionalized superparamagnetic Fe3O4 composites for effective removal of Pb(Ⅱ) and Cd(Ⅱ) from aqueous solution[J]. Chemical Engineering Journal, 2018, 347: 574-584. DOI:10.1016/j.cej.2018.04.151 |
| [34] |
LV Y, ZHANG R S, ZENG S L, et al. Removal of p-arsanilic acid by an amino-functionalized indium-based metal-organic framework: Adsorption behavior and synergetic mechanism[J]. Chemical Engineering Journal, 2018, 339: 359-368. DOI:10.1016/j.cej.2018.01.139 |
| [35] |
张国胜, 程红艳, 张海波, 等. 双孢菇菌糠生物炭吸附Pb2+机制及其环境应用潜力[J]. 农业环境科学学报, 2021, 40(3): 659-667. |
| [36] |
KIJJANAPANICH P, PAKDEERATTANAMINT K, LENS P N L, et al. Organic substrates as electron donors in permeable reactive barriers for removal of heavy metals from acid mine drainage[J]. Environmental Technology, 2012, 33(23): 2635-2644. |
| [37] |
YAO L, YE Z F, TONG M P, et al. Removal of Cr3+ from aqueous solution by biosorption with aerobic granules[J]. Journal of Hazardous Materials, 2009, 165(1/2/3): 250-255. |
 2022, Vol. 42
2022, Vol. 42