2. 中国石油 石油化工研究院,北京 100195
2. Petrochina Petrochemical Research Institute, Beijing 100195, China
植物油作为一种储量丰富且可再生的能源,是具有重要潜在利用价值的新型能源[1]。植物油的主要成分为高级脂肪酸,具有相对分子量较大、氧含量较高等特点[2, 3],将其加氢脱氧可制得高品质的生物柴油。植物油的加氢脱氧反应主要有两个路径,即路径1为直接加氢脱水反应,具有柴油馏分收率高、耗氢较多的特点;路径2为加氢脱羧基反应和加氢脱羰基反应,具有柴油馏分收率低、耗氢较少的特点[4]。
将MoNi/La-Al2O3用于催化大豆油加氢脱氧,在大豆油加氢脱氧率为94.3%时,其直接加氢脱水和加氢脱羧基/脱羰基的选择性分别为31.4%和68.6%[5]。以MoNi/Al2O3为催化剂,张超等[6]的棕榈油加氢脱氧结果表明,在棕榈油脱氧率为100%时,其直接加氢脱水的选择性为53.9%,而加氢脱羧基/脱羰基的选择性则为41.6%。以Fe/SBA-15为催化剂加氢处理油酸,所得加氢脱羧基/脱羰基的选择性约为84%[7]。上述的催化剂及植物油的加氢脱氧研究仅着眼于催化剂的综合加氢脱氧性能及植物油中氧的总脱除,而没有关注氧的脱除是以哪个路径为主的问题,即催化剂的哪个路径性能占优的问题。
有文献报道[2, 8],Ni有利于加氢脱羧基/脱羰基反应,Mo有利于加氢脱水反应。Rocha等[9]考察了Mo2C/Al2O3催化剂对丙烯酸加氢脱氧的影响,结果显示Mo能抑制丙烯酸中C-C键的断裂,而促进丙烯酸中C-O键的断裂,从而使丙烯酸的氧以水的形式脱除。Leng等[10]研究NiFe/γ-Al2O3催化剂的加氢脱氧性能时,发现助剂Fe的加入有利于生物油中C-O键的断裂。
加氢脱氧需要在氢气的环境下进行,应根据当地的氢气资源状况来选用性能适宜的催化剂以实现植物油加氢脱氧路径的可调控,进而实现资源的合理利用和生物柴油生产成本的降低。达到此目的的关键是开发两个路径的催化性能分别占优的加氢脱氧催化剂。本文以MgAl2O4为载体,通过调节活性组分钼镍的比例和助剂改性等以获得两个路径的催化性能分别占优的加氢脱氧催化剂。
2 实验部分 2.1 主要原料硝酸镁(Mg(NO3)2·6H2O)、硝酸铝(Al(NO3)3·9H2O)、硝酸铁(Fe(NO3)3·9H2O)、硝酸钴(Co(NO3)2·6H2O)、浓氨水(沉淀剂)、钼酸铵((NH4)6Mo7O24·4H2O)、硝酸镍(Ni NO3) 2·6H2O)、柠檬酸(C6H8O·7H2O,CA)、十六烷基三甲基溴化铵(C19H42BrN,CTAB)。以上均为AR级,均购自天津科密欧试剂有限公司。田菁粉,化学纯,江苏灌南县宏图植物胶有限公司;小桐子油为大庆化工研究中心提供。
2.2 催化剂的制备1) 镁铝尖晶石粉体的制备
将一定量的硝酸镁、硝酸铝和十六烷基三甲基溴化铵溶解到蒸馏水中,加热搅拌至均匀,用氨水调节混合溶液的pH,将混合液置于80℃水浴锅中机械搅拌3 h得到沉淀物;沉淀物在室温下静态老化1 h;经120℃干燥后研磨,于马弗炉中700℃焙烧6 h,制得镁铝尖晶粉体。
2) 载体的制备
将MgAl2O4粉体、氢氧化铝干胶、田菁粉按摩尔比为6:4:0.5混合均匀,滴加3%的稀硝酸,用挤条器挤压成直径为2 mm的圆柱体条,置于室温下自然晾干,晾干后将其截为2~3 mm长的圆柱形颗粒,然后于马弗炉中700℃焙烧6 h得催化剂载体。
3) 活性组分的负载
按比例称取一定量的硝酸镍、钼酸铵、柠檬酸,摩尔比为Ni:Mo = 0~∞,(Mo+Ni):柠檬酸摩尔比=3,溶于去离子水中,采用等体积浸渍法负载活性组分(活性组分MoO3+NiO的负载量为载体质量的30%),室温下静置10 h,于烘箱110℃下干燥12 h后,把助剂溶于去离子水中,浸渍到载体上,室温下静置12 h,于马弗炉中分别在110℃干燥3 h和500℃焙烧3 h,得到催化剂。催化剂记为Cat1~Cat11(未添加助剂Ni/Mo=0、0.2、0.4、0.6、0.8、1、1.25、1.67、2.5、5、∞);对Cat1分别(Ni/Mo = 0)添加助剂(分别为0.5%H3BO3、1%NH4F、3%W(NO3)3、2%Co(NO3)3、1%Fe(NO3)3、10% Fe(NO3)3)得催化剂Cat12~Cat17。
2.3 催化剂的活性评价以含体积分数20%小桐子油的正辛烷(由于加氢脱氧反应属于强放热反应,加入溶剂稀释了反应原料,有利于反应热的及时移除,避免出现局部过热,以便有效地控制反应温度)溶液为原料评价催化剂的性能。催化剂的评价在固定床反应装置上进行,反应器长约300 mm,外径21 mm,内径10 mm;催化剂颗粒长2~3 mm,直径2 mm,装填量5 mL,催化剂两端填充粒径20~40目石英砂。催化剂首先在温度400℃、压力0.1 MPa、氢气流速30 mL·min-1条件下还原活化3 h,当温度降至370℃时,调节反应压力2 MPa,液时空速1 h-1,氢油体积比200,用高压微量进样泵将原料泵入反应器进行反应。冷凝后的反应产物在北分瑞利公司生产的SP-3420A气相色谱仪上进行分析。
2.4 反应产物的分析方法植物油的加氢脱氧反应路径包括直接加氢脱水反应(HDW)和加氢脱羧(羰)基反应(DCX)[11],反应机理见图 1。在图 1中,路径1为直接加氢脱水反应,生成物主要是C16、C18等偶碳数烃和C3H8、H2O;路径2为加氢脱羧(羰)基反应,生成物主要是C15、C17等奇碳数烃和C3H8、CO、CO2。以气相色谱分析液相产物中的偶碳数烃选择性(SHDW)和奇碳数烃的选择性(SDCX)评价催化剂的加氢脱氧性能。
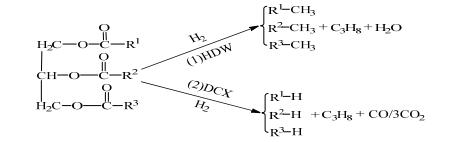
|
图 1 甘油三酸酯的加氢脱氧路径 Fig.1 Reaction pathways of triglyceride hydrodeoxygenation |
| $ {S_{{\rm DCX}}} = \frac{{{A_{C15}} + {A_{C17}}}}{{{A_{C15}} + {A_{C16}} + {A_{C17}} + {A_{C18}}}} \times 100\% $ |
| $ {S_{{\rm HDW}}} = \frac{{{A_{C16}} + {A_{C18}}}}{{{A_{C15}} + {A_{C16}} + {A_{C17}} + {A_{C18}}}} \times 100\% $ |
其中AC15、AC16、AC17、AC18分别为色谱谱图上的C15、C16、C17、C18的峰面积。
2.5 催化剂的表征催化剂(氧化态)的X射线衍射(XRD)表征在D/Max-2500上进行,采用CuKα光源,RS为0.15 nm,狭缝SS/DS为1°,扫描2θ为5~90°,扫描速度为12°·min-1。催化剂的NH3-TPD、H2-TPD和H2-TPR表征皆在Micromeritics公司的Auto ChemII-2920型化学吸附分析仪上进行。NH3-TPD测试,称取100 mg样品用量,以He气作为载气,将样品在低于焙烧温度下净化,之后降温至吸附温度110℃,吸附NH3至饱和,以流量50 mL·min-1进行氦气吹扫除去NH3,然后以10℃·min-1的升温速率升温至700℃,采用热导(TCD)检测器。催化剂的H2-TPD测试,称取0.3 g样品,在500℃下用氢还原1 h,然后在氢气中缓慢降至室温,切换高纯氮气吹扫,待色谱基线稳定后,以10℃·min-1程序升温至900℃,采用热导(TCD)检测器。催化剂的H2-TPR测试,称取0.1 g样品,在还原气体为5%H2~95%A r混合气(体积分数),气体流量50 mL·min-1,升温速率10℃·min-1,升温至900℃,采用热导检测器检测信号。催化剂的孔结构性质分析在美国Micromeritics公司生产的ASPA2020型比表面积和孔隙度分析仪上进行,样品在423 K下抽真空,脱附4 h,在液氮温度下吸附N2,根据催化剂的N2吸附脱附特性,获得催化剂的比表面积(BET法)和孔径分布(BJH法,脱附分支)数据。催化剂的吡啶吸附红外(Py-IR)表征在NICOLET NEXUS-470型傅里叶变换红外光谱仪上进行,仪器分辨率为4 cm-1,DTGS检测器。
3 结果与讨论 3.1 镍钼比对催化剂性质的影响 3.1.1 镍钼比对催化剂晶相结构的影响图 2为不同镍钼比催化剂的XRD谱图。由图 2可见,在2θ =19.0°,31.2°,36.8°,44.9°,59.4°,65.4°,77.4°及82.9°处均出现了MgAl2O4的特征衍射峰,这表明Ni和Mo的负载对载体的晶相结构未产生明显的影响。Ni/Mo =2.5时,无明显的MoO3和NiO的特征衍射峰,表明MoO3和NiO在催化剂中具有良好的分散度。
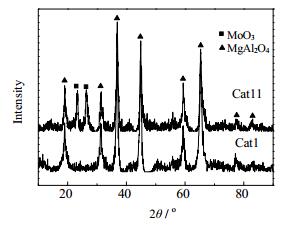
|
图 2 不同镍钼比催化剂的XRD谱图 Fig.2 XRD patterns of catalysts with different Ni/Mo ratios |
图 3为不同钼镍比催化剂的H2-TPR图谱。由图 3可见,催化剂Cat1在中温480℃附近和高温790℃附近各出现一个还原峰,并在中温500℃出现一个伴峰。通常中温峰为MoO3的还原峰;高温峰为MoO3与载体MgAl2O4的强相互作用的还原峰。在镍钼比为2.5时,MoO3高温峰消失,且在低温380℃处出现一个伴峰,此为NiO的还原峰,表明镍的加入减弱了活性组分MoO3与载体的相互作用,促进了MoO3的还原,降低了MoO3的还原温度,使其高温处的峰消失,更有利于催化剂的还原[12]。同时由于MoO3的存在使NiO还原性也得到改善,形成大量的Ni金属单质,而Ni金属单质有利于C-C键的断裂[8],这将相应地可提高催化剂的加氢脱羰/脱羧性能。
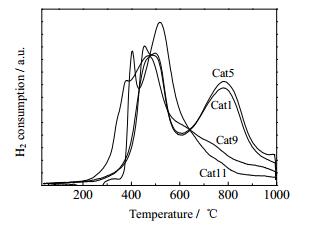
|
图 3 不同镍钼比催化剂的H2-TPR图谱 Fig.3 H2-TPR patterns of catalysts with different Ni/Mo ratios |
催化剂的NH3–TPD表征可以确定其表面酸性的强弱和酸量。通常根据脱附温度,可把酸分为弱酸(150~250℃)、中强酸(250~400℃)和强酸(400℃以上)[14]。图 4为不同镍钼比催化剂的NH3–TPD谱图。从图可知,Cat1、Cat5、Cat9和Cat11催化剂在200℃均存在脱附峰,即这四个催化剂皆存在弱酸中心,且Cat9和Cat11的总酸量多于Cat1的,催化剂的总酸量多有利于C-C键的断裂[15]。Cat1的弱酸酸量较多,弱酸酸性位有利于C-O键的断裂,即弱酸是催化植物油加氢脱水反应所需的;Cat9具有较多的中强酸酸性位,中强酸酸性位有利于C-C键的断裂[16]。
|
图 4 不同镍钼比催化剂的NH3-TPD图谱 Fig.4 NH3-TPD patterns of catalysts with different Ni/Mo ratios |
Cat16和Cat17分别为由Cat1添加1% Fe(NO3)3和10% Fe(NO3)3所得的催化剂。由图 5可见,三者的XRD谱图中均出现了MoO3的衍射峰,但随着助剂Fe添加量的增加,MoO3衍射峰高度明显降低且宽度增加,这表明助剂Fe的加入增加了MoO3在催化剂表面的分散性。在Cat16和Cat17的XRD谱图中未见Fe2O3的衍射峰,这可能因为Fe的添加量较少或分散度较好所致[17]。
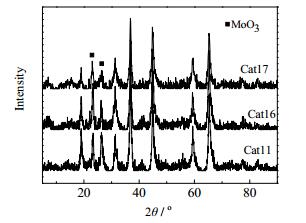
|
图 5 催化剂的XRD谱图 Fig.5 XRD patterns of the catalysts |
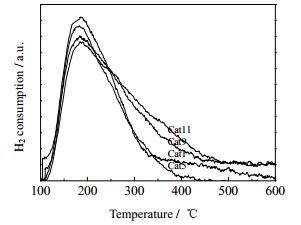
H2-TPD法是测定还原态金属催化剂活性表面的有效方法之一,脱附温度高低可以反映H在金属表面吸脱附的难易,且脱附峰面积的大小反映了脱附量多少[18]。图 6为Cat1、Cat16和Cat17的H2-TPD图谱。由图 6可见,Cat1、Cat16和Cat17的H2-TPD图谱均有一个低温脱附峰和一个高温脱附峰。低温脱附峰可归属为吸附在金属表面氢的脱附,高温脱附峰为吸附在氧化物表面的溢流氢的脱附[19]。与Cat1相比,Cat16和Cat17的高温处峰面积明显增大,且都在850℃附近出现了新的脱附峰,这表明其溢流氢的数量增多,即助剂Fe的加入可提高催化剂表面活性氢的数量。与Cat16相比,Cat17的高温处峰面积明显增大,即增加助剂Fe的添加量有利于增加催化剂表面活性氢(溢流氢)的数量,从而有助于提高催化剂的活性。随着助剂Fe添加量的增加,高温脱附峰向低温处移动,由于助剂Fe的加入促进了活性组分的分散,活性中心能更好地与H2接触,减弱了催化剂表面强吸附H2活性中心与H2的键和能力[20]。由文献[17]可知,助剂Fe还可增加催化剂表面氧空穴的数量,从而促进C-O键断裂。催化剂表面溢流氢数量的增多将增加H与高级脂肪酸的接触几率,从而增强了催化剂的加氢能力,促进C-O键的活化。因此在Mo基催化剂中加入Fe有利于催化剂的加氢脱羧(羰)基性能向直接加氢脱水性能转换。
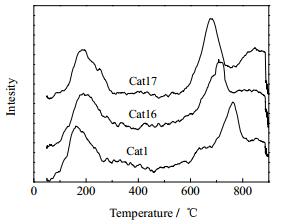
|
图 6 不同催化剂的H2-TPD曲线 Fig.6 H2-TPD profiles of different catalysts |
图 7为Cat1、Cat16和Cat17的NH3-TPD谱图。由图 7可见,Cat1、Cat16和Cat17在200℃处皆存在脱附峰,这表明三个催化剂都存在弱酸中心。加入10% Fe(NO3)3后,Cat17的脱附峰峰高明显降低,即Fe的加入降低了催化剂表面的酸量。比较Cat16和Cat17可知,随着Fe添加量的增加,脱附峰的高度降低,峰面积明显减少。这是因为助剂Fe的加入使催化剂表面暴露的金属位点减少[21, 22],从而使催化剂表面的酸性中心减少。较少的酸量可提高催化剂的催化直接加氢脱水性能。
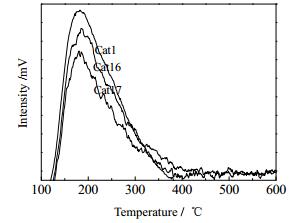
|
图 7 催化剂的NH3-TPD图谱 Fig.7 NH3-TPD patterns of different catalysts |
Cat1、Cat16和Cat17的Py-IR表征结果见图 8。由图 8可知,Cat1、Cat16和Cat17都在1450 cm-1和1620 cm-1处存在吡啶配位与L酸位键合的特征峰,这表明在这三个催化剂上都存在L酸中心;1490 cm-1处的吸收峰则是L酸和B酸共同作用的结果[22];三个催化剂在1540 cm-1处没有明显峰,说明催化剂不存在B酸中心。由图 8可见,L酸吸收峰较强,说明催化剂中主要以L酸为主。与Cat1相比,Cat17中的L酸酸量明显增加。比较Cat16和Cat17可知,增加助剂Fe的添加量,使催化剂中L酸酸量增加。这可能是由于大部分的铁原子以氧化物的形式存在于催化剂的表面,而铁氧化物是一种L酸,故加入Fe后催化剂的L酸明显增多[23],Fe的添加量越多,L酸酸量增加越明显。L酸增多,越有利于C-O键的断裂,因此助剂Fe的加入可催化剂的直接加氢脱水性能。
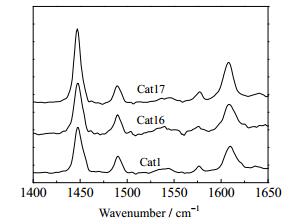
|
图 8 催化剂的Py-IR图谱 Fig.8 Py-IR patterns of different catalysts |
Cat1、Cat16和Cat17的N2吸附脱附等温曲线和孔径分布分别见图 9(a)、图 9(b),对应的结构参数见表 1。由图 9(a)可以看出,Cat1、Cat16和Cat17的吸附曲线均为典型的Ⅳ型吸附曲线,在相对较高的压力下均呈现出明显的滞后环,这表明所测催化剂均具有介孔结构。从图 9(b)中可以看出,Cat1、Cat16和Cat17的孔径主要分布在2~20 nm。由表 1中的数据可知,随着助剂Fe添加量的增加,孔容和孔径都有所减小,可能是因为助剂Fe添加量的增加,使更多的Fe附着在孔表面。
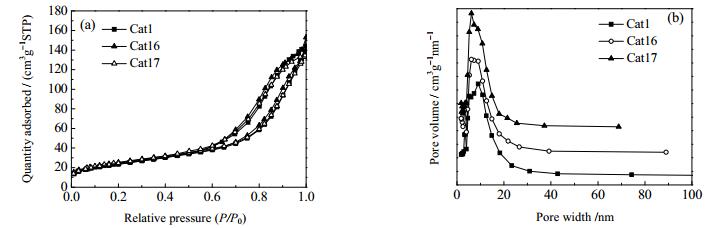
|
图 9 催化剂的N2吸附-脱附曲线和孔径分布曲线 Fig.9 N2 adsorption/desorption isotherms and pore diameter distribution of different catalysts |
|
|
表 1 催化剂的结构参数 Table 1 Structural parameters of different catalysts |
在连续固定床上考察了不同催化剂的催化小桐子油的加氢脱氧性能,结果见图 10、11。由图 10可见,不同Ni/Mo催化剂作用的植物油的加氢脱氧率(HDO)皆大于98%;在Ni/Mo =0时,植物油加氢脱氧的脱羰/脱羧产物选择性最低,植物油直接加氢脱氧的脱水产物选择性可达49.8%;随着镍钼比的增加,催化剂催化性能向路径2移动,即植物油加氢脱氧反应路径由直接加氢脱水反应向加氢脱羧/脱羰基反应方向移动,在Ni/Mo = 2.5时,其植物油加氢脱氧的脱羰/脱羧产物选择性最高可达90.2%;继续增加镍钼比,则催化剂催化性能向路径2移动,对应的植物油加氢反应路径由加氢脱羧基/脱羰基反应向直接加氢脱水反应方向移动。由图 11可知,添加不同助剂(H3BO3、NH4F、W(NO3)3、Co(NO3)3、Fe(NO3)3)均可以不同程度地调变催化剂的催化性能。比较Cat16和Cat17的评价结果可知,增加助剂Fe(NO3)3的添加量,可以使催化剂的催化性能明显地向路径1移动。在Cat17上,植物油直接加氢脱氧的脱水产物选择性可达91.8%。
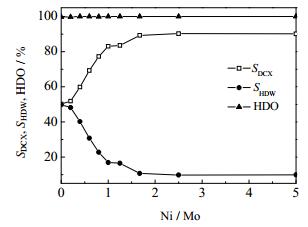
|
图 10 镍钼比对催化剂加氢脱氧性能的影响 Fig.10 Effects of Ni/Mo ratios on hydrodeoxygenation performance of the catalysts |
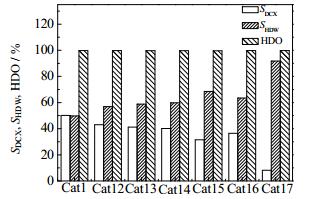
|
图 11 助剂改性对催化剂加氢脱氧性能的影响 Fig.11 Effects of auxiliary modification on hydrodeoxygenation performance of the catalysts |
a) 增大Ni/Mo比可增加MoNi/MgAl2O4催化剂的总酸量,酸量的增多有利于植物油加氢脱氧时C-C键的断裂;加入适量的镍可以减弱活性组分MoO3与载体的相互作用,促进了MoO3的还原,降低了MoO3的还原温度,使其高温处的峰消失,更有利于催化剂的还原;减小Ni/Mo比,可以增加MoNi/MgAl2O4催化剂表面的弱酸酸量,弱酸的增加有利于植物油加氢脱氧时C-O的断裂。
b) 助剂Fe的加入,使催化剂的孔容和孔径都有所减小、Mo/MgAl2O4催化剂的总酸量减少、L酸量和催化剂的表面活性氢量明显增加。L酸有利于C-O的断裂,较多的表面活性氢有利于提高催化剂的直接加氢脱氧性能。
c) 在不同Ni/Mo催化剂上植物油的加氢脱氧率皆大于98%;Ni/Mo =2.5的MoNi/MgAl2O4催化剂表现出较高的加氢脱羰/脱羧性能,对应的植物油加氢脱氧的脱羰/脱羧产物选择性高达90.2%;添加助剂H3BO3、NH4F、W(NO3)3、Co(NO3)3、Fe(NO3)3等均可不同程度地调变Mo/MgAl2O4催化剂的催化性能,添加10% Fe(NO3)3的Mo/MgAl2O4具有较高的直接加氢脱氧性能,对应的植物油加氢脱氧的脱水产物选择性达到为91.8%。
| [1] | Bezergianni S, Dimitriadis A. Comparison between different types of renewable diesel[J]. Renew Sustain Energy Reviews, 2013, 21(5): 110-116. |
| [2] | Kubička D, Kaluža L. Deoxygenation of vegetable oils over sulfided Ni, Mo and NiMo catalysts[J]. Applied Catalysis A General, 2010, 372(2): 199-208. DOI:10.1016/j.apcata.2009.10.034. |
| [3] | Lestari S, Mäkiarvela P, Beltramini J, et al. Transforming triglycerides and fatty acids into biofuels[J]. Chemsuschem, 2009, 2(12): 1109-1119. DOI:10.1002/cssc.v2:12. |
| [4] | ZHAO Yang(赵阳), MENG Xiang-kun(孟祥堃), WANG Xuan(王宣), et al. Hydrotreating of palm oil for diesel fraetion with high cetane number(棕榈油加氢制备高十六烷值柴油组分)[J]. Acta Petrolei Sinica(石油学报), 2011, 27(4): 501-507. DOI:10.3969/j.issn.1001-8719.2011.04.001. |
| [5] | YU Shuang (于爽). Hydrodeoxygenation of soybean oil to the second generation biodiesel over NiMo/La-Al2O3 catalysts (NiMo/La-Al2O3催化大豆油加氢脱氧制第二代生物柴油)[D]. Dalian (大连):Dalian University of Technology (大连理工大学), 2015. http://cdmd.cnki.com.cn/Article/CDMD-10141-1015357578.htm |
| [6] | ZHANG Chao(张超), NIE Hong(聂红), GAO Xiao-dong(高晓冬), et al. Hydrodeoxygenation rules of palm oil(棕榈油加氢脱氧反应的规律)[J]. Acta Petrolei Sinica(石油学报), 2014, 30(4): 587-594. DOI:10.3969/j.issn.1001-8719.2014.04.003. |
| [7] | Bhattacharjee S, Tan C S. Hydrodeoxygenation of oleic acid in hexane containing pressurized CO2 using Fe/SBA-15 as catalyst[J]. Journal of Cleaner Production, 2017, 156(7): 203-213. |
| [8] | Duan Y N, Wu Y L, Zhang Q H, et al. Towards conversion of octanoic acid to liquid hydrocarbon via hydrodeoxygenation over Mo promoter nickel-based catalyst[J]. Journal of Molecular Catalysis A Chemical, 2015, 398(3): 72-78. |
| [9] | Rocha A S, Leandro A S, Ricardo R, et al. Hydrodeoxygenation of acrylic acid using Mo2C/Al2O3[J]. Applied Catalysis A General, 2017, 531(3): 69-78. |
| [10] | Leng S, Wang X D, He X B, et al. NiFe/γ-Al2O3:a universal catalyst for the hydrodeoxygenation of bio-oil and its model compounds[J]. Catalysis Communications, 2013, 41(11): 34-37. |
| [11] | Pattanaik B P, Misra R D. Effect of reaction pathway and operating parameters on the deoxygenation of vegetable oils to produce diesel range hydrocarbon fuels:A review[J]. Renewable & Sustainable Energy Reviews, 2017, 73(6): 545-557. |
| [12] | YANG Jun(杨骏), CHEN Man-ying(陈满英), CHEN Yun-hong(陈运红), et al. Study of Ni-Mo/Al2O3 catalyst for hydrodeoxygenation(Ni-Mo/Al2O3加氢脱氧催化剂的研究)[J]. Modern Chemical Industry(现代化工), 2005, 25(z1): 119-122. DOI:10.3321/j.issn:0253-4320.2005.z1.030. |
| [13] | Imai H, Kimura T, Terasaka K, et al. Hydroconversion of fatty acid derivative over supported Ni-Mo catalysts under low hydrogen pressure[J]. Catalysis Today, 2018, 303(4): 185-190. |
| [14] | Bunch A Y, Wang X, Ozkan U S. Adsorption characteristics of reduced Mo and Ni-Mo catalysts in the hydrodeoxygenation of benzofuran[J]. Applied Catalysis A General, 2008, 364(1): 96-103. |
| [15] | Ameen M, Azizan M T, Yusup S, et al. Catalytic hydrodeoxygenation of triglycerides:An approach to clean diesel fuel production[J]. Renewable & Sustainable Energy Reviews, 2017, 80(5): 1072-1088. |
| [16] | Zuo H L, Liu Q Y, Wang T J, et al. Hydrodeoxygenation of methyl palmitate over supported Ni catalysts for diesel-like fuel production[J]. Energy & Fuels, 2012, 26(6): 3747-3755. |
| [17] | Phan T N, Chang H K. Synergistic effects of Ru and Fe on titania-supported catalyst for enhanced anisole hydrodeoxygenation selectivity[J]. Catalysis Today, 2018, 303(4): 219-226. |
| [18] | YANG Yan-ping (杨艳萍). Preparation, characterization of Ni/TiO2-SiO2 and catalytic performance for maleic anhydride hydrogenation (Ni/TiO2-SiO2:催化剂的制备、表征及顺配加氢性能研究)[D]. Taiyuan (太原):Shanxi University (山西大学), 2011. http://cdmd.cnki.com.cn/Article/CDMD-10108-1012279023.htm |
| [19] | Boudjahem A G, Monteverdi S, Mercy M, et al. Acetylene cyclotrimerization over Ni/SiO2catalysts in hydrogen atmosphere[J]. Applied Catalysis A General, 2003, 250(1): 49-64. DOI:10.1016/S0926-860X(03)00221-7. |
| [20] | WU Jian-min(吴建民), SUN Qi-wen(孙启文), ZHANG Zong-sen(张宗森), et al. Chemisorption characteristics of CO and H2 over iron-based fischer tropsch synthesis catalyst(费托合成铁基催化剂上CO和H2的吸附特性)[J]. The Chinese Journal of Process Engineering(过程工程学报), 2013, 13(2): 327-332. |
| [21] | Pan Z Y, Wang R J, Nie Z Y, et al. Effect of a second metal (Co, Fe, Mo and W) on performance of Ni2P/SiO2 for hydrodeoxygenation of methyl laurate[J]. Journal of Energy Chemistry, 2016, 25(3): 418-426. DOI:10.1016/j.jechem.2016.02.007. |
| [22] | Kong X J, Zhang X L, Han C, et al. Ethanolysis of biomass based furfuryl alcohol to ethyl levulinate over Fe modified USY catalyst[J]. Molecular Catalysis, 2017, 443(12): 186-192. |
| [23] | Sreeja V, Smitha T S, Nand D, et al. Size dependent coordination behavior and cation distribution in MgAl2O4 nanoparticles from 27Al solid state NMR studies[J]. Journal of Physical Chemistry C, 2008, 112(38): 14737-14744. DOI:10.1021/jp800412k. |
| [24] | ZHANG Li-dong(张立东), GAO Jun-hua(高俊华), HU Jin-xian(胡津仙), et al. Preparation of Fe/ZSM-5 and catalytic behavior for toluene alkylation with methanol(Fe/ZSM-5的制备及其催化甲苯/甲醇烷基化反应行为)[J]. Chemical Industry and Engineering Progress(化工进展), 2009, 28(8): 1360-1364. DOI:10.3321/j.issn:1000-6613.2009.08.014. |




