神经系统疾病多由神经细胞的死亡或功能缺失引起[1],由于这些疾病受损神经元位置的局限性,只需替换少量细胞即可达到治疗目的,因此细胞移植有望成为理想的治疗手段[2]。但是由于可移植的细胞来源有限,且移植后细胞存活率低,在很大程度上限制了该技术的临床应用。随着组织工程技术的发展,具有多孔结构的三维支架材料可以为细胞提供足够的生长空间,有利于细胞间的信息传递及营养运输,从而有效地促进细胞增殖分化,实现组织工程及再生医学的应用[3]。
已有研究表明,电信号作为重要的生长信息可以改善伤口愈合效果[4],促进神经再生[5],并且在骨修复[6]及心血管疾病治疗方面具有潜在应用[7],这也使在神经组织工程领域中引入电信号成为可能。通过电刺激促进神经干细胞生长及分化,极大提高神经组织工程治疗神经系统疾病的治疗效果,因此需要在支架中引入导电材料制备导电支架从而将电信号有效地传递给种子细胞[8]。目前导电材料主要分为导电聚合物和碳材料,其中导电聚合物以聚苯胺、聚噻吩和聚吡咯为主[9~11],但是制备的复合材料具有孔隙率低、机械强度小、导电性差等缺点[12, 13],限制了其在组织工程领域中的应用。多壁碳纳米管(multi-walled carbon nanotubes, MWCNTs)具有机械强度大、电导率高、热稳定性好等优异的性质[14],可以极大改善支架的性能。Huang等[15]制备了不同直径的MWCNTs/Cs复合纤维,制备的复合纤维可以促进细胞的粘附,且无细胞毒性,对突触的生长具有导向作用。MWCNTs的加入还可以改善材料结构,增加材料孔隙率,为细胞提供更多粘附位点[16]。
目前MWCNTs复合材料的制备方法主要有溶液共混[17]、熔融共混[18~20]、原位聚合[21, 22]、静电纺丝[23]等。本研究在实验室已有研究的基础上[24],以Cs/Gel/HA为基体,加入MWCNTs制备了Cs/Gel/HA/MWCNTs导电支架,研究了导电支架的物理化学性能及生物相容性,同时进一步考察了适宜的MWCNTs加入比例,探索MWCNTs在神经组织工程中应用的可行性。
2 实验材料和方法 2.1 实验材料壳聚糖(Cs, 脱乙酰度≥85%, 上海生物科技有限公司);明胶(Gel, 国药集团化学试剂有限公司);透明质酸(HA,大连英斯特生物技术有限公司);多壁碳纳米管(MWCNTs, 北京博宇高科新材料公司);N-羟基琥珀酰亚胺(NHS, 上海共价化学科技有限公司);碳化二亚胺(EDC, 上海共价化学科技有限公司);MTT检测试剂盒(南京凯基生物科技发展有限公司);胎牛血清(FBS, 金元康生物科技有限公司);DMEM培养基(Life Technologies Corporation);冷冻干燥机(上海豫明仪器有限公司);傅立叶变换红外光谱仪(FTIR, Perkin Elmer., USA);倒置相差显微镜(OLYMPUS Ⅸ70);扫描电子显微镜(SEM, S2520, Hitachi, Japan)。
2.2 导电支架的制备60℃水浴条件下将Cs溶解于醋酸水溶液(2%, v/v)中,制备2.6% (w/v)的Cs溶液,离心脱气泡。将MWCNTs分散于醋酸水溶液(2%, v/v),与Cs溶液混合,磁力搅拌。将Gel和HA溶解于三蒸水中,室温下磁力搅拌,制备含Gel 2.6% (w/v)和HA 0.04% (w/v)的混合液。将两种混合液以1:1比例混合,搅拌12 h,获得Cs/Gel/HA/MWCNTs混合液。将混合液注入24孔板,每孔1.5 mL,-20℃预冻12 h,冷冻干燥24 h。使用0.05 mol·L-1 EDC和0.05 mol·L-1 NHS的混合溶液浸泡支架24 h,使其充分交联。之后用0.1 mol·L-1 H2PO4中和多余醋酸,三蒸水洗至中性,冷冻干燥,支架成型。通过控制MWCNTs的加入量制备出MWCNTs含量为2%,6%,10%的Cs/Gel/HA/MWCNTs导电支架,以Cs/Gel/HA为对照组。
2.3 导电支架分子结构及微观形貌表征采用傅立叶变换红外光谱仪(FTIR)及扫描电子显微镜(SEM)分别对干支架的官能团及微观形貌进行考察。
2.4 导电支架接触角及电导率的测定采用接触角测量仪对导电支架表面的亲水性进行测定,以去离子水为工作液,体积2 μL,测试前将支架压片。采用四探针测试仪在恒定电流0.5 mA,室温条件下测定干燥且压片的支架的电导率。
2.5 导电支架孔隙率、孔径及溶胀率的测定孔隙率:干支架称重,质量记为w0,将其浸入到无水乙醇中,抽真空,排出支架孔隙中的气体。取装满无水乙醇的比重瓶,总质量记为w1。取出支架,吸去表面多余乙醇并浸入比重瓶中,吸出瓶中多余乙醇,称重记为w2。取出支架,比重瓶与余下的乙醇质量记为w3。通过如下公式计算支架孔隙率:
| $ P(\% ) = \frac{{{w_2}-{w_3}-{w_0}}}{{{w_1}-{w_3}}} \times 100\% $ | (1) |
孔径:从复合支架的SEM图中随机选取20个孔,测定其孔径大小,计算平均值。
溶胀率:通过测定干支架的吸水性能表示支架的溶胀率。将干支架称重,记为wd,将其浸入PBS中24 h,吸去支架表面多余的PBS,称重记为ww,采用如下公式计算支架的溶胀率:
| $ W = \frac{{{w_{\rm{w}}}-{w_{\rm{d}}}}}{{{w_{\rm{d}}}}} $ | (2) |
细胞粘附率:使用高糖DMEM (10% FBS,1%双抗)对PC12细胞进行培养。将灭菌的导电支架(0.5 cm×0.5 cm×0.5 cm)置于96孔板中,加入培养基,培养箱孵育12 h。接种细胞,接种密度(C) 5×105cells·mL-1,体积(V) 0.1 mL,培养箱培养4 h。取出支架,孔板中剩余细胞数记为R,根据如下公式计算细胞粘附率:
| $ 粘附率(\% ) = \frac{{(CV-R)}}{{CV}} \times 100\% $ | (3) |
细胞活力:将细胞(2×105cells·mL-1,0.1 mL)接种于导电支架上培养72 h,加入10 μL MTT,继续培养4 h,吸出孔板中混合液,加入150 μL DMSO,吹打后取100 μL转移至另一孔板中,以570 nm波长下的吸光度(O.D.值)表示细胞活力。
细胞死活染色:使用Calcein、Hoechst及PI三种染料分别对导电支架上的细胞进行染色,考察细胞在支架上的生长状况。
2.7 统计分析每组实验重复三次,origin7.5对数据进行处理,所得数据以mean±S.E.M.表示,以t-检验对数据显著性进行评价,P < 0.05认为有显著性差异。
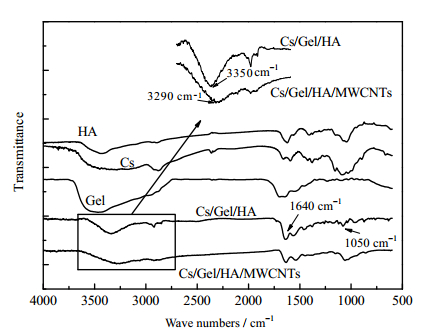
3 结果与讨论 3.1 导电支架的分子结构及微观形貌FT-IR谱图结果显示(如图 1),在3350 cm-1处产生-CONH-的N–H伸缩震动峰,且与明胶的酰胺键相比发生偏移,1640 cm-1处是-C=O的弯曲震动峰,1050 cm-1处是-CONH-的N–H弯曲震动峰,表明Cs/Gel/HA支架交联成功。相比于Cs/Gel/HA支架,Cs/Gel/HA/MWCNTs支架的出峰位置明显向低波数位移,这可能是由于MWCNTs与相邻官能团之间发生了共轭反应所致。导电支架的扫描电镜结果显示(图 2),含有MWCNTs的支架孔径更小,而且由于MWCNTs的存在使支架的孔壁上出现一些颗粒状物质,使表面变得相对粗糙,而已有研究表明粗糙的表面更利于细胞的粘附[25]。
|
图 1 复合支架的红外谱图 Fig.1 FT-IR spectra of the scaffolds |

|
图 2 复合支架的扫描电镜图 Fig.2 Scanning electron micrographs of: (A) Cs/Gel/HA scaffolds, (B) Cs/Gel/HA scaffolds with 2% MWCNTs, (C) Cs/Gel/HA scaffolds with 6% MWCNTs, (D) Cs/Gel/HA scaffolds with 10% MWCNTs |
随着MWCNTs含量的增加,复合支架的电导率呈增大趋势,最大可增加致对照组的133.82%(如表 1所示)。这可能是因为MWCNTs含量增多使管与管之间的接触增加,π电子可以在管与管之间高速移动,从而提高支架的电导率[16]。随着MWCNTs的加入,支架的接触角逐渐增大,当MWCNTs的含量达到10%时支架的接触角达到85.77o。分析原因可能是因为MWCNTs本身的疏水性降低了支架的亲水性能,导致接触角增大,而已有研究表明适当的疏水性会有利于细胞的粘附和生长[26]。
| 表 1 各组支架的电导率及接触角结果 Table 1 Electrical conductivity and contact angles of the scaffolds |
如表 2所示,加入MWCNTs使支架孔隙率逐渐增大,孔径逐渐减小,这是由于在预冻过程中,悬浮的MWCNTs阻碍了溶剂晶核的生长,使得生成的晶核相对较小,从而导致冷冻干燥后产生的孔相对较多孔径较小[27]。支架的溶胀率结果显示,MWCNTs的加入降低了支架溶胀率,这可能是因为MWCNTs本身具有的疏水性阻碍了水分子与支架接触导致的。但是当MWCNTs的含量达到10%时支架较大的孔隙率增加了水分子与支架的接触面积,因此溶胀率略有升高。
| 表 2 复合支架的孔隙率、孔径及溶胀率 Table 2 Porosity, pore sizes and swelling ratios of the scaffolds |
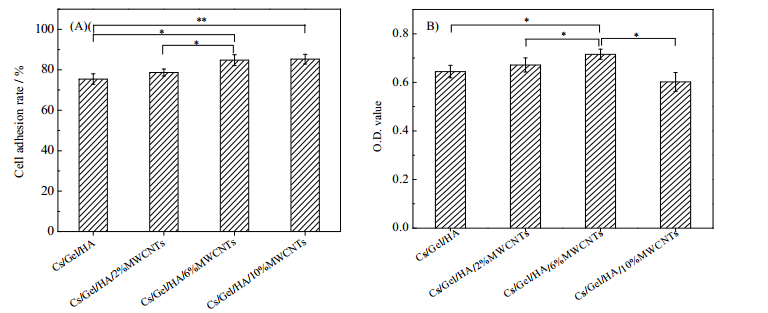
首先考察了导电支架的细胞粘附性影响。一般而言,由于细胞膜具有亲水性,所以亲水的材料表面会有利于细胞的粘附,但是由于细胞的粘附需要蛋白介导,这就要求支架具有一定的疏水性[25]。如图 3 (A)显示,MWCNTs的加入使细胞粘附率逐渐增大,从表 1的结果中也可以看出,MWCNTs的加入提升了支架的疏水性,这可能是导致粘附率逐渐增大的主要原因。细胞的粘附率还与支架的孔径、孔隙率、表面粗糙程度等有关[28],孔隙率大会增加细胞与支架的接触面积,而且粗糙的表面会促进润湿作用,从而促进细胞的粘附[25],综合以上因素,导致含有MWCNTs的支架的粘附率高于Cs/Gel/HA支架。细胞活力检测结果如图 3(B)所示,MWCNTs含量为6%的支架具有更大的细胞活力,这可能是因为加入的MWCNTs能够吸附培养基中的营养物质,使其在贴壁细胞周围富集,从而利于细胞的生长[29]。
|
图 3 细胞在不同支架上的粘附率(A)及活力(B) Fig.3 Cell adhesion (A) and viability (B) on scaffolds with different MWCNTs contents Data were averaged from three repeats and (*) p < 0.05, (**) p < 0.01 |
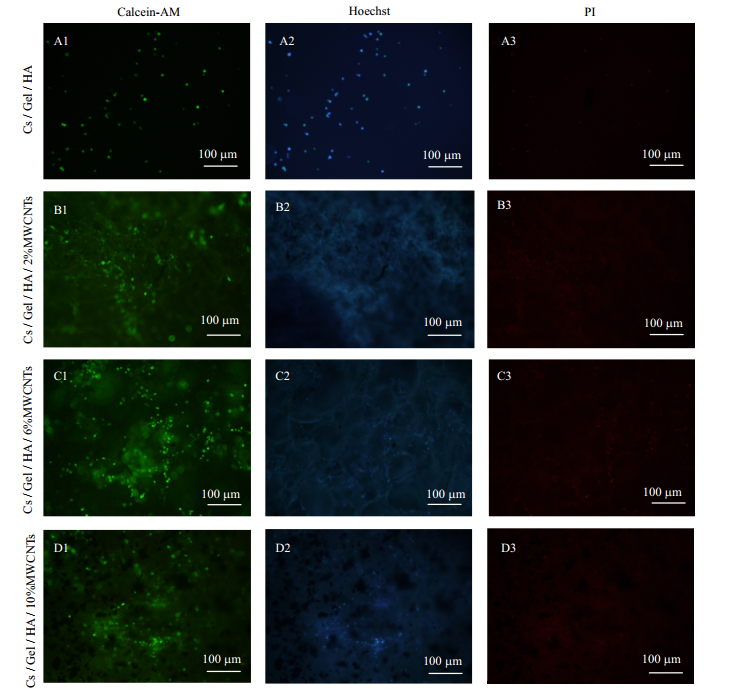
细胞在支架上生长的死活染色结果如图 4所示,细胞能够分布在支架当中,且MWCNTs含量为6%的支架上细胞更多,与细胞活力检测结果一致。以上结果表明本研究制备的支架具有良好的生物相容性。
|
图 4 PC12在不同支架上的荧光图片 Fig.4 Fluorescent images of PC12 in different scaffolds (A1~D3×100) A1-D3: MWCNTs contents are 0%, 2%, 6% and 10%, respectively |
通过以上分析,MWCNTs的加入能够提高支架电导率和孔隙率,MWCNTs含量为6%的支架细胞活力提高至对照组的111.07%,且细胞粘附率与含量为10%的支架相比无显著差异,综合以上因素,采用MWCNTs含量为6%的支架用于后续研究。
4 结论本实验制备了MWCNTs含量分别为2%、6%及10%的Cs/Gel/HA/MWCNTs导电支架。制备的支架孔径为90~130 μm,孔隙率为83%~96%,能够满足细胞生长要求。MWCNTs的加入使支架孔壁粗糙度增加,电导率增大,疏水性提高。MWCNTs的加入利于细胞粘附和增殖,培养72 h后,MWCNTs含量为6%的支架细胞活力提高至对照组的111.07%。本研究初步证明,制备的Cs/Gel/HA/MWCNTs导电支架具有良好的生物相容性,可进一步用于研究电刺激对细胞增殖及分化行为的影响。
符号说明:
| [1] | Bettens K, Sleegers K, Van Broeckhoven C. Current status on Alzheimer disease molecular genetics:from past, to present, to future[J]. Human Molecular Genetics , 2010, 19(R1): R4-R11. DOI:10.1093/hmg/ddq142. |
| [2] | Einstein O, Grigoriadis N, Mizrachi-Kol R, et al. Transplanted neural precursor cells reduce brain inflammation to attenuate chronic experimental autoimmune encephalomyelitis[J]. Experimental Neurology , 2006, 198(2): 275-284. DOI:10.1016/j.expneurol.2005.11.007. |
| [3] | Egawa E Y, Kato K, Hiraoka M, et al. Enhanced proliferation of neural stem cells in a collagen hydrogel incorporating engineered epidermal growth factor[J]. Biomaterials , 2011, 32(21): 4737-4743. DOI:10.1016/j.biomaterials.2011.03.033. |
| [4] | Wang E, Zhao M. Regulation of tissue repair and regeneration by electric fields[J]. Chinese Journal of Traumatology , 2010, 13(1): 55-61. |
| [5] | Ghasemi-Mobarakeh L, Prabhakaran M P, Morshed M, et al. Application of conductive polymers, scaffolds and electrical stimulation for nerve tissue engineering[J]. Journal of Tissue Engineering and Regenerative Medicine , 2011, 5(5): 17-35. |
| [6] | Kim I S, Song J K, Song Y M, et al. Novel effect of biphasic electric current on in vitro osteogenesis and cytokine production in human mesenchymal stromal cells[J]. Tissue Engineering Part A , 2009, 15(9): 2411-2422. DOI:10.1089/ten.tea.2008.0554. |
| [7] | Ghafar-Zadeh E, Waldeisen J R, Lee L P. Engineered approaches to the stem cell microenvironment for cardiac tissue regeneration[J]. Lab on a Chip , 2011, 11(18): 3031-3048. DOI:10.1039/c1lc20284g. |
| [8] | Guiseppielie A. Electroconductive hydrogels:synthesis, characterization and biomedical applications[J]. Biomaterials , 2010, 31(10): 2701-2716. DOI:10.1016/j.biomaterials.2009.12.052. |
| [9] | Prabhakaran M P, Ghasemi-Mobarakeh L, Jin G, et al. Electrospun conducting polymer nanofibers and electrical stimulation of nerve stem cells[J]. Journal of Bioscience and Bioengineering , 2011, 112(5): 501-507. DOI:10.1016/j.jbiosc.2011.07.010. |
| [10] | Mawad D, Stewart E, Officer D L, et al. A single component conducting polymer hydrogel as a scaffold for tissue engineering[J]. Advanced Functional Materials , 2012, 22(13): 2692-2699. DOI:10.1002/adfm.v22.13. |
| [11] | Xu H, Holzwarth J M, Yan Y, et al. Conductive PPY/PDLLA conduit for peripheral nerve regeneration[J]. Biomaterials , 2014, 35(1): 225-235. DOI:10.1016/j.biomaterials.2013.10.002. |
| [12] | Sill T J, von Recum H A. Electrospinning:applications in drug delivery and tissue engineering[J]. Biomaterials , 2008, 29(13): 1989-2006. DOI:10.1016/j.biomaterials.2008.01.011. |
| [13] | Mottaghitalab F, Farokhi M, Mottaghitalab V, et al. Enhancement of neural cell lines proliferation using nano-structured chitosan/poly(vinyl alcohol) scaffolds conjugated with nerve growth factor[J]. Carbohydrate Polymers , 2011, 86(2): 526-535. DOI:10.1016/j.carbpol.2011.04.066. |
| [14] | Serrano M C, Nardecchia S, Garcia-Rama C, et al. Chondroitin sulphate-based 3D scaffolds containing MWCNTs for nervous tissue repair[J]. Biomaterials , 2014, 35(5): 1543-1551. DOI:10.1016/j.biomaterials.2013.11.017. |
| [15] | Huang Y, Hsu S, Kuo W, et al. Effects of laminin-coated carbon nanotube/chitosan fibers on guided neurite growth[J]. Journal of Biomedical Materials Research Part A , 2011, 99A(1): 86-93. DOI:10.1002/jbm.a.v99a.1. |
| [16] | Arslantunali D, Budak G, Hasirci V. Multiwalled CNT-pHEMA composite conduit for peripheral nerve repair[J]. Journal of Biomedical Materials Research Part A , 2014, 102(3): 828-841. DOI:10.1002/jbm.a.v102.3. |
| [17] | Wang S F, Shen L, Zhang W D, et al. Preparation and mechanical properties of chitosan/carbon nanotubes composites[J]. Biomacromolecules , 2005, 6(6): 3067-3072. DOI:10.1021/bm050378v. |
| [18] | Haggenmueller R, Gommans H H, Rinzler A G, et al. Aligned single-wall carbon nanotubes in composites by melt processing methods[J]. Chemical Physics Letters , 2000, 330(3-4): 219-225. DOI:10.1016/S0009-2614(00)01013-7. |
| [19] | Seo M, Park S. Electrical resistivity and rheological behaviors of carbon nanotubes-filled polypropylene composites[J]. Chemical Physics Letters , 2004, 395(1-3): 44-48. DOI:10.1016/j.cplett.2004.07.047. |
| [20] | Chafidz A, Kaavessina M, Al-Zahrani S, et al. Multiwall carbon nanotubes filled polypropylene nanocomposites:rheological and electrical properties[J]. Polymer Engineering and Science , 2013, 54(5): 1134-1143. |
| [21] | Feng W, Bai X D, Lian Y Q, et al. Well-aligned polyaniline/carbon-nanotube composite films grown by in-situ aniline polymerization[J]. Carbon , 2003, 41(8): 1551-1557. DOI:10.1016/S0008-6223(03)00078-2. |
| [22] | Wu T, Lin Y, Liao C. Preparation and characterization of polyaniline/multi-walled carbon nanotube composites[J]. Carbon , 2005, 43(4): 734-740. DOI:10.1016/j.carbon.2004.10.043. |
| [23] | Liao G, Zhou X, Chen L, et al. Electrospun aligned PLLA/PCL/functionalised multiwalled carbon nanotube composite fibrous membranes and their bio/mechanical properties[J]. Composites Science and Technology , 2012, 72(2): 248-255. DOI:10.1016/j.compscitech.2011.11.009. |
| [24] | ZHANG Xiao-qing(张晓庆), GUAN Shui(关水), GE Dan(葛丹), et al. The synergistic effect of modified chitosan-gelatin-hyaluronate-heparan sulfate scaffolds and PCA on NS/PCs adhesion and differentiation(C-G-Ha-HS支架改性协同原儿茶酸对NS/PCs粘附及定向分化的影响)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2014, 28(5): 1051-1058. |
| [25] | Kooten T G V, Spijker H T, Busscher H J. Plasma-treated polystyrene surfaces:model surfaces for studying cell-biomaterial interactions[J]. Biomaterials , 2004, 25(10): 1735-1747. DOI:10.1016/j.biomaterials.2003.08.071. |
| [26] | Menzies K L, Jones L. The impact of contact angle on the biocompatibility of biomaterials[J]. Optometry & Vision Science Official Publication of the American Academy of Optometry , 2010, 87(6): 387-399. |
| [27] | Mounesi Rad S, Khorasani M T, Daliri Joupari M. Preparation of HMWCNT/PLLA nanocomposite scaffolds for application in nerve tissue engineering and evaluation of their physical, mechanical and cellular activity properties[J]. Polymers for Advanced Technologies , 2016, 27(3): 325-338. DOI:10.1002/pat.v27.3. |
| [28] | Matsuzaka K, Frank Walboomers X, Yoshinari M, et al. The attachment and growth behavior of osteoblast-like cells on microtextured surfaces[J]. Biomaterials , 2003, 24(16): 2711-2719. DOI:10.1016/S0142-9612(03)00085-1. |
| [29] | Mooney E, Dockery P, Greiser U, et al. Carbon nanotubes and mesenchymal stem cells:biocompatibility, proliferation and differentiation[J]. Nano Letters , 2008, 8(8): 2137-2143. DOI:10.1021/nl073300o. |




