2. 广西清洁化制浆造纸与污染控制重点实验室,广西 南宁 530004;
3. 华南理工大学 制浆造纸国家重点实验室,广东 广州 510640
2. Guangxi Key Laboratory of Clean Pulp & Papermaking and Pollution Control, Nanning 530004, China;
3. State Key Laboratory of Pulp and Paper Engineering, South China University of Technology, Guangzhou 510640, China
TEMPO (2, 2, 6, 6-四甲基哌啶-1-氧自由基)/NaBr/NaClO体系是一种有效的纤维素选择性氧化体系,可以选择性地将纤维素C6位上的伯羟基氧化为羧基而不影响纤维形态,也不改变纤维素的晶体结构,从而可以改善纤维性能,扩大其应用范围[1-2]。在氧化过程中大量羧基阴离子的引入纤维表面,形成较强的静电斥力作用,可以减弱纤维素分子层结构中氢键连接,极大程度地促进纳米原纤化过程,降低机械作用中的能耗。将TEMPO氧化纤维素再经温和地均质处理便能够制得尺寸均一,长径比大,分散性好的纳米纤维素[3]。因此,利用氧化纤维素进行纳米纤维素的制备[4-5]也受到越来越多的关注,SAITO等[6-7]研究了TEMPO氧化体系对各种纤维素材料的氧化性,并采用此体系氧化天然纤维成功地制备出了纳米纤维素。TEMPO法是一种极具潜力的纳米纤维素制备方法,但TEMPO氧化过程控制以及氧化反应效率的提升,仍然存在较大的探索空间。
漂白浆因纤维素含量高,几乎不含木素,是制备氧化纤维素的主要原料之一[8],但一般情况下漂白浆中仍含有10%~20%半纤维素,在植物细胞壁中半纤维素与纤维素微细纤维之间以氢键和范德华力作用紧密连接[9]。半纤维素和纤维素之间的这种相互作用,会在一定程度上阻碍试剂的可及性,降低氧化效果。并且半纤维素上的羟基也会和氧化剂发生反应,从而对纤维素的氧化产生影响[10-11]。目前对于TEMPO氧化反应过程的研究多集中在在纤维素和木素上[12-14],鲜少系统地研究半纤维素在整个氧化体系的影响作用。并且根据已有的文献报道,对于纸浆氧化过程中半纤维素的含量变化,仍存在一定的争议。如ISOGAI等[7]认为在氧化过程中,半纤维素在NaClO的作用下会发生降解,生成可溶性小分子而被除掉。KURAMAE等[10]以不同原料的综纤维素制备TOCNs,研究发现即使是在更苛刻的TEMPO/Na Br/NaClO氧化体系下(NaClO用量10 mmol·g-1),氧化后的综纤维素中仍然含有至少5%的木糖,尤其是阔叶木和草类原料。在与KURAMAE等相同的氧化条件下,RODIONOVA等[15]的研究结果显示,桉木浆中木糖含量从20.1%降至7.3%,同样表明了木糖在TEMPO氧化过程中会发生降解而部分溶出。蒙启骏[16]研究了对半纤维素对纸浆TEMPO氧化的影响,结果证明半纤维素的存在对TEMPO氧化和羧基生成都有不利的影响。但没有对其具体氧化过程及其对于不同氧化程度的影响进行分析。因此,本文将不同半纤维素含量的漂白蔗渣浆进行TEMPO/NaClO/NaBr体系氧化,并设定不同的氧化程度,通过测定氧化过程中pH下降速率、NaOH消耗量以及氧化浆料中羧基生成量、聚合度及得率来系统的分析半纤维素含量对TEMPO氧化过程及氧化浆性能的影响,从而揭示氧化过程中半纤维素的作用,为TEMPO氧化过程控制以及后续纳米纤维素的制备提供技术支持和理论基础。
2 实验 2.1 原料与试剂蔗渣原料取自广西贵糖股份有限公司,风干后装入密封袋平衡水分备用;TEMPO购于Aladdin-阿拉丁试剂有限公司。
2.2 实验步骤 2.2.1 漂白蔗渣浆的制备碱预抽提:对蔗渣原料进行碱预抽提。碱抽提工艺条件1为:用碱量8%,最高温度90 ℃,保温时间4 h,液比1:5;碱抽提工艺条件2为:用碱量12%,其他均与碱抽提条件1一致。
烧碱法制浆:将两种预处理后的蔗渣和未预处理的蔗渣进行烧碱法蒸煮。蒸煮的工艺条件为:用碱量12%,最高温度160 ℃,时间2 h,液比1:5。
D0-EP-D1三段漂白:对蒸煮后的纸浆采用D0-Ep-D1三段漂进行漂白,具体参考文献[17]中的漂白工艺,漂白结束后,将浆料洗净、风干、平衡水分后待用。
2.2.2 漂白蔗渣浆TEMPO氧化称取适量的漂白浆分散于水中,调节浆浓为w = 1%,依次加入TEMPO、NaBr、NaClO,每种浆设置3种氧化程度,即NaClO用量分别是2.2、5.2、8.2 mmol·g-1 (均为相对于绝干浆)。加入NaClO后,开始计时并观察反应体系pH值,使用1 mol·L-1的NaOH溶液控制反应的pH值维持在10.0±0.2。当反应进行至pH值为9.8~10.0并在15 min内保持稳定时,完成氧化反应,随即加入20 mL无水乙醇终止反应。
2.3 分析方法 2.3.1 半纤维素糖单元组分含量分析纸浆中半纤维素糖单元组分含量通过离子色谱法测定[18],所用仪器为ICS-5000+SP型离子色谱仪(美国Thermo scientific公司)。具体步骤参照美国国家可再生能源实验室(NERL)标准方法TP-510-42618。
2.3.2 羧基含量测定采用顶空气相色谱法测定纸浆中的羧基含量(HS-GC),所用仪器为7890B型气质联用仪(美国Agilent Technologies公司)。具体步骤参照侯庆喜等[19]的方法。
2.3.3 纸浆聚合度测定纸浆聚合度采用铜乙二胺黏度法进行测定,具体步骤参照GB/T1548-1989。
2.3.4 漂白浆及氧化浆的XRD分析使用Miniflex600X型射线衍射分析仪(日本Rigaku公司)测定纸浆的结晶度。X射线衍射分析条件如下:铜靶,40 kV,15 mA,衍射范围(2θ) 5°~50°,扫描步长0.02°,扫描速度9°·min-1。对于各种天然纤维素(纤维素Ι)根据Segal峰强度法的经验公式来计算结晶度指数[20]。
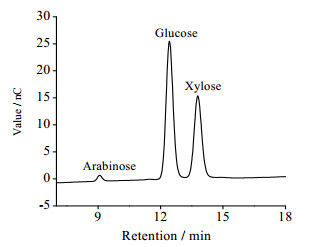
3 结果与讨论 3.1 纸浆中半纤维素含量分析PENG等[21]研究表明蔗渣半纤维素中木糖是主要的单糖组成,其次是阿拉伯糖,还有少量的葡萄糖、葡萄糖醛酸和半乳糖。图 1为蒸煮后纸浆中半纤维素单糖含量的离子色谱图,可知经过蒸煮后纸浆中不含半乳糖和甘露糖。这是因为这些糖基一般是通过苷键以支链的形式连接在主链的糖基上,苷键易反应发生断裂,溶解于蒸煮液中,所以不存在于蒸煮后的纸浆中。图 1中葡萄糖含量较高,其主要来自于酸水解过程中纸浆中纤维素降解产生的葡萄糖。
|
图 1 蒸煮后纸浆中糖组分测定图谱 Fig.1 Chromatogram of Hemicellulose in pulp after cooking |
由表 1数据可以看出,纸浆中半纤维素含量会在氧化过程大量减少,尤其是阿拉伯糖在氧化后几乎检测不到。阿拉伯糖在C5位有伯羟基[22],在TEMPO氧化反应中很容易被氧化成羧基而发生降解,以小分子形式溶出[23],不存在于氧化后的纸浆中,但这部分阿拉伯糖含量较低,对氧化反应过程不会产生较大的影响。因此文中以不同木糖含量的纸浆样品为对象,研究不同半纤维素含量对纸浆TEMPO氧化性能的影响,3种预处理条件得到的木糖含量分别为20.30%、12.23%、8.75%。
|
|
表 1 不同碱预处理下浆料在漂白前后和氧化后半纤维素单糖含量的变化 Table 1 Variation of hemicellulose contents during pretreatment and oxidation |
将不同半纤维素含量的漂白浆进行TEMPO氧化,研究半纤维素对整个氧化过程的影响。根据TEMPO/NaBr/NaClO体系的氧化机理,纤维素C6伯羟基被氧化生成羧基,使得反应体系pH值会持续下降,反应时需加入用1 mol·L-1的NaOH溶液来调节体系pH维持在9.8~10.2,直至反应到达终点。因此,反应初始阶段pH值下降情况,以及消耗的NaOH溶液体积可以间接反映TEMPO氧化过程。根据氧化体系pH变化情况,将氧化过程划分为两个阶段进行分析:第一阶段为体系pH下降阶段,从加入NaClO反应开始,至体系pH值第一次下降至9.8为止。第二阶段为体系pH调节阶段,即体系pH降至9.8以下时,用1 mol·L-1的NaOH溶液来调节体系pH。
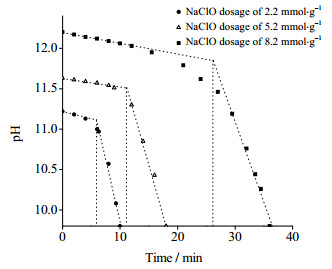
3.2.1 半纤维素含量对TEMPO氧化体系pH下降速率的影响NaClO用量对pH-时间对应关系的影响如图 2所示,可以看出氧化体系的pH变化起初比较平缓,这一阶段为氧化剂在纤维内进行渗透扩散。当NaClO用量为2.2 mmol·g-1时,反应进行至6 min,pH迅速下降,TEMPO氧化生成的产物羧基呈酸性,导致体系的pH不断下降。随着NaClO用量增加,pH下降至9.8所需的时间也相应增长,这是由于NaClO本身呈碱性,尽管氧化产物羧基呈酸性,但反应初期羧基产生量较低,所以NaClO用量越高,体系pH下降至9.8用时越长。这表明氧化剂的渗透在TEMPO氧化中起重要作用,尤其在初始阶段。
|
图 2 NaClO用量对pH-时间对应关系的影响 Fig.2 Effects of NaClO dosage on pH-time relationship |
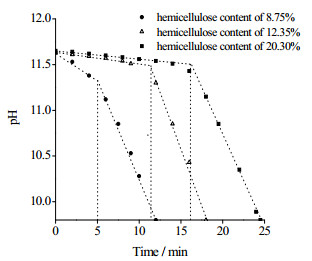
而在相同氧化程度下,NaClO浓度为5.2 mmol·g-1时,3种不同半纤维素含量纸浆氧化体系的pH随时间变化如图 3所示。在相同氧化程度下,不同半纤维素含量的纸浆氧化体系pH值表现出不同的变化,木糖含量为8.75%的漂白浆最先出现拐点,其次是木糖含量为13.25%,最后是木糖含量为20.30%,表明半纤维素含量的降低可以促进氧化剂的扩散从而缩短扩散时间[24],这也充分说明半纤维素的存在会阻碍氧化剂与纤维素的接触,不利于氧化剂的扩散,与文献中报道的结果是类似的。并且在相同氧化条件下,漂白浆中半纤维素的含量越少,体系pH下降越快,氧化剂扩散阶段完成得越快。
|
图 3 半纤维素含量对pH-时间对应关系的影响 Fig.3 Effects of hemicellulose contents on pH-time relationship |
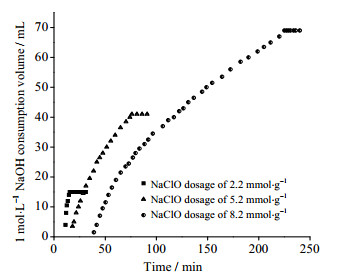
图 4为漂白浆中木糖含量为12.35%时,对浆料进行3种不同程度氧化时所消耗的NaOH溶液体积变化。由图 4可以看出,起初NaOH体积消耗的速率都较快,后期慢慢平缓,最终NaOH体积消耗的总量保持不变即氧化反应结束。这是因为一开始氧化反应是在纤维素无定形区上进行[25],但随着反应进行,氧化剂进入到结晶区的表面,氧化速率减缓,这一点在本文的XRD图谱分析中也得到了证实。随着NaClO用量的增加,反应时间随之增加,这说明NaClO的用量及其与纤维素的接触程度会对TEMPO氧化速率产生影响。
|
图 4 NaClO用量对NaOH体积消耗速率的影响 Fig.4 Effects of NaClO dosage on volumetric consumption of NaOH |
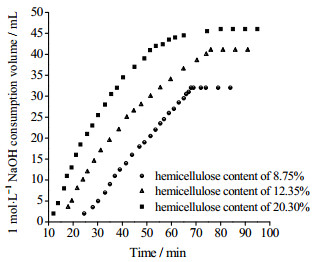
在氧化剂用量相同,NaClO浓度为5.2 mmol·g-1时,3种不同半纤维素含量纸浆氧化体系的NaOH消耗量变化如图 5所示。由图 5可知,木糖含量为8.75%的纸浆进行TEMPO氧化消耗NaOH的速率较快且反应时间较长,随着半纤维素含量的增加,NaOH的消耗速率减慢,反应时间缩短。说明漂白浆中半纤维素含量越少,氧化初期其反应速率越快,反应时间越长,氧化反应进行越彻底。这是由于漂白浆中半纤维素含量越少,纤维素与氧化剂接触的阻碍物就越少,反应开始越快,氧化剂越容易进入到结晶区的表面,暴露的纤维素增多也使氧化反应进行越彻底,从而反应时间增长,氧化程度提高。
|
图 5 半纤维素含量对NaOH体积消耗的影响 Fig.5 Effects of hemicellulose contents on volumetric consumption of NaOH |
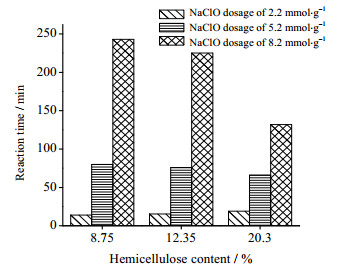
从图 6中可以看出,在NaClO用量分别为5.2和8.2 mmol·g-1时,氧化反应的总时间都是随半纤维素含量的减少而增加的,这与上文中的分析是一致的。但NaClO用量为2.2 mmol·g-1时,氧化反应的总时间随半纤维素含量的减少而减少。这可能是因为最先发生反应的无定形区纤维素密度小结合力小,氧化反应较容易进行,氧化剂的用量过少不能充分地与结晶区表面的纤维素反应,氧化反应很快结束。总体而言,在氧化剂用量充足的情况下,半纤维素含量的减少有利于改善纤维素可及性并加快氧化速率,从而促进氧化反应的进行,对于TEMPO氧化反应越有利。
|
图 6 半纤维素含量在不同氧化程度下对反应时间的影响 Fig.6 Effects of hemicellulose contents on reaction time at different oxidation degrees |
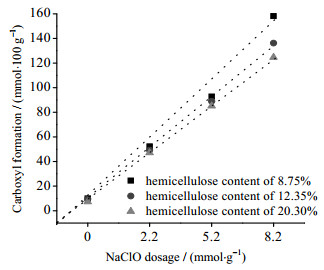
不同半纤维素含量漂白浆经氧化后其羧基生成量变化如图 7所示,从图中可以明显地看出在相同氧化程度时,半纤维素含量低的漂白浆经氧化后羧基生成量明显高于半纤维素含量高的漂白浆;在不同氧化程度(NaClO用量分别为2.2、5.2、8.2 mmol·g-1)时,木糖含量为8.75%的漂白浆经氧化后其羧基生成量比木糖含量为20.30%的分别增加了11%、10%、27%。这表明漂白浆中半纤维素含量的减少对氧化时羧基生成量有明显的促进作用,并且这种促进作用随着氧化程度的增强愈加明显。半纤维素含量的减少使纤维素更容易与氧化剂接触,更多的羟基会被氧化为羧基。因此,半纤维素含量越少,对羧基的生成越有利,这与蒙启骏[16]的研究结果是一致的。
|
图 7 半纤维素含量对纸浆羧基生成量的影响 Fig.7 Effects of hemicellulose contents on carboxyl production of pulp |
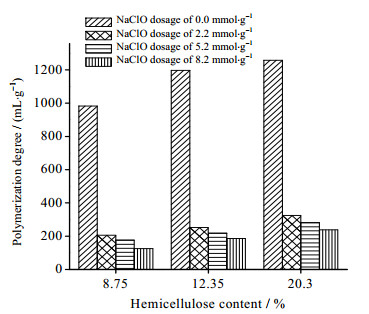
从图 8中可看出,漂白浆的聚合度明显高于氧化浆,说明在氧化过程中,部分纤维素会发生氧化降解。在不同氧化程度的纸浆中,半纤维素含量越少则纤维的聚合度越小。木糖含量为20.30%的纸浆在氧化前后其聚合度均大于木糖含量为12.35%和8.75%。由表 2可看出,在NaClO用量同为2.2 mmol·g-1时,木糖含量为20.3%时其氧化后纸浆的得率比木糖含量为12.35%和8.75%的都高,分别增加了1.77%和3.84%。氧化程度的增强,也会导致氧化后浆料的得率有所下降,当NaClO用量为8.2 mmol·g-1时,木糖含量为8.75%的漂白浆经氧化后的得率为79.94%。根据SANG等[26]对TEMPO氧化机理的研究推测这可能是由于碱预处理使纤维结构受到了一定破坏,随着半纤维素含量的减少,纤维素与氧化剂的反应也就更加剧烈,从而使得纤维素被氧化的同时,又受到了一定程度的降解作用导致其最终纸浆的聚合度和得率下降[26-27]。但TEMPO氧化纸浆进一步均质处理制备纳米纤维素的目的就是减小纤维尺寸,机械研磨会伴随大量的纤维损失,因此氧化过程中聚合度和得率的降低不会对其产生不利影响。
|
图 8 半纤维素含量对不同氧化程度聚合度的影响 Fig.8 Effects of hemicellulose contents on polymerization degree of bleached pulp at different oxidation degrees |
|
|
表 2 半纤维素含量对氧化浆得率的影响 Table 2 Effects of hemicellulose contents on oxidized-pulp yield |
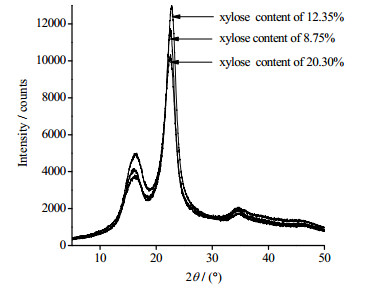
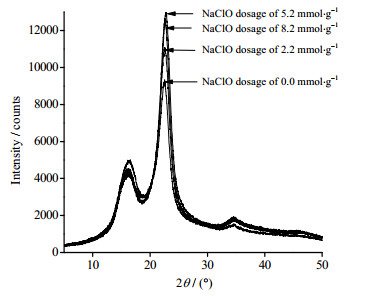
如图 9所示,在氧化程度为NaClO用量为5.2 mmol·g-1时不同半纤维素含量的漂白浆经氧化后进行XRD分析,其X射线衍射图没有发生明显改变。在2θ = 22.6°时出现时衍射峰是典型天然纤维素的I002结晶峰,在2θ = 18°的峰为无定形区衍射的强度。在图 10中可以看出在半纤维素含量相同的条件下,不同氧化程度纤维素的XRD衍射图也无明显变化,经过半纤维素含量及氧化程度都对氧化纤维素的晶型没有影响,氧化前后纤维素的结晶区也没有发生破坏,这说明氧化反应是主要是在纤维素无定形区反应,而难以进入结晶区内部发生氧化反应,但半纤维素的大量去除,会使纤维素暴露出更多的非结晶区面,与氧化剂接触更充分,有利于TEMPO反应的进行。
|
图 9 不同半纤维素含量的氧化浆XRD分析 Fig.9 XRD analysis of oxidized pulp with different hemicellulose contents |
|
图 10 不同氧化程度氧化浆XRD分析 Fig.10 XRD analysis of slurries with different oxidation levels |
通过不同的碱预处理制备出不同半纤维素含量的漂白蔗渣浆,探讨了半纤维素含量对不同氧化程度漂白浆氧化过程及氧化后浆料性能的影响。结果表明半纤维素的存在一定程度上阻碍了氧化剂与纸浆纤维,不利于TEMPO氧化反应的进行。在氧化剂用量充足的情况下,减少纸浆中的半纤维素含量有利于加快氧化速率并延长氧化时间,从而促进羧基的生成,并且氧化程度越高促进作用越明显。由于氧化降解反应,纸浆中半纤维素含量的减少以及氧化剂用量增加,会使氧化后浆料的聚合度和得率有所降低。
| [1] |
LEE H V, HAMID S B, ZAIN S K. Conversion of lignocellulosic biomass to nanocellulose:structure and chemical process[J]. The Scientific World Journal, 2014, 2014(4): 631013-631033. |
| [2] |
陈良, 汤骏, 李丹杰, 等. 桥连结构对聚合物微球负载型TEMPO稳定性及催化氧化性能的影响[J]. 高校化学工程学报, 2017, 31(4): 877-883. CHEN L, TANG J, LI D J, et al. Effects of bridge structure on stability and catalytic oxidation performance of polystyrene microsphere supported TEMPO[J]. Journal of Chemical Engineering of Chinese Universities, 2017, 31(4): 877-883. DOI:10.3969/j.issn.1003-9015.2017.04.017 |
| [3] |
FRASCHINI C, CHAUVE G, BOUCHARD J. TEMPO-mediated surface oxidation of cellulose nanocrystals (CNCs)[J]. Cellulose, 2017, 24(7): 2775-2790. DOI:10.1007/s10570-017-1319-5 |
| [4] |
OKITA Y, SAITO T, ISOGAI A. Entire surface oxidation of various cellulose microfibrils by TEMPO-mediated oxidation[J]. Biomacromolecules, 2010, 11(6): 1696-1700. DOI:10.1021/bm100214b |
| [5] |
李英豪, 耿延训, 徐化能. 乙酰化纳米纤维素纤维的制备及其凝胶机制研究[J]. 高校化学工程学报, 2018, 32(1): 208-214. LI Y H, GENG Y X, XU H N. Preparation of acetylated cellulose nanofibrils and its gelation behavior[J]. Journal of Chemical Engineering of Chinese Universities, 2018, 32(1): 208-214. DOI:10.3969/j.issn.1003-9015.2018.01.028 |
| [6] |
SAITO T, NISHIYAMA Y, PUTAUX J L, et al. Homogeneous suspensions of individualized microfibrils from TEMPO-catalyzed oxidation of native cellulose[J]. Biomacromolecules, 2006, 7(6): 1687-1691. DOI:10.1021/bm060154s |
| [7] |
ISOGAI A, SAITO T, FUKUZUMI H. TEMPO-oxidized cellulose nanofibers[J]. Nanoscale, 2011, 3(1): 71-85. DOI:10.1039/C0NR00583E |
| [8] |
SAITO T, HIROTA M, TAMURA N, et al. Oxidation of bleached wood pulp by TEMPO/NaClO/NaClO2 system:effect of the oxidation conditions on carboxylate content and degree of polymerization[J]. Journal of Wood Science, 2010, 56(3): 227-232. DOI:10.1007/s10086-009-1092-7 |
| [9] |
杨淑蕙. 植物纤维化学[M]. 北京: 中国轻工业出版社, 2010: 264-284. YANG S H. Lignocellulosic chemistry[M]. Beijing: China Light Industry Press, 2010: 264-284. |
| [10] |
KURAMAE R, SAITO T, ISOGAI A. TEMPO-oxidized cellulose nanofibrils prepared from various plant holocelluloses[J]. Reactive & Functional Polymers, 2014, 85(S1): I 126-133. |
| [11] |
CHAKER A, ALILA S, MUTJ P, et al. Key role of the hemicellulose content and the cell morphology on the nanofibrillation effectiveness of cellulose pulps[J]. Cellulose, 2013, 20(6): 2863-2875. DOI:10.1007/s10570-013-0036-y |
| [12] |
SAITO T, HIROTA M, TAMURA N, et al. Individualization of nano-sized plant cellulose fibrils by direct surface carboxylation using TEMPO catalyst under neutral conditions[J]. Biomacromolecules, 2009, 10(7): 1992-1996. DOI:10.1021/bm900414t |
| [13] |
HIROTA M, TAMURA N, SAITO T, et al. Water dispersion of cellulose Ⅱ nanocrystals prepared by TEMPO-mediated oxidation of mercerized cellulose at pH 4.8[J]. Cellulose, 2010, 17(2): 279-288. DOI:10.1007/s10570-009-9381-2 |
| [14] |
LⅡMATAINEN H, VISANKO M, SIRVI J A, et al. Enhancement of the nanofibrillation of wood cellulose through sequential periodate-chlorite oxidation[J]. Biomacromolecules, 2012, 13(5): 1592-1597. DOI:10.1021/bm300319m |
| [15] |
RODIONOVA G, SAITO T, LENES M, et al. TEMPO-mediated oxidation of norway spruce and eucalyptus pulps:preparation and characterization of nanofibers and nanofiber dispersions[J]. Journal of Polymers & the Environment, 2013, 21(1): 207-214. |
| [16] |
蒙启骏.半纤维素对TEMPO氧化纸浆制备纳米纤维素的影响[D].广州: 华南理工大学, 2015 MENG Q J. The effects of hemicellulose on nanocellulose preparation by TEMPO-mediated oxidation from pulps[D]. Guangzhou: South China University of Technology, 2015. |
| [17] |
邓仲斌.蔗渣浆二氧化氯漂白过程中AOX减量技术研究[D].南宁: 广西大学, 2012. DENG Z B. Study on AOX reduction technology in the process of chlirine bleaching for bagasse pulp[D]. Nanning: Guangxi University, 2012. |
| [18] |
彭云云, 武书彬, 程江娜, 等. 离子色谱法测定蔗渣半纤维素中的单糖及糖醛酸含量[J]. 造纸科学与技术, 2009, 28(5): 10-12. PENG Y Y, WU S B, CHENG J N, et al. Determination of monosaccharides and uronic acids in bagasse hemicellulose by ion chromatography[J]. Paper Science & Technology, 2009, 28(5): 10-12. |
| [19] |
侯庆喜, 柴欣生, 朱俊勇. 应用顶空气相色谱测定纸浆纤维的羧基含量[J]. 中国造纸, 2005, 24(9): 5-9. HOU Q X, CHAI X S, ZHU J Y. Determination of the carboxyl groups in fibers by headspace gas chromatography[J]. China Pulp & Paper, 2005, 24(9): 5-9. DOI:10.3969/j.issn.0254-508X.2005.09.002 |
| [20] |
李海龙, 詹怀宇, 张倩, 等. TEMPO氧化对硫酸盐竹浆性能及纤维形态的影响[J]. 湖北造纸, 2012(3): 2-5. LI H L, ZHAN H Y, ZHANG Q, et al. Effect of TEMPO oxidation on properties and fiber morphology of kraft bamboo slurry[J]. Hubei Pulp & Paper, 2012(3): 2-5. DOI:10.3969/j.issn.1006-9631.2012.03.002 |
| [21] |
PENG F, REN J L, XU F, et al. Fractional study of alkali-soluble hemicelluloses obtained by graded ethanol precipitation from sugar cane bagasse[J]. Journal of Agricultural & Food Chemistry, 2010, 58(3): 1768-1776. |
| [22] |
SYVERUD K, CHINGA-CARRASCO G, TOLEDO J, et al. A comparative study of eucalyptus and pinus radiata pulp fibres as raw materials for production of cellulose nanofibrils[J]. Carbohydrate Polymers, 2011, 84(3): 1033-1038. DOI:10.1016/j.carbpol.2010.12.066 |
| [23] |
HAQUE M A, CHO K M, BARMAN D N, et al. A potential cellulose microfibril swelling enzyme isolated from Bacillus sp. AY8 enhances cellulose hydrolysis[J]. Process Biochemistry, 2015, 50(5): 807-815. DOI:10.1016/j.procbio.2015.02.003 |
| [24] |
戴路.预处理对TEMPO氧化体系的促进及动力学研究[D].南京: 南京林业大学, 2011. DAI L. The effect of pretreatment on TEMPO oxidation system and kinetic study[D]. Nanjing: Nanjing Forestry University, 2011. |
| [25] |
BESBES I, VILAR M R, BOUFI S. Nanofibrillated cellulose from alfa, eucalyptus and pine fibres:preparation, characteristics and reinforcing potential[J]. Carbohydrate Polymers, 2011, 86(3): 1198-1206. DOI:10.1016/j.carbpol.2011.06.015 |
| [26] |
SANG X, QIN C, TONG Z, et al. Mechanism and kinetics studies of carboxyl group formation on the surface of cellulose fiber in a TEMPO-mediated system[J]. Cellulose, 2017, 24(6): 2415-2425. DOI:10.1007/s10570-017-1279-9 |
| [27] |
HOMMA I, ISOGAI T, SAITO T, et al. Degradation of TEMPO-oxidized cellulose fibers and nanofibrils by crude cellulase[J]. Cellulose, 2013, 20(2): 795-805. DOI:10.1007/s10570-013-9872-z |




