氢气作为一种高效清洁的能源,近年作为燃料电池的原料展示了广阔的应用前景[1, 2]。利用生物乙醇蒸汽重整制氢方法提供燃料电池氢气受到国内外学者的广泛关注[3, 4]。生物乙醇以生物质等可再生资源为原料制得,环境友好,能量密度高,便于储存。生物乙醇是由生物质转化制得的乙醇水溶液(8%~15% V/V)或粗蒸馏浓缩溶液(15%~50% V/V),可直接用作重整制氢反应一定水醇比例的原料,不仅节省了精蒸馏浓缩乙醇水溶液所需的能耗[5],而且水中的氢通过蒸汽重整反应转化为氢气,具有反应条件温和,产氢效率高,适合于氢燃料电池和移动制氢设备使用等优点[6, 7]。
目前乙醇制氢比较先进的是在水汽重整的基础上加入吸附强化技术,其原理是将重整制氢过程中产生的CO2用吸附剂脱除,降低产物中CO2浓度,从而使反应平衡向生成氢气方向移动,达到强化制氢效果的目的。
CaO作为高温CO2吸附剂,具有吸附容量大,反应吸附速率快,强化效果明显的特点而受到重视。Gunduz等[8]用Ni-MCM-41催化剂,煅烧后石灰石作为吸附剂,在反应温度550℃,常压,水醇摩尔比3.2:1条件下得到氢气的收率为94%。Lysikov等[9]用Ni基催化剂,微米级CaO作为吸附剂,在反应压力5 atm,反应温度在650~750℃变温操作,水醇摩尔比6:1条件下制得97%~99%浓度氢气,CO含量为0.8%~1.0%,CO2含量在0.6~1.1%,CH4含量0.1%。Li等[10]用Co-Ni/HTlc催化剂,CaO基吸附剂,在反应温度550℃,常压,水醇摩尔比6:1,醇体积空速300 h-1条件下制得浓度99%的H2产物,CO含量为0.1%,CO2含量0.2%,CH4含量0.4%。
上述研究者主要使用的是微米级CaO吸附剂进行乙醇蒸汽重整制氢实验研究。但与微米级CaO相比,纳米级氧化钙具有更大的反应吸附速率和吸附容量的优势。唐琪等[11, 12]制备了不同CaO含量的纳米CaO/Al2O3吸附剂,吸附性能测试结果表明,随着CaO含量从12%提高到83%,吸附容量从1.02 mol·kg-1增加到7.05 mol·kg-1,同时吸附速率提高。师琦等[13]研究了纳米钙基吸附剂反应吸附和分解动力学,证明了纳米钙基吸附剂拥有更低的反应吸附和分解反应的活化能,反应吸附和再生分解速率快。从理论上分析,吸附速率的提高降低了二氧化碳浓度,促进了反应吸附强化作用[14]。在反应吸附强化甲烷蒸汽重整制氢过程中纳米钙基CO2吸附剂已经有成功应用经验。贺隽等[15]采用纳米CaO复合Ni催化剂在温度600℃,压力0.2 MPa,水碳摩尔比5的反应条件下制得了95.4%浓度的氢气,强化因子达到1.27,甲烷转化率在81.4%;李联豹[16]使用纳米CaO复合Ni催化剂在流化床反应器600℃,常压,水碳摩尔比4的条件下制得了95.7%浓度的氢气,甲烷转化率在90.8%。
此外,纳米CaO作为吸附剂可以克服微米CaO再生温度较高的缺点[17]。陈建峰等[18]制备平均表观粒径在17.5~21.5 nm的纳米CaCO3,在630℃时碳酸钙开始分解为CaO和CO2,790℃时完全分解。Wu等[19],Liu等[20],岳林海等[21, 22]都研究对比了纳米碳酸钙和微米碳酸钙的分解特性,结果表明纳米级碳酸钙的起始分解温度和最终分解温度均比微米级碳酸钙的低。较低的再生温度能够直接降低再生能耗,从而降低了整个乙醇制氢工艺的成本。
因此,本文提出研究采用纳米钙基吸附剂作为高温二氧化碳反应吸附剂,用于反应吸附强化生物乙醇水蒸气重整制氢(reactive sorption enhanced reforming of ethanol,ReSER-EtOH),利用纳米钙基吸附剂大的吸附容量以及与CO2的极高的反应吸附速率等性能提高制氢的效果,研究反应的温度、水醇摩尔比以及醇空速等工艺条件对ReSER-EtOH的影响并优化工艺条件,同时用强化因子E定量比较反应吸附强化的制氢效果。
2 实验材料和方法 2.1 实验材料乙醇,纯度 > 99.7%,国药集团化学试剂有限公司,与蒸馏水配置成一定浓度的乙醇水溶液,模拟生物乙醇。Ni催化剂,工业级,四川天一科技股份有限公司。自制纳米钙基CO2吸附剂,以粒径大约为70 nm纳米CaCO3(含量 > 95%,浙江菱化集团有限公司)和铝溶胶(淄博金琪化学试剂公司)为原料,加蒸馏水混合均匀,在红外灯下干燥后挤条成型,然后放入80℃干燥箱下干燥8 h,在800℃下焙烧1 h后备用,所有样品都经过研磨后过筛,得到0.9~1.5 mm的吸附剂颗粒。
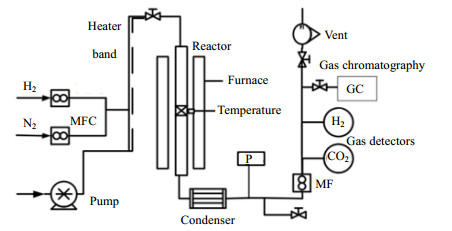
2.2 实验装置固定床反应器装置如图 1所示,反应器规格为Φ19 mm×2.5 mm,长600 mm的不锈钢管。再生气氛N2和还原气氛H2由钢瓶供给,并通过质量流量计控制流量。液体进料由液体进料泵(精度0.001 mL·min-1)控制。原料乙醇水混合液体经过预热段后,蒸发为气体,然后通入反应器。固定床反应器由电脑程序控温。出口气体经过冷水冷凝器后,通过气体流量计测量气体流量,然后进入在线色谱和气体检测器检测反应出口气体的组分和含量。
|
图 1 固定床ReSER制氢系统 Fig.1 Schematic diagram of fixed bed ReSER hydrogen production |
反应吸附强化乙醇蒸汽重整制氢工艺评价过程包括催化剂、吸附剂装填,再生,还原以及反应等过程。实验过程将5 g (粒径小于0.8 mm)研磨好的催化剂与9 g吸附剂混合均匀,装填在固定床恒温段中;通入N2,升温至800℃煅烧30 min,使吸附剂脱除H2O,CO2;然后降温至650℃,在N2/H2氛围中,将Ni催化剂中的Ni还原;最后升温至设定的反应温度下,用水泵通入一定摩尔比的乙醇/水溶液,经过加热带(150℃)预热汽化后,进入催化剂床层反应,出口气体流量由质量流量计进行监测记录,反应后气体冷凝,除去未反应的H2O,C2H5OH后气体直接进入在线色谱和气体检测器分析记录。在线的气相色谱检测条件为载气压力0.12 MPa,柱温140℃,进样器140℃,检测器140℃,TCD电流150 mA,并加装气体自动进样器。
2.4 计算方法反应吸附强化段乙醇转化率为在吸附强化段时乙醇的转化率,而平衡段的乙醇转化率即为吸附剂完全突破后乙醇的转化率,此时无吸附强化作用,反应过程同普通乙醇蒸汽重整过程类似。乙醇在反应吸附强化段以及平衡反应段的转化率计算公式如(1)和(2)所示。
反应吸附强化段乙醇转化率:
| $ {X_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = \frac{{{F_{{\rm{outlet}}}} \times {{\rm{H}}_{\rm{2}}}\% }}{{6{F_{{\rm{EtOH}}}}}} $ | (1) |
平衡反应段乙醇转化率:
| $ {X'_{{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}}} = \frac{{{F_{{\rm{outlet}}}} \times ({{\rm{H}}_{\rm{2}}}{\rm{\% }} + {\rm{C}}{{\rm{O}}_{\rm{2}}}\% )}}{{8{F_{{\rm{EtOH}}}}}}{\rm{ }} $ | (2) |
其中Foutlet为干基出口气体流量,mL·min-1,FEtOH为反应进料气体中乙醇蒸气流量,mL·min-1。
强化因子E定义:
| $ E = \frac{{吸附强化段{{\rm{H}}_2}体积分率}}{{平衡段{{\rm{H}}_2}体积分率}} $ | (3) |
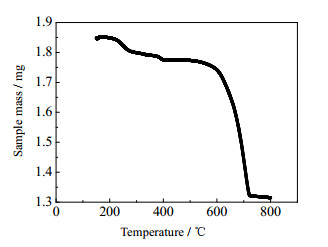
实验使用的纳米钙基CO2吸附剂的分解温度曲线如图 2所示:
|
图 2 纳米钙基吸附剂分解曲线 Fig.2 Decomposition curve of nano Ca-based adsorbent |
在热重分析仪(TGA)测试下,经过150℃脱水处理10 min后,吸附剂以15℃·min-1的升温速率进行非等温分解,得到的结果为纳米钙基CO2吸附剂的初始分解温度为550℃,于720℃下完全分解。相比于微米级钙基吸附剂900℃以上的分解温度,纳米钙基CO2吸附剂的再生温度低,能够减少再生过程能耗。
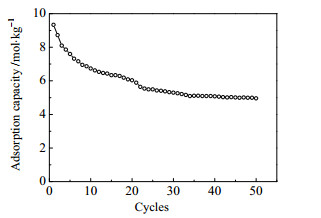
图 3为纳米钙基CO2吸附剂使用TGA测试的循环吸附容量变化图。测试条件为:吸附温度600℃,气体为20% CO2 (N2平衡);再生温度800℃,气体为100% N2。升温速率为15℃·min-1,降温速率为40℃×min-1。纳米氧化钙基二氧化碳吸附剂35次循环后吸附容量稳定在5 mol·kg-1。说明实验采用的吸附剂对二氧化碳有较大的反应吸附容量和循环稳定性,能够用于本文乙醇蒸汽重整过程二氧化碳的吸附。
|
图 3 吸附容量随循环次数的变化 Fig.3 Adsorption capacity as a function of reaction cycles |
图 4(a)为纳米钙基吸附剂制备的前驱体纳米级碳酸钙。图 4(b)为再生后的吸附剂颗粒形貌,经过800℃再生后仍能保持着原有颗粒结构。

|
图 4 纳米钙基吸附剂扫描电镜图 Fig.4 SEM micrographs of (a) nano Ca-based sorbents precursor; (b) nano Ca-based sorbents structure after spray |
温度对纳米钙基CO2吸附剂的反应吸附性能以及镍基催化剂的催化反应活性有重要影响。根据镍基催化剂的使用温度,反应吸附强化乙醇蒸汽重整的反应温度应在500~700℃,因此,选取520,560,600,640℃四个温度条件研究了温度对吸附强化乙醇蒸汽重整反应的影响,其中,反应醇体积空速为600 h-1,水醇摩尔比Steam/EtOH为5:1,吸附剂和催化剂的质量比为9:5。表 1为不同温度下反应吸附强化段出口气体浓度。
| 表 1 温度对吸附强化段反应的影响 Table 1 Effects of temperature on enhanced adsorption reaction |
由表 1可知,在520~640℃,ReSER-EtOH反应能够产生浓度98%左右的H2,氢气浓度随温度升高略有下降,主要是因为温度升高导致氧化钙与二氧化碳反应生成的碳酸钙在高温下略有分解,从而一定程度上削弱了吸附强化的效果。吸附平衡段的氢气浓度在70%~80%,且随着反应温度的增加而增加,这是因为乙醇蒸汽重整过程为吸热反应。由表 1还可以看出,吸附强化反应中生成的CO极少量(< 0.2%),气相色谱中无CO2检测出,为产物气体直接应用于燃料电池提供了有利条件。此外,由表 1可以发现,在吸附强化段有少量副产物CH4生成,仅改变反应温度并不能显著影响产物中甲烷浓度。结合乙醇蒸汽重整反应体系所含物质种类与反应[23],推测生成甲烷的反应步骤很多,同时含有吸热反应及放热反应。因此,产物中甲烷浓度不随温度变化而改变。若要进一步减少甲烷生成,需要更深入明确反应机理,优化催化剂选择性。
反应温度对乙醇转化率的影响如图 5所示。随着温度增加,平衡段和反应吸附强化段的乙醇转化率均逐渐增加;在相同温度下,吸附强化段乙醇转化率比平衡反应段平均高出20%以上。乙醇蒸汽重整制氢是吸热反应,温度越高越利于提高氢气浓度,乙醇转化率和反应速率。但是在吸附强化过程中,过高的温度会使破坏吸附剂中CaO与CO2间的吸附平衡,降低吸附性能,影响吸附强化效果,从而降低了产物氢气浓度。综合反应速率、产物氢气浓度以及钙基吸附剂活性等因素,采用纳米钙基CO2吸附剂的乙醇反应吸附强化蒸汽重整制氢的反应温度应控制在560℃。相比于普通乙醇水蒸汽重整制氢,加入吸附强化可以在不改变反应温度情况下提高乙醇转化率和氢气浓度,或者在达到相同结果的情况下降低反应温度,从而进一步降低能耗。

|
图 5 温度对乙醇转化率的影响 Fig.5 Effects of temperature on ethanol conversion (5 g/9 g, Steam/EtOH = 5, 600 h-1) |
除了反应温度外,水醇摩尔比对乙醇蒸汽重整制氢过程也有重要影响。理论上,水醇摩尔比越高,乙醇的转化率越大,氢气浓度越高;但过高的水醇摩尔比需要消耗更多的能量来汽化反应物,增加重整制氢过程的能耗。当反应温度为560℃时,水醇摩尔比为3:1、5:1、7:1、10:1四个条件对乙醇蒸汽重整制氢产物浓度的影响如表 2所示。在实验设定的乙醇摩尔比提条件下,吸附强化段反应中均未检测到CO2存在,表明产生的CO2均被吸附,且水醇摩尔比改变对纳米钙基吸附剂的吸附活性没有影响。
| 表 2 水醇摩尔比对ReSER-EtOH制氢结果的影响 Table 2 Effect of steam-to-ethanol molar ratio on hydrogen production of ReSER-EtOH |
此外,随着水醇摩尔比的增加,乙醇转化率明显增加,同时产物中CO浓度逐渐减少,甲烷浓度也略有下降。主要因为水汽含量的增加可以促进乙醇重整反应,同时也促进了水汽变换反应以及甲烷水汽重整反应。在水醇摩尔比3~10,吸附强化段反应所得到的氢气浓度均较高,且随水醇摩尔比变化较小,氢气浓度平均高出平衡反应段30%,强化因子在1.3左右。
图 6表示水醇摩尔比对乙醇转化率的影响。在相同水醇摩尔比下,吸附强化段的乙醇转化率高于平衡反应段约30%,二者均随水醇摩尔比增加而增加,但增幅逐渐趋缓。综上,相比于普通水汽重整,吸附强化技术具有很大优势,其可得到较高的乙醇转化率与高浓度的氢气产物。随水醇摩尔比增加,ReSER-EtOH反应中氢气浓度与乙醇转化率均增加。水醇摩尔比大于5时,产物氢气浓度能够达到98%以上,水醇摩尔比从7增大至10时,乙醇转化率提升并不明显。因此本实验条件下水醇摩尔比在7:1比较合适。生物乙醇的含水量一般比较大,高于反应所需要的水醇比。考虑到较大的水醇摩尔比将会进一步增大反应能耗,在实际应用中,应当选取在达到合适的乙醇转化率情况下尽量小的水醇摩尔比。

|
图 6 水醇摩尔比对乙醇转化率的影响 Fig.6 Effects of steam-to-ethanol molar ratio on ethanol conversion (5 g/9 g, 500℃, 600 h-1) |
反应空速反映了停留时间,从而影响反应的转化率。对于吸附强化乙醇蒸汽重整制氢过程,反应空速增大,停留时间变短,催化反应转化率降低,吸附剂吸附效果也可能下降。反应温度560℃、水醇摩尔比为7时,醇体积空速分别为600,800,1000 h-1的制氢吸附强化段结果如表 3所示。
| 表 3 不同空速条件下ReSER-EtOH制氢结果 Table 3 Effects of space velocity on hydrogen production of ReSER-EtOH |
由表 3可知,随着空速的增大,产物气体中CO浓度和CH4浓度逐渐增加;当空速增幅超过催化剂的处理能力时,H2浓度与乙醇转化率会有明显下降。增大空速会缩短反应物在反应器床层中的停留时间,削弱吸附强化过程,从而使得乙醇转化率有所下降,此外也增加副反应发生概率,增加了中间产物(CO、CH4)的浓度。但在所有产物气体中均未检测到CO2,因此可以认为即使是在催化剂能处理的制氢反应最大空速下,纳米钙基吸附剂吸附活性依然很高,确保了吸附强化反应的进行。综合空速对产物气体浓度分布以及乙醇转化率的影响,实验使用的催化剂与吸附剂乙醇重整制氢最大处理量为醇体积空速800 h-1。
图 7给出了在560℃水醇比为5,催化剂与吸附剂质量比5:9,醇体积空速800 h-1下各出口气体浓度随时间的变化,可以看到在反应开始至18 min的时间段为反应吸附强化段,此时产物H2浓度很高,杂质气体量很少。当反应进行到18 min以后,由于吸附剂逐渐达到吸附饱和,重整反应逐渐趋向反应平衡段,主要表现为CO2浓度突破,开始检测到CO2的产生,此时H2浓度逐渐下降,CH4,CO,CO2浓度相应逐渐上升,直至吸附剂完全饱和,最终达到平衡反应段。

|
图 7 出口气体浓度随时间变化 Fig.7 Outlet gas concentration as a function of time (space velacity 800 h-1, 5g/9g, T = 560℃, Steam/EtOH = 5) |
本文将工业级镍重整催化剂与纳米钙基CO2吸附剂物理混合,使用固定床研究生物乙醇反应吸附强化蒸汽重整制氢(ReSER-EtOH)反应。研究了不同温度、水醇摩尔比和空速等反应条件对ReSER-EtOH制氢结果的影响,主要结论如下:
(1) 在热重分析仪测试下,纳米钙基CO2吸附剂初始分解温度为550℃,于720℃下完全分解。吸附剂初次循环吸附容量为9.34 mol·kg-1,循环稳定后的吸附容量为5 mol·kg-1,再生后吸附剂微球颗粒保持稳定外形,能够用作强化乙醇蒸汽重整制氢过程的吸附剂。
(2) ReSER-EtOH在反应温度520~640℃和水醇摩尔比在3~10,能够直接得到98%浓度的氢气,产物中未检出CO2,CO含量低于0.2%,含副产CH4气体2%以下。乙醇转化率随着温度的升高而增加。反应温度越低,吸附强化作用越明显。随着水醇比的增加,反应后H2浓度和乙醇转化率增加,CH4和CO浓度降低。但过高的水醇比将增大反应能耗,优化的反应水醇摩尔比选择为7:1。
(3) 以32%(V/V)生物乙醇作为原料,即反应水醇摩尔比7:1,采用镍重整催化剂,在纳米钙基CO2吸附剂的强化作用下得到优化的工艺条件为:常压下,醇体积空速800 h-1,反应温度560℃,能够得到98.2%浓度的氢气产物,乙醇转化率为90.5%,其中CO浓度为500 ppm,其余副产气体为甲烷。研究结果对用生物乙醇制氢应用于燃料电池和移动制氢设备具有重要的意义。
| [1] | Sartbaeva A, Kuznetsov V L, Wells S A, et al. Hydrogen nexus in a sustainable energy future[J]. Energy & Environmental Science , 2008, 1(1): 79-85. |
| [2] | MAO Zong-qiang(毛宗强). Nations quicken pace of developing hydrogen energy market:a brief introduction to WHEC2010(世界各国加快氢能源市场化步伐——记第18届世界氢能大会(WHEC 2010))[J]. Sino-Global Energy(中外能源) , 2010, 15(7): 29-34. |
| [3] | LANG Lin(郎林), LI Jian-ming(李键铭), YANG Wen-shen(杨文申), et al. Bio-ethanol catalytic steam reforming over Ni/KZSM-5 catalysts(Ni/KZSM-5催化剂的生物乙醇水蒸气重整制氢催化性能)[J]. Renewable Energy Resources(可再生能源) , 2017, 35(2): 185-191. |
| [4] | Lapola D M, Turner B L. Indirect land-use changes can overcome carbon savings from biofuels in Brazil[J]. Proceedings of the Natconal Academy of Sciences of the United States of America , 2010, 107(8): 3388-3393. DOI:10.1073/pnas.0907318107. |
| [5] | ZHANG Chao(张超), LANG Lin(郎林), YIN Xiu-li(阴秀丽). Reactors for hydrogen production by bio-ethanol reforming(生物乙醇重整制氢反应器)[J]. Progress in Chemistry(化学进展) , 2011, 23(4): 810-818. |
| [6] | Deluga G A, Salge J R, Schmidt L D, et al. Renewable hydrogen from ethanol by autothermal reforming[J]. Science , 2004, 303(5660): 993. DOI:10.1126/science.1093045. |
| [7] | Meng N, Dennis Y C, Michael K H. A review on reforming bio-ethanol for hydrogen production[J]. International Journal of Hydrogen Energy , 2007, 32(15): 3238-3247. DOI:10.1016/j.ijhydene.2007.04.038. |
| [8] | Gunduz S, Dogu T. Sorption-enhanced reforming of ethanol over Ni-and Co-incorporated MCM-41 type catalysts[J]. Industrial & Engineering Chemistry Research , 2011, 51(26): 8796-8805. |
| [9] | Lysikov A, Derevschikov V, Okunev A. Sorption-enhanced reforming of bioethanol in dual fixed bed reactor for continuous hydrogen production[J]. International Journal of Hydrogen Energy , 2015, 40(42): 14436-14444. DOI:10.1016/j.ijhydene.2015.06.029. |
| [10] | He L, Berntsen H, Chen D. Approaching sustainable H2 production:sorption enhanced steam reforming of ethanol[J]. Journal of Physical Chemistry A , 2010, 114(11): 3834-44. DOI:10.1021/jp906146y. |
| [11] | TANG Qi(唐琪), WU Su-fang(吴素芳). The effect of CaO content on sorption performance of nano-CaO based CO2 adsorbent(CaO含量对纳米CaO/Al2O3吸附剂性能的影响)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2012, 26(1): 31-36. |
| [12] | SHI Yu-yao(史余耀), LAN Pei-qiang(兰培强), WANG Yan(王燕). Modified kinetics model of nano-CaO reactions with CO2 in a CaO-based adsorbent(钙基吸附剂中纳米CaO与CO2反应动力学模型的改进)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2015, 29(1): 96-101. |
| [13] | SHI Qi(师琦), WU Su-fang(吴素芳), JIANG Ming-zhe(蒋明哲), et al. Reactive sorption-decomposition kinetics of nano Ca-based CO2 sorbents(纳米钙基CO2吸附剂反应吸附与分解动力学)[J]. CIESC Journal(化工学报) , 2009, 60(3): 641-648. |
| [14] | Wu S F, Beum T H, Yang J I, et al. The characteristics of a sorption-enhanced steam-methane reaction for the production of hydrogen using CO2 sorbent[J]. Chinese Journal of Chemical Engineering , 2005, 13(1): 43-47. |
| [15] | HE Jun(贺隽), WU Su-fang(吴素芳). The characteristics of sorption enhanced steam methane reforming for hydrogen production on a complex catalyst(吸附强化的甲烷水蒸汽重整制氢反应特性)[J]. Chemical Reaction Engineering and Technology(化学反应工程与工艺) , 2007, 23(5): 470-473. |
| [16] | 李联豹. RSER制氢过程复合催化剂反应特性及动力学研究[D]. 杭州: 浙江大学, 2008. LI Lian-bao. Study on the reactive characteristics and kinetics of the reactive sorption catalyst in the RSER process for hydrogen production [D]. Hangzhou : Zhejiang University, 2008. http://cdmd.cnki.com.cn/article/cdmd-10335-2008091372.htm |
| [17] | LU Shang-qing(卢尚青), WU Su-fang(吴素芳). Advances in calcium carbonate thermal decomposition(碳酸钙热分解进展)[J]. CIESC Journal(化工学报) , 2015, 66(8): 2895-2902. |
| [18] | CHEN Jian-feng(陈建峰), JIA Zhi-qian(贾志谦), WANG Yu-hong(王玉红), et al. Synthesis and characterization of cube-shaped CaCO3 nanometer particles in high gravity field(超重力场中合成立方形纳米CaCO3颗粒与表征)[J]. Chinese Journal of Chemical Physics(化学物理学报) , 1997, 10(5): 457-460. |
| [19] | Wu S F, Li Q H, Kim J N, et al. Properties of a nano CaO/Al2O3 CO2 sorbent[J]. Industrial & Engineering Chemistry Research , 2008, 47(1): 180-184. |
| [20] | Liu R J, Chen J F, Guo F, et al. Kinetics and mechanism of decomposition of nano-sized calcium carbonate under non-isothermal condition[J]. Chinese Journal of Chemical Engineering , 2003, 11(3): 302-306. |
| [21] | YUE Lin-hai(岳林海), SHUI Miao(水淼), XU Zhu-de(徐铸德), et al. The crystal structure of ultra-fine CaCO3 and its thermal decomposition(超细碳酸钙微晶结构与热分解特性)[J]. Chemical Research In Chinese Universities(高等学校化学学报) , 2000, 21(10): 1555-1559. DOI:10.3321/j.issn:0251-0790.2000.10.020. |
| [22] | YUE Lin-hai(岳林海), SHUI Miao(水淼). Decomposition kinetics of nano-particle calcite(纳米级粒径超细碳酸钙热分解动力学)[J]. Chinese Journal of Inorganic Chemistry(无机化学学报) , 1999, 15(2): 225-229. |
| [23] | 王文举. Ni催化剂催化乙醇重整制氢的研究[D]. 天津: 天津大学, 2009. WANG Wen-jun. Reforming of ethanol for hydrogen production catalyzed by nickel catalysts [D]. Tianjin : Tianjin University, 2009. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1677724 |




