2. 中国科学院可再生能源重点实验室,广东 广州 510640;
3. 广东省新能源和可再生能源研究开发与应用重点实验室,广东 广州 510640;
4. 中国科学院大学,北京 100871
2. CAS Key Laboratory of Renewable Energy, Guangzhou 510640, China;
3. Guangdong Provincial Key Laboratory of New and Renewable Energy Research and Development, Guangzhou 510640, China;
4. University of Chinese Academy of Sciences, Beijing 100871, China
木质素是自然界中含量仅次于纤维素的芳香性高聚物(占生物质的15%~30%)[1]。近年来,随着纤维素乙醇商业化生产的发展,作为水解残渣主要成分的木质素高值化利用引起了科技工作者的极大兴趣[2]。
由于木质素是由苯丙烷结构单体组成的大分子物质,因此有望成为生产苯酚、愈创木酚等单酚类高附加值芳香类精细化学品以及芳烃、环烷烃、烷烃等高品位生物燃油的主要可再生原料[3]。利用木质素生产高价值精细化学品可以减少对化石资源的依赖,同时还能减少制浆过程对环境的污染和降低二氧化碳排放,此外还将极大地提高生物炼制产业的竞争力。
尽管木质素在自然界中含量丰富并具有很高的利用潜能,却难以真正被利用,98%的木质素在纸浆和造纸工业中作为能源被焚烧。复杂的三维网状堆积结构、化学键合方式以及氢键作用,使得木质素大分子难以高效降解为酚类单体或化学品,限制了其利用[4]。近年来对木质素的催化解聚转化为高附加值燃料和化学品的研究虽然取得了较大进展,但是工业化生产和应用还面临着许多问题与挑战。本文重点综述了木质素催化氧化解聚的最新进展, 也对微波等辅助解聚手段进行了分析讨论。
2 木质素种类与特性 2.1 木质素组成与结构木质素结构和组成取决于物种种类、植物部位和生长条件等因素,使得木质素的研究更为复杂,原生木质素的确切结构几乎未知[5]。幸运的是,鉴定降解产物方法的改进以及光谱技术的进步揭示了许多与木质素结构特征相关的信息[6]。研究表明,组成木质素的3种醇单体(香豆醇、松柏醇和芥子醇)之间是通过一系列的C─O键和C─C键连接的,包括β-O-4 (超过50%), 4-O-5,β-β,5-5,β-1等连接方式[7]。由于木质素的结构与组成的复杂性,促使人们在木质素利用研究中引入几种较简单的低分子量模型化合物来获得与木质素的反应性和断键机理相关的信息。文献报道最多的模型化合物是存在于木质素结构中的芳香族单体(愈创木酚,香草醇,紫丁香醇,藜芦醇等)以及含有特定C─O键的模型化合物(如β-O-4型)和C─C模型化合物(如α-1,β-1,5-5型)[8]。
2.2 木质素种类预处理是生物炼制操作中的重要初始步骤,不同的预处理方法(包括温度、压力、溶剂以及pH值)将不同程度地改变木质素的结构与连接方式[9-10]。根据预处理方法的不同,可将工业木质素分为木质素硫酸盐[11]、木质素磺酸盐[6]、有机溶剂木质素[12]、热解木质素[13]以及蒸汽爆破木质素[14]等,它们的平均分子重量和单体分子式见表 1。
|
|
表 1 几种常见的工业木质素及单体分子式 Table 1 Typical lignin types and their monomeric molecule formula |
要实现木质素转化为高附加值燃料和化学品的高效综合利用,首先需要选择性断裂木质素分子中的特征化学键[16]。为了实现这一目的而发展出来的主要热化学方法有热解、氧化、还原等[17]。
热解是木质纤维素生物质直接制备生物油的主要化学方法之一。通常在无氧的条件下,在450~600 ℃的温度下快速(通常在100 ℃·s-1以上)加热生物质以生成不凝气体(10%)、液体油(40%)和固体(50%)的混合物[2]。热解油(也称生物油)是一种低品质的液体燃料,具有低pH值,高黏度,高氧含量和稳定性差等许多不良特性,不能与常规石油燃料调和[18]。另外,来自生物炼制或者大多数制浆过程的湿木质素在进入热解炉之前必须干燥,原料中的大量水的蒸发需要大量能量,降低了该过程的经济性[19]。
还原解聚能够高效地将木质素降解成木质素片段、酚类以及其他高值化合物,通过精炼将这些解聚产物转化为芳环平台化合物。华盛顿州立大学LASKAR等[20]采用贵金属催化剂与酸性沸石组成的双功能催化剂对蒸汽爆破木质素进行加氢脱氧,转化率达到35%~60%,同时甲苯的选择转化达到65%~70%。国内ZHAI等[21]用双金属Ni─Fe/AC催化剂在225 ℃、2 MPa H2条件下对有机溶剂木质素的解聚行为进行了系统研究,发现该催化体系不仅能显著降低β-O-4键的解离能,还得到了w = 39.5%的最高单体收率(主要是丙基愈创木酚和丙基丙烯醇)。研究结果表明,加氢还原方法虽然能够提高酚类化合物的产率,但是这些过程仍然存在一个共同的问题:焦炭的生成导致催化剂的失活,而且,在高温高氢压条件下,芳环氢化副反应的发生破坏了木质素中的苯环结构。此外,由于木质素含氧量高,加氢过程产生的水也容易造成催化剂失活[6]。
热解和还原解聚方法在破坏木质素大分子的时候,倾向于破坏木质素结构单元之间的连接键,以及除去苯环上的基团,同时需要更苛刻的反应条件(高温、高压以及更长的反应时间)。相反,氧化在破坏木质素大分子的时候,倾向于增加解聚产物的功能基团,如形成羧基、醛基等,可以直接用做平台化学品或转化为精细化学品,而且反应条件更加温和。SCHUTYSER等[22]系统研究了一系列无机金属基催化剂(金属盐,金属氧化物以及多金属氧酸盐)对杨木木质素在碱性介质中的解聚行为,使用CuSO4催化剂时在175 ℃下反应仅10 min就得到了w = 30 %的单酚收率(含w = 13%的丁香醛,w = 7%的香草醛和w = 6%的对羟基苯甲酸)。
3 木质素氧化解聚木质素催化氧化解聚具有以下几个明显的优势:(1)与热解(450~700 ℃)和加氢还原(100~350 ℃)等大多数热化学方法相比,氧化方法的反应温度(0~250 ℃)比较温和,反应时间更短[23];(2)生成更为复杂的平台芳烃化合物,具有特征官能团的产物更易于分离;(3)氧化过程在侧链或者芳环中引入氧,减小了电子密度并增大了木质素芳环间的空间位阻,进而削弱了π-π相互作用,使木质素结构单元间易于解离[24];(4)木质素中含有大量的羟基官能团,其中侧链Cα羟基的氧化可促进β-O-4键的断裂[25-26]。因此以芳香醛和羧酸为主要产物的氧化裂解是一种极富吸引力的解聚方法。以下对木质素氧化解聚过程使用的溶剂、氧化剂、催化剂种类和可能的转化路线进行详细的总结。
3.1 溶剂溶剂对木质素的解聚反应及后续的分离过程具有重要的影响。用于木质素氧化解聚的介质主要包括有机溶剂、酸溶液、碱溶液以及离子液体[27]。有机溶剂通常是非绿色的且有一定的危险性(易燃),如吡啶、甲苯、乙腈、甲醇等。易燃溶剂与氧气组合具有潜在的爆炸危害,这取决于溶剂和氧气在气相中的浓度[8]。为了降低爆炸的风险,采取的主要方法是降低氧气浓度,但是低氧气浓度对氧化反应不利。强碱(NaOH,KOH)溶液是应用最多的,因为在该介质中的木质素氧化能够选择性地生产香草醛和丁香醛。但是碱性溶剂的使用给后续的产物分离带来繁琐的步骤:酸化后用有机溶剂萃取,需要消耗大量的酸和有机溶剂并产生大量的盐溶液[8]。为了避免酸化或有机溶剂的使用,目前提出了用超临界CO2萃取或用树脂吸附等方法,但是需要深化研究并有效分离反应产物[28]。近年来离子液体因其独特的性能被广泛应用到生物质溶解中,其优点是对气体(氧化剂O2)和木质纤维素类材料具有良好的溶解性,但是在使用时需要考虑离子液体的成本、毒性、氧化稳定性,产物分离和离子液体的回收等因素[6]。强酸性溶液因其对容器的腐蚀性大,在木质素氧化解聚研究中不如其他3种溶剂应用广泛,这里不展开叙述。
3.2 氧化剂各种类型的氧化剂已被用于木质素及其模型化合物的氧化,常见的包括:O2,H2O2,硝基苯,臭氧等[23]。其中O2、H2O2和硝基苯是研究最多的氧化剂。文献报道碱性介质中硝基苯氧化木质素生产香草醛是十分有效的反应过程,然而,硝基苯有毒有害性并不适合工业化[29]。近年来在碱性条件下O2氧化木质素过程受到大量关注,然而该反应的局限主要在于O2在NaOH溶液中的低溶解度和产物复杂的问题[30-31]。
3.3 催化剂木质素催化氧化解聚催化剂可分为均相催化剂和非均相催化剂。非均相催化剂在木质素解聚研究中具有易于分离回收和引入气相和液相中的有机污染物最少的优点[2]。而均相催化剂虽然在分离和回收方面还存在一定挑战,但是配体的电子和空间特性显著影响了催化剂的活性、稳定性和溶解性[6]。下面对这两类催化剂进行详细分析。
3.3.1 非均相催化剂过渡金属和贵金属催化剂
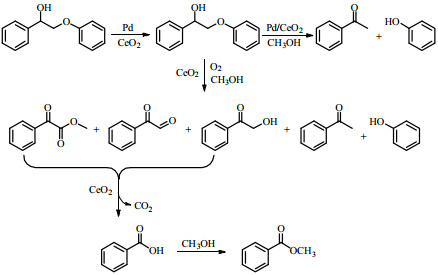
过渡金属和Pt、Pd等贵金属广泛应用于木质素的催化氧化[34]。BHARGAVA等[35]对比了Cu、Mn和Pd等单一金属和负载的双金属催化剂(如Mn负载Cu或Pd负载Cu)在纸浆废液氧化过程中的表现,发现Pd负载的Cu催化解聚效果最好。在VILLAR等[36]的研究中,将Al2O3负载的Pt催化剂应用于150 ℃、7 atm条件下硬木硫酸盐木质素的氧化,发现与无催化条件相比醛或酸的产率不仅没有增加反而有所下降,作者提出,Pt-Al2O3可能过度氧化木质素成为更小的分子或CO2。DENG等[37]报道氧化铈负载的钯纳米粒子(Pd/CeO2)可以有效催化β-O-4模型化合物2-苯氧基-1-苯乙醇在O2气氛和甲醇溶剂中转化为苯酚、苯乙酮等单环芳烃化合物,其转化过程见图 1。在Pd纳米粒子的作用下,2-苯氧基-1-苯乙醇的Cα-羟基首先被氧化成Cα-酮基,Cα-酮基活化了β-O-4键,随后在Pd/CeO2催化剂上裂解,得到苯酚和苯乙酮,同时,Cα─Cβ键发生氧化裂解,生成苯甲酸和酯化产物苯甲酸甲酯。
|
图 1 Pd/CeO2催化2-苯氧基-1-苯乙醇氧化转化路线图[37] Fig.1 Proposed pathway for oxidative conversion of 2-phenoxy-1-phenylethanol with a Pd/CeO2 catalyst[37] |
钙钛矿型金属氧化物
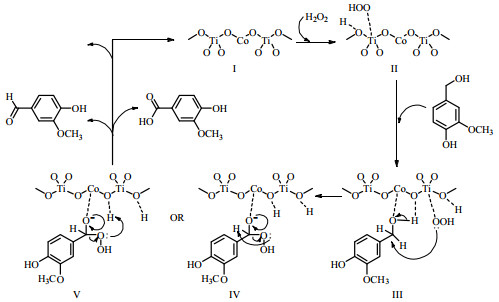
钙钛矿在木质素解聚研究中的应用是基于DENG等[38-39]的工作,Co,Mn和Fe基钙钛矿显著提高了碱性木质素氧化产物的产率,Cu掺杂(如LaCo0.8Cu0.2O3和LaMn0.8Cu0.2O3)可以改善反应性能。SCHUTYSER等[22]使用溶胶-凝胶法合成了LnMnO3、LaFeO3和LaCoO3等钙钛矿型混合金属氧化物催化剂,在碱性条件下氧化杨木木质素。与非催化反应相比,LnMnO3催化条件下获得了更高收率的香草醛、丁香醛和对羟基苯甲醛(w = 13%);而反应中LaFeO3无活性,LaCoO3表现出轻微的活性。证实了掺杂Cu可以提高催化性能,因为该反应是自由基反应,Cu的掺杂提高了表面晶格氧的百分比,从而提高了芳香醛的产率和选择性。在酸性以及碱性介质中以H2O2为氧化剂时,由Co(OAc)2和Ti(iPro)4在甲醇溶剂中制备的CoTiO3催化香草醇氧化反应获得了相当高的转化率(91%~99.8%),对香草醛的选择性为68%~99% (取决于反应介质)[40]。其反应机理见图 2,CoTiO3催化剂首先与H2O2反应形成氢过氧自由基,作为高活性氧化剂的来源;当催化剂表面的香草醇被活化时,富电子氢过氧基通过氧攻击带部分正电的碳和羟基的氢以形成活化的氧物质,促进氢过氧基中羟基的脱除并产生副产物水;同时,香草酸阳离子释放出质子,该质子受到氢过氧基的富电子氧的攻击,生成香草醛和香草酸。
|
图 2 CoTiO3催化氧化香草醇转化为香草醛和香草酸的机理图[40] Fig.2 Suggested mechanism for the formation of vanillin and vanillic acid from vanillyl alcohol with CoTiO3[40] |
多金属氧酸盐
多金属氧酸盐(POMs)是最早用于纸浆脱木质素的催化剂[6]。POMs由主要和次要杂原子组成,其中前者决定结构,后者通常是过渡金属离子,可以在不改变结构的情况下被取代。具有可逆氧化、可溶于水溶液或有机溶液的优点;缺点是产生大量的自由基中间体,导致重聚现象严重。TOBIAS等[41]在甲醇-水体系中使用H3PMo12O40催化硫酸盐木质素解聚,提出H3PMo12O40催化氧化木质素是分两步进行的,氧化解聚产物主要是低聚物和单酚。
| $ {\mathop{\rm lignin}\nolimits} + {\left[ {{{{\mathop{\rm PMo}\nolimits} }_{12}}{{\rm{O}}_{40}}} \right]^{3 - }} \to {{\mathop{\rm lignin}\nolimits} _{\left( {{\rm{OX}}} \right)}} + {\left[ {{\rm{PM}}{{\rm{o}}_{12}}{{\rm{O}}_{40}}} \right]^{(3 + n) - }} + \quad m{{\rm{H}}^ + } $ | (1) |
| $ {\left[ {{\rm{PM}}{{\rm{o}}_{12}}{{\rm{O}}_{40}}} \right]^{(3 + n) - }} + (n/4){{\rm{O}}_2} + n{{\rm{H}}^ + } \to {\left[ {{\rm{PM}}{{\rm{o}}_{12}}{{\rm{O}}_{40}}} \right]^{3 - }} + \left( {(n/2){{\rm{H}}_2}{\rm{O}}} \right. $ | (2) |
金属(salen)配合物
Salen配合物具有显著的优点,它们便宜,更容易合成并且相对稳定[2]。其中,Co(salen)络合物由于与水性反应介质相容成为木质素氧化降解中研究最多的一种催化剂。应用Co(salen)络合物时,可能会发生脂肪链上羟基的氧化反应、β-O-4裂解、开环反应和脱甲氧基化反应。GAO等[42]将Co(salen)粉末均匀地分散在陶瓷纤维上制成Co(salen)浸渍纸,以H2O2作为氧化剂氧化硫酸盐木质素,解聚结果表明,与传统粉末相比,三维网状的Co(salen)催化剂对硫酸盐木质素的氧化更有效,香草醛、丁香醛和2, 6-二甲氧基苯酚等单体酚的产率从w = 10.6%提高到w = 23.3%;2D-NMR(HSQC)结果证实了β-O-4键的氧化裂解。
碱催化剂
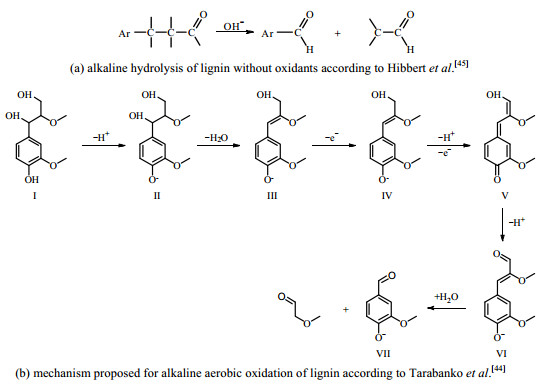
强碱(NaOH,KOH)不仅能有效促进木质素的水解,还可以加速氧化反应[43]。文献中提出了多种碱氧化木质素生成香草醛的机理,TARABANKO等[44]提出的自由基反应机理目前得到普遍认可,是在碱促逆Aldol反应断裂C─C键机理的[45]基础上提出的(见图 3(a))。碱性介质中木质素氧化解聚生成香草醛的机理见图 3(b):木质素中的酚阴离子(Ⅱ)经脱水后再失去一个电子形成酚氧自由基(Ⅳ),随后脱去一个质子,形成具有醌式结构的中间体(Ⅴ),最后经历与HIBBERT等[45]提出的碱促逆Aldol反应类似的过程,断裂Cα─Cβ键得到香草醛(Ⅶ)。
|
图 3 碱氧化木质素生成香草醛机理图 Fig.3 Mechanism of alkaline aerobic oxidation of lignin for the formation of vanillin |
过渡金属盐催化剂
简单金属盐催化剂的发展起源于烃氧化催化剂,特别是用于选择性氧化芳香烃如对二甲苯以生成对苯二甲酸(是用于生产塑料的重要平台化学品)[46]。最常见的过渡金属盐催化剂如CuSO4、FeCl3,具有高氧化电位并容易使电子在木质素的芳环上发生迁移。XIANG等[47]利用CuSO4和FeCl3在160~180 ℃下对黄杨木屑进行了氧化处理,主要产物包括芳香醛、酮和酸,香草醛和丁香醛,产率约为w = 15%。研究证实CuSO4对于沉淀的硬木木质素氧化非常有效,Fe3+能提高醛的选择性。同时加入Cu2+和Fe3+比不加催化剂或单独添加其中一种金属离子时对木质素氧化解聚的转化率和选择性更为有利。与WU等[48-49]的研究结果类似,使用CuSO4和FeCl3在w = 13.5%的NaOH溶剂中氧化蒸汽爆破硬木木质素,获得了w = 14.6%的醛产率(其中香草醛w = 4.7%),转化率比无催化剂时高10%~15%,比单独使用Cu2+时高5%~10 %。机理研究显示Cu2+加速了苯氧基的形成,从而加速了自由基氧化反应;而Fe3+与酚类化合物形成配合物作为氧化过程中的氧载体,加速了离子反应[50]。金属盐催化木质素氧化解聚不仅能在碱溶剂中进行,酸也被证明是一种有效的介质。WERHAN等[51]在酸氧化硫酸盐木质素研究中,发现CoCl2是最有效的催化剂:反应1 h后香草醛和甲基香草酸酯的收率为w = 6.5 %。ZHANG等[52]以CuI为催化剂,O2为氧化剂,甲苯为溶剂,70 ℃条件下通过氧化反应和逆Aldol反应的耦合实现了β-O-4木质素模型化合物的高效催化氧化,获得了w = 88%的目标产物收率。ZAKZESKI等[53]研究了在温和条件下,离子液体中金属催化剂对木质素的氧化降解。结果表明,过渡金属阳离子的一般活性顺序为Co > Cr > Fe > Ni > Mn > Cu,然而,金属盐的阴离子不一致,可能会影响结果的准确性。
综合来看,以上催化剂在木质素模型化合物解聚中,转化率和产率相当高,然而用于真实木质素的解聚研究时,单体产率却只有w = 5%~30%(见表 3)[11]。这是因为,木质素原料结构的复杂性以及官能团和连接键的多样性,使得模型化合物并不能完全代表真实的木质素;另外,真实木质素体系下解聚产物的重聚和再缩合现象也是一个重要的原因。
|
|
表 3 真实木质素催化氧化解聚 Table 3 Summary of oxidative depolymerization of raw lignin materials |
木质素的催化氧化解聚转化为高附加值燃料和化学品是一个重要且有前景的方向,以下几个问题不容忽视:(1)尽管木质素的氧化具有相对温和的反应温度,但是通常还需要苛刻的条件(如高压,酸性或碱性环境,添加有毒或昂贵的催化剂以及使用特定的反应器等)。因此温和条件下木质素特征化学键的催化断裂仍然是该领域当前和今后的一个热点和难点问题;(2)由于生物质原料的特殊性,前期研究绝大多数采用的是间歇釜式反应器,但随着研究的不断深入,越来越多的学者提出木质素的氧化是非常迅速的,高压釜反应器的升温和降温过程会引发更多的副反应从而导致单体产率下降[55]。如近期SCHUTYSER等[22]对杨木木质素在碱性条件下的氧化研究中提出,在升温阶段存在一定程度的解聚和产物的缩聚,因此要想获得高单体产率需要在加热阶段快速升温,而普通的高压釜反应器并不能满足快速升温的要求。
针对上述问题,近年来,各国学者们在木质素氧化解聚方向上提出的新策略包括引入能使反应条件更温和、升温更迅速的非常规活化方法(如微波、机械化学、光催化和电催化等)辅助解聚[53];另外,能提供高温进料并及时将产物分离以避免过度氧化和重聚积碳等副反应的连续性反应方式也越来越多的引起学者的关注。
4.1 非常规活化方法辅助解聚 4.1.1 微波微波照射方法已被证实在许多不同的领域非常有效。它能够大大缩短反应体系的升温时间,加速有机反应,并在某些情况下提高选择性。德国耶拿大学的HOFFMANN等[56]首先研究了微波辐射下1, 3-二烷基咪唑鎓的加热行为,在400 W的微波功率下,离子液体的温度从40升到140 ℃只需约30 s。日本京都大学CHEN等[57]以日本雪松为原料,分别在微波照射和常规加热的条件下对碱溶液CuO-H2O2体系中直接生成香草醛和香草酸的反应进行了研究。在微波条件下,原料在2 min内就从室温被加热至180~200 ℃;还发现在180 ℃微波照射10 min得到香草醛和香草酸的产率是常规加热条件下的近3倍(w = 10.1% vs w = 3.4%)。国内华南理工大学ZHU等[58]比较了微波辅助和不锈钢高压反应釜中FeSO4催化Sigma木质素和有机溶剂木质素解聚,在微波条件下(功率400 W)从25 ℃加热至160 ℃只需4 min,而高压反应釜(功率1 000 W)从25 ℃升温至同样温度需要15 min。浙江大学PAN等[59]在微波照射的条件下以乙腈和水的混合溶液为溶剂测试了14种金属盐在木质素模型化合物的氧化反应中的催化效果,并与常规加热方法进行比较。发现微波照射对木质素模型化合物的氧化降解有促进作用,其中催化效果最好的是CrCl3和MnCl2两种金属盐催化剂。OU YANG[60-62]课题组利用微波强化的手段对碱木质素的氧化过程进行了系统的研究,发现微波可显著增强木质素中β-O-4键的断裂行为,可明显降低氧化剂的用量、反应温度和反应时间。
4.1.2 机械化学这里的机械化学方法主要指球磨或研磨。硫酸盐木质素用KOH和甲苯球磨处理后,引起羰基官能团的显著增多以及其他化学变化[63],该机械化学方法与卟啉催化剂的协同作用使木质素解聚得更彻底,获得了w = 7.8%的香草酸甲酯和w = 2.2%的5-甲酯基香草酸甲酯。DABRAL等[64]在碳化钨(WC)研磨罐中以HO─TEMPO/KBr/Oxone催化氧化β-O-4模型化合物和真实木质素,酚类β-O-4模型化合物发生芳基Cα键裂解反应,形成相应高产率的醌类化合物和愈创木酚;在真实木质素实验中,机械处理导致生物大分子中C─C/C─O键的部分裂解。
4.1.3 光(电)催化光催化氧化技术也被应用于木质素的解聚过程。与热过程相比,光化学反应具有更温和的条件和更短的反应时间,并且不会产生二次污染。TiO2光催化剂因其高活性、化学稳定性、低成本的特点,已成为在木质素催化氧化解聚中最广泛使用的光催化剂,MA等[65]的研究表明通过掺杂贵金属(如Pt)可以显著提高TiO2的光催化能力。近期GONG等[66]就合成了一种新型的Bi/Pt-TiO2催化剂,在室温下光催化反应1 h后,近85%的木质素磺酸盐转化为愈创木酚、香草酸、香草醛、4-苯基-1-丁烯-4-醇和其他中间体。虽然TiO2催化剂在木质素解聚方面表现出优异的性能,但木质素容易与TiO2形成稳定的悬浮体。Ta2O5-IrO2薄膜是一种电催化剂,与TiO2纳米管结合时,液相中的光化学-电化学过程使硫酸盐木质素发生解聚,在365 nm波长和20 mW·cm-2强度的紫外光照射下产生香草醛和香草酸产物[67]。TOLBA等[68]提出使用氧化铱电极氧化木质素的电化学方法,制备了涂有Ti、Ta、Ru和Sn氧化物的氧化铱电极,以100 mg·L-1的纸浆厂木质素为原料,通过UV/vis光谱测试电极的活性。在测试的所有组合中,发现Ti-RuO2-IrO2具有最高的活性。木质素在NaOH中的氧化遵循假一级反应并具有较低的活化能,表明是自由基氧化反应。最近CAI等[69]则以Pb/PbO2作为阳极、Cu/NiMoCo作为阴极,在NaOH溶液中系统研究了玉米秸秆木质素的氧化解聚行为,获得了不俗的结果。
4.2 反应方式木质素氧化解聚研究的反应方式可分为间歇式反应和连续式反应,目前国内外对木质素的催化解聚研究主要采用以高压反应釜为反应容器的间歇反应。如能采用连续性反应方式,将很好地规避间歇反应方式的不足之处:一方面,由于反应器壁的尺寸是为高压应用而设计的,需要较长的加热时间和冷却时间,在研究反应时不可忽视,在此期间,反应器中可能存在完全不同的反应行为,可能会导致错误的结论;另一方面,间歇反应方式无法将生成的解聚产物及时从反应体系中分离出来,导致目标产物的二次反应及重聚现象;再者,木质素解聚转化为高附加值燃料或者化学品要应用到工业中,必然需要从间歇反应过渡到连续性生产过程[29]。
连续性反应方式在木质素解聚研究中并不常见,前期仅有少数文献报导。瑞典学者WERHAN等[51, 70]采用一种连续的两相流动微反应器研究酸性条件下木质素氧化解聚的动力学,在250 ℃下反应相当短时间就可达到文献报道的最大香草醛产率w = 89.3%。波尔图大学的DA SILVA等[71]研究了木质素在连续的气-液对流填料鼓泡塔反应器中生产香草醛的反应,发现氧气在液相中的传质常数可以显著提高(转移到液相中的氧气可增加35%)。最近,基于反应速率的有效控制和产物实时分析的需求,ANDERSON等[72]采用连续反应系统对木质素氢解进行了系统的研究,实现了反应中间产物的快速监测和终产物的实时收集,为木质素研究开辟了新方向。
5 总结木质素在生物质中约15%~30%质量占比和高达40%的能量占比,可以预见木质素生产化学品和燃料将极大地提高整个生物炼制过程的经济性。尽管木质素在自然界中的含量和其特有的结构优势使得其成为部分替代化石燃料等不可再生能源的最佳自然资源之一,但是木质素的回收与增值的市场化,必须满足以下基本条件:(1)开发一种高效、便宜、绿色的解聚方法,(2)产品的分离纯化手段必须有效且具有成本竞争力,(3)使用相对温和的反应条件,以及(4)使用可放大的连续反应过程,并最终在生物炼制中实现产品多样化。
木质素氧化解聚作为木质素解聚一个重要且有前景的方法之一,反应条件相对温和,能显著降低木质素连接键键能,生成高度官能化的芳香族化合物等。但是还有许多研究亟待完善:(1)绝大多数这些方法使用苛刻的反应条件,目标产物的选择性和收率低(一般在w = 5%~30%),产物复杂、单一产物的选择性低,分离提纯难;解聚过程中解聚中间体与解聚产物的重聚问题也不容忽视;(2)当前的许多解聚工艺参数与解聚规律均是以简单模型化合物为研究对象,而木质素分子内部存在多种相互交错的复杂的化学键合方式与立体构型,因此,模型化合物的研究结果与真实体系存在一定的距离;(3)木质素结构中的C─C和C─O键断键规律尚不清晰,因而基于催化解聚调控机制对产物高选择性定向制备比较困难,尚存较大研究空间。
| [1] |
RAGAUSKAS A J, BECKHAM G T, BIDDY M J, et al. Lignin valorization:improving lignin processing in the biorefinery[J]. Science, 2014, 344(6185): 1246843. DOI:10.1126/science.1246843 |
| [2] |
XU C, ARANCON R A D, LABIDI J, et al. Lignin depolymerisation strategies:Towards valuable chemicals and fuels[J]. Chemical Society Reviews, 2014, 43(22): 7485-7500. DOI:10.1039/C4CS00235K |
| [3] |
HUANG Y, DUAN Y J, QIU S, et al. Lignin-first biorefinery:A reusable catalyst for lignin depolymerization and application of lignin oil to jet fuel aromatics and polyurethane feedstock[J]. Sustainable Energy & Fuels, 2018, 2(3): 637-647. |
| [4] |
NARRON R H, KIM H, CHANG H, et al. Biomass pretreatments capable of enabling lignin valorization in a biorefinery process[J]. Current opinion in biotechnology, 2016, 38: 39-46. DOI:10.1016/j.copbio.2015.12.018 |
| [5] |
KEY R E, BOZELL J J. Progress toward lignin valorization via selective catalytic technologies and the tailoring of biosynthetic pathways[J]. ACS Sustainable Chemistry & Engineering, 2016, 4(10): 5123-5135. |
| [6] |
ZAKZESKI J, BRUIJININCX P C A, JONGERIUS A L, et al. The catalytic valorization of lignin for the production of renewable chemicals[J]. Chemical reviews, 2010, 110(6): 3552-3599. DOI:10.1021/cr900354u |
| [7] |
LI C Z, ZHAO X C, WANG A Q, et al. Catalytic transformation of lignin for the production of chemicals and fuels[J]. Chemical Reviews, 2015, 115(21): 11559-11624. DOI:10.1021/acs.chemrev.5b00155 |
| [8] |
VANGEEL T, SCHUTYSER W, RENDERS T, et al. Perspective on lignin oxidation:advances, challenges, and future directions[J]. Topics in Current Chemistry, 2018, 376(4): 30. |
| [9] |
UPTON B M, KASKO A M. Strategies for the conversion of lignin to high-value polymeric materials:Review and perspective[J]. Chemical Reviews, 2015, 116(4): 2275-2306. |
| [10] |
RINALDI R, JASTRZEBSKI R, CLOUGH M T, et al. Paving the way for lignin valorisation:Recent advances in bioengineering, biorefining and catalysis[J]. Angewandte Chemie International Edition, 2016, 55(29): 8164-8215. DOI:10.1002/anie.201510351 |
| [11] |
CHKAR F S, RAGAUSKAS A J. Review of current and future softwood kraft lignin process chemistry[J]. Industrial Crops and Products, 2004, 20(2): 131-141. DOI:10.1016/j.indcrop.2004.04.016 |
| [12] |
TOLEDANO A, SERRANO L, LABIDI J. Organosolv lignin depolymerization with different base catalysts[J]. Journal of Chemical Technology & Biotechnology, 2012, 87(11): 1593-1599. |
| [13] |
JIANG X X, Ellis N, ZHONG Z P. Characterization of pyrolytic lignin extracted from bio-oil[J]. Chinese Journal of Chemical Engineering, 2010, 18(6): 1018-1022. DOI:10.1016/S1004-9541(09)60162-2 |
| [14] |
LI J B, GELLERSTEDT G, TOVEN K. Steam explosion lignins; their extraction, structure and potential as feedstock for biodiesel and chemicals[J]. Bioresource Technology, 2009, 100(9): 2556-2561. DOI:10.1016/j.biortech.2008.12.004 |
| [15] |
BEHLING R, VALANGE S, CHATEL G. Heterogeneous catalytic oxidation for lignin valorization into valuable chemicals:What results? What limitations? What trends?[J]. Green Chemistry, 2016, 18(7): 1839-1854. DOI:10.1039/C5GC03061G |
| [16] |
BRUIJININCX P C A, WECHUYSEN B M. Biomass conversion:lignin up for break-down[J]. Nature Chemistry, 2014, 6(12): 1035. DOI:10.1038/nchem.2120 |
| [17] |
舒日洋, 徐莹, 张琦, 等. 木质素催化解聚的研究进展[J]. 化工学报, 2016, 67(11): 4524-4532. SHU R Y, XU Y, ZHANG Q, et al. Progress in catalytic depolymerization of lignin[J]. CIESC Journal, 2016, 67(11): 4524-4532. |
| [18] |
CHAN M K, YE Q, PENG Z M, et al. Valorization of lignin:effective conversion of depolymerized lignin to oil by simple chemical modifications[J]. Waste and Biomass Valorization, 2017, 8(6): 2029-2036. DOI:10.1007/s12649-016-9737-4 |
| [19] |
PANDEY M P, KIM C S. Lignin depolymerization and conversion:A review of thermochemical methods[J]. Chemical Engineering & Technology, 2011, 34(1): 29-41. |
| [20] |
LASKAR D D, TUCKER M P, CHEN X, et al. Noble-metal catalyzed hydrodeoxygenation of biomass-derived lignin to aromatic hydrocarbons[J]. Green Chemistry, 2014, 16(2): 897-910. DOI:10.1039/c3gc42041h |
| [21] |
ZHAI Y X, LI C, Xu G Y, et al. Depolymerization of lignin via a non-precious Ni-Fe alloy catalyst supported on activated carbon[J]. Green Chemistry, 2017, 19(8): 1895-1903. DOI:10.1039/C7GC00149E |
| [22] |
SCHUTYSER W, KRUGER J S, ROBINSON A M, et al. Revisiting alkaline aerobic lignin oxidation[J]. Green Chemistry, 2018, 20(16): 3828-3844. DOI:10.1039/C8GC00502H |
| [23] |
DAS L, KOLAR P, et al. Heterogeneous catalytic oxidation of lignin into value-added chemicals[J]. Biofuels, 2012, 3(2): 155-166. |
| [24] |
MA R S, GUO M, ZHANG X. Recent advances in oxidative valorization of lignin[J]. Catalysis Today, 2018, 302: 50-60. DOI:10.1016/j.cattod.2017.05.101 |
| [25] |
RAHIMI A, ULBRICH A, COON J J, et al. Formic-acid-induced depolymerization of oxidized lignin to aromatics[J]. Nature, 2014, 515(7526): 249-252. DOI:10.1038/nature13867 |
| [26] |
沈晓骏, 黄攀丽, 文甲龙, 等. 木质素氧化还原解聚研究现状[J]. 化学进展, 2017, 29(1): 162-178. SHEN X J, HUANG P L, WEN J L, et al. Research status of lignin oxidative and reductive depolymerization[J]. Progress in Chemistry, 2017, 29(1): 162-178. |
| [27] |
YUAN Z, EDEN M R. Recent advances in optimal design of thermochemical conversion of biomass to chemicals and liquid fuels[J]. Current Opinion in Chemical Engineering, 2015, 10: 70-76. DOI:10.1016/j.coche.2015.09.002 |
| [28] |
MOTA M I F, LOUREIRO J M, et al. Recovery of vanillin and syringaldehyde from lignin oxidation:A review of separation and purification processes[J]. Separation & Purification Reviews, 2016, 45(3): 227-259. |
| [29] |
TARABANKO V E, TARABANKO N. Catalytic oxidation of lignins into the aromatic aldehydes:General process trends and development prospects[J]. International Journal of Molecular Sciences, 2017, 18(11): 2421. DOI:10.3390/ijms18112421 |
| [30] |
PINTO P C R, DA SILVA E A B, RODRIGUES A E. Biomass conversion[M]. Berlin: Springer, 2012.
|
| [31] |
SCHUTYSER W, RENDERS T, et al. Chemicals from lignin:An interplay of lignocellulose fractionation, depolymerisation, and upgrading[J]. Chemical Society Reviews, 2018, 47(3): 852-908. |
| [32] |
SCHOENHERR S, EBRAHIMI M, CZERMAK P. Lignin-trends and applications[M]. London: IntechOpen, 2018.
|
| [33] |
FACHE M, BOUTEVIN B, CAILLOL S. Vanillin production from lignin and its use as a renewable chemical[J]. ACS Sustainable Chemistry & Engineering, 2015, 4(1): 35-46. |
| [34] |
SALES F G, MARANHAO L C A, LIMA FILHO N M, et al. Kinetic evaluation and modeling of lignin catalytic wet oxidation to selective production of aromatic aldehydes[J]. Industrial & Engineering Chemistry Research, 2006, 45(20): 6627-6631. |
| [35] |
BHARGAVA S, JANI H, TARDIO J, et al. Catalytic wet oxidation of ferulic acid (a model lignin compound) using heterogeneous copper catalysts[J]. Industrial & Engineering Chemistry Research, 2007, 46(25): 8652-8656. |
| [36] |
VILLAR J C, CAPEROS A, et al. Oxidation of hardwood kraft-lignin to phenolic derivatives with oxygen as oxidant[J]. Wood Science and Technology, 2001, 35(3): 245-255. DOI:10.1007/s002260100089 |
| [37] |
DENG W, ZHANG H, WU X, et al. Oxidative conversion of lignin and lignin model compounds catalyzed by CeO 2-supported Pd nanoparticles[J]. Green Chemistry, 2015, 17(11): 5009-5018. DOI:10.1039/C5GC01473E |
| [38] |
DENG H, LIN L, SUN Y, et al. Perovskite-type oxide LaMnO3:An efficient and recyclable heterogeneous catalyst for the wet aerobic oxidation of lignin to aromatic aldehydes[J]. Catalysis Letters, 2008, 126(1/2): 106-111. |
| [39] |
DENG H, LIN L, SUN Y, et al. Activity and stability of perovskite-type oxide LaCoO3 catalyst in lignin catalytic wet oxidation to aromatic aldehydes process[J]. Energy & Fuels, 2008, 23(1): 19-24. |
| [40] |
SHILPY M, EHSAN M A, ALI T H, et al. Performance of cobalt titanate towards H2O2 based catalytic oxidation of lignin model compound[J]. RSC Advances, 2015, 5(97): 79644-79653. DOI:10.1039/C5RA14227J |
| [41] |
VOITL T, RUDOLF VON ROHR P. Oxidation of lignin using aqueous polyoxometalates in the presence of alcohols[J]. ChemSusChem:Chemistry & Sustainability Energy & Materials, 2008, 1(8/9): 763-769. |
| [42] |
GAO T T, ZHOU X F, ZHU Z L. Catalytic conversion of kraft lignin using paper-like Co (salen) as an effective catalyst[J]. Drewno. Prace Naukowe. Doniesienia. Komunikaty, 2015, 58(195): 79-90. |
| [43] |
DEMESA A G, LAARI A, TURENUN I, et al. Alkaline partial wet oxidation of lignin for the production of carboxylic acids[J]. Chemical Engineering & Technology, 2015, 38(12): 2270-2278. |
| [44] |
TARABANKO V E, HENDOGINA Y V, PETUHOV D V, et al. On the role of retroaldol reaction in the process of lignin oxidation into vanillin. Kinetics of the vanillideneacetone cleavage in alkaline media[J]. Reaction Kinetics and Catalysis Letters, 2000, 69(2): 361-368. |
| [45] |
CREIGHTON R H J, GIBBS R D, HIBBERT H. Studies on lignin and related compounds. lxxv. alkaline nitrobenzene oxidation of plant materials and application to taxonomic classification1[J]. Journal of the American Chemical Society, 1944, 66(1): 32-37. DOI:10.1021/ja01229a010 |
| [46] |
DEUSS P J, BARTA K. From models to lignin:Transition metal catalysis for selective bond cleavage reactions[J]. Coordination Chemistry Reviews, 2016, 306: 510-532. DOI:10.1016/j.ccr.2015.02.004 |
| [47] |
XIANG Q, Lee Y Y. Production of oxychemicals from precipitated hardwood lignin[C]//Twenty-Second Symposium on Biotechnology for Fuels and Chemicals. Totowa: Humana Press, 2001: 71-80.
|
| [48] |
WU G X, HEITZ M, CHORNET E. Improved alkaline oxidation process for the production of aldehydes (vanillin and syringaldehyde) from steam-explosion hardwood lignin[J]. Industrial & Engineering Chemistry Research, 1994, 33(3): 718-723. |
| [49] |
WU G X, HEITZ M. Catalytic mechanism of Cu2+ and Fe3+ in alkaline O2 oxidation of lignin[J]. Journal of Wood Chemistry and Technology, 1995, 15(2): 189-202. DOI:10.1080/02773819508009507 |
| [50] |
TARABANKO V E, FOMOVA N A, Kuznetsov B N, et al. On the mechanism of vanillin formation in the catalytic oxidation of lignin with oxygen[J]. Reaction Kinetics and Catalysis Letters, 1995, 55(1): 161-170. |
| [51] |
WERHAN H, MIR J M, VOITL T, et al. Acidic oxidation of kraft lignin into aromatic monomers catalyzed by transition metal salts[J]. Holzforschung, 2011, 65(5): 703-709. |
| [52] |
ZHANG J, LIU Y, CHIBA S, et al. Chemical conversion of β-O-4 lignin linkage models through Cu-catalyzed aerobic amide bond formation[J]. Chemical Communications, 2013, 49(97): 11439-11441. DOI:10.1039/c3cc46912c |
| [53] |
ZAKZESKI J, JONGERIUS A L, WECKHUYSEN B M. Transition metal catalyzed oxidation of Alcell lignin, soda lignin, and lignin model compounds in ionic liquids[J]. Green Chemistry, 2010, 12(7): 1225-1236. DOI:10.1039/c001389g |
| [54] |
SEDAI B, BAKER R T, et al. Comparison of copper and vanadium homogeneous catalysts for aerobic oxidation of lignin models[J]. ACS Catalysis, 2011, 1(7): 794-804. DOI:10.1021/cs200149v |
| [55] |
ZHU Y T, LIU J, LIAO Y H, et al. Degradation of vanillin during lignin valorization under alkaline oxidation[J]. Topics in Current Chemistry, 2018, 376(4): 29. |
| [56] |
HOFFMANN J, NÜCHTER M, ONDRUSCHKA B, et al. Ionic liquids and their heating behaviour during microwave irradiation-A state of the art report and challenge to assessment[J]. Green Chemistry, 2003, 5(3): 296-299. DOI:10.1039/B212533A |
| [57] |
CHEN Q, KANEKO M, KASHIMURA K, et al. Direct production of vanillin from wood particles by copper oxide-peroxide reaction promoted by electric and magnetic fields of microwaves[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(12): 11551-11557. |
| [58] |
ZHU G D, JIN D X, ZHAO L S, et al. Microwave-assisted selective cleavage of CαCβ bond for lignin depolymerization[J]. Fuel Processing Technology, 2017, 161: 155-161. DOI:10.1016/j.fuproc.2017.03.020 |
| [59] |
PAN J Y, FU J, LU X Y. Microwave-assisted oxidative degradation of lignin model compounds with metal salts[J]. Energy & Fuels, 2015, 29(7): 4503-4509. |
| [60] |
OUYANG X P, LIN Z X, DENG Y H, et al. Oxidative degradation of soda lignin assisted by microwave irradiation[J]. Chinese Journal of Chemical Engineering, 2010, 18(4): 695-702. DOI:10.1016/S1004-9541(10)60277-7 |
| [61] |
OUYANG X P, TAN Y D, QIU X Q. Oxidative degradation of lignin for producing monophenolic compounds[J]. Journal of Fuel Chemistry and Technology, 2014, 42(6): 677-682. DOI:10.1016/S1872-5813(14)60030-X |
| [62] |
OUYANG X P, HUANG X, RUAN T, et al. Microwave-assisted oxidative digestion of lignin with hydrogen peroxide for TOC and color removal[J]. Water Science and Technology, 2015, 71(3): 390-396. |
| [63] |
YAO S G, MOBLEY J K, RALPH J, et al. Mechanochemical treatment facilitates two-step oxidative depolymerization of kraft lignin[J]. ACS Sustainable Chemistry & Engineering, 2018, 6(5): 5990-5998. |
| [64] |
DABRAL S, WOTRUBA H, HERNANDEZ J G, et al. Mechanochemical oxidation and cleavage of lignin β-O-4 model compounds and lignin[J]. ACS Sustainable Chemistry & Engineering, 2018, 6(3): 3242-3254. |
| [65] |
MA Y S, Chang C N, Chiang Y P, et al. Photocatalytic degradation of lignin using Pt/TiO2 as the catalyst[J]. Chemosphere, 2008, 71(5): 998-1004. DOI:10.1016/j.chemosphere.2007.10.061 |
| [66] |
GONG J Y, IMBAULT A, FARNOOD R. The promoting role of bismuth for the enhanced photocatalytic oxidation of lignin on Pt-TiO2 under solar light illumination[J]. Applied Catalysis B:Environmental, 2017, 204: 296-303. DOI:10.1016/j.apcatb.2016.11.045 |
| [67] |
TIAN M, WEN J L, MACDONALD D, et al. A novel approach for lignin modification and degradation[J]. Electrochemistry Communications, 2010, 12(4): 527-530. |
| [68] |
TOLBA R, TIAN M, WEN J, et al. Electrochemical oxidation of lignin at IrO2-based oxide electrodes[J]. Journal of Electroanalytical Chemistry, 2010, 649(1/2): 9-15. |
| [69] |
CAI P, FAN H X, CAO S, et al. Electrochemical conversion of corn stover lignin to biomass-based chemicals between Cu/Ni Mo Co cathode and Pb/PbO2 anode in alkali solution[J]. Electrochimica Acta, 2018, 264: 128-139. DOI:10.1016/j.electacta.2018.01.111 |
| [70] |
WERHAN H, ASSMANN N, et al. Lignin oxidation studies in a continuous two-phase flow microreactor[J]. Chemical Engineering and Processing:Process Intensification, 2013, 73: 29-37. DOI:10.1016/j.cep.2013.06.015 |
| [71] |
DA SILVA E A B, ZABKOVA M, ARAÜJO J D, et al. An integrated process to produce vanillin and lignin-based polyurethanes from Kraft lignin[J]. Chemical Engineering Research and Design, 2009, 87(9): 1276-1292. DOI:10.1016/j.cherd.2009.05.008 |
| [72] |
ANDERSON E M, STONE M L, KATAHIRA R, et al. Flowthrough reductive catalytic fractionation of biomass[J]. Joule, 2017, 1(3): 613-622. DOI:10.1016/j.joule.2017.10.004 |




