2. 崇左南方水泥有限公司, 广西 崇左 532200;
3. 广西大学 化学化工学院, 广西 南宁 530004;
4. 广西北投环保水务集团有限公司, 广西 南宁 530004
2. Chongzuo South Cement Co. Ltd., Chongzuo 532200, China;
3. School of Chemistry and Chemical Engineering, Guangxi University, Nanning 530004, China;
4. Guangxi Beitou Environmental Protection Water Group Co. Ltd., Nanning 530004, China
随着工业化的发展,大量重金属直接排放到环境中,对人类健康构成严重威胁[1]。在这些重金属中,Cu(Ⅱ)和Zn(Ⅱ)属于二类重金属污染物,虽然不会直接对人体造成较大的危害,但会对水体中的鱼类和水生植物产生毒害作用,并可通过废水污染在动植物中积累,进而影响生态系统[2]。由于重金属持久性和不可生物降解的性质,去除废水中的重金属污染引起了广泛的关注[3]。吸附法因具有成本低、操作简单和高效的优点,成为一种常用、有效的重金属废水处理技术[4]。然而,在吸附过程中不可避免地会出现一些难以克服的缺点,特别是在解吸过程中,固液分离难等问题阻碍了该技术实现商业化应用。
膨润土(bentonite,BT)比表面积大、产量丰富且经济性强,并且对废水中的重金属离子具有良好的去除性能[5]。但粉末状的膨润土很难从溶液中分离出来,且对环境易造成二次污染和材料浪费。因此有研究将磁性纳米颗粒(Fe3O4 nanoparticles,Fe3O4−MNPs)负载在BT表面,解决材料固液分离和循环利用的问题[6]。然而,若Fe3O4−MNPs与膨润土结合而不进行任何化学修饰,当Fe3O4−MNPs暴露于空气和溶液中时,易发生腐蚀和氧化,导致磁性稳定性降低[7]。同时,未改性的Fe3O4−MNPs由于吸附位点的缺失,不利于磁性复合材料吸附性能的提升。为了解决这些问题,用一些功能性有机物对磁性膨润土(magnetic bentonite,MB)进行改性修饰。壳聚糖(chitosan,CS)是一种亲水、环保的聚阳离子材料,对有机污染物和金属离子具有显著的吸附能力,其结构中含有大量─NH2和─OH等吸附基团[8]。羧甲基纤维素钠(sodium carboxymethyl cellulose,SCMC)是一种具有良好溶解性、成本低和可生物降解性的聚阴离子纤维素,近年来受到越来越多的关注[9]。SCMC与CS通过席夫碱反应,制备了绿色、经济、吸附容量高的复合有机物(SCMC/CS)。SCMC/CS负载在MB表面,可以为MB提供了大量的阴离子活性基团(─COOH、─NH2、─OH),进而与金属阳离子产生络合作用增强了复合材料SC/MB对金属阳离子的专性吸附能力。
在微波合成系统中,通过席夫碱反应制备了SCMC/CS改性磁性膨润土(SC/MB)。将膨润土作为负载Fe3O4−MNPs的载体,然后在磁性膨润土表面负载SCMC/CS,以提高改性膨润土对金属离子的吸附性能和Fe3O4−MNPs的磁饱和稳定性。采用场发射扫描电子显微镜(field emission scanning electron microscope,FE−SEM),透射电镜(transmission electron microscope,TEM),傅里叶变换红外光谱仪(Frustrated total internal reflection,FTIR),X射线衍射仪(X-ray diffraction,XRD),全自动比表面和孔隙分析仪(N2−Brunauer−Emmett−Teller,N2−BET),振动样品磁强计(vibrating sample magnetometer,VSM)研究了SC/MB的表面形貌、基团组成、晶面结构、比表面积和磁分离能力。考虑了影响吸附的主要因素,考察了制备的SC/MB对水溶液中Cu(Ⅱ)和Zn(Ⅱ)的吸附性能和去除机理。本研究可以为黏土材料去除废水中重金属污染的研究提供理论依据。
2 实验 2.1 试剂和仪器主要试剂药品:膨润土,天津光复精细化工研究院,化学纯;壳聚糖,(C6H11NO4)n,脱乙酰度大于95%,黏度为100 ~ 200 mPa·s;羧甲基纤维素钠,[C6H7O2(OH)2CH2COONa]n,黏度为800~1 200 mPa·s,购于阿拉丁化工有限公司,化学纯;FeCl3·6H2O、FeCl2·4H2O、CuCl2、ZnNO3和NH3·H2O来自广东光华化学试剂有限公司,均为分析纯。
主要仪器:原子吸收分光光度计,AA−7000型,日本岛津公司;微波固液相合成/萃取仪,XH−200A型,北京祥鹄科技发展有限公司。
2.2 材料的制备及表征制备MB样品:采用微波共沉淀法制备了Fe3O4−MNPs,将含有FeCl3·6H2O和FeCl2·4H2O(Fe3+和Fe2+物质的量比为n(Fe3+): n(Fe2+)=2:1)的混合溶液添加到含有10 mL NH3·H2O的250 mL圆底烧瓶中,并在60 ℃下在微波装置中搅拌30 min。Fe3O4−MNPs制备成功后,向圆底烧瓶中加入5 g BT,微波60 ℃加热1 h。然后产物经外加磁场分离,并用无水乙醇和去离子水清洗,最终产物在60 ℃的真空烘箱中干燥10 h。研磨后过200目筛,制备得到MB筛样品。
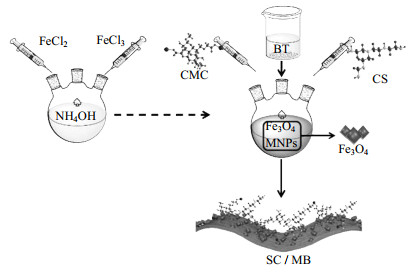
制备SC/MB样品:Fe3O4−MNPs制备方法与MB相同,然后依次向圆底烧瓶中加入20 mL SCMC溶液(质量分数为0.5 %)、20 mL CS溶液(质量分数为0.5 %),加热搅拌10 min后加入5 g BT,微波60 ℃加热搅拌1 h。随后,所得产物经外磁场分离,再用无水乙醇洗涤数次。最终产物在60 ℃的真空烘箱中干燥10 h。MB和SC/MB的制备过程如图 1所示。
|
图 1 SC/MB的合成过程示意图 Fig.1 Schematic illustration of SC/MB synthesis |
采用FE−SEM(日本日立SU8020)和TEM(日本日立JEM−1200)研究了有机改性磁性膨润土的形貌特征。采用FTIR(德国Bruker VERTEX 70)检测材料中的基团组成。在XRD(日本D/max 2500 V)上,用扫描速率为0.05(°)·s−1的Cu kα辐射(λ =0.154 06 nm,θ = 5°~ 80°)测定样品的晶体结构。用N2−BET(美国康塔公司NOVA4200E型)测定样品的孔隙结构;用VSM(美国湖滨温7410)测定吸附剂的磁分离性能。
2.3 吸附实验通过优化pH值(1.0 ~ 7.0)、反应时间(0 ~ 600 min)、Cu(Ⅱ)或Zn(Ⅱ)溶液初始质量浓度(0 ~ 1 000 mg·L−1),考察了MB和SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附效率。在室温下,将0.07 g MB或SC/MB投入50 mL不同浓度的Cu(Ⅱ)或Zn(Ⅱ)溶液中进行振荡吸附,于不同时间取上清液,然后用原子吸收分光光度仪(日本岛津AA−7000)测定溶液中金属离子的质量浓度差异。
Cu(Ⅱ)或Zn(Ⅱ)的吸附容量的计算式为
| $ {{{q}}_{\rm{e}}}{{ = }}({\rho _0} - {\rho _{\rm{e}}}) \times \frac{{{V}}}{{{m}}} $ | (1) |
式中:qe为平衡吸附量,mg·g−1;ρ0和ρe分别为原始状态和平衡状态下Cu(Ⅱ)或Zn(Ⅱ)的质量浓度,mg·L−1;m为吸附剂质量,g;V为液体体积,L。
2.4 吸附模型 2.4.1 吸附等温模型配制一系列质量浓度梯度为0 ~ 1 000 mg·L−1的Cu(Ⅱ)、Zn(Ⅱ)溶液,分别称取0.07 g的MB和SC/MB,分散到50 mL Cu(Ⅱ)或Zn(Ⅱ)溶液中进行吸附等温实验(投加量:1.4 g·L−1,pH = 5),室温条件下在水浴摇床中振荡吸附3 h,达到吸附平衡状态时在外加磁场的作用下固液分离,取上清液测定Cu(Ⅱ)、Zn(Ⅱ)的质量浓度。
采用Langmuir模型和Freundlich模型[10]对MB和SC/MB吸附Cu(Ⅱ)、Zn(Ⅱ)的数据进行等温吸附模型的研究,模型方程如下:
| $ \frac{{{\rho _{\rm{e}}}}}{{{q_{\rm{e}}}}} = \frac{{{\rho _{\rm{e}}}}}{{{q_{\rm{m}}}}} + \frac{1}{{{K_{\rm{L}}}{q_{\rm{m}}}}} $ | (2) |
| $ \ln {q_{\rm{e}}} = \ln {K_{\rm{f}}} + \frac{1}{n}\ln {\rho _{\rm{e}}} $ | (3) |
式中:qm为Langmuir模型的最大吸附容量,mg·g−1;KL为Langmuir模型常数,L·mg−1;Kf为Freundlich模型常数,L·g−1;n为Freundlich吸附常数。
2.4.2 吸附动力学模型配制质量浓度为500 mg·L−1的Cu(Ⅱ)、Zn(Ⅱ)溶液,分别称取0.07 g的MB和SC/MB分散到50 mL的Cu(Ⅱ)或Zn(Ⅱ)溶液中进行吸附动力学实验(投加量:1.4 g·L−1,pH = 5),室温下在水浴摇床中进行振荡吸附,并且在0~360 min的不同时间间隔内,利用外加磁场固液分离取上清液测定Cu(Ⅱ)、Zn(Ⅱ)的浓度。
采用准一级动力学模型、准二级动力学和颗粒内扩散模型[11]对MB和SC/MB吸附Cu(Ⅱ)、Zn(Ⅱ)的数据进行拟合,分别如式(4)、(5)和(6)所示:
| $ {\ln _\;}({q_{\rm{e}}} - {q_t}) = {\ln _\;}{q_{\rm{e}}} - {k_1}t $ | (4) |
| $ \frac{t}{{{q_t}}} = \frac{1}{{{k_2}q_{\rm{e}}^2}} + \frac{t}{{{q_{\rm{e}}}}} $ | (5) |
| $ {q_t} = {K_i}{t^{1/2}} $ | (6) |
式中:qt为t时刻时的吸附量,mg·g−1;k1为一级吸附速率常数,min−1;k2为二级吸附速率常数,g·mg−1·min−1;t为吸附时间,min;Ki为颗粒内扩散常数,mg·g−1·min−1/2。
3 实验结果与讨论 3.1 MB和SC/MB的表征结果 3.1.1 FE-SEM及TEM分析通过FE−SEM和TEM研究了吸附剂的形貌和微观结构,如图 2所示。从FE−SEM图像可以看出,BT表面(图 2(a))相对光滑,而MB(图 2(b))和SC/MB(图 2(c))的表面相对粗糙,部分被颗粒状凸起覆盖。在TEM图像中,颗粒凸起证实为球形Fe3O4−MNPs。特别是从图 2(d)中可以看出,Fe3O4−MNPs具有规则的外观,其尺寸为10~15 nm,且尺寸相对均匀,表明微波共沉淀法成功制备出Fe3O4−MNPs负载在膨润土表面。与图 2(e)中的MB相比,图 2(f)显示SC/MB上的Fe3O4−MNPs被改性剂覆盖,证明SCMC/CS成功地与MB结合。并且在TEM测试之前,材料在超声分散下用无水乙醇反复洗涤。这表明用本方法制备的Fe3O4−MNPs与SCMC/CS层之间结合紧密,SC/MB材料稳定性好,有利于循环利用[12]。

|
图 2 BT, MB和SC/MB的FE−SEM图像以及Fe3O4、MB和SC/MB的TEM图像 Fig.2 FE‒SEM micrographs of bentonite, MB and SC/MB and TEM micrographs of Fe3O4, MB and SC/MB |
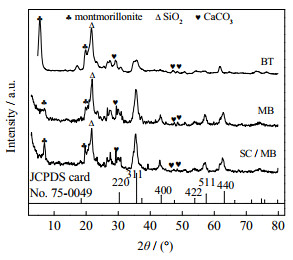
制备材料的XRD图谱如图 3所示。图 3中位于2 θ = 30.1°、35.4°、43.1°、53.4°、57°和62.5°处的衍射峰,分别与(220)、(311)、(400)、(442)、(511)和(440)的晶面相对应,符合Fe3O4的标准卡片(JCPDS 19−0629)。MB和SC/MB的XRD图谱中均出现了Fe3O4的6个特征峰,证明Fe3O4纳米粒子成功地负载在BT上。此外,MB和SC/MB中BT的衍射峰强度远弱于天然BT的特征衍射峰,这是由于MB和SC/MB中Fe3O4纳米粒子的沉积所致[13]。在2θ = 5.8°处的衍射峰属于BT的特征衍射峰[14],表明膨润土经过微波共沉淀负载Fe3O4和SCMC/CS,改性后BT的晶体结构没有被破坏。XRD表征表明,通过微波共沉淀法成功地将Fe3O4纳米粒子负载在膨润土表面,提升了吸附剂的磁分离能力和吸附性能,材料磁分离效果可利用VSM进行佐证。
|
图 3 BT、MB和SC/MB的XRD图谱 Fig.3 XRD patterns of BT, MB and SC/MB |
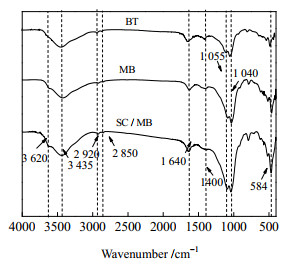
BT、MB和SC/MB样品的FT−IR光谱如图 4所示。在582 cm−1处的典型吸收峰归因于Fe−O拉伸振动[15],证明Fe3O4磁性纳米粒子的存在。3 628和1 038 cm−1的峰可分别归因于膨润土的(Si、Al)−OH拉伸和Si─O─Si拉伸[16]。MB和SC/MB谱线中同时出现了Fe3O4和膨润土的特征峰值,证明磁性膨润土的成功制备。在SC/MB的FTIR谱线中出现了特征峰变化,3 430 cm−1处的衍射峰属于N─H和O─H拉伸振动,在2 920和2 880 cm−1处识别出C─H键[17]。在1 630和1426 cm−1处的衍射峰分别对应于─COOH的不对称和对称拉伸振动峰[18]。表明SCMC/CS负载在MB表面并提供了大量的─NH2,─COOH和─OH活性基团。1 321和1 055 cm−1处的峰与SCMC/CS复合有机物有关,但峰强度很小。这是因为在SC/MB复合材料中,BT占主体地位,而且改性剂CS和SCMC的用量很小,所以形成的峰强度很弱[19]。以上结果表明SCMC/CS对MB进行了成功的改性,负载在SC/MB表面的大量阴离子活性基团提升了对金属阳离子的吸附性能。
|
图 4 BT、MB和SC/MB的FTIR光谱 Fig.4 FTIR spectra of BT, MB and SC/MB |
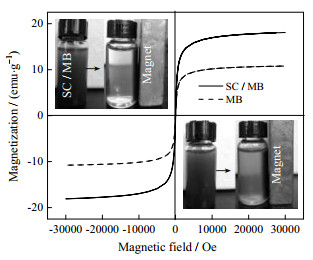
用VSM测量了SC/MB和MB的磁滞回线(如图 5所示),测量的饱和磁化值MS分别为18.1和10.8 emu·g−1。XRD分析表明,SC/MB和MB均呈现出高饱和磁化值,说明Fe3O4纳米粒子成功地赋予了BT磁响应能力。当Fe3O4的添加量相同时,MB的磁饱和强度低于SC/MB。这表明,SCMC/CS层可以提高Fe3O4纳米粒子在环境中的稳定性。此外,在SC/MB和MB分别吸附金属离子后,通过在样品附近放置磁铁来分离吸附剂和溶液(效果见图 5)。结果表明,SC/MB和MB悬浮液都能迅速被磁铁吸引,表现出很高的磁响应能力,在实际应用中具有重要意义。此外,与MB相比,SC/MB悬浮液固液分离速度更快且不产生浑浊,这表明向MB中添加SCMC/CS可降低悬浮液的浊度,使溶液具有更高的透明度。VSM结果显示SC/MB和MB均具有较高的磁饱和强度和超顺磁性,有利于材料的固液分离和循环利用。
|
图 5 SC/MB、MB的磁滞回线以及外加磁场前后SC/MB和MB分离情况 Fig.5 VSM hysteresis loops of MB and SC/MB and magnetic separation of SC/MB and MB after applying external magnetic fields |
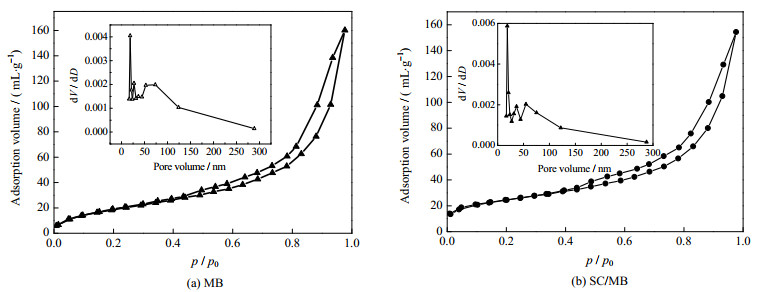
用N2−BET对MB和SC/MB的比表面积、孔容、孔径分布进行分析,结果如表 1所示,测量的比表面积分别为86和74 m2·g−1。MB和SC/MB的吸附脱附曲线和孔径分布如图 6所示,根据国际纯粹与应用化学联合会(IUPAC)等温模型,由压力与饱和蒸气压之比p/p0规律曲线看出,SC/MB和MB均属于Ⅳ型等温线和H3型滞回线,表明这些样品中存在介孔结构[20]。相比于纯的MB,改性后SC/MB比表面积较小,这是因为SCMC/CS负载在SC/MB表面占据了材料表面的孔道结构,导致比表面积减小。但SCMC/CS有机修饰剂提供了大量的活性基团并改善了材料的孔径分布情况,根据孔容随孔径变化率(dV/dD)看出,SCMC/CS的孔容和孔径增大到0.47 cm3·g−1和6.98 nm,更有利于对金属阳离子的吸附。SC/MB具有更多的─COOH、─NH2、─OH基团和更大的孔容和孔径,对金属离子具有更强的吸附性能。
|
|
表 1 MB和SC/MB的N2−BET分析结果 Table 1 N2−BET results of MB and SC/MB |
|
图 6 MB和SC/MB的N2−BET吸附脱附曲线和孔径分布图 Fig.6 Nitrogen adsorption-desorption isotherms and pore size distributions of MB and SC/MB |
以上表征结果表明,以BT为载体、以Fe3O4−MNPs和SCMC/CS为修饰剂的SC/MB复合材料成功制备,在利用外加磁场快速分离吸附剂与溶液方面具有很大的优势,并且针对废水中的金属阳离子具有更强的吸附性能。
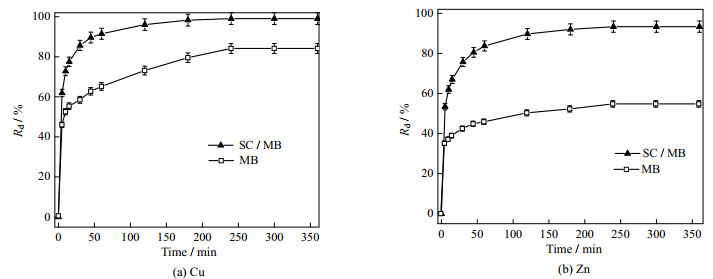
3.2 吸附实验结果 3.2.1 吸附时间对SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的影响考察了接触时间对MB和SC/MB吸附重金属离子的影响,探讨了吸附Cu(Ⅱ)和Zn(Ⅱ)的动力学方程,结果如图 7所示,吸附过程开始是快速的,然后减缓,最后达到吸附平衡。MB在0.5 h内达到平衡吸附,而SC/MB则在1 h内达到平衡吸附,这可能是由于SC/MB表面负载了大量的SCMC/CS,延缓了Cu(Ⅱ)和Zn(Ⅱ)在SC/MB上的扩散速度[21]。3 h的反应时间足以使MB和SC/MB达到平衡,因此,后续的实验设置反应时间为3 h。平衡时SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的去除率Rd分别为99% 和93%,均高于MB对Cu(Ⅱ)和Zn(Ⅱ)的去除效率(83%、55%)。主要是因为SCMC/CS复合有机物为SC/MB提供的─COOH、─NH2、─OH可与Cu(Ⅱ)和Zn(Ⅱ)产生络合和静电吸引作用,进而提升了SC/MB的吸附性能。
|
图 7 吸附时间对MB和SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的影响 Fig.7 Effects of contact time on Cu(Ⅱ) and Zn(Ⅱ) adsorption by MB and SC/MB |
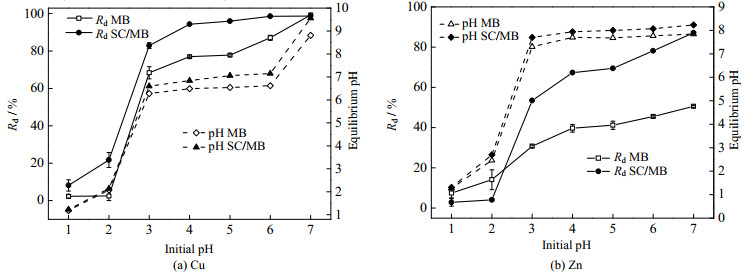
Cu(Ⅱ)和Zn(Ⅱ)溶液pH值对吸附剂的吸附性能起着关键作用,因为它影响复合材料上有机官能团的质子化以及水中金属离子的形态[22]。如图 8所示pH值为1.0~7.0,溶液的初始pH值对SC/MB吸附的影响,表明去除效率与pH值有直接关系,当pH < 2.0时,吸附容量几乎为零。这可能是由于─NH2和─OH在强酸性条件下发生质子化反应(≡MNH2+H+→≡MNH3+,≡MOH+H+→≡MOH2+),金属阳离子和带正电荷吸附剂之间产生静电斥力[23]。随着pH值的增加,SC/MB上的─COOH转变为羧酸阴离子,─NH2发生脱质子化(≡MNH2−H+→≡MNH−),从而提高了整体去除效率。
|
图 8 初始pH值对MB和SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的影响 Fig.8 Effects of initial pH on Cu(Ⅱ) and Zn(Ⅱ) adsorption by MB and SC/MB |
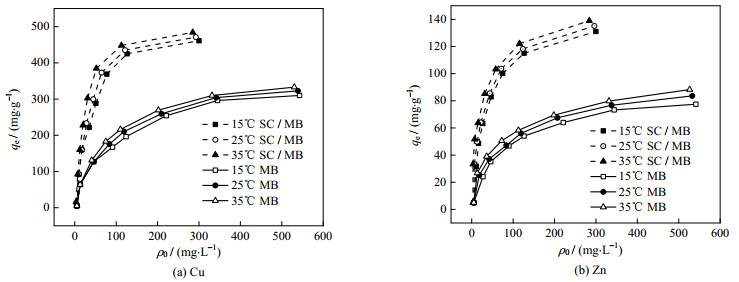
为了进一步研究合成材料的吸附性能,考察了Cu(Ⅱ)和Zn(Ⅱ)溶液初始质量浓度对MB和SC/MB吸附影响。如图 9所示,不同温度下SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的平衡吸附容量qe明显大于MB,表明前者对重金属离子的吸附能力强于后者。这些结果证实了SCMC/CS改性增强了SC/MB对Cu(Ⅱ)、Zn(Ⅱ)的吸附能力,在25 ℃下,拟合出SC/MB和MB去除Cu(Ⅱ)的qe值分别为483、123 mg·g−1;去除Zn(Ⅱ)qe值分别为335、76 mg·g−1。
|
图 9 初始质量浓度对MB和SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的吸附容量 Fig.9 Effects of initial concentration on Cu(Ⅱ) and Zn(Ⅱ) adsorption by MB and SC/MB |
如表 2所示为Langmuir和Freundlich吸附等温模型的拟合参数。从表中的数据可知,在温度θt=15、25、35 ℃时,SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的Langmuir吸附模型拟合相关系数R2 > 0.998,均高于Freundlich模型的相关系数;同时,SC/MB在Langmuir模型中的最大吸附容量qm, cal与实验值qm, exp更为接近,结果表明SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附过程更加符合Langmuir吸附等温模型,且为单分子层吸附[24],MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附也表现出相同的结果。结合Langmuir模型常数KL值可以看出,SC/MB对重金属离子的吸附性能明显高于MB,这说明经过SCMC/CS修饰后,SC/MB的吸附性能得到提升。
|
|
表 2 SC/MB和MB对Cu(Ⅱ)、Zn(Ⅱ)的吸附等温模型参数 Table 2 Fitting parameters of adsorption isotherms models for Cu(Ⅱ) and Zn(Ⅱ) adsorption on MB and SC/MB |
如表 3所示为在室温条件下,SC/MB和MB分别对Cu(Ⅱ)、Zn(Ⅱ)的准一级动力学、准二级动力学和颗粒内扩散模型的拟合参数。表中,K1、K2、K3分别为一、二、三级颗粒内扩散常数,mg·g−1·min−1/2。相较于准一级动力学模型的拟合相关系数而言,准二级动力学模型的相关系数R2更高(R2 = 0.999),且得到的吸附容量qe, cal与实验得到的吸附容量qe, exp更加接近。说明SC/MB和MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附过程更加符合准二级动力学模型,说明吸附过程属于先快速后慢速的过程[25]。根据颗粒内扩散模型的参数结果,可以看出SC/MB和MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附过程分为3个阶段。第1阶段为吸附开始阶段,溶液中大量的Cu(Ⅱ)和Zn(Ⅱ)迅速扩散到SC/MB和MB的表面,被活性吸附位点所吸附;第2阶段为缓慢吸附阶段,当SC/MB和MB的外表面吸附位点被完全占据后,重金属会扩散进入SC/MB和MB的介孔孔道中并被吸附;第3阶段为吸附平衡阶段。
|
|
表 3 SC/MB和MB对Cu(Ⅱ)、Zn(Ⅱ)的吸附动力学模型参数 Table 3 Fitting parameters of adsorption kinetic models for Cu(Ⅱ) and Zn(Ⅱ) adsorption on MB and SC/MB |
室温下,计算出SC/MB和MB去除Cu(Ⅱ)和Zn(Ⅱ)的qm值分别为483、123 mg·g−1和335、76 mg·g−1。与当前研究不同类型的吸附剂相比(如表 4所示),SC/MB复合材料仍具有较好的吸附性能,证SCMC/CS的改性有利于提高对重金属的吸附能力。该吸附剂具有制备方法简单、成本效益高、吸附容量大等优点,可作为工业应用的理想选择。
|
|
表 4 不同吸附剂对Cu(Ⅱ)和Zn(Ⅱ)吸附能力的比较 Table 4 Comparison of adsorption capacities of different adsorbents for Cu(Ⅱ) and Zn(Ⅱ) |
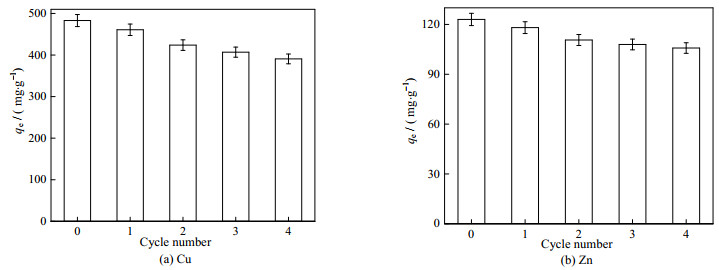
在实际应用中,可重复使用是提高吸附性价比和节约材料的重要因素。如图 10所示,经过4次循环后,SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附性能逐渐降低,吸附性能的下降是每次吸附-解吸循环的步骤中吸附剂活性位点的缺失导致的。此外Cu(Ⅱ)和Zn(Ⅱ)在SC/MB上的一些活性位点可能无法通过无机酸处理的解吸而完全恢复。但其去除能力仍保持在361和106 mg·g−1以上,证明SC/MB具有良好的循环利用性和稳定性,在去除污染水体中的重金属污染领域具有巨大的潜力。
|
图 10 SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的循环利用性能 Fig.10 Recycling performance of SC/MB for Cu(Ⅱ) and Zn(Ⅱ) adsorption |
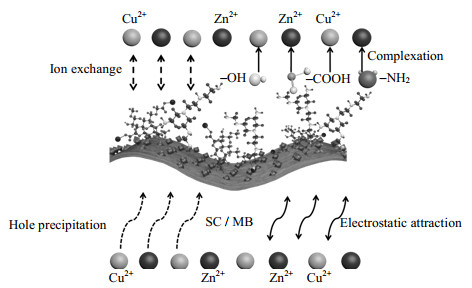
如图 11所示为SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的吸附机理图,通过实验分析和表征结果,推测出SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附机理分别为络合作用、离子交换、微孔固定和静电吸引。(1)络合作用:络合反应是增强SC/MB对Cu(Ⅱ)、Zn(Ⅱ)吸附性能的最主要作用机理,如FTIR表征结果所示,SCMC/CS为SC/MB复合材料提供了丰富的活性基团(─COOH、─NH2、─OH),可以与溶液中的Cu(Ⅱ)和Zn(Ⅱ)产生络合反应将其吸附在SC/MB表面;(2)离子交换:离子交换也对SC/MB吸附Cu(Ⅱ)、Zn(Ⅱ)的过程产生重要影响,SC/MB上大量的Al3+,Ca2+,Na+与溶液中的Cu(Ⅱ)和Mn(Ⅱ)产生阳离子交换作用,增强了SC/MB吸附金属阳离子的能力,SC/MB上可交换吸附点位上的Al3+,Ca2+,Na+等阳离子被溶液中Cu(Ⅱ)和Zn(Ⅱ)置换过程如式(7)所示;(3)微孔固定:根据N2−BET和Fe−SEM结果,SC/MB表面存在大量的介孔结构,Cu(Ⅱ)和Zn(Ⅱ)通过沉积作用成功吸附在SC/MB孔洞结构中,增强了SC/MB的吸附能力;(4)静电吸引:SC/MB表面的阴离子基团OH−、COO−等与金属阳离子Cu2+、Zn2+产生静电吸引作用,进而增强SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附性能。
| $ a{{\rm{G}}^{2 + }} + 2{M^{a + }}({\rm{Bentonite}}) \to 2{M^{a + }} + a{{\rm{G}}^{2 + }}({\rm{Bentonite}}) $ | (7) |
|
图 11 SC/MB吸附Cu(Ⅱ)和Zn(Ⅱ)的吸附机理示意图 Fig.11 Adsorption mechanisms of Cu(Ⅱ) and Zn(Ⅱ) adsorption on SC/MB |
式中:a为可交换离子的化合价数,M为可交换金属离子,G为Cu(Ⅱ)或Zn(Ⅱ)。
4 结论本研究通过简单绿色的方法成功制备羧甲基纤维素和壳聚糖复合改性磁性膨润土(SC/MB)。由于SCMC/CS的修饰作用,SC/MB复合材料比单纯的MB具有更好的磁分离性能以及在低pH溶液中更强的稳定性。同时SCMC/CS提供了大量的阴离子活性基团(─COOH、─NH2、─OH),增强了SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附性能。当温度为(25±1) ℃、pH = 5时,投加1.4 g·L−1的SC/MB吸附Cu(Ⅱ)、Zn(Ⅱ)溶液3 h达到平衡状态,SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的去除率分别为99% 和93%。SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附符合Langmuir模型,Langmuir吸附容量分别为483和123 mg·g−1,吸附为单分子层吸附;吸附过程符合准二级动力学和颗粒内扩散模型,是一个表面迅速吸附,继而缓慢扩散,最后趋于平衡的过程。SC/MB对Cu(Ⅱ)和Zn(Ⅱ)的吸附机理以络合作用为主,同时离子交换、静电吸引和微孔固定作用也具有重要影响。本研究基于简化的制备方法,原料成本低,制备出具有磁分离方便、重复利用性好、效率高等优点的SC/MB复合材料。因此,SC/MB可作为潜在的重金属离子去除材料进行应用,并为黏土材料吸附重金属离子的研究提供参考。
| [1] |
LIU L, LIU J, ZHAO L, et al. Synthesis and characterization of magnetic Fe3O4@CaSiO3 composites and evaluation of their adsorption characteristics for heavy metal ions[J]. Environmental Science and Pollution Research International, 2019, 26: 8721-8736. DOI:10.1007/s11356-019-04352-6 |
| [2] |
JOSEPH I V, TOSHEVA L, DOYLE A M. Simultaneous removal of Cd(Ⅱ), Co(Ⅱ), Cu(Ⅱ), Pb(Ⅱ), and Zn(Ⅱ) ions from aqueous solutions via adsorption on FAU-type zeolites prepared from coal fly ash[J]. Journal of Environmental Chemical Engineering, 2020, 8(4): 103895. DOI:10.1016/j.jece.2020.103895 |
| [3] |
CHITPONG N, HUSSON S M. High-capacity, nanofiber-based ion-exchange membranes for the selective recovery of heavy metals from impaired waters[J]. Separation and Purification Technology, 2017, 179: 94-103. DOI:10.1016/j.seppur.2017.02.009 |
| [4] |
JORGE G F, ALVESl G L V, CATONE S L, et al. Application of pyridine-modified chitosan derivative for simultaneous adsorption of Cu(Ⅱ) and oxyanions of Cr(Ⅵ) from aqueous solution[J]. Journal of Environmental Management, 2021, 282: 111939. DOI:10.1016/j.jenvman.2021.111939 |
| [5] |
林越呈, 王宏鹏, 龚金炎, 等. 改性壳聚糖微球制备及其对阴离子染料的吸附行为研究[J]. 高校化学工程学报, 2017, 31(2): 470-477. LIN Y C, WANG H P, GONG J Y, et al. Preparation of modified chitosan microspheres and their anionic dye adsorption behaviors[J]. Journal of Chemical Engineering of Chinese Universities, 2017, 31(2): 470-477. DOI:10.3969/j.issn.1003-9015.2017.02.029 |
| [6] |
GONZALEZ V, WALLEZ G, CALLIGARO T, et al. Synchrotron-based high angle resolution and high lateral resolution X-ray diffraction: revealing lead white pigment qualities in old masters paintings[J]. Analytical Chemistry, 2017, 89: 13203-13211. DOI:10.1021/acs.analchem.7b02949 |
| [7] |
HUANG S, YU Z, ZHANG Y, et al. In situ green synthesis of antimicrobial carboxymethyl chitosan-nanosilver hybrids with controlled silver release[J]. International Journal of Nanomedicine, 2017, 12: 3181-3191. DOI:10.2147/IJN.S130397 |
| [8] |
张佳勋, 李颖, 胡柏松, 等. 壳聚糖催化正丁醛自缩合反应性能[J]. 高校化学工程学报, 2020, 34(5): 1189-1195. ZHANG J X, LI Y, HU B S, et al. Catalytic performance of chitosan for n-butyraldehyde aldol self-condensation[J]. Journal of Chemical Engineering of Chinese Universities, 2020, 34(5): 1189-1195. DOI:10.3969/j.issn.1003-9015.2020.05.013 |
| [9] |
YU Y, YANG H C, CHOI J, et al. Multi-barrier approach for removing organic micropollutants using mobile water treatment systems[J]. Science of the Total Environment, 2018, 639: 331-338. DOI:10.1016/j.scitotenv.2018.05.079 |
| [10] |
ZHANG H, OMER A M, HU Z, et al. Fabrication of magnetic bentonite/carboxymethyl chitosan/sodium alginate hydrogel beads for Cu (Ⅱ) adsorption[J]. International Journal of Biological Macromolecules, 2019, 135: 490-500. DOI:10.1016/j.ijbiomac.2019.05.185 |
| [11] |
MENG B, GUO Q, MEN X, et al. Modified bentonite by polyhedral oligomeric silsesquioxane and quaternary ammonium salt and adsorption characteristics for dye[J]. Journal of Saudi Chemical Society, 2020, 24: 334-344. DOI:10.1016/j.jscs.2020.01.007 |
| [12] |
FU F L, WANG Q. Removal of heavy metal ions from wastewaters: a review[J]. Journal of Environmental Management, 2011, 92(3): 407-418. DOI:10.1016/j.jenvman.2010.11.011 |
| [13] |
高余良, 朱光明, 马拖拖. Fe3O4磁性纳米粒子及其生物医学应用研究进展[J]. 化工进展, 2017, 36(3): 973-980. GAO Y L, ZHU G M, MA T T. Progress in Fe3O4 magnetic nanoparticles and its application in biomedical fields[J]. Chemical Industry and Engineering Progress, 2017, 36(3): 973-980. |
| [14] |
张寒冰, 张天顺, 唐艳葵, 等. 碱性钙基膨润土对亚甲基蓝和刚果红的吸附去除[J]. 精细化工, 2013, 30(6): 656-660. ZHANG H B, ZHANG T S, TANG Y K, et al. Adsorption of methylene blue and congo red on alkaline Ca-bentonite[J]. Fine Chemicals, 2013, 30(6): 656-660. |
| [15] |
ZHANG H B, TONG Z F, WEI T Y, et al. Sorption characteristics of Pb(Ⅱ) on alkaline Ca-bentonite[J]. Applied Clay Science, 2012, 65/66: 21-23. DOI:10.1016/j.clay.2012.06.010 |
| [16] |
王迎亚, 施华珍, 张寒冰, 等. 磁性柠檬酸膨润土对六价铬吸附性能的研究[J]. 高校化学工程学报, 2017, 31(3): 726-732. WANG Y Y, SHI H Z, ZHANG H B, et al. Research on Cr(Ⅵ) Adsorption with magnetic citric acid bentonite[J]. Journal of Chemical Engineering of Chinese Universities, 2017, 31(3): 726-732. DOI:10.3969/j.issn.1003-9015.2017.03.030 |
| [17] |
朱芳瑶, 常莎, 陈尧, 等. 化学氧化法应急处理甲醛污染饮用水源的工艺研究[J]. 工业水处理, 2018, 38(9): 29-32. ZHU F Y, CHANG S, CHEN Y, et al. Technical studies on the emergency treatment of formaldehyde polluted drinking water by chemical oxidation method[J]. Industrial Water Treatment, 2018, 38(9): 29-32. |
| [18] |
KUMARARJA P, MANJAJAH K M, DATTA S C, et al. Chitosan-g-poly(acrylic acid)-bentonite composite: a potential immobilizing agent of heavy metals in soil[J]. Cellulose, 2018, 25(7): 3985-3999. DOI:10.1007/s10570-018-1828-x |
| [19] |
覃岳隆, 张寒冰, 陈宁华, 等. 乙酸膨润土对孔雀石绿的吸附去除[J]. 化工进展, 2015, 35(3): 944-949. QIN Y L, ZHANG H B, CHEN N H, et al. Malachite green adsorption on acetic acid bentonite[J]. Chemical Industry and Engineering Progress, 2015, 35(3): 944-949. |
| [20] |
PAWR R R, LALHMUNSIAMA, INGOLE P G, et al. Use of activated bentonite-alginate composite beads for efficient removal of toxic Cu2+ and Pb2+ ions from aquatic environment[J]. International Journal of Biological Macromolecules, 2020, 164: 3145-3154. DOI:10.1016/j.ijbiomac.2020.08.130 |
| [21] |
ALI R M, HAMAD H A, HUSSEIN M M, et al. Potential of using green adsorbent of heavy metal removal from aqueous solutions: adsorption kinetics, isotherm, thermodynamic, mechanism and economic analysis[J]. Ecological Engineering, 2016, 91: 317-332. DOI:10.1016/j.ecoleng.2016.03.015 |
| [22] |
LI L, WANG F, SHAO Z, et al. Chitosan and carboxymethyl cellulose-multilayered magnetic fluorescent systems for reversible protein immobilization[J]. Carbohydrate Polymers, 2018, 201: 357-366. DOI:10.1016/j.carbpol.2018.08.088 |
| [23] |
LI Z, WANG L, MENG J, et al. Zeolite-supported nanoscale zero-valent iron: New findings on simultaneous adsorption of Cd(Ⅱ), Pb(Ⅱ), and As(Ⅲ) in aqueous solution and soil[J]. Journal of Hazardous Materials, 2018, 344: 1-11. DOI:10.1016/j.jhazmat.2017.09.036 |
| [24] |
任爽, 孟昭福, 王腾, 等. 阳(阴)离子复配修饰两性磁性膨润土的表面特征差异及对苯酚吸附的影响[J]. 环境科学, 2018, 39(1): 187-194. REN S, MENG Z F, WANG T, et al. Comparison of amphoteric-cationic and amphoteric-anionic modified magnetic bentonites: characterization and sorption capacity of phenol[J]. Environmental Science, 2018, 39(1): 187-194. DOI:10.3969/j.issn.1673-1212.2018.01.042 |
| [25] |
PAWAR R R, GUPTA P, LALHMUNSIAMA, et al. Al-intercalated acid activated bentonite beads for the removal of aqueous phosphate[J]. Science of the Total Environmental, 2016, 572: 1222-1230. DOI:10.1016/j.scitotenv.2016.08.040 |
| [26] |
PARK J H, WANG J J, KIM S H, et al. Recycling of rice straw through pyrolysis and its adsorption behaviors for Cu and Zn ions in aqueous solution[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2017, 533: 330-337. DOI:10.1016/j.colsurfa.2017.08.041 |
| [27] |
CHEN Z, TANG B, NIU Y, et al. Synthesis of silica supported thiosemicarbazide for Cu(Ⅱ) and Zn(Ⅱ) adsorption from ethanol: A comparison with aqueous solution[J]. Fuel, 2021, 286: 119287. DOI:10.1016/j.fuel.2020.119287 |
| [28] |
WANG Y Y, LIU Y X, LU H H, et al. Competitive adsorption of Pb(Ⅱ), Cu(Ⅱ), and Zn(Ⅱ) ions onto hydroxyapatite-biochar nanocomposite in aqueous solutions[J]. Journal of Solid State Chemistry, 2018, 261: 53-61. DOI:10.1016/j.jssc.2018.02.010 |
| [29] |
TOHDEE K, KAEWSICHANN L, ASADULLAH. Enhancement of adsorption efficiency of heavy metal Cu(Ⅱ) and Zn(Ⅱ) onto cationic surfactant modified bentonite[J]. Journal of Environmental Chemical Engineering, 2018, 6(2): 2821-2828. DOI:10.1016/j.jece.2018.04.030 |




