2. 四川省攀西战略矿产资源综合利用协同创新中心, 四川 成都 610059
2. Collaborative Innovation Center of Panxi Strategic Mineral Resources Multi-Purpose Utilization, Chengdu 610059, China
硼是一种用途非常广泛的化工原料,其用途超过300种,玻璃工业、农业用肥和陶瓷工业约占全球硼消费量90%以上。世界硼矿储量约2.1×108 t (B2O3计),其中土耳其、美国、俄罗斯、智利、中国等五国硼矿储量约占世界储量98%以上[1]。我国硼矿数量超过100个,资源遍布14省区,类型以盐湖沉积型和沉积变质型为主,部分以地下卤水和矽卡岩型分布。总体而言,我国硼矿平均品位较低,仅为8.4% B2O3,远低于土耳其和美国硼矿品位(土耳其26% ~ 31%、美国25.3% ~ 31.9%)[2]。
我国蕴藏有丰富的盐湖卤水和地下卤水,除Na+, K+, Ca2+, Mg2+, Cl-, SO42-, CO32-等主要化学成分外,还伴生有Li+, Rb+, Cs+, B3+等多种有益组分。据不完全统计,青藏高原地区已发现的盐湖硼矿产地达113处,硼矿资源量约占全国的50%[3]。四川盆地是地下卤水异常丰富的地区,平落构造地下卤水是四川盆地品质最优异的地下卤水,其H3BO3储量以Ⅰ+ Ⅱ级储量计约2.987×107 t,平落卤水中B3+含量为4.99 g·L-1,是DZ/T0212-2002给出的综合评价指标的80倍,具有非常高的开发价值[4, 5]。国内外卤水资源开发工艺制定多以其特征体系相平衡研究结果为指导[6, 7],因此,开展四川盆地含硼地下卤水相平衡研究具有重要意义。
硼是典型的缺电子原子,成键以共价性为特征,有BO3和BO4两种配位键型。由于其特殊的配位性质,使得硼酸盐以多种硼氧配阴离子形式存在,增加了研究的复杂性[8]。因此,开展含硼体系热力学研究,对于阐明含硼卤水的形成和演化规律特别是制定从天然卤水中提取硼产品的工艺过程具有重要意义。
针对含硼水盐体系,国内外学者开展了部分研究工作。Churikov[9]开展了Na+ (K+) // BO2-, OH--H2O三元体系263 K相平衡研究。高世扬团队针对盐卤硼酸盐相化学关系进行了研究[10, 11]。宋彭生、孙柏等[12]完成了五元体系Li+, Mg2+ // Cl-, SO42-, B4O72--H2O及其相关子体系298 K的相平衡研究。曾英、桑世华等[13, 14]研究了扎布耶盐湖富硼卤水体系相关子体系的相平衡关系。针对四川盆地地下卤水含硼体系,本课题组开展了部分三元、四元、五元体系稳定相平衡研究工作[15~18]。对于本文研究的两个三元体系而言,现有文献报道的为硼酸铷+硼酸镁+水348 K稳定相平衡[19]。因此,本文将展开两个三元体系硼酸钾+硼酸铷+水和硼酸铷+硼酸镁+水323 K稳定相平衡研究,为研究323 K五元、六元等复杂体系提供基础热力学数据,同时为平落卤水中硼、铷等资源的高效开发利用提供数据支撑。
2 实验(材料与方法) 2.1 实验材料与仪器 2.1.1 实验材料K2B4O7·4H2O(成都科龙化工试剂厂,纯度≥ 99.0 %),MgB4O7·9H2O和RbB5O8·4H2O均为实验室合成,纯度均≥ 99.0 %,合成MgB4O7·9H2O和RbB5O8·4H2O的试剂均为优级纯,其他分析用试剂均为基准试剂。去离子水pH ≈ 6.60,κ ≤ 1.5×10-4 S·m-1,使用前煮沸除去CO2。
2.1.2 实验仪器BSA124S型电子分析天平(Sartorius科学仪器(北京)有限公司,精度±0.0002 g);WAY型阿贝折射仪(上海精科,精度±0.0001);HH - 501型超级恒温水浴(常州国华电器有限公司,精度值±0.50 K);HZS - HA型水浴振荡器(哈尔滨市东联电子技术开发有限公司,温度精度值±0.50 K);Optima 5300 V型ICP - OES (PerkinElmer Inc.);DX - 2700型X - ray衍射仪(丹东方圆仪器有限公司)。
2.2 实验方法稳定相平衡的研究采用等温溶解法。具体过程为:从二元体系共饱点开始(即单盐溶解度),梯度加入另一种新盐,在硬质玻璃瓶中配制试液。所配试液置于(323 ±0.5) K恒温水浴振荡器中,不断振荡以达平衡。定期取上层清液,测定其物化性质及组成,组成不变时达到平衡。平衡后,分取湿固渣和液相以分析其化学组成,测定液相物化性质(密度、折光率),同时取平衡固相进行固相鉴定。平衡液相密度采用称量瓶法,折光率采用阿贝折射仪测定。
2.3 分析方法[20~22]总硼浓度:甘露醇存在下的碱量法;Mg2+:EDTA容量法;K+、Rb+:ICP - OES测定。平行测定三次取平均值为最终实验结果。平衡固相组成采用Schreinemakers湿渣法以及X - ray粉晶衍射法联用确定。
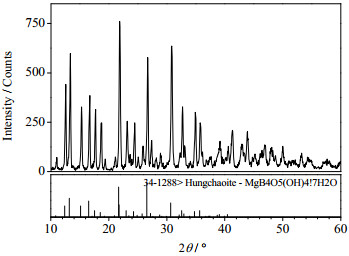
3 实验结果与讨论 3.1 MgB4O7·9H2O和RbB5O8·4H2O的合成 3.1.1 MgB4O7·9H2O的合成采用景燕[23]报道的章氏硼镁石合成方法。以优级纯试剂氧化镁(MgO)、硼酸(H3BO3)为原料,按照质量比m(MgO):m(H3BO3):m(H2O) = 1:8:66称取MgO、H3BO3、H2O混合,298 K下持续搅拌使其充分反应,待溶液由浑浊变澄清后,停止搅拌过滤,滤液在298 K下持续搅拌,出现大量白色沉淀后,过滤,滤饼于298 K下恒温蒸发至恒重。制备得到的章氏硼镁石经化学分析其纯度可达99.0%,可满足本实验研究。制备得到的章氏硼镁石的XRD谱图如图 1所示。
|
图 1 MgB4O7·9H2O的XRD谱图 Fig.1 XRD pattern of MgB4O7·9H2O |
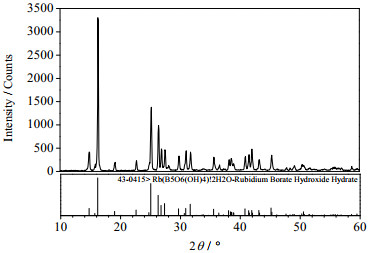
采用本课题组[24]报道的五硼酸铷合成方法。以优级纯试剂碳酸铷(Rb2CO3)、硼酸(H3BO3)为原料,按照质量比m(Rb2CO3): m(H3BO3): m(H2O) = 3:8:32称取Rb2CO3、H3BO3、H2O混合,348 K下持续搅拌使其充分反应,待溶液澄清后,停止搅拌,澄清液于348 K下恒温蒸发结晶,获得晶体348 K下恒温至恒重。制备得到的五硼酸铷经化学分析其纯度可达99.0%,能满足本实验研究。制备得到的五硼酸铷的XRD谱图如图 2所示。
|
图 2 RbB5O8·4H2O的XRD谱图 Fig.2 XRD pattern of RbB5O8·4H2O |
三元体系硼酸钾+硼酸铷+水323 K时溶解度、湿固相组成及溶液物化性质(密度、折光率)等测定结果如表 1所示,溶解度及湿固相组成均采用质量分数表示。由于硼酸盐在水溶液中溶解行为复杂,硼酸根存在多种聚阴离子形式,B4O72-是溶液中各种可能存在的硼酸根离子的综合统计形式。因此,研究中平衡液相中的硼均采用B4O72-形式表示。图 3为该体系323 K稳定相图,图 4为点14处XRD图谱,图 5为共饱点F处XRD图谱。
|
|
表 1 三元体系硼酸钾+硼酸铷+水323 K相平衡组成及液相物化性质数据 Table 1 Solid-liquid equilibrium and physicochemical properties of potassium borate + rubidium borate + H2O at 323 K |
|
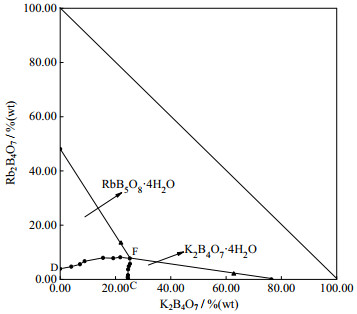
图 3 三元体系硼酸钾+硼酸铷+水323 K相图 Fig.3 Phase diagram of potassium borate + rubidium borate + H2O at 323 K |
|
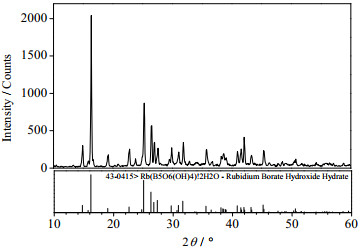
图 4 三元体系硼酸钾+硼酸铷+水323 K点14处平衡固相XRD图谱 Fig.4 XRD pattern of the chemicals at invariant point 14 of potassium borate + rubidium borate + H2O at 323 K |

|
图 5 三元体系硼酸钾+硼酸铷+水323 K共饱点F处平衡固相XRD图谱 Fig.5 XRD pattern of the chemicals at invariant point F of potassium borate + rubidium borate + H2O at 323 K |
由图 3可知,该体系323 K时为简单共饱型,无固溶体或复盐形成。其稳定相图由1个共饱点,2条溶解度单变量曲线和2个结晶区组成。该体系相图有水合盐K2B4O7·4H2O和RbB5O8·4H2O的溶解度曲线CF、DF,且无相应无水盐的溶解度曲线,属水合物相图Ⅰ型。由图 4可知,在该点处硼酸铷结晶形式未发生变化,仍为RbB5O8·4H2O。由图 5及表 1可知,共饱点F对应的固相盐为:K2B4O7·4H2O和RbB5O8·4H2O,液相组成为:K2B4O7 = 25.14%(wt),Rb2B4O7 = 7.73%(wt),H2O = 67.13%(wt)。
氯化物体系中,由于钾、铷离子半径相近,极易形成固溶体[25]。然而,在本文硼酸盐体系中,钾、铷离子共存条件下,并未有固溶体形成。这可能是由于在硼酸盐体系中,虽钾、铷离子半径相近,但其硼酸盐存在形式不同,分别为层状四聚结构B4O5(OH)42-和双环状的五聚结构B5O6(OH)4-,由于结构不同,难以形成固溶体。
高世扬[26]指出,硼酸盐溶液中,五硼和四硼配阴离子可能发生可逆解聚反应:
| $ {{\rm{B}}_{\rm{5}}}{{\rm{O}}_{\rm{6}}}{{\rm{(OH)}}_{\rm{4}}}^ - {\rm{ + B(OH}}{{\rm{)}}_{\rm{4}}}^ - {\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \mathbin{\lower.3ex\hbox{$\buildrel\textstyle\rightarrow\over {\smash{\leftarrow}\vphantom{_{\vbox to.5ex{\vss}}}}$}} {{\rm{B}}_{\rm{4}}}{{\rm{O}}_{\rm{5}}}{{\rm{(OH)}}_{\rm{4}}}^{{\rm{2}} - }{\rm{ + 2B(OH}}{{\rm{)}}_{\rm{3}}} $ | (1) |
本体系中,K2B4O7溶解度远大于Rb2B4O7溶解度,随着溶液中B4O5(OH)42-离子浓度的逐渐较大,上述可逆反应逐步朝着逆反应方向进行,使得溶液中B5O6(OH)4-浓度增大,即随着溶液中K2B4O7含量的增大,Rb2B4O7含量也逐渐增大,表现出增溶作用。同时也由于溶液中B4O5(OH)42-离子浓度较大,使得溶液中B5O6(OH)4-难以朝着正反应方向进行转化,因此溶液中硼酸铷存在形式表现为五硼酸盐形式,而硼酸钾表现为四硼酸钾形式。
由于K2B4O7溶解度远大于Rb2B4O7溶解度,且K2B4O7对Rb2B4O7有较强增溶作用。因此,据表 1数据,以物化性质数据为纵坐标、K2B4O7/%(wt)为横坐标,绘制了密度-组成图(图 6)、折光率-组成图(图 7)。由物化性质-组成图可知,随着溶液中K2B4O7含量的增加物化性质呈现整体增大的趋势,在共饱点F处达到最大值。

|
图 6 三元体系硼酸钾+硼酸铷+水323 K密度-组成图 Fig.6 Density-composition diagram of potassium borate + rubidium borate + H2O at 323 K |

|
图 7 三元体系硼酸钾+硼酸铷+水323 K折光率-组成图 Fig.7 Refractive index-composition diagram of potassium borate + rubidium borate + H2O at 323 K |
三元体系硼酸铷+硼酸镁+水323 K时溶解度、湿固相组成及溶液物化性质(密度、折光率)等测定结果见表 2,溶解度及湿固相组成均采用质量分数表示。图 8为该体系323 K稳定相图,图 9为图 8的局部放大图,图 10为点25处XRD图谱。图 11为共饱点E处XRD图谱。图 12、图 13分别为密度-组成图、折光率-组成图。
|
|
表 2 三元体系硼酸铷+硼酸镁+水323 K相平衡组成及液相物化性质数据 Table 2 Solid - liquid equilibrium and physicochemical properties of rubidium borate + magnesium borate + H2O at 323 K |

|
图 8 三元体系硼酸铷+硼酸镁+水323 K相图 Fig.8 Phase diagram of rubidium borate + magnesium borate + H2O at 323 K |

|
图 10 三元体系硼酸铷+硼酸镁+水323 K点25处平衡固相XRD图谱 Fig.10 XRD pattern of the chemicals at invariant point 25 of rubidium borate + magnesium borate + H2O at 323 K |

|
图 11 三元体系硼酸铷+硼酸镁+水323 K共饱点E处平衡固相XRD图谱 Fig.11 XRD pattern of the chemicals at invariant point E of rubidium borate + magnesium borate + H2O at 323 K |
|
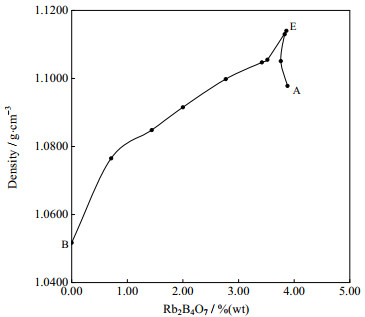
图 12 三元体系硼酸铷+硼酸镁+水323 K密度-组成图 Fig.12 Density-composition diagram of rubidium borate + magnesium borate + H2O at 323 K |

|
图 13 三元体系硼酸铷+硼酸镁+水323 K折光率-组成图 Fig.13 Refractive index-composition diagram of rubidium borate + magnesium borate + H2O at 323 K |
由图 8及图 9可知,该体系323 K相图存在水合盐RbB5O8·4H2O和MgB4O7·9H2O的溶解度曲线AE、BE,且无相应无水盐的溶解度曲线,属水合物相图Ⅰ型。同时由图 10可知,在该点处硼酸镁结晶形式未发生变化,仍为MgB4O7·9H2O。该三元体系稳定相图由1个共饱点,2条溶解度单变量曲线和2个结晶区组成。共饱点E对应的液相组成为:Rb2B4O7 = 3.86%(wt),MgB4O7 = 0.38%(wt),H2O = 95.76%(wt);经X-ray粉晶衍射法可知(图 11),其平衡固相盐分别以四聚结构[MgB4O5(OH)4·7H2O]和五聚结构的[RbB5O6(OH)4·2H2O]形式存在。
对比323 K和348 K[19]相图发现,二者相图构型一致,且盐类结晶形式未发生变化。随着温度升高,盐类结晶区域发生改变,RbB5O6(OH)4·2H2O结晶区增大,MgB4O5(OH)4·7H2O结晶区减小。
由图 12、图 13可知,随溶液中Rb2B4O7含量的增加,物化性质数据逐渐增大,并在共饱点E处达到最大值。
4 结论(1) 采用等温溶解平衡法研究了323 K下三元体系硼酸钾+硼酸铷+水和硼酸铷+硼酸镁+水的相平衡关系,获得了两个体系平衡时各组分的溶解度和平衡液相密度、折光率,根据溶解度数据和固相组成绘制了三元体系相图、密度-组成图、折光率-组成图。
(2) 三元体系硼酸钾+硼酸铷+水323 K时为简单共饱和型,其相图由1个共饱点,2条单变量曲线和2个结晶区组成,2个结晶区对应K2B4O7·4H2O和RbB5O8·4H2O。
(3) 三元体系硼酸铷+硼酸镁+水323 K时为简单共饱和型,其相图由1个共饱点,2条单变量曲线和2个结晶区组成,2个结晶区对应MgB4O7·9H2O和RbB5O8·4H2O。
(4) 对比三元体系硼酸铷+硼酸镁+水323 K和348 K相图发现,盐类结晶形式未发生变化。随着温度升高,RbB5O8·4H2O结晶区增大,MgB4O7·9H2O结晶区减小。
| [1] | USGS. Mineral commodity summaries 2014[R]. Washington: U. S. Department of the Inerior, U. S. Geological Survey. 2014. |
| [2] | Crangle R D. 2011 Minerals yearbook Boron[R]. Washington: U. S. Department of the Inerior, U. S. Geological Survey. 2013. |
| [3] | LIN Yong-jie(林勇杰), ZHENG Mian-ping(郑绵平), LIU Xi-fang(刘喜方). Boron resource of salt lakes in Qinghai-Tibet Plateau(青藏高原盐湖硼矿资源)[J]. Science & Technology Review(科技导报) , 2017, 35(12): 77-82. |
| [4] | LI Wu(李武), DONG Ya-ping(董亚萍), SONG Peng-sheng(宋彭生), et al. The development and utilization of salt lake brine resource(盐湖卤水资源开发利用)[M].Beijing(北京): Chemical Industry Press(化学工业出版社), 2012. |
| [5] | Ministry of Land and Resources of the People’s Republic of China (中华人民共和国国土资源部). Specifications for salt-lake, salt mineral exploration (盐湖和盐类矿产资质勘查规范): DZ/T 0212-2002 [S]. Beijing (北京): Geological Publishing House (地质出版社), 2003. |
| [6] | LIAO Ling(廖玲), HUANG Xue-li(黄雪莉), SONG Huan(宋欢). Phase equilibria of a Na+, K+//Cl-, SO42-, NO3--H2O quinary system at 258.15 K(258.15 K下五元体系Na+, K+//Cl-, SO42-, NO3--H2O相平衡研究)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2016, 30(1): 7-12. |
| [7] | WANG Shuo(王硕), ZHAO Bin(赵斌), GUO Hong-fei(郭宏飞), et al. Solid-liquid equilibrium of the NH4Cl-MgCl2-KCl-H2O system at 0℃ and its application(0℃时NH4Cl-MgCl2-KCl-H2O四元体系相平衡研究及应用)[J]. Journal of Chemical Engineering of Chinese Universities(高校化学工程学报) , 2017, 31(3): 515-520. |
| [8] | LI Jun(李军), GAO Shi-yang(高世扬). Chemistry of borates(硼酸盐化学)[J]. Journal of salt lake research(盐湖研究) , 1993, 1(3): 62-67. |
| [9] | Churikov A V, Zapsis K V, Khramkov V V, et al. Phase diagrams of the ternary systems NaBH4 + NaOH + H2O, KBH4 + NaOH + H2O, NaBO2 + NaOH + H2O, KBO2+ NaOH + H2O at -10℃[J]. Journal of Chemical & Engineering Data , 2011, 56(1): 9-13. |
| [10] | Zhu L X, Yue T, Gao S Y, et al. Thermochemistry of hydrated rubidium teraborate[J]. Thermochimica. Acta , 2003, 101(1-2): 259-263. |
| [11] | Zhu L X, Gao S Y, Xia S P. Phase diagram of thermodynamic non-equilibrium state of MgO-B2O3-18% MgCl2-H2O system at 0℃[J]. Indian Journal of Chemistry , 2003, 42A(1): 35-41. |
| [12] | SUN Bai(孙柏), SONG Peng-sheng(宋彭生), DU Xian-hui(杜宪惠). Phase equilibrium of salt lake brine system Li+, Mg2+//Cl-, SO42-, borate-H2O(盐湖卤水体系Li+, Mg2+//Cl-, SO42-, borate-H2O的研究)[J]. Journal of salt lake research(盐湖研究) , 1994, 2(4): 26-30. |
| [13] | Wang R L, Zeng Y. Metastable phase equilibrium of the quinary aqueous system Li+ + K++ Cl-+ CO32- + B4O72- + H2O at 273.15 K[J]. Journal of Chemical & Engineering Data , 2014, 59(3): 903-911. |
| [14] | Sang S H, Zhang X, Zeng X X, et al. Solid-liquid equilibria in the quinary Na+, K+//Cl-, SO42-, B4O72--H2O system at 298 K[J]. Chinese Journal of Chemistry , 2011, 29(6): 1285-1289. DOI:10.1002/cjoc.201190238. |
| [15] | Yu X D, Luo Y L, Wu L T, et al. Solid-liquid equilibrium on the reciprocal aqueous quaternary system Li+, Mg2+//Cl-, and borate-H2O at 323 K[J]. Journal of Chemical & Engineering Data , 2016, 61(9): 3311-3316. |
| [16] | Zeng Y, Xie G, Wang C, et al. Stable phase equilibrium in the aqueous quaternary system Rb+, Mg2+//Cl-, borate-H2O at 323 K[J]. Journal of Chemical & Engineering Data , 2016, 61(7): 2419-2425. |
| [17] | Guo S S, Yu X D, Zeng Y. Phase equilibria for the aqueous reciprocal quaternary system K+, Mg2+//Cl-, borate-H2O at 298 K[J]. Journal of Chemical & Engineering Data , 2016, 61(4): 1566-1572. |
| [18] | Yu X D, Zeng Y, Guo S S, et al. Stable phase equilibrium and phase diagram of the quinary system Li+, K+, Rb+, Mg2+//borate-H2O at T=348.15 K[J]. Journal of Chemical & Engineering Data , 2016, 61(3): 1246-1253. |
| [19] | ZHANG Yu-juan(张玉娟), ZENG Ying(曾英), YU Xu-dong(于旭东), et al. Study on phase equilibrium of ternary system Rb+, Mg2+//borate-H2O at 348 K(三元体系Rb+, Mg2+//borate-H2O 348 K相平衡研究)[J]. Highlights of Sciencepaper Online(中国科技论文在线精品论文) , 2013, 6(7): 673-678. |
| [20] | Institute of Qinghai Salt-Lake of Chinese Academy of Sciences (中国科学院青海盐湖研究所). Analytical methods of brines and salts(卤水和盐的分析方法)[M].2nd ed.Beijing(北京): Chinese Science Press(科学出版社), 1988. |
| [21] | SHANG Chuan-sheng(尚传胜), AN Lian-ying(安莲英), HU Zi-wen(胡子文). ICP-OES determination of rubidium in bitter(电感耦合等离子体发射光谱法测定卤水中铷)[J]. Chemical Research and Application(化学研究与应用) , 2012, 24(4): 642-645. |
| [22] | Fosbol P L, Thomsen K, Stenby E H. Reverse schreinemakers method for experimental analysis of mixed-solvent electrolyte systems[J]. Journal of Solution Chemistry , 2009, 38(1): 1-14. DOI:10.1007/s10953-008-9353-4. |
| [23] | JING Yan(景燕). A new synthesis method for magnesium borate(合成章氏硼镁石的新方法)[J]. Sea-Lake Salt & Chemical Industry(海湖盐与化工) , 2000, 29(2): 24-25. |
| [24] | ZENG Ying (曾英), YU Xu-dong (于旭东), LIU Ling-li (刘玲利), et al. Method for preparation rubidium pentaborate tetrahydrate(五硼酸铷的制备方法): CN 103172078 A[P]. 2013-06-26. |
| [25] | Yu X D, Zeng Y, Yin Q H, et al. The solubilities, densities, and refractive indices of the ternary systems KCl + RbCl + H2O and KCl + MgCl2 + H2O at 348.15 K[J]. Journal of Chemical & Engineering Data , 2012, 57(12): 3658-3663. |
| [26] | GAO Shi-yang(高世扬), JIA Yong-zhong(贾永忠), XIA Shu-ping(夏树屏), et al. Chemistry of borate in salt lake brine XXX. the existed form of polyborate anion and interaction among them in solution(盐卤硼酸盐化学XXX.含硼水溶液中硼氧配阴离子存在形式及其相互作用)[J]. Journal of Shaanxi Normal University (Natural Science Edition)(陕西师范大学学报(自然科学版)) , 2000, 28(3): 70-78. |





