NOx是燃煤电厂的主要烟气污染物之一。目前,最广泛应用的燃煤电站烟气脱硝技术是选择性催化还原法(SCR)[1],通过加入还原剂NH3,在催化剂的催化作用下将NOx转化为N2;且SCR脱硝装置大多布置在省煤器与空预器之间(高尘布置方式)。作为SCR核心的催化剂,商业中广泛采用的是V2O5-WO3 (或MoO3)/TiO2催化剂[2, 3],其中的钒氧化物是主要催化活性组分,它不仅能催化脱硝反应,同时还会将烟气中的部分SO2催化氧化为SO3[4, 5]并随烟气进入后续设备。此外,还原剂NH3在SCR脱硝设备中无法全部与NOx反应,未反应部分NH3 (逃逸氨)会随烟气进入到空预器中,并与SO3、H2O发生以下反应,生成(NH4)2SO4、NH4HSO4等硫酸铵盐。
| $ {\rm{N}}{{\rm{H}}_{\rm{3}}}{\rm{ + S}}{{\rm{O}}_{\rm{3}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{ N}}{{\rm{H}}_{\rm{4}}}{\rm{HS}}{{\rm{O}}_{\rm{4}}} $ | (1) |
| $ {\rm{2N}}{{\rm{H}}_{\rm{3}}}{\rm{ + S}}{{\rm{O}}_{\rm{3}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\left( {{\rm{N}}{{\rm{H}}_{\rm{4}}}} \right)_{\rm{2}}}{\rm{S}}{{\rm{O}}_{\rm{4}}} $ | (2) |
而空预器的中低温段区域的温度范围正好处于硫酸铵盐的凝结温度区间,在此区间内硫酸铵盐会大量凝结生成,其中黏性的NH4HSO4是导致空预器堵塞的主要原因之一[6~8]。
关于NH4HSO4的形成已有部分研究。Saleem等[9]研究表明NH4HSO4与(NH4)2SO4两种铵盐的形成取决于温度和反应物体积分数。Radian公司建立了空预器中NH4HSO4生成的动力学方程[10],并定性说明了NH4HSO4的形成与温度和反应物体积分数呈正相关。之后Matsuda[11]、Wei[12]、Menasha[13]和马双忱[14]通过实验方法不断缩小了NH4HSO4形成温度区间,但在某些反应物浓度下不同研究者所得到的NH4HSO4形成温度仍相差很大,且缺少针对国内常见SO3浓度下NH4HSO4形成温度的研究。而国内的研究主要关注NH4HSO4造成的空预器堵塞问题及其防治措施,但对空预器中NH4HSO4的形成特性还缺乏详尽认识。马大卫等[15]通过对垢样与飞灰的成分分析发现,空预器结垢主要是由黏性的NH4HSO4造成,并提出通过定期喷氨优化解决;刘海啸[16]通过分析氨逃逸导致的空预器堵塞问题,提出采用空预器在线升温的办法进行防治。此外,有关SCR脱硝造成细颗粒物物性变化的研究也在近几年逐渐展开。李振[17]对比两家典型燃煤电厂SCR脱硝系统前后的测试结果发现,脱硝后粒径大小为0.1~1 μm的细颗粒明显增多,且随喷氨量的增加而增加,并估计燃煤电厂安装SCR脱硝装置都会导致一次PM2.5排放量增长,表明只要脱硝反应存在,就可能对电厂PM2.5排放产生影响[18]。同时,张玉华,史雅娟[19~21]等针对商用V2O5-WO3/TiO2催化剂,开展了脱硝前后PM2.5物性变化的试验室研究并发现,经SCR脱硝后,亚微米级细颗粒数量浓度(颗粒个数/标准立方米烟气)明显上升,且形貌特征及元素组成发生了变化,形成的细颗粒主要为硫酸铵盐,形成量与NH3、SO2、O2、H2O浓度及运行温度有关。束航等[22, 23]通过原位红外试验证明烟气中的NH3能同时参与硫酸铵盐生成与脱硝反应。但已有研究主要针对SCR脱销反应器中的细颗粒物变化,对空预器中NH4HSO4生成对颗粒物排放特性的影响缺乏关注。因此,充分了解空预器中NH4HSO4的形成特性及其对颗粒物排放特性的影响具有重要意义。
研究通过自制模拟空预器试验平台,探究了NH4HSO4的生成对颗粒物排放造成的影响,进一步确定试验气氛下NH4HSO4的形成温度并与已有研究进行对比。
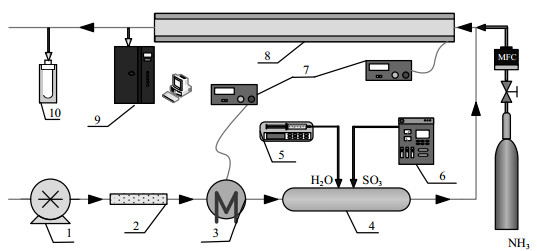
2 试验系统与方法 2.1 实验装置模拟空预器试验平台如图 1所示,主要由气体配制系统、空预器模拟系统及测量系统组成。反应气体由NH3/N2钢瓶气、空气、SO3和水蒸气组成。模拟气体各组分体积分数分别为φ(NH3) = (2~10)× 10-6,φ(SO3) = (20~75)×10-6,φ(H2O) = 0.08,洁净空气作平衡气,反应气体总流量为3 m3·h-1。SO3由SO3发生装置利用催化剂催化氧化SO2产生,并经伴热管线加热后进入静态混合器出口端。水蒸气则通过微量注射泵将去离子水注入加热管路中气化来实现。NH3于模拟空预器入口处加入。
|
图 1 试验系统示意图 Fig.1 Schematic diagram of the experimental setup 1. blower 2. purifier 3. pre-heater 4. mixer 5. micro-injection pump 6. SO3 generation 7. temperature controller 8. simulated air pre-heater 9. ELPI 10. particle |
模拟空预器的主体是一个尺寸为0.65 cm×2.58 cm×100 cm的扁平通道。通道的上下表面为碳钢材质并铺设加热带及14个热电偶。左右两侧表面采用透明石英玻璃并利用高温密封胶进行密封,可观察玻璃上是否有颗粒物沉积。
2.2 试验方法试验前期先针对模拟空预器通道进行温度与通道长度关系的校准。向模拟空预器中通入总流量为3 m3·h-1的洁净空气并进行加热使空预器入口处温度达到320℃,同时记录布设的14个热电偶对应温度,由此得到模拟空预器的通道长度与温度的关系曲线。正式试验时,首先通过观察模拟空预器两侧玻璃窗口上是否有颗粒物沉积确定NH4HSO4的形成位置,进一步利用通道长度与温度的关系曲线来确定NH4HSO4的形成温度。文中描述的NH4HSO4形成温度是指在模拟空预器壁面上最早形成沉积时所对应的温度。
细颗粒物浓度及粒径分布利用芬兰Dekati公司生产的电称低压冲击器(electrical low pressure impactor,ELPI)进行实时在线监测,同时需要采样枪、旋风分离器、稀释器、真空泵等相关辅助设备。颗粒物样品由芬兰Dekati公司生产的PM10/PM2.5采样器进行采集,并利用分光光度法与离子色谱对采集到的样品分别进行NH4+与SO42-的离子测试。
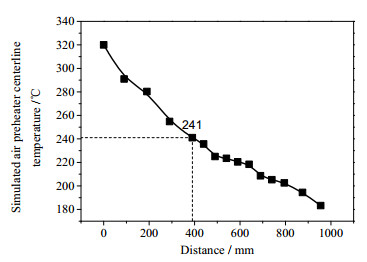
3 结果与讨论 3.1 NH4HSO4形成温度的研究图 2为φ(NH3) = 2×10-6、φ(SO3) = 50×10-6时的NH4HSO4生成情况,其中上图为未开始试验时观察窗口的情况,下图为试验开始后观察窗口的变化。从图中可以对比发现,当试验开始后,于标识处观察到一条白色颗粒状固体的沉积带。图 3为当空预器入口达到320℃,φ(NH3) = 2×10-6、φ(SO3) = 50×10-6时NH4HSO4的形成温度与热电偶到空预器入口的距离之间的关系。试验时,首先在第四个热电偶所对应的2#观察窗口的中段观察到有白色沉积出现,此位置距空预器入口39 cm,并由此得到该浓度下NH4HSO4的形成温度为241℃。

|
图 2 硫酸氢铵试验生成情况 Fig.2 Formation of ammonium bisulfate (ABS) |
|
图 3 φ(NH3) = 2×10-6、φ(SO3) = 50×10-6时的硫酸氢铵形成温度 Fig.3 ABS formation temperatures under conditions of φ(NH3) = 2×10-6, φ(SO3) = 50×10-6 |
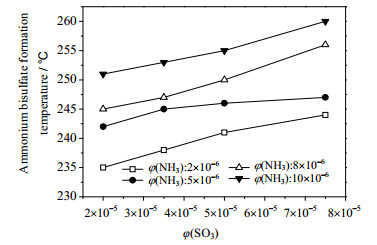
图 4为不同NH3、SO3浓度下NH4HSO4的形成温度,为保证生成物为NH4HSO4而使NH3和SO3物质的量之比小于1。根据Saleem[9]的研究,在试验气氛条件下,生成物只可能是NH4HSO4而不会有(NH4)2SO4产生。
|
图 4 不同NH3和SO3浓度时硫酸氢铵的形成温度 Fig.4 ABS formation temperatures under different NH3 and SO3 concentrations |
从图 4可观察到,NH4HSO4的形成温度在235~260℃,且与烟气中NH3、SO3浓度有着直接关联,随着NH3、SO3浓度的增大而升高。此外,从图 4还可发现,NH3浓度对NH4HSO4形成温度的影响比SO3浓度的影响更加明显。当φ(NH3)固定时(如2×10-6、8×10-6、10×10-6),增加φ(SO3),NH4HSO4的形成温度最大可升高9℃;而当φ(SO3)固定(如20×10-6、75×10-6)时,增加φ(NH3),NH4HSO4的形成温度最大可升高16℃。这可能是因为试验气氛中SO3一直处于过量的状态,从化学平衡角度来看,增加SO3浓度对反应的促进效果并没有增加NH3浓度明显。
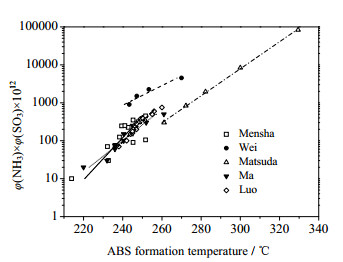
图 5综合了四个团队[11~14]对NH4HSO4形成温度与反应物浓度乘积之间关系的研究结果,并与本文结果进行了对比。表 1为对五组数据拟合后得到的函数关系。综合图 5和表 1可知,NH4HSO4的形成温度与两种反应物浓度乘积的对数值呈正相关的函数关系,NH3和SO3浓度乘积越大,NH4HSO4的形成温度越高,但具体的形成温度仍取决于两种反应物的具体浓度。
|
图 5 硫酸氢铵形成曲线 Fig.5 ABS formation profiles under different conditions |
|
|
表 1 NH4HSO4形成曲线拟合结果 Table 1 Fitting results of NH4HSO4 formation process |
试验工况:模拟空预器的入口温度320℃,φ(NH3) = 2×10-6、5×10--6、8×10-6、10×10-6,φ(SO3) = 50×10-6。
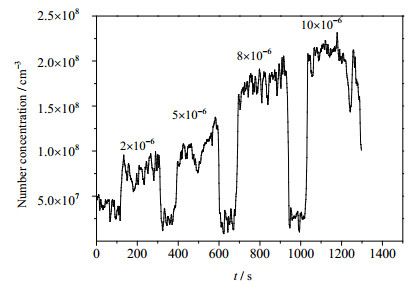
NH3对模拟空预器出口颗粒物数量浓度的影响如图 6所示。从图 6中可以观察到,φ(NH3)从2×10-6升至5×10-6时,模拟空预器出口的颗粒物数量浓度有小幅度上升,数量浓度均值从7.79×107上升至1.03×108个·cm-3,增加了31.8%。当NH3浓度继续增加,达8×10-6时,颗粒物数量浓度有大幅度的提高,均值增加到1.76×108个·cm-3,升高了71.6%,而继续提高NH3浓度,颗粒物数量浓度虽有提高但幅度不大,仅增加了18.1%。这可能是由于反应气体中生成的NH4HSO4在经过模拟空预器通道的降温之后会凝结成固态颗粒物,而NH3作为生成NH4HSO4的主要反应物之一,提高NH3浓度能促使更多的NH4HSO4生成,导致模拟空预器出口处产生更多的由NH4HSO4凝结而成的固态颗粒物,使测得的数量浓度升高。
|
图 6 NH3浓度对空预器出口颗粒物数量浓度的影响 Fig.6 Effects of NH3 concentrations on particle number concentration in air preheater |
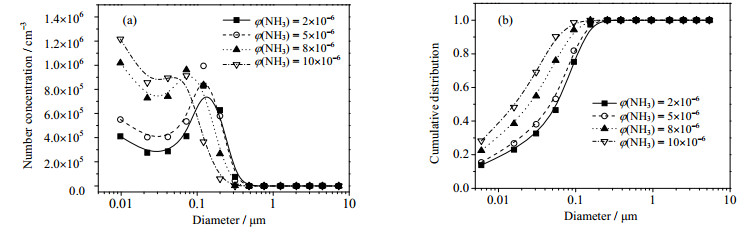
图 7为NH3对模拟空预器出口颗粒物粒径分布的影响。结果表明,所测到的颗粒物粒径基本都小于0.3 μm,特别是从图 7(a)中可以发现,细颗粒物的粒径分布大致呈双峰分布,两个波峰分别位于0.01与0.1 μm。一般而言,颗粒物呈三模态分布,即粒径小于0.2 μm的超细模态、粒径在0.2~3 μm的中间模态和粒径大于3 μm的粗模态,其中超细模态的颗粒物是由气化-凝结机理形成的[24]。从图 7(a)与(b)可以看出,当NH3浓度增大,粒径小于0.1 μm的颗粒物数量浓度明显升高,且占比均在70%以上,结合张玉华[20]的研究结果可以判断,模拟空预器出口处因NH4HSO4的形成而增加的细颗粒物主要为粒径小于0.2 μm的超细模态颗粒物。因此,NH4HSO4应该是先于气相中通过化学反应形成气溶胶,之后凝结于空预器壁面上。
|
图 7 NH3浓度对空预器出口颗粒物粒径的影响 Fig.7 Effects of NH3 concentrations on particle diameter distribution |
此外,从图 7(a)中还能发现,当φ(NH3)从5×10-6升至8×10-6时,图 7(a)中的曲线出现较大变化,粒径小于0.1 μm的颗粒物的数量浓度迅速升高,特别是粒径为0.01 μm的颗粒物,其数量浓度从5.49×105升至1.01×106个·cm-3,甚至超过了其他粒径的颗粒物数量。由于NH3作为NH4HSO4生成的主要反应物之一,在电厂实际中,应采取例如优化喷氨等措施,保证空预器入口处逃逸氨浓度低于φ(NH3) = 5×10-6,从而尽量减少空预器中可能生成的二次颗粒物。
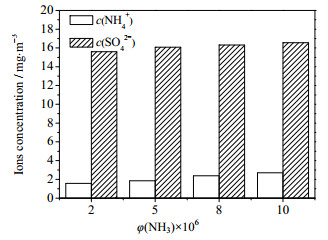
将PM10/PM2.5采样器中采集了颗粒物的铝箔与滤膜进行超声波提取,并对NH4+和SO42-进行浓度分析,得到NH3浓度对空预器出口的颗粒物化学组分的影响,如图 8所示。从图 8中可以看出,试验条件下颗粒物中SO42-浓度始终大于NH4+浓度,这可能是由于试验气氛一直保持SO3浓度过量,当颗粒物一旦形成,反应气氛中过量的SO3则会吸附在颗粒物上,导致采集到的颗粒物中SO42-浓度明显高于NH4+浓度。当NH3浓度增大,出口颗粒物中的NH4+明显增多,从1.575增加到2.7 mg·m-3。与此同时,SO42-浓度的变化并不明显,仅从15.6增大到16.56 mg·m-3。从化学平衡角度来说,当试验气氛中SO3浓度一定时,作为反应物之一的NH3浓度增加会促使反应向生成NH4HSO4方向移动,生成更多的NH4HSO4,使模拟空预器出口处颗粒物的数量浓度与粒径分布及组成成分均出现差异。
|
图 8 NH3浓度对空预器出口颗粒物成分的影响 Fig.8 Effects of NH3 concentrations on particle composition |
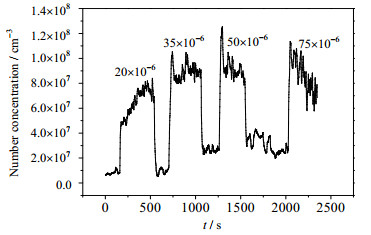
试验工况:模拟空预器入口温度320℃,φ(SO3) = 20×10-6、35×10-6、50×10-6、75×10-6,φ(NH3) = 5×10-6。不同浓度的SO3对模拟空预器出口颗粒物的影响试验结果如图 9所示。可以看出,当φ(SO3)从20×10-6增大到35×10-6时,模拟空预器出口颗粒物的数量浓度均值从6.52×107增大至8.93×107个·cm-3,增加了36.8%。而继续增大SO3浓度,颗粒物数量浓度变化不大,基本维持在9×107个·cm-3,这说明SO3浓度对颗粒物数量浓度的影响不大。造成这种现象的原因可能是,SO3浓度相对NH3浓度过量,增加SO3浓度虽可能使更多的NH3参与反应,增加NH4HSO4的生成量,但效果并无直接增加NH3明显。
|
图 9 SO3浓度对空预器出口颗粒物数量浓度的影响 Fig.9 Effects of SO3 concentrations on particle number concentration in air preheater |
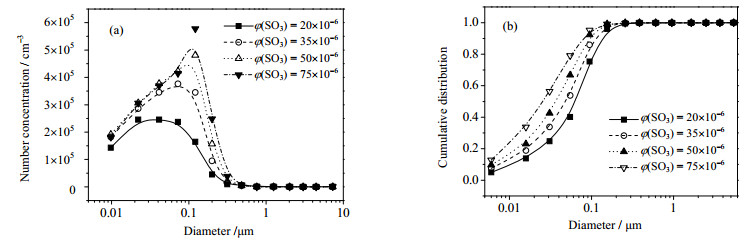
SO3对颗粒物粒径分布的影响则如图 10所示。从图 10(a)中可以发现,所测到的颗粒物的粒径基本小于0.3 μm,其粒径分布大致呈单峰分布,峰值随SO3浓度的增大而向右有小幅度偏移,这可能是由于试验气氛中NH3保持恒定,增加SO3浓度对NH4HSO4的生成影响不大,但气相中过量的SO3会更多的吸附于颗粒物上,使其粒径增大。此外,对比图 7(a)与图 10(a)也可以观察到,因SO3浓度变化所造成的颗粒物数量浓度变化明显小于因NH3浓度变化而出现的颗粒物数量浓度变化。
|
图 10 SO3浓度对空预器出口颗粒物粒径的影响 Fig.10 Effects of SO3 concentrations on particle diameter distribution |
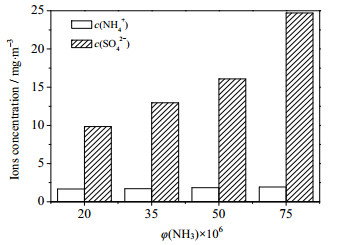
图 11表示了SO3浓度对空预器出口颗粒物化学组分的影响。从图 11中可以看出,随着SO3浓度的升高,出口颗粒物中的SO42-含量明显增大,从9.84增大到24.72 mg·m-3,而NH4+浓度的变化并不明显,仅从1.665增加到1.935 mg·m-3。这可能是由于相对NH3浓度而言,SO3浓度过量,NH4HSO4的生成量主要由NH3浓度决定[25]。提高SO3的浓度虽会使反应平衡向生成NH4HSO4方向移动但由于NH3浓度固定,限制了NH4HSO4的生成量,提高SO3浓度对NH4HSO4生成量的影响并没有提高NH3浓度的影响显著,因此采集到的颗粒物中NH4+浓度仅增长了16.2%。而随着SO3浓度的升高,气氛中SO3增多,会有更多的SO3吸附到已经生成的颗粒物上,使得颗粒物中SO42-离子浓度增长了151.2%,因此出现了NH4+浓度基本不变而SO42-浓度不断升高的现象。
|
图 11 SO3浓度对空预器出口颗粒物成分的影响 Fig.11 Effects of SO3 concentrations on particle composition |
(1) NH4HSO4的形成温度在235~260℃,是反应物浓度乘积的函数,随反应物浓度乘积的增大而升高;
(2) 空预器出口因NH4HSO4生成而产生的颗粒物主要为粒径小于0.2 μm的亚微米级颗粒,且颗粒物中SO42-浓度远高于NH4+。升高NH3浓度会明显增加颗粒物中NH4+浓度,说明有更多NH4HSO4生成,而升高SO3浓度不会明显增加NH4+浓度。
(3) NH3和SO3浓度升高均会使空预器出口颗粒物数量浓度增大,NH3浓度的增加会明显增加空预器出口处粒径小于0.1 μm的颗粒物数量浓度,相比之下,增加SO3浓度对颗粒物数量浓度的影响较小,但会使颗粒物粒径出现小幅度增大。
| [1] | TAN Qing(谭青), FENG Ya-chen(冯雅晨). Present status and perspective of China's flue gas denitration industry and research progress of SCR catalysts(我国烟气脱硝行业现状与前景及SCR脱硝催化剂的研究进展)[J]. Chemical Industry and Engineering Progress(化工进展) , 2011, 30(S1): 709-713. |
| [2] | Casagrande L, Lietti L, Nova I, et al. SCR of NO by NH3 over TiO2-supported V2O5-MoO3 catalysts:reactivity and redox behavior[J]. Applied Catalysis B Environmental , 1999, 22(1): 63-77. DOI:10.1016/S0926-3373(99)00035-1. |
| [3] | ZHU Lin(朱林), WU Bi-jun(吴碧君), DUAN Jiu-xiang(段玖祥), et al. Situation of production and application on selective catalytic reduction flue gas de-NOx catalysts(SCR烟气脱硝催化剂生产与应用现状)[J]. Electric Power(中国电力) , 2009, 42(8): 61-64. |
| [4] | WANG Hong-liang(王宏亮), XUE Jian-ming(薛建明), XU Yue-yang(许月阳), et al. Formation and control of SO3 from coal-fired power plants(燃煤电站锅炉烟气中SO3的生成及控制)[J]. Electric Power Technology and Environmental Protection(电力科技与环保) , 2014, 30(5): 17-20. |
| [5] | HUA Hui(华卉). Formation and speciation of SO3 from coal-fired power plants(燃煤烟气中SO3的生成及存在形态)[J]. Shandong Chemical Industry(山东化工) , 2016, 45(3): 138-139. |
| [6] | SHEN Jian-jun(沈建军), HE Zhi-qiang(禾志强). Prevention measures for air-preheater blockage in super-low emission situation of coal-fired power plants(燃煤电厂超低排放形势下空预器堵塞预防措施)[J]. Environmental Protection Science(环境保护科学) , 2017, 43(1): 88-91. |
| [7] | LI Wen-jie(李文杰). Influence and control of SCR denitration on air-heater blockage(SCR脱硝对空预器堵塞的影响及控制措施)[J]. Mechanical Management and Development(机械管理开发) , 2016, 31(7): 99-101. |
| [8] | SONG Guang-hui(宋光辉). Reason analysis and preventive measures of air preheater(空预器堵塞原因分析及预防措施)[J]. Equipment Manufacturing Technology(装备制造技术) , 2015(10): 125-127. DOI:10.3969/j.issn.1672-545X.2015.10.039. |
| [9] | Saleem A, Galgano M, Inaba S. Hitachi-zosen deNOx process for fossil fuel-fired boilers[C]//Proceedings of the Second NOx Control Technology Seminar. Denver: EPRI, 1978. |
| [10] | Wilburn R T, Wright T L. SCR ammonia slip distribution in coal plant effluents and dependence upon SO3[J]. Powerplant Chemistry , 2004, 6(5): 295-304. |
| [11] | Matsuda S, Kamo T, Kato A, et al. Deposition of ammonium bisulfate in the selective catalytic reduction of nitrogen oxides with ammonia[J]. Industrial & Engineering Chemistry Product Research & Development , 1982, 21(1): 1888-1900. |
| [12] | Wei J Y, Muzio L J, Dunn-Rankin D. Formation temperature of ammonium bisulfate at simulated air preheater conditions[C]//5th US Combustion Meeting. San Diego: the Western States Section of the Combustion Institute, 2007: 3369-3378. |
| [13] | Menasha J, Dunn-Rankin D, Muzio L, et al. Ammonium bisulfate formation temperature in a bench-scale single-channel air preheater[J]. Fuel , 2011, 90(7): 2445-2453. DOI:10.1016/j.fuel.2011.03.006. |
| [14] | MA Shuang-chen(马双忱), DENG Yue(邓悦), WU Wen-long(吴文龙), et al. Experimental research on ABS formation characteristics in SCR denitrification process(SCR脱硝过程中硫酸氢铵形成特性实验研究)[J]. Chinese Journal of Power Engineering(动力工程学报) , 2016, 36(2): 143-150. |
| [15] | MA Da-wei(马大卫), HUANG Qi-shun(黄齐顺), ZHA Zhi-ming(查智明), et al. Analysis and solution of air-preheater scaling in coal-fired power plants(燃煤电厂空预器结垢成因分析及处理措施)[J]. Electric Power Technology and Environmental Protection(电力科技与环保) , 2017, 33(2): 56-59. |
| [16] | LIU Hai-xiao (刘海啸). Air preheater jams caused by ammonia hydrogen sulfate governance counter measure research (硫酸氢氨造成的空预器堵塞治理对策研究) [D]. Beijing (北京): North China Electric Power University (华北电力大学), 2017. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=cyyt201518032&dbname=CJFD&dbcode=CJFQ |
| [17] | Li Z, Jiang J K, Ma Z Z, et al. Effect of selective catalytic reduction (SCR) on fine particle emission from two coal-fired power plants in China[J]. Atmospheric Environment , 2015, 120: 227-233. DOI:10.1016/j.atmosenv.2015.08.046. |
| [18] | YANG Lin-jun(杨林军), SHI Ya-juan(史雅娟), LUO Lv-yuan(骆律源). Review of emission characteristics of fine particles during coal-fired SCR deNOxprocess(燃煤烟气SCR脱硝系统中细颗粒物排放特性综述)[J]. Proceedings of the CSEE(中国电机工程学报) , 2016, 36(16): 4342-4348. |
| [19] | ZHANG Yu-hua(张玉华), SHU Hang(束航), FAN Hong-mei(范红梅), et al. Research on emission characteristics and influencing factors of PM2.5 for selective catalytic reduction based on V2O5-WO3/TiO2 commercial catalysts(商业V2O5-WO3/TiO2催化剂SCR脱硝过程中PM2.5的排放特性及影响因素研究)[J]. Proceedings of the CSEE(中国电机工程学报) , 2015, 35(2): 383-389. |
| [20] | ZHANG Yu-hua (张玉华). Investigation on the effects of SCR on emission characteristics of PM2. 5 from coal-fired flue gas (燃煤烟气SCR脱硝对细颗粒物排放特性影响的试验研究) [D]. Nanjing (南京): Southeast University (东南大学), 2015. http://cdmd.cnki.com.cn/Article/CDMD-10286-1016753361.htm |
| [21] | SHI Ya-juan(史雅娟), ZHANG Yu-hua(张玉华), SHU Hang(束航), et al. Effect of SO2 and NH3 on emission characteristics of PM2.5 in SCR(SO2与NH3/NO对SCR脱硝中PM2.5排放特性的影响)[J]. Modern Chemical Industry(现代化工) , 2016, 36(2): 90-94. |
| [22] | SHU Hang (束航). Investigation on the formation and decomposition mechanism of ammonium sulfate and ammonium bisulfate fine particles during SCR process of coal-fired flue gas. (SCR烟气脱硝过程中硫酸(氢)铵细颗粒生成及分解特性研究) [D]. Nanjing (南京): Southeast University (东南大学), 2015. http://cdmd.cnki.com.cn/Article/CDMD-10286-1016050375.htm |
| [23] | SHU Hang(束航), ZHANG Yu-hua(张玉华), FAN Hong-mei(范红梅), et al. FT-IR study of formation and decomposition of ammonium bisulfates on surface of SCR catalyst for nitrogen removal(SCR脱硝中催化剂表面NH4HSO4生成及分解的原位红外研究)[J]. Journal of Chemical Industry and Engineering(化工学报) , 2015, 66(11): 4460-4468. |
| [24] | YU Dun-Xi (于敦喜). Particle mode identification and formation mechanisms during coal combustion (燃煤细微颗粒物的模态识别及其形成机理) [D]. Wuhan (武汉): Huazhong University of Science and Technology (华中科技大学), 2007. http://cdmd.cnki.com.cn/Article/CDMD-10487-2009033850.htm |
| [25] | DENG Yue (邓悦). The formation mechanism and regulation of hydrogen sulfate in the process of the SCR denitration (SCR脱硝过程中硫酸氢铵的形成机理与调控) [D]. Beijing (北京): North China Electric Power University (华北电力大学), 2016. http://cdmd.cnki.com.cn/Article/CDMD-10079-1016276279.htm |




