辛醇(2-乙基己醇,2EHO)是一种重要的有机化工产品,主要用于生产对苯二甲酸二辛酯、邻苯二甲酸二辛酯、己二酸二辛酯等增塑剂。辛醇的工业生产主要由辛烯醛加氢反应获得[1]。辛烯醛是一种α, β-不饱和醛,分子中既含有C=C键又含有C=O键。C=C键的键能为615 kJ·mol-1,C=O键的键能为715 kJ·mol-1,因而C=C双键比C=O双键更容易加氢[2]。但在α, β-不饱和醛中的C=C和C=O双键形成共轭体系,使C=O双键也很容易被还原,发生C=C与C=O双键的竞争加氢反应,得到的产物往往是α, β-不饱和醛中C=C或C=O双键以及二者都被加氢饱和的多种物质的混合物[2~4]。所以,提高辛醇的选择性是催化体系研究的重点。
反应体系的酸碱性对加氢产物的选择性有很大的影响。Ekou等[5]以Rh/TiO2为催化剂催化柠檬醛加氢反应,采用氨水对催化剂进行处理,柠檬醛的转化率达到100%,主要产物为香茅醛。这是因为在碱性条件下,柠檬醛分子中的C=C键比C=O键更容易与催化剂吸附,提高了C=C键的加氢选择性。Du等[6]以Pd/C催化α-甲基-β-对叔丁基苯基丙烯醛的C=C键加氢,发现在反应体系中加入碱性物质Na2CO3和NaOH后,Pd/C表面的电荷密度提高,C=O键的吸附被抑制,C=C键比C=O键更适合吸附在催化剂Pd上,从而可以提高α-甲基-β-对叔丁基苯基丙醛的选择性。Gerrit等[7]以[FeF(L)][BF4](L=P(PhPPh3))催化柠檬醛的C=O键加氢生成不饱和醇反应,发现在反应中添加三氟乙酸后不饱和醇的收率大大提高了,柠檬醛的转化率可以达到99%以上,不饱和醇的收率和选择性都为98%,说明在酸性条件下[FeF(L)][BF4]适宜对C=O键的加氢。目前,尚未见到体系酸碱性对辛烯醛加氢反应影响的文献报道。
为了便于阐明体系酸碱性对辛烯醛加氢反应的影响,实现高选择性合成辛醇的目的,本文首先制备大孔径比表面积相对较小的中性载体α-Al2O3,然后筛选出了适宜的金属活性组分,在此基础上,研究了反应体系酸碱性对负载型Ni基催化剂催化辛烯醛加氢反应的影响。
2 实验部分 2.1 原料与试剂辛烯醛(98.5%(wt),自制);正丁醛和醋酸(分析纯,天津大茂化学试剂厂);NaOH、蔗糖、硝酸镍(分析纯,天津市风船化学试剂有限公司);氢氧化锂、氢氧化钾、硼酸、乙酸锌(分析纯,国药集团化学试剂有限公司);硬脂酸锌(工业级,百灵威科技有限公司);拟薄水铝石(工业级,山东铝业鲁中实业贸易公司化学品氧化铝厂)。
2.2 催化剂的制备 2.2.1 α-Al2O3采用蔗糖辅助法[8]制备α-Al2O3。首先将0.10 mol的Al(NO3)3∙9H2O和0.05 mol蔗糖共溶于200 mL去离子水中,在机械搅拌条件下滴加氨水调节溶液pH = 5.2。然后,在搅拌条件下于80℃水浴中老化2 h。最后,将生成的胶状物在110℃条件下干燥24 h,研磨后以2℃·min-1的速率升温至1100℃并保持2 h。
2.2.2 γ-Al2O3将拟薄水铝石置于马弗炉中,在空气气氛下由室温以10℃·min-1的速率升温至500℃,焙烧4 h。
2.2.3 加氢催化剂以Ni/α-Al2O3的制备方法为例:将3.964 g的Ni(NO3)2∙6H2O(负载量为10%(wt))溶于8 mL蒸馏水中配制成硝酸镍溶液。用等体积浸渍法将镍负载在8 g α-Al2O3上,室温下老化24 h,110℃下干燥8 h,在马弗炉中500℃下焙烧4 h,最后在N2:H2= 80:20的气氛下,550℃下还原4 h后得到Ni/α-Al2O3催化剂。制备Co/α-Al2O3催化剂的还原条件为在500℃下还原4 h;制备Cu/α-Al2O3催化剂还原条件为在300℃下还原4 h;制备Fe/α-Al2O3催化剂还原条件为在500℃下还原4 h;制备Pd/α-Al2O3催化剂还原条件为在350℃下还原4 h;制备Rh/α-Al2O3和Ru/α-Al2O3催化剂的还原条件均在300℃下还原4 h。
2.3 催化剂表征 2.3.1 物相测定(XRD)采用日本理学D/MAX-2500型X射线衍射仪对催化剂样品进行物相分析。操作条件为:Cu靶,石墨单色滤光片,狭缝SS/DS=1°,RS=0.15 mm,工作电压为40 kV,电流100 mA,扫描范围10~90°,扫描速率8°·min-1。
2.3.2 比表面积、孔容和孔径分析(BET)催化剂样品的比表面及孔结构测定在美国Micromeritics公司生产的ASAP2020M + C型比表面及孔隙度分析仪上进行。称取样品0.2 g左右,先在150℃下真空脱气4 h,液氮冷肼中进行N2吸附及脱附测定。催化剂的比表面积采用BET法进行计算,孔体积和孔径采用BJH脱附法计算。
2.4 催化剂活性评价辛烯醛加氢反应在100 mL的高压反应釜中进行。具体操作步骤如下:量取30 mL的辛烯醛(约24 g)置于反应釜中,加入3.6 g催化剂;密封后用H2置换3次;在搅拌条件下升至180℃,待达到反应温度后开始通入H2 (反应压力为2.0 MPa);反应80 min后停止通入氢气。将反应釜置于冰水浴中冷却至室温后,放气泄压;将反应液减压抽滤,用气相色谱分析滤液组成。
2.5 产物分析采用北京分析仪器厂SP 2100型气相色谱仪对产物进行定量分析,以环己醇为内标物。载气N2,流速30 mL·min-1。氢火焰检测器,检测室温度220℃,气化室温度220℃,进样量0.4 µL。KB-1毛细管柱,采用程序升温控制色谱柱温:初温80℃并保持3 min,以10℃·min-1的速度升温至160℃并保持2 min,再以10℃·min-1的速率升温至200℃并保持6 min。
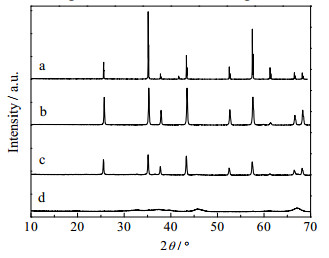
3 结果与讨论 3.1 α-Al2O3表征对蔗糖辅助法制备的氧化铝进行XRD分析,结果如图 1所示。通过与α-Al2O3的标准卡片比对可以看出,在1200和1100℃下制备的氧化铝均呈α晶型,而在1000℃下无法得到α-Al2O3。通过N2吸附-脱附实验测定,采用蔗糖辅助法制备的α-Al2O3的比表面积为53.3 m2·g-1,孔体积为0.14 cm3·g-1,平均孔径为5.39 nm。
|
图 1 蔗糖辅助法制备的α-Al2O3的XRD谱图 Fig.1 XRD patterns of α-Al2O3 prepared by a sucrose-assisted method a. standard card of α-Al2O3 b. 1200℃ c. 1100℃ d. 1000℃ |
分别将非贵金属Ni、Co、Cu、Fe和贵金属Rh、Ru、Pd负载在α-Al2O3载体上,考察金属种类对辛烯醛加氢反应的影响,结果如表 1所示。其中,非贵金属的负载量为10%(wt),贵金属的负载量为1%(wt)。从表中可以看出,以不同金属催化辛烯醛加氢反应时,辛醇收率的大小次序为:Ni > Co > Ru > Cu > Pd > Rh > Fe。其中,以Ni/α-Al2O3为催化剂催化辛烯醛加氢反应性能最好,辛烯醛的转化率为100%,辛醇收率为92.8%。从表中还可以看出,Ni/α-Al2O3和Co/α-Al2O3催化剂均具有较好的催化活性,但Ni/α-Al2O3的选择性好于Co/α-Al2O3催化剂,而且两者均没有辛醛生成,说明金属Ni和Co可以同时催化C=C键和C=O键加氢。而以Cu/α-Al2O3、Pd/α-Al2O3、Rh/α-Al2O3和Ru/α-Al2O3为催化剂时,不仅催化活性低,而且除了有少量的辛醇生成外,还有辛醛生成。其中,以Pd/α-Al2O3为催化剂时,辛醛选择性较高,说明其利于C=C键加氢[9]。文献[6, 10, 11]中均以Pd作为加氢活性组分制备的催化剂催化不饱和醛加氢反应,产物主要是饱和的醛,说明以Pd作为加氢活性组分,该催化剂有利于C=C键加氢。以Fe/α-Al2O3为催化剂时,加氢活性较低,辛醇的收率仅为0.2%,无辛醛生成,说明金属Fe几乎无加氢活性。Steffen等[12]研究了铁催化不饱和醛加氢反应,发现单纯的铁催化剂催化不饱和醛加氢,反应几乎不进行,说明以Fe作为加氢活性组分,催化剂没有加氢活性。综上所述,Ni/α-Al2O3催化剂既具有较高的加氢活性,又具有很好的辛醇选择性。故确定最适宜的催化剂为Ni/α-Al2O3。
| 表 1 加氢活性组分的筛选 Table 1 Screening of metals for hydrogenation of 2-ethyl-2-hexenal |
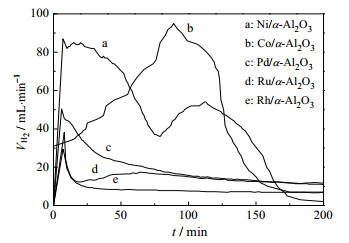
图 2为金属Ni、Co、Rh、Ru和Pd催化辛烯醛加氢反应的加氢速率图。由图可知,以Ni作为加氢金属时,辛烯醛加氢反应的加氢速率较快,而且加氢过程分为两个阶段,而其他金属没有明显的区分。由此可以推测,金属Ni催化辛烯醛加氢反应时,可能首先对C=C键加氢,然后再对C=O键进行加氢。
|
图 2 M/α-Al2O3 (M = Ni、Co、Rh、Ru和Pd)催化辛烯醛加氢速率图 Fig.2 Profiles of 2-ethyl-2-hexenal hydrogenation rates catalyzed by M/α-Al2O3 |
在反应体系中分别加入碱性物质LiOH、NaOH和KOH,考察碱性对Ni/α-Al2O3催化辛烯醛加氢反应性能的影响,结果如表 2所示。可以看出,加入碱性物质LiOH、NaOH和KOH后,辛醇的收率随着碱性强度的增强逐渐下降,分别为85.8%、50.5%和2.0%,而辛醛的收率逐渐增大,分别为0%、22.8%和69.1%。只有加入KOH时,辛烯醛的转化率才下降,为95.7%。以上结果表明,碱性物质会抑制C=O键的加氢,且随着碱性强度的增强,C=O键的加氢受到抑制程度增大(辛醛收率增加),该结论与Ekou等[5]和Du等[6]的结论一致。
| 表 2 碱性对Ni/α-Al2O3催化辛烯醛加氢反应的影响 Table 2 Effects of basicity on 2-ethyl-2-hexenal hydrogenation catalyzed by Ni/α-Al2O3 |
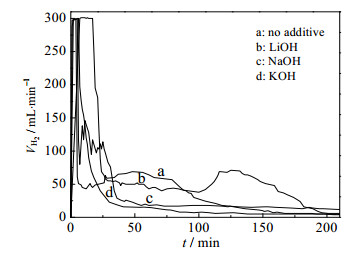
图 3为碱性物质对Ni/α-Al2O3催化辛烯醛加氢速率的影响。可以看出,不添加碱性物质时,从开始进氢气(氢气流量为300 mL·min-1)到反应釜压力达到2.0 MPa用时3 min;添加碱性物质LiOH、NaOH和KOH后,从开始进氢气到反应釜压力达到2.0 MPa用时分别为24,4和6 min。说明加入碱性物质后,反应釜压力达到2.0 MPa的时间延长了,即辛烯醛初始加氢速率(C=C键加氢速率)提高了。从加氢速率图还可以看出,与中性体系相比,加入碱性物质后,第一阶段C=C键的加氢速率明显提高,而第二阶段C=O键的加氢速率明显下降,说明碱性体系,有利于C=C键加氢[6, 13]。
|
图 3 碱性物质对Ni/α-Al2O3催化辛烯醛加氢速率的影响 Fig.3 Effects of basic substances on 2-ethyl-2-hexenal hydrogenation rates catalyzed by Ni/α-Al2O3 |
综上所述,在Ni/α-Al2O3催化辛烯醛加氢反应体系中加入碱性物质,增加了催化剂表面的电荷密度,C=C键比C=O键更适于与催化剂吸附,从而抑制C=O键加氢,辛醇的选择性降低,辛醛的选择性提高;且加入碱性物质,可以提高C=C键的加氢速率。
3.3.2 酸性的影响在反应体系中分别加入作为B酸的乙酸和硼酸(酸强度:乙酸 > 硼酸),以及作为L酸的乙酸锌和硬脂酸锌(酸强度:乙酸锌 > 硬脂酸锌),考察酸性对Ni/α-Al2O3催化辛烯醛加氢反应的影响,结果如表 3所示。可以看出,添加不同强度的B酸(乙酸和硼酸)后,辛烯醛的转化率不变,均为100%。而添加不同强度的L酸(乙酸锌和硬脂酸锌)后,辛烯醛的转化率分别下降为90.8%和97.8%,且随着L酸性增强而逐渐下降。无论添加B酸还是L酸,辛醇的收率均下降而辛醛的收率均增加。除此之外,还有少量的辛烯醇生成且L酸比B酸对辛烯醇的生成促进作用更大。Patricia等[14]以Pt/Sn-β分子筛作为催化剂显著的提高了α, β-不饱和醛中C=O键的加氢速率,这是由于作为Lewis酸的Sn4+可以通过降低C=O键中C原子上的电子密度来活化C=O,从而提高不饱和醇的选择性,同时加快反应速率。李涛等[15]在研究负载型Pt催化剂上肉桂醛加氢的反应规律时也得到该结论。作者发现未修饰催化剂Pt/Al2O3上,主要以C=C键加氢为主;加入少量Sn助剂后肉桂醛加氢活性大幅度提高,而且C=O键加氢选择性有所提高。黄朋勉等[16]对不饱和醛选择性加氢生成不饱和醇的反应机理进行分析时,发现不饱和醇不易得到的原因是C=O键的π体系不易被利用,而C=C键的吸附易于发生。可以通过添加L酸助剂,来活化羰基和降低πco轨道的电子接受能力,有利于C=O键吸附,从而提高不饱和醇的选择性。Smid等[17]用有酸性位的催化剂(Pt/SiO2-TiO2和Pt/SiO2-ZrO2)催化柠檬醛加氢生成不饱和醇反应,发现不饱和醇的生成与载体的酸性有直接关系。作者推测柠檬醛氧原子上的电子被催化剂表面的酸性所吸引,这种吸引能够促进羰基氧的加氢生成不饱和醇。而且酸性越强,不饱和醇的选择性越高。
| 表 3 酸性对Ni/α-Al2O3催化辛烯醛加氢反应的影响 Table 3 Effects of acidity on 2-ethyl-2-hexenal hydrogenation catalyzed by Ni/α-Al2O3 |
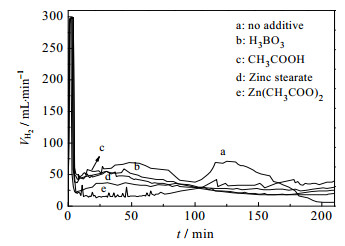
综上可知,反应体系中的酸性有利于C=O键加氢生成不饱和醇,尤其是L酸对C=O键选择性加氢影响较大,且酸性越强越有利于辛烯醇的生成。辛醛收率较高的原因解释如下:由本课题组在线反应红外分析得到的辛烯醛加氢反应历程可知,C=O键加氢在C=C键之后,C=C键不能完全加氢会阻碍C=O键加氢。由于C=O键能较C=C键能大,而且二者具有共轭作用,使得反应要在C=O键上选择加氢而不还原C=C键较难。但是由于酸性物质的加入,有利于C=O键加氢,提高了C=O键加氢的竞争力,在辛醛生成的过程中有辛烯醇生成。虽然C=O键加氢竞争力得到了提高,但是C=C键的加氢速率还是大于C=O键的加氢速率,所以辛醛的收率远远高于辛烯醇的收率。然而,由于C=O键与C=C键的竞争加氢,造成第一阶段C=C键的加氢速率较慢,进而阻碍了第二阶段C=O键的加氢。从图 4的加氢速率图可以看出,在酸性体系中,从开始进气到反应釜压力达到2.0 MPa用时均在3~4 min,与中性体系相差不大。当压力达到2.0 MPa后,加氢速率都比中性条件下低。说明加入酸性物质后,使C=C键的加氢速率下降,进而影响辛醇的生成速率,所以造成辛醛的收率较高而辛醇的收率较低。
|
图 4 酸性物质对Ni/α-Al2O3催化辛烯醛加氢反应加氢速率的影响 Fig.4 Effects of acidic substances on 2-ethyl-2-hexenal hydrogenation rates catalyzed by Ni/α-Al2O3 |
在Ni/α-Al2O3反应体系中加入了两性物质γ-Al2O3,考察了酸-碱性物质对辛烯醛加氢反应的影响,结果如表 4所示。可以看出,在反应体系中加入γ-Al2O3后,辛烯醛的转化率为100%,辛醇的收率由92.8%提高到94.7%,没有辛醛和辛烯醇的生成。说明在酸碱活性位都存在的条件下不仅不会降低辛烯醛的转化率,并且可以提高辛醇的收率。在此基础上,我们还考察了Ni/γ-Al2O3催化辛烯醛加氢反应的催化效果,从表 4可以看出,将Ni直接负载在γ-Al2O3的催化效果与在Ni/α-Al2O3体系中加入γ-Al2O3的催化效果是一致的。
| 表 4 两性物质对Ni/α-Al2O3催化辛烯醛加氢反应的影响 Table 4 Effects of amphiprotic substance on 2-ethyl-2-hexenal hydrogenation catalyzed by Ni/α-Al2O3 |
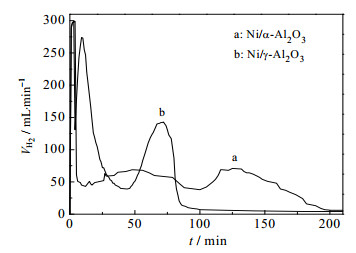
从图 5的加氢速率图可以看出,Ni/α-Al2O3和Ni/γ-Al2O3催化加氢均分为两个阶段,但Ni/γ-Al2O3催化加氢速率较快。以Ni/γ-Al2O3为催化剂时,不仅提高了C=C键的加氢速率,而且也提高了C=O键的加氢速率。这与γ-Al2O3表面既含有L酸位又含有少量的弱碱位有直接关系。酸-碱两性物质中的碱性位可以促进C=C键的加氢,提高C=C键加氢速率;酸性位可以促进C=O键加氢,提高C=O键加氢速率。
|
图 5 Ni/α-Al2O3与Ni/γ-Al2O3催化辛烯醛加氢反应的加氢速率对比图 Fig.5 Comparison of 2-ethyl-2-hexenal hydrogenation rates catalyzed by Ni/α-Al2O3 and Ni/γ-Al2O3 |
(1) 采用蔗糖辅助法制备的α-Al2O3为载体制备了负载型金属催化剂,评价了其催化辛烯醛加氢反应的催化性能。结果表明,Ni/α-Al2O3具有较好的催化性能,辛烯醛的转化率为100%,辛醇收率为92.8%。
(2) 考察了碱性(LiOH、NaOH和KOH)、酸性(醋酸、硼酸、乙酸锌和硬脂酸锌)和酸碱两性(γ-Al2O3)物质对Ni/α-Al2O3催化辛烯醛液相加氢反应的影响,结果表明:碱性物质的添加有助于C=C键加氢,提高了C=C键的加氢速率,酸性物质的添加促进了C=O键加氢,提高了C=O键的加氢速率,而兼具弱酸和弱碱中心的γ-Al2O3添加既有助于C=C键加氢,又有助于C=O键加氢。
(3) 以Ni/γ-Al2O3为催化剂或在Ni/α-Al2O3中加入γ-Al2O3可以提高辛醇的收率,辛醇的收率从92.8%分别提高到94.7%和94.2%。
| [1] | Hanna D G, Shylesh S, Li Y P, et al. Experimental and theoretical study of n-butanal self-condensation over Ti species supported on silica[J]. ACS Catalysis , 2014, 4(9): 2908-2916. DOI:10.1021/cs500704b. |
| [2] | Noller H, Lin W M. Activity and selectivity of Ni-Cu/Al2O3 catalysts for hydrogenation of crotonaldehyde and mechanism of hydrogenation[J]. Journal of Catalysis , 1984, 85(1): 25-30. DOI:10.1016/0021-9517(84)90106-4. |
| [3] | GE Chang-hua(葛昌华), LI Yan(李艳), ZHAO Jie(赵杰), et al. Selective hydrogenation of cinnamaldehyde over carbon nanotubes supported Pd catalysts under atmospheric pressure(常压下碳纳米管负载钯催化剂上肉桂醛选择性加氢)[J]. Petrochemical Technology(石油化工) , 2010, 39(2): 136-140. |
| [4] | LI Jie(李杰), LI Ling(李玲), JIANG Da-hao(江大好), et al. Research progress in the catalysts for selective hydrogenation of C=C double bond in α, β-unsaturated carbonyl compounds(α, β-不饱和醛/酮中C=C双键选择性加氢催化剂的研究进展)[J]. Industrial Catalysis(工业催化) , 2012, 20(8): 13-19. |
| [5] | Ekou T, Ekou L, Vicente A, et al. Citral hydrogenation over Rh and Pt catalysts supported on TiO2:influence of the preparation and activation protocols of the catalysts[J]. Journal of Molecular Catalysis A:Chemical , 2011, 337(1-2): 82-88. DOI:10.1016/j.molcata.2011.01.020. |
| [6] | Du W Q, Ze M R, Yan L, et al. Chemoselective hydrogenation of α, β-unsaturated aldehydes with modified Pd/C catalyst[J]. Chinese Chemical Letters , 2012, 23(7): 773-776. DOI:10.1016/j.cclet.2012.05.002. |
| [7] | Gerrit W, Felix A, Junge K, et al. A molecularly defined iron-catalyst for the selective hydrogenation of α, β-unsaturated aldehydes[J]. Chemistry-A European Journal , 2013, 19(24): 7701-7707. DOI:10.1002/chem.v19.24. |
| [8] | WANG Chun-ming(王春明), ZHAO Bi-ying(赵璧英), ZHU Yue-xiang(朱月香), et al. Preparation of high-surface-area γ-alumina by assistance of sucrose(蔗糖辅助制备大比表面积氧化铝)[J]. Chinese Journal of Catalysis(催化学报) , 2004, 25(5): 341-343. |
| [9] | Zhang Y K, Liao S J, Xu Y, et al. Catalytic selective hydrogenation of cinnamaldehyde to hydrocinnamaldehyde[J]. Applied Catalysis A:General , 2000, 192(2): 247-251. DOI:10.1016/S0926-860X(99)00400-7. |
| [10] | Anderson K, Cortinas F S, Christopher H, et al. Preparation of nanoparticulate metal catalysts in porous supports using an ionic liquid route[J]. Inorganic Chemistry Communications , 2004, 7(1): 73-76. DOI:10.1016/j.inoche.2003.10.008. |
| [11] | Pasi V, Mikkola J P, Salmi T, et al. Kinetics of citral hydrogenation by supported ionic liquid catalysts (SILCA) for fine chemicals[J]. Industrial & Engineering Chemistry Research , 2007, 46(26): 9022-9031. |
| [12] | Steffen F, Zhou S L, Junge K, et al. General and highly efficient iron-catalyzed hydrogenation of aldehydes, ketones, and α, β-unsaturated aldehydes[J]. Angewandte Chemie International Edition , 2013, 52(19): 5120-5124. DOI:10.1002/anie.201301239. |
| [13] | Stolle A, Thomas G, Christine S, et al. Hydrogenation of citral:a wide-spread model reaction for selective reduction of α, β-unsaturated aldehydes[J]. RSC Advances , 2012, 3(7): 2112-2153. |
| [14] | Patricia C, Yolanda P, Garrido J C H, et al. The promotional effect of Sn-beta zeolites on platinum for the selective hydrogenation of α, β-unsaturated aldehydes[J]. Physical Chemistry Chemical Physics , 2013, 15(29): 12048-12055. DOI:10.1039/c3cp50519g. |
| [15] | LI Tao(李涛), LI Guang-jin(李光进), XU Yi-de(徐奕德). The modification effect of Sn on Pt/Al2O3 catalyst for selective hydrogenation of cinnamaldehyde(Sn对肉桂醛加氢催化剂Pt/Al2O3的修饰作用)[J]. Chinese Journal of Catalysis(Chinese Journal of Catalysis) , 1999, 20(3): 219-223. |
| [16] | HUANG Peng-mian(黄朋勉), LIU Zi-li(刘自力), ZHENG Miao(郑淼), et al. Developmants of the catalysts for selective hydrogenation of crotonaldehyde to crotyl alcohol(巴豆醛选择性加氢制巴豆醇催化剂的研究进展)[J]. Industrial Catalysis(工业催化) , 2003, 11(6): 27-30. |
| [17] | Smid S P, Victoria T G, Tomas V G. Effect of the acid-base properties of the support on the performance of Pt catalysts in the partial hydrogenation of citral[J]. Catalysis Today , 2013, 213(18): 101-108. |




