2. 浙江新安化工集团股份有限公司, 浙江 杭州 311600;
3. 浙江省生态环境监测中心, 浙江 杭州 310012
2. Zhejiang Xinan Chemical Industrial Group Co. Ltd., Hangzhou 311600, China;
3. Zhejiang Ecological and Environmental Monitoring Center, Hangzhou 310012, China
大气中的氮氧化物(nitrogen oxides,NOx)是导致光化学烟雾和酸雨的主要污染物之一[1-2],我国“十三五”规划纲要要求十三五期间NOx排放量累计增速不超过15%[3]。当前非电力行业污染物排放问题日益突出,其中工业锅炉烟气中NOx的控制及治理成为我国城市建设和大气污染治理工作的重要内容[4]。NH3选择性催化还原NOx技术(selective catalytic reduction of NOx by ammonia,NH3-SCR)是目前国际上应用最为广泛的烟气脱硝技术[5]。NH3-SCR技术的核心是催化剂,由于非电力行业的工业锅(窖)炉的排烟温度低,因此,开发低温NH3-SCR催化剂具有重要意义[5]。近年来多项研究表明,由于铈(cerium,Ce)表面独特的储氧能力和氧化还原性能,其表现出优异的NH3-SCR活性。Ce3+的存在可以使催化剂表面产生更多的化学吸附氧或较弱的吸附氧物种,有助于SCR反应进行[6-7]。但是目前报道的Ce基催化剂活性温度窗口均接近或高于200 ℃,因此,降低反应温度(< 200 ℃)、拓宽活性温度范围、提高催化剂N2选择性是目前的研究重点[8]。三氧化钨(WO3)作为一种价格低廉的过渡金属氧化物,被普遍用作NH3-SCR反应中的稳定剂和促进剂[9]。如Chen等[10]在对CeTi和CeWTi催化剂的研究中发现WO3的掺杂会提供更多的酸位,加速NH4NO3与NO之间的反应,从而获得优异的低温活性。Shin等[11]通过浸渍法制备的W改性Mn/TiO2催化剂,可提高表面的Mn4+比率、酸度等,使得该催化剂在175~350 ℃下具有优异的活性和选择性。
本研究拟使用浸渍法合成不同WO3掺杂量的CeO2催化剂并探究其NH3-SCR性能,筛选出最优WO3掺杂量的WO3/CeO2催化剂。利用多晶X射线衍射(X-ray diffraction,XRD)、X射线光电子能谱(X-ray photoelectron spectroscopy,XPS)、氨气程序升温脱附(NH3-temperature programmed desorption,NH3-TPD) NH3-TPD)等各种表征技术对WO3掺杂量与催化活性之间的关系进行详细探究。
2 实验部分 2.1 实验试剂催化剂合成实验使用的试剂为六水合硝酸铈(分析纯AR,国药)、硅钨酸(AR,国药)。活性测试实验使用的气体分别为NO-Ar混合气(NO的体积分数为2.00%)、NO2-Ar混合气(NO2的体积分数为0.50%)、N2O-Ar混合气(N2O的体积分数为0.50%)、NH3-Ar混合气(NH3的体积分数2.00%)、O2 (体积分数≥99.99%)和N2 (体积分数≥99.99%),气体均购自杭州今工特种气体有限公司。
2.2 活性评价通过固定床反应器(由石英管反应器和电阻炉构成)测试所制备催化剂的NH3-SCR催化活性,具体测试方法为:将筛至0.25~0.425 mm(40~60目)的定量催化剂装入内径为0.6 cm的石英管中,并使装填的催化剂床层高度为0.6 cm。在测试活性之前,催化剂需在质量分数为10% 的O2/N2气氛中500 ℃下活化30 min,以去除表面吸附物。在反应过程中加热炉进行自动温度控制,通入流量为500 mL·min-1,成分为500 ×10-6 NH3、500 ×10-6 NO、5% (质量分数)O2和N2的气体作为平衡气,其体积空速为177 000 h-1。气体分析系统为装有PIKE气体池iS50傅里叶红外光谱仪,通过测定气体的标线来计算尾气中各气体的摩尔浓度(用c表示,其中进气用cin,出气用cout)。本实验主要通过氮氧化物转化率(NOx coversion)和氮气选择性(N2 selectivity)进行催化剂活性评估,其计算公式如下:
| $ {\rm{N}}{{\rm{O}}_x}\;{\rm{ conversion = }}\frac{{{c_{{\rm{N}}{{\rm{O}}_x}_{{\rm{, in}}}}} - {c_{{\rm{N}}{{\rm{O}}_x}_{{\rm{, out}}}}}}}{{{c_{{\rm{N}}{{\rm{O}}_x}_{{\rm{, in}}}}}}} $ | (1) |
| $ {c_{{\rm{N}}{{\rm{O}}_x}}} = {c_{{\rm{NO}}}} + {c_{{\rm{N}}{{\rm{O}}_{\rm{2}}}}} + {c_{{{\rm{N}}_2}{\rm{O}}}} $ | (2) |
| $ {{\rm{N}}_{\rm{2}}}\;{\rm{ selectivity = }}\left( {{\rm{1}} - \frac{{{\rm{2}}{c_{{{\rm{N}}_2}{\rm{O}}}}}}{{{c_{{\rm{N}}{{\rm{O}}_x}_{{\rm{, in}}}}}{\rm{ + }}{c_{{\rm{N}}{{\rm{H}}_{\rm{3}}}{\rm{, in}}}} - {c_{{\rm{NO, out}}}} - {c_{{{\rm{N}}_{\rm{2}}}{\rm{O, out}}}} - {c_{{\rm{N}}{{\rm{H}}_{\rm{3}}}{\rm{, out}}}}}}} \right){\rm{ }} $ | (3) |
本实验使用XRD对样品晶型进行分析,仪器为PANalytical公司的X’Pert PRO X射线衍射仪,采用Cu靶的Kα射线、电压为40 kV、电流为40 mA、扫描角度2θ为10°~90°;使用XPS进行表面元素及价态分析,仪器型号是Thermo Scientific Escalab 250Xi,X射线为Al Kα射线、束斑为650 μm、实际功率为153 W、通过能为30 eV、真空度为5×10-8 Pa;使用NH3-TPD进行表面酸量分析,仪器为美国麦克斯公司的型号为AutoChem Ⅱ 2920的高性能全自动化学吸附仪,具体操作步骤为:先将50 mg催化剂装在U型管中,30 mL·min-1氦气氛围和350 ℃下加热4 h以除去表面上的吸附质,冷却到100 ℃后通入吸附质(NH3的体积分数为10% 的NH3-He混合气) 至催化剂吸附饱和为止,最后在100 ℃下吹扫30 min以除去非化学吸附的吸附质,再以10 ℃·min-1的速率进行程序升温至500 ℃脱附。
2.4 催化剂合成使用两步法进行WO3/CeO2的合成。首先通过煅烧法合成CeO2载体,将六水合硝酸铈前驱体在管式炉中550 ℃下煅烧4 h得到淡黄色的CeO2载体,然后通过过量浸渍法进行WO3的掺杂,即将载体研磨至0.25 mm(60目)以下取3.44 g溶于10 mL去离子水中,在搅拌状态下加入一定量的硅钨酸,室温下搅拌10 h后,将产物在N2气氛中600 ℃下煅烧6 h,再将产物在空气中400 ℃下煅烧4 h,最后得到WO3/CeO2催化剂。本实验合成了W与Ce的物质的量比分别为0.1%、1%、2%、4% 和8% 的WO3/CeO2催化剂,记为x WO3/CeO2。
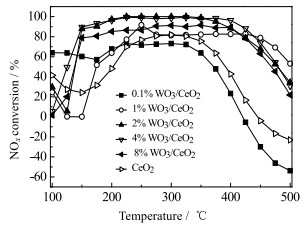
3 实验结果与讨论 3.1 WO3/CeO2的NH3-SCR活性测试在177 000 h-1高空速条件下,CeO2、0.1% WO3/CeO2、1% WO3/CeO2、2% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2催化下NH3-SCR反应的NOx转化率如图 1所示。由图可见,从1% WO3/CeO2开始,催化剂活性和活性温度窗口均出现明显提升;当WO3摩尔掺杂量增加至4% (4% WO3/CeO2)时,NOx转化率在150~425 ℃时均保持在90% 以上,在200~400 ℃时则维持在95% 以上,达到最佳水平。随后,进一步增大WO3的掺杂量,催化剂的活性开始下降,活性温度区间也缩小。由此可见WO3掺杂对NOx转化率的促进作用存在一个极值点。对于纯CeO2催化剂和较低WO3掺杂量的0.1% WO3/CeO2催化剂而言,NOx转化率在高温段出现负值,这是由于具有较强氧化性的CeO2在高温下易催化NH3发生非选择性氧化这类副反应,并生成NOx。对于WO3/CeO2系列催化剂,若高温下NH3被氧化成NOx的比例上升,则相应温度段的NOx转化率就会下降[12]。
|
图 1 WO3/CeO2催化下NH3-SCR反应的NOx转化率 Fig.1 NOx conversion of NH3-SCR reaction catalyzed by WO3/CeO2 |
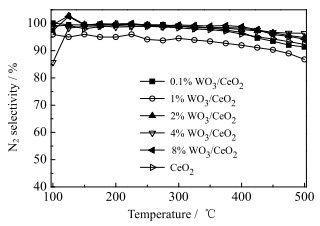
图 2为WO3掺杂对CeO2系列催化剂的N2选择性的影响。总体而言,各催化剂的N2选择性随反应温度升高而逐渐降低,但是下降幅度有所差异:4% WO3/CeO2的N2选择性在100~400 ℃时保持近100%,400 ℃以后略微下降到90%;而其他催化剂的N2选择性400 ℃以后出现了明显下降,造成这种现象的原因主要是不同催化剂高温段的非选择性氧化能力存在差异。总之,该系列催化剂在高温段(400~500 ℃)的N2选择性曲线走势与NOx转化率曲线走势基本一致,两者呈正相关。
|
图 2 NH3-SCR反应中WO3/CeO2催化剂的N2选择性 Fig.2 N2 selectivity of NH3-SCR reaction catalyzed by WO3/CeO2 |
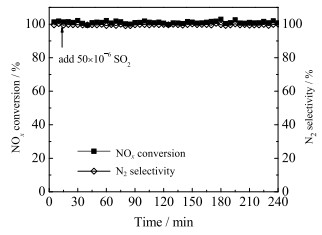
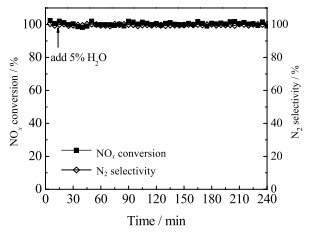
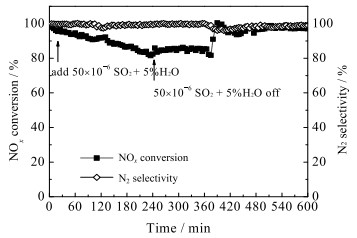
图 3为300 ℃下通入SO2体积分数为50 ×10-6的混合气体时,4% WO3/CeO2抗SO2中毒性能测试结果。由图可见,0~240 min时催化剂的NOx转化率和N2选择性均保持不变,并一直维持在100% 左右,说明该催化剂具有优异的抗SO2中毒性能。图 4考察了300 ℃下通入水蒸气体积分数为5% 的混合气体时,4% WO3/CeO2的抗H2O中毒性能。经过240 min反应时间,NOx转化率及N2选择性均为100% 左右,且未随反应时间延长而降低,表明4% WO3/CeO2有着优异的抗H2O中毒性能。图 5考察了300 ℃下通入SO2体积分数为50 ×10-6和水蒸气体积分数为5% 的混合气体时,4% WO3/CeO2的抗SO2 + H2O中毒性能。0~240 min时,NOx转化率逐渐下降,而N2选择性则维持在近100%,这是因为SO2、H2O同时存在会与NH3在催化剂表面生成NH4HSO4和(NH4)2S2O7等物质,导致反应活性位被堵塞[13-14]。但是当停止通入SO2和H2O后,催化剂的NOx转化率恢复至100%,说明SO2和H2O对4% WO3/CeO2催化剂的中毒反应都是可逆的。
|
图 3 4% WO3/CeO2的抗SO2中毒性能 Fig.3 Anti-SO2 poisoning performance of 4% WO3/CeO2 |
|
图 4 4% WO3/CeO2的抗H2O中毒性能 Fig.4 Anti-H2O poisoning performance of 4% WO3/CeO2 |
|
图 5 4% WO3/CeO2的抗SO2+H2O中毒性能 Fig.5 Anti-SO2 + H2O poisoning performance of 4% WO3/CeO2 |
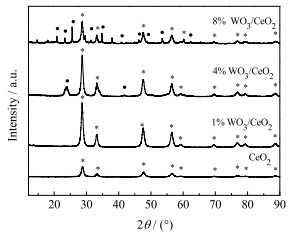
CeO2、1% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2的XRD表征结果如图 6所示,在2θ为28.7°、33.3°、47.6°、56.5°、59.2°、69.6°、76.7°、79.1°、88.4°处所有催化剂均出现了X射线衍射峰,分别对应于CeO2的(111)、(200)、(220)、(311)、(222)、(400)、(331)、(420)、(222)晶面,这表明纯CeO2催化剂和不同WO3掺杂改性的CeO2催化剂晶体均为立方萤石晶体结构[15]。但是,WO3掺杂改性使得CeO2的峰值强度变大,根据谢乐计算公式可知CeO2立方体的晶体尺寸变大。由于W6+离子半径(0.06 nm)小于Ce4+离子半径(0.09 nm),推测负载的WO3没有掺入CeO2晶格中形成固溶体[16],所以,图 6中的衍射曲线上既未观察到由于WO3掺杂改性引发的立方萤石结构CeO2衍射峰的明显移动,也未观察到CeO2混合固溶体(例如Ce2(WO4)3或钨酸铈)的新衍射峰。然而,当WO3负载量继续增加至4% 时,检测到单斜WO3晶体特征峰,如图中·处所示,并且WO3衍射峰强度随其负载量增多而增强,说明其分散度在下降[17],且部分WO3在CeO2表面发生团聚,但是4% WO3/CeO2催化剂出现的2个WO3晶体特征峰仍表现出最佳的NH3-SCR催化性能,说明WO3的团聚并不是导致高含量WO3掺杂催化剂活性降低的关键因素。
|
图 6 WO3/CeO2的粉末多晶X射线衍射图谱 Fig.6 Powder polycrystalline X-ray diffraction pattern of WO3/CeO2 |
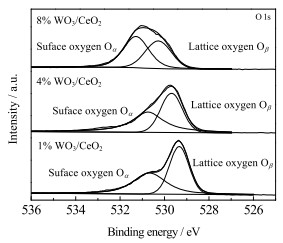
图 7、8和9考察了1% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2催化剂的X射线光电子能谱图(XPS)。其中O 1s图谱如图 7所示,Oβ表示晶格氧的能谱峰,Oα表示表面化学活性氧(─OH, O2)的能谱峰[18-19]。表面化学活性氧升高有益于催化剂将NO氧化为NO2、促进“快速SCR”(fast-SCR)反应的发生,从而能够大幅度提高中低温催化活性[20-21]。通过峰面积分别对不同氧物种进行定量分析,积分计算出1% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2的表面化学活性氧占比Oα/(Oα+Oβ)依次为46%、52%、46%,很明显4% WO3/CeO2表面化学活性氧最多、催化活性最好,这表明表面化学活性氧对SCR反应过程至关重要。
|
图 7 WO3/CeO2的X射线光电子能谱O1s Fig.7 X-ray photoelectron spectroscopy results of WO3/CeO2 Ols |
|
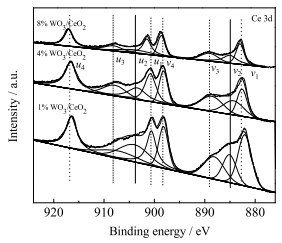
图 8 WO3/CeO2的X射线光电子能谱Ce3d Fig.8 X-ray photoelectron spectroscopy results of WO3/CeO2 Ols Ce3d |
|
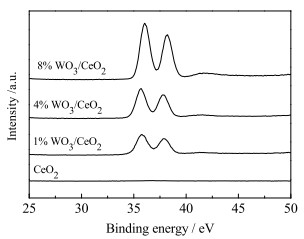
图 9 WO3/CeO2的X射线光电子能谱W4f Fig.9 X-ray photoelectron spectra of WO3/CeO2 W4f |
图 8为具有不同WO3掺杂量的CeO2催化剂的Ce3d图谱,由于Ce元素特征光电子所在的3d轨道存在轨道分裂,出峰较为复杂,故对Ce3d出峰进行了分峰拟合。图中的u和v分别表示Ce 3d3/2和Ce 3d5/2自旋轨道峰,其中u4、u3、u1、v4、v3、v1是Ce4+的特征峰,u2、v2则是Ce3+的特征峰[22]。Ce3+的存在会引起CeO2晶体内部电荷不平衡,从而形成不饱和化学键,而不饱和化学键的出现能诱导氧气等分子在催化剂表面(氧空位/缺陷)形成化学活性氧,参与SCR反应中的氧化还原循环过程[23]。通过对不同的Ce物种峰面积积分可得,1% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2催化剂的Ce3+物质的量与Ce3+和Ce4+总物质的量之比分别为23%、32%、22%,可见,4% WO3/CeO2催化剂的表面Ce3+最多,意味着其表面化学活性氧最多,这与O1s的表征结果一致。由此可以得出以下结论:WO3掺杂量存在一个最优值。最优值之前,WO3掺杂量越多,催化剂表面化学活性氧数量越多、催化剂活性越强;极值点之后,WO3掺杂量越多,催化剂表面化学活性氧数量之越少、催化剂活性越弱。综上所述,Ce3+和表面化学活性氧是影响WO3掺杂改性的CeO2催化剂的NH3-SCR反应活性的关键因素。
图 9为CeO2、1% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2的W4f图谱,处于32~40 eV的2个主峰代表W4f 7/2(大约35.6 eV)和W4f 5/2(大约37.6 eV),均为W6+的能谱峰[24]。由图可见,随着WO3掺杂量增加,W4f 7/2和W4f 5/2的峰面积增大。
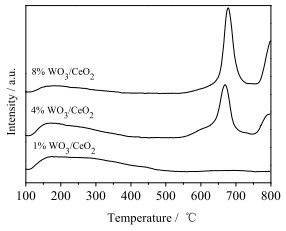
3.5 WO3/CeO2的表面酸性分析图 10为WO3掺杂改性的3种CeO2催化剂(1% WO3/CeO2、4% WO3/CeO2、8% WO3/CeO2)的表面酸性NH3-TPD曲线。图中处于150~200 ℃的脱附峰代表弱酸性位,处于600~800 ℃的脱附峰代表强酸性位。显然,WO3的掺杂有效增强了CeO2表面的强酸性位。对脱附峰峰面积进行积分以便定量分析表面酸性位,积分结果为4% WO3/CeO2 > 8% WO3/CeO2 > 1% WO3/CeO2,可知,4% WO3/CeO2催化剂的表面酸量最多。大部分文献研究结果表明[25-26],低温脱附峰主要与Lewis酸性位相对应,而高温脱附峰主要与Brönsted酸性位相关。由图 10各曲线的出峰位置以及峰面积定量计算可得出,随WO3掺杂量增大,催化剂表面出现了Brönsted酸性位并且含量逐渐上升,催化剂表面酸性位由以Lewis酸性位为主逐渐转变为以Brönsted酸性位为主。上述表征结果说明WO3掺杂量对表面酸量的作用存在极值点,当适量地掺杂WO3时表面出现大量Brönsted酸性位,从而使表面总酸量出现最大值。相关研究表明Brönsted酸性位更有利于反应物种NH3在催化剂表面的吸附和储存[27-30],进一步结合该系列催化剂的活性测试结果,当催化剂表面的主要酸性位由Lewis酸性位转变为Brönsted酸性位后,其催化活性大幅上升,说明Brönsted酸性位是影响WO3/CeO2催化活性的关键因素。
|
图 10 WO3/CeO2的氨气程序升温脱附曲线 Fig.10 NH3-temperature programmed desorption curves of WO3/CeO2 |
本研究通过浸渍法合成了不同WO3掺杂量的CeO2催化剂,并筛选出最佳WO3掺杂量的催化剂为4% WO3/CeO2,该催化剂在150~425 ℃的宽温度区间NOx转化率和N2选择性均保持在90% 以上,并且拥有较好的抗SO2和H2O中毒性能。相对于其他WO3掺杂量的催化剂,该催化剂拥有更多的表面化学活性氧和Ce3+物种,能够促进“fast-SCR”反应的进行,从而大幅提升了催化剂的中、低温催化活性。WO3掺杂导致催化剂表面酸性位由以Lewis酸性位为主逐渐转变为以Brönsted酸位为主、酸性位数量增加、强度增强,从而增强了反应物种NH3在催化剂表面的吸附活化过程,进而提高了催化剂的NH3-SCR活性。该催化剂制作成本低廉、合成方法简单,拥有较强的应用前景。
| [1] |
王旭睿. 氮氧化物危害及处理方法[J]. 当代化工研究, 2018(10): 116-117. WANG X R. The hazards and treatment methods of nitrogen oxides[J]. Modern Chemical Research, 2018(10): 116-117. DOI:10.3969/j.issn.1672-8114.2018.10.070 |
| [2] |
WANG X X, CONG Q L, CHEN L, et al. The alkali resistance of CuNbTi catalyst for selective reduction of NO by NH3: A comparative investigation with VWTi catalyst[J]. Applied Catalysis B: Environmental, 2019, 246: 166-179. DOI:10.1016/j.apcatb.2019.01.049 |
| [3] |
郭艳军, 陈昊宇, 刘超. 能源相关的氮氧化物排放现状与控制研究[J]. 建筑热能通风空调, 2018, 37(9): 48-51. GUO Y J, CHEN H Y, LIU C. The study on current status and control of energy-related nitrogen oxide emissions[J]. Building Energy & Environment, 2018, 37(9): 48-51. DOI:10.3969/j.issn.1003-0344.2018.09.012 |
| [4] |
李威. 低温SCR脱硝催化剂的分析及研究[J]. 化工管理, 2019(25): 75-76. LI W. Analysis and research of low temperature SCR denitrification catalyst[J]. Chemical Enterprise Management, 2019(25): 75-76. DOI:10.3969/j.issn.1008-4800.2019.25.048 |
| [5] |
LI S J, WANG X, TAN S, et al. CrO3 supported on sargassum-based activated carbon as low temperature catalysts for the selective catalytic reduction of NO with NH3[J]. Fuel, 2017, 191(12): 511-517. |
| [6] |
REDDY B M, KHAN A, YAMADA Y, et al. Structural characterization of CeO2 -TiO2 and V2O5/CeO2-TiO2 catalysts by raman and XPS techniques[J]. The Journal of Physical Chemistry B, 2003, 107(22): 5162-5167. DOI:10.1021/jp0344601 |
| [7] |
YANG S X, ZHU W P, JIANG Z P, et al. The surface properties and the activities in catalytic wet air oxidation over CeO2-TiO2 catalysts[J]. Applied Surface Science, 2006, 252(24): 8499-8505. DOI:10.1016/j.apsusc.2005.11.067 |
| [8] |
张志平, 杨飘萍. Ce基低温NH3-SCR催化剂的研究进展[J]. 黑龙江大学自然科学学报, 2018, 35(5): 539-547. ZHANG Z P, YANG P P. Research of Ce-based catalysts for the low temperature NH3-SCR[J]. Journal of Natural Science of Heilongjiang University, 2018, 35(5): 539-547. |
| [9] |
WU Z H, ZENG Y Q, SONG F J, et al. Active sites assembly effect on CeO2-WO3-TiO2 catalysts for selective catalytic reduction of NO with NH3[J]. Molecular Catalysis, 2019, 479: 100-108. |
| [10] |
CHEN L, WENG D, WANG J, et al. Low-temperature activity and mechanism of WO3-modified CeO2-TiO2 catalyst under NH3-NO/NO2 SCR conditions[J]. Chinese Journal of Catalysis, 2018, 39(11): 1804-1813. DOI:10.1016/S1872-2067(18)63129-8 |
| [11] |
SHIN B, LEE H, PARK H. Catalytic activity and surface characteristics of WO3-doped MnOx-TiO2 catalysts for low-temperature selective catalytic reduction of NOx with NH3[J]. Korean Journal Metals Materials, 2016, 54(10): 787-792. DOI:10.3365/KJMM.2016.54.10.787 |
| [12] |
XIE L J, LIU F D, SHI X Y, et al. Effects of post-treatment method and Na co-cation on the hydrothermal stability of Cu-SSZ-13 catalyst for the selective catalytic reduction of NOx with NH3[J]. Applied Catalysis B: Environmental, 2015, 179: 206-212. DOI:10.1016/j.apcatb.2015.05.032 |
| [13] |
HUANG Z, LI H, GAO J, et al. Alkali- and sulfur-resistant tungsten-based catalysts for NOx emissions control[J]. Environment Science & Technology, 2015, 49(24): 14460-14465. |
| [14] |
SHI Y J, SHU H, ZHANG Y H, et al. Formation and decomposition of NH4HSO4 during selective catalytic reduction of NO with NH3 over V2O5-WO3/TiO2 catalysts[J]. Journal of Fuel & Processing Technology, 2016, 150: 141-147. |
| [15] |
CONG Q L, CHEN L, WANG X X, et al. Promotional effect of nitrogen-doping on a ceria unary oxide catalyst with rich oxygen vacancies for selective catalytic reduction of NO with NH3[J]. Chemical Engineering Journal, 2020, 379: 122302. DOI:10.1016/j.cej.2019.122302 |
| [16] |
IWASAKI M, DOHMAE K, NAGAI Y, et al. Experimental assessment of the bifunctional NH3-SCR pathway and the structural and acid-base properties of WO3, dispersed on CeO2, catalysts[J]. Journal of Catalysis, 2018, 359: 55-67. DOI:10.1016/j.jcat.2017.12.032 |
| [17] |
LIU S, ZHANG R, LI P, et al. Morphology effect of diverse ceria with active tungsten species on NH3-SCR behaviors[J]. Catalysis Today, 2019, 339: 241-253. |
| [18] |
HOLGADO J P, MUNUERA G, ESPINÓS J P, et al. XPS study of oxidation processes of CeOx defective layers[J]. Applied Surface Science, 2000, 158(1/2): 164-171. |
| [19] |
FAÏ LARACHI A, PIERRE M, ADNOT A, et al. Ce 3d XPS study of composite CexMn1-xO2-y wet oxidation catalysts[J]. Applied Surface Science, 2002, 195(1/2/3/4): 236-250. |
| [20] |
WANG X X, SHI Y, LI S J, et al. Promotional synergistic effect of Cu and Nb doping on a novel Cu/Ti-Nb ternary oxide catalyst for the selective catalytic reduction of NOx with NH3[J]. Applied Catalysis B: Environmental, 2018, 220: 234-250. DOI:10.1016/j.apcatb.2017.08.021 |
| [21] |
KANG M, PARK E D, KIM J M, et al. Manganese oxide catalysts for NOx reduction with NH3 at low temperatures[J]. Applied Catalysis A: General, 2007, 327(2): 261-269. DOI:10.1016/j.apcata.2007.05.024 |
| [22] |
PENG Y, LI K, LI J. Identification of the active sites on CeO2-WO3 catalysts for SCR of NOx with NH3: An in situ IR and Raman spectroscopy study[J]. Applied Catalysis B: Environmental, 2013, 140: 483-492. |
| [23] |
CHEN L, LI J H, GE M F. The poisoning effect of alkali metals doping over nano V2O5-WO3/TiO2 catalysts on selective catalytic reduction of NOx by NH3[J]. Chemical Engineering Journal, 2011, 170(2/3): 531-537. |
| [24] |
SI Z C, WENG D, WU X D, et al. Roles of Lewis and Bronsted acid sites in NO reduction with ammonia on CeO2-ZrO2-NiO-SO42-catalyst[J]. Journal of Rare Earths, 2010, 28(5): 727-731. DOI:10.1016/S1002-0721(09)60189-7 |
| [25] |
DONG W, YUE P, YANG Q L, et al. NH3-SCR performance of WO3 blanketed CeO2 with different morphology: Balance of surface reducibility and acidity[J]. Catalysis Today, 2019, 332(15): 42-48. |
| [26] |
ZHANG T, QU R Y, SU W K, et al. A novel Ce-Ta mixed oxide catalyst for the selective catalytic reduction of NOx with NH3[J]. Applied Catalysis B Environmental, 2015, 176/177: 338-346. DOI:10.1016/j.apcatb.2015.04.023 |
| [27] |
LIANG C, LI J H, MAO F G. DRIFT study on cerium-tungsten/titiania catalyst for selective catalytic reduction of NOxwith NH3[J]. Environmental Science & Technology, 2010, 44(24): 9590-9596. |
| [28] |
MARBERGER A, FERRI D, ELSENER M, et al. The significance of Lewis acid sites for the selective catalytic reduction of nitric oxide on vanadium-based catalysts[J]. Angewandte Chemie-International Edition, 2016, 55(39): 11989-11994. DOI:10.1002/anie.201605397 |
| [29] |
YU K, WEN J H, SI C L. Surface acidity enhancement of CeO2 catalysts via modification with a heteropoly acid for the selective catalytic reduction of NO with ammonia[J]. Catalysis Science & Technology, 2019, 9(20): 5774-5785. |
| [30] |
CHEN L, WANG X X, CONG Q L, et al. Design of a hierarchical Fe-ZSM-5@CeO2 catalyst and the enhanced performances for the selective catalytic reduction of NO with NH3[J]. Chemical Engineering Journal, 2019, 369: 957-967. DOI:10.1016/j.cej.2019.03.055 |




