天然气脱水方法有溶剂吸收法、固体吸附法和冷却分离法等[1, 2]。溶剂吸收法是目前使用最广泛的天然气脱水方法,而国内三甘醇法最为普遍,其具有吸收能力强、成本低、易再生和运行可靠等优点,但其再生能耗大,脱水能力易受外来杂质以及自身降解产物等影响,进而导致溶液失活[3, 4]。
三甘醇杂质主要包括固体悬浮物、热稳定盐、有机杂质等,生产过程中可通过强化在线过滤和离子交换处理措施等方法减缓或避免固体悬浮物和热稳定盐的产生和累积[5]。而三甘醇降解产物是一类无法有效去除的有机杂质,一般来源于热降解、氧化降解和化学降解[6, 7]。由于三甘醇脱水过程是净化工段的最后一步,故化学降解不易发生。在生产过程中,三甘醇降解是溶液损耗严重、发生失活的一个重要原因,脱水系统中氧气进入或再生温度偏高都会引起三甘醇的氧化变质、脱水缩合或热分解[8]。目前,对于三甘醇降解特性及防控措施少有研究[9~11]。
不同的杂质对三甘醇脱水能力的抑制作用程度不一,如何从中找出影响三甘醇脱水能力的关键因素和探索不同杂质对溶液失活度的影响规律是三甘醇失活研究的重点[12]。此外,热重分析是研究物质受热分解和氧化分解过程规律的重要手段,可通过分析热重曲线来研究物质随温度的变化过程,估算分解反应活化能,判断分解反应机理及影响因素[13~15]。
本文在XRD、IC和GC-MS检测三甘醇杂质成分的基础上,利用三甘醇溶液失活评价装置探讨不同含量杂质成分对三甘醇失活度的影响规律,并借助热重分析法对三甘醇的降解特性进行研究,初步探索三甘醇降解动力学并提出避免三甘醇降解失活的措施,为后续三甘醇溶液净化及更换提供理论支撑。
2 实验部分 2.1 试剂与仪器鄂尔多斯某净化厂提供的失活三甘醇;硫化亚铁、四氧化三铁、碳化铁、氯化钠、氯化钾、氯化钙、氯化镁、硫酸钠、氯化钡、氟化钠、氯化铁、氯化亚铁、甲苯、N-甲基二乙醇胺、二甘醇、乙二醇、乙二酸和甘醇酸,分析纯,天津市科密欧化学试剂有限公司;其余试剂均为市售分析纯。美国TA公司Q500型TGA热重分析仪;若干温度计、压力表、流量计、温度及压力变送器和水分分析仪。
2.2 三甘醇杂质测定固体悬浮物采用日本理学D\max-2550 X射线衍射仪测定。热稳定盐采用TH-980C离子色谱仪测定。有机杂质采用气质联用仪(GC为美国Agilent 6890;MS为美国Agilent 5973)测定。
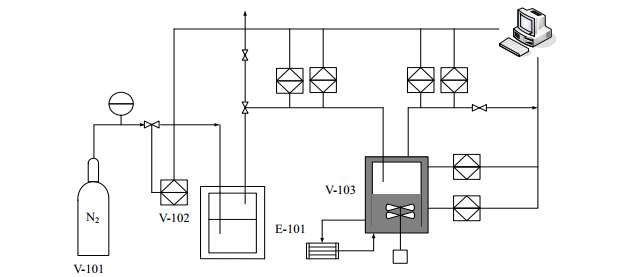
2.3 三甘醇失活评价三甘醇溶液失活评价装置由温度控制系统、压力控制系统、溶液吸收系统、数据采集系统和在线分析系统组成,见图 1。根据三甘醇实际脱水工况选择操作温度为30℃,操作压力为6.8 MPa,有效体积为300 mL,内置鼓泡吸收管和磁力搅拌器,控制系统温度为5~80℃,精度为±0.1 ℃,通过背压阀控制压力为0~10 MPa,精度为±0.1 MPa。分别将CPLWQ型气体流量计、PT100型温度变送器、3051TA型压力变送器以及EEXD型水分在线分析仪经数据采集系统与微机相连,对整个装置进行监测[16]。
|
图 1 三甘醇溶液失活评价装置图 Fig.1 Schematic diagram of the experimental setup for TEG solution inactivation evaluation V-101:nitrogen cylinder V-102:moisture generator V-103:high-pressure reactor E-101:super thermostat water bath |
该装置以高纯携水氮气模拟湿天然气,以鼓泡方式将其缓慢通入新鲜三甘醇溶液以及含有不同杂质的三甘醇溶液中,污染物的加入种类与含量范围根据检测结果确定。通过取样口实时在线采集、分析吸收前后气体中的水分含量,待吸收时间大于30 min后,当吸收前后的水分含量基本不变时,即可停止实验。每组实验平行3次,由差量法得到三甘醇溶液脱水能力变化即失活度φ,其计算公式为式(1):
| $ \varphi = 1-\frac{{{{c'}_0}{{q'}_{\rm{v}}}t'-\int_0^{t'} {c'{{q'}_{\rm{v}}}{\rm{d}}t'} }}{{{c_0}{q_{{\rm{v}}0}}t-\int_0^t {c{q_{\rm{v}}}{\rm{d}}t} }} $ | (1) |
式中,c0、c0′分别为在空白和杂质实验条件下吸收前气体中水的摩尔分数;c、c′分别为在空白和杂质实验条件下吸收后t、t′时刻气体中水的摩尔分数;qV0为在空白实验条件下吸收前气体的摩尔流量,mol·min-1;qV、qV′分别为在空白和杂质实验条件下吸收后t、t′时刻气体的摩尔流量,mol·min-1。
2.4 三甘醇降解分析准确称取20 mg三甘醇,采用美国TA公司Q500型TGA同步热重分析仪分别在氮气、氧气气氛下以5,10,15℃·min-1的升温速率将三甘醇由室温升至350℃,气体流量为100.0 mL·min-1。对三甘醇降解过程进行动力学分析,并分别通过Coats-Redfer法和分布活化能模型(DAEM)法研究三甘醇的降解行为,以获得降解过程的降解级数、反应活化能及其分布等动力学参数。
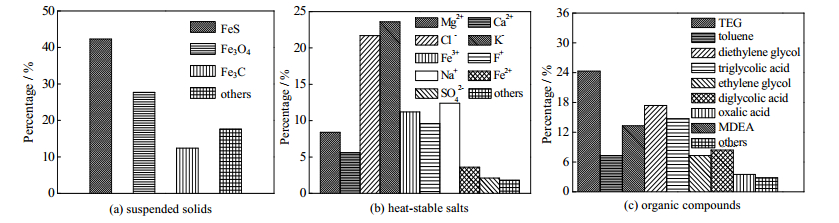
3 结果与讨论 3.1 三甘醇杂质分析与失活评价结果对失活三甘醇溶液进行检测与分析,其杂质成分分析结果见图 2。利用失活评价装置对各杂质成分在不同含量下对三甘醇溶液失活度的影响规律结果见图 3,其多因素方差分析结果见表 1。
|
图 2 失活三甘醇溶液中各杂质分析结果 Fig.2 Mass percentages of contaminations in inactive TEG solutions |
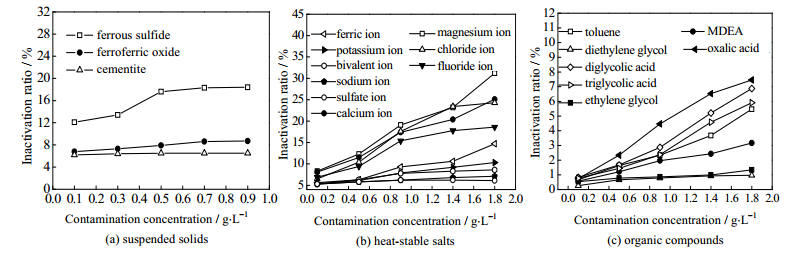
|
图 3 各污染物在不同含量下对三甘醇溶液失活度的作用规律 Fig.3 Effects of contaminant concentration on the inactivation of TEG solutions |
| 表 1 各污染物在不同含量下对三甘醇溶液失活度的影响大小 Table 1 Effects of contamination concentrations on the inactivation of TEG solutions |
由图 2可知,失活三甘醇溶液中,固体悬浮物主要包括FeS、Fe3O4及Fe3C,尤以FeS居多,湿气中携带和溶解于三甘醇中的H2S将直接导致装置管线发生金属腐蚀,腐蚀产物剥落后混入三甘醇溶液,成为固体悬浮物的主要来源。热稳定盐以Ca2+、Mg2+、Cl-和F-为主,大多源于采出天然气携带的高矿化度地层水。有机杂质主要包括二甘醇、二甘醇酸、乙二醇、乙二酸、甲苯和N-甲基二乙醇胺,其中,N-甲基二乙醇胺和甲苯是天然气集输和脱酸过程的抑制剂或吸收剂,而甘醇类及有机酸类杂质是三甘醇溶液中的主要降解产物。一方面,在固体悬浮物以及热稳定盐等杂质条件下,三甘醇解吸再生过程易出现换热器堵塞、塔板结焦等问题,特别是三甘醇与热稳定盐形成络合物,改变长链结构,严重抑制其脱水作用[17]。
另一方面,尽管失活三甘醇溶液仍含有约24 %的有效成分,但随着脱水系统长周期运行,三甘醇在氧化及受热作用下将不断发生氧化降解、热降解和脱水缩合等反应而生成有机酸或高聚物等,严重影响三甘醇脱水性能,最终导致三甘醇溶液失活[8]。
由图 3及表 1可知,除Fe3O4、Fe3C、Na+和SO42-以外的各杂质的F检验值均大于其临界值F0.01(4,10)=5.99,且概率p全部小于临界值0.01,这说明大部分杂质都能加剧三甘醇溶液的失活。其中,乙二酸、甘醇酸类、Mg2+、Ca2+和FeS对三甘醇溶液失活的影响最为显著。为确保三甘醇脱水效果良好,有效避免或减缓三甘醇溶液失活,需严格控制三甘醇溶液中的固体悬浮物(如FeS)、热稳定盐(如Mg2+和Ca2+等)和有机杂质(如乙二酸及甘醇酸类)等杂质的含量。
此外,针对固体悬浮物和热稳定盐可采用多级过滤措施和深层离子交换技术有效去除,而对于有机杂质,尤其是显著影响溶液失活的三甘醇降解产物如乙二酸以及甘醇酸类的去除尚无理想方法[18]。鉴于上述原因,本文将在不同条件下研究三甘醇溶液的降解特性和降解动力学,旨在提出避免三甘醇降解失活的措施,为后续三甘醇溶液净化及更换提供一定理论支撑。
3.2 三甘醇溶液降解特性研究 3.2.1 三甘醇降解过程分析利用同步热重分析仪对三甘醇溶液在连续升温条件下的热降解和氧化降解过程进行了研究。在氮气、氧气气氛下,分别以5,10,15℃·min-1的升温速率将三甘醇由室温升至350℃,其热失重及热失重速率曲线见图 4和图 5。
|
图 4 氮气与氧气气氛下三甘醇的TG曲线 Fig.4 TG curves of TEG under nitrogen and oxygen atmosphere |
|
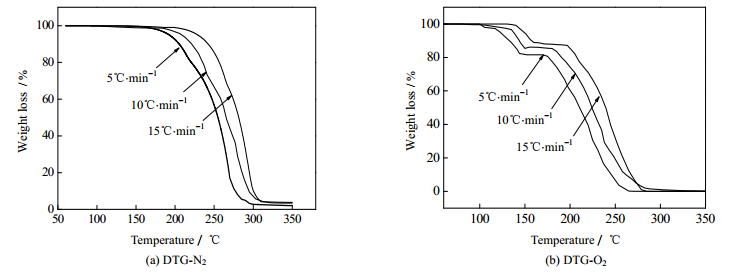
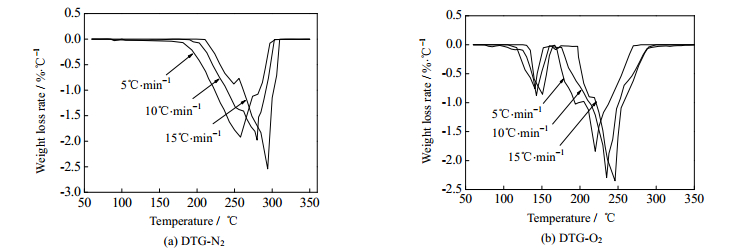
图 5 氮气与氧气气氛下三甘醇的DTG曲线 Fig.5 DTG curves of TEG under nitrogen and oxygen atmosphere |
由图 4(a)与图 5(a)可知,三甘醇在氮气气氛下的降解是一步质量损失过程,其初始分解温度约为202℃,其降解主要发生在202~304℃。升温速率从5℃·min-1升至15℃·min-1时的最大热降解速率由1.92%℃·min-1增至2.57% ℃·min-1,并且在254℃、279℃和293℃时达到最大热降解速率;320℃后曲线趋于平缓,剩余残渣含量约为3.41 %,是三甘醇的高温聚合产物。
由图 4(b)和图 5(b)可知,三甘醇在氧气气氛下的降解分两部分完成,在125~160℃时发生第一步降解,为快速降解阶段,且失重比例较小,占总失重的3%~16%,可能是两个醇羟基上的氧化反应[21];在170~285℃发生第二步降解,为主要失重阶段,约85 %的失重在这一阶段发生,且在220℃、235℃和246℃达到最大降解速率,终温时三甘醇已分解完全;该阶段主要为羟基脱水、碳氮键断裂以及易挥发物质生成[22, 23]。
此外,三甘醇降解的初始温度、失重峰温度、降解终温和最大失重速率均随着升温速率的加快向高温方向移动。这表明相同失重率下所需温度会随升温速率的加快而升高,这是由于升温速率加快时,样品内部受热不均无法吸收充足热量,而需要更多热量使其分解[19, 20]。
3.2.2 三甘醇降解动力学分析初始质量为m0的样品,在某一时刻t时质量为m,则其分解速率可表示为
| $ \frac{{{\rm{d}}\alpha }}{{{\rm{d}}t}} = kf(\alpha ) $ | (2) |
式中,α为分解程度,即
| $ \frac{{\rm{d}}{\alpha }}{{\rm{d}}{t}} = kf(\alpha ) = A{\rm{exp}}(-\frac{{{E_a}}}{{RT}}){(1-\alpha )^n} $ | (3) |
当升温速率β为一定值,即
| $ \int_0^\infty {\frac{{\rm{d}}{\alpha }}{{{{(1-\alpha )}^n}}}} = \frac{A}{\beta }\int_{{T_0}}^T {{\rm{exp}}(-\frac{{{E_a}}}{{RT}}){\rm{d}}T} $ | (4) |
由于初始温度T0较低,分解速率很小,可忽略不计,故有
| $ \int_0^\infty {\frac{{\rm{d}}{\alpha }}{{{{(1-\alpha )}^n}}}} = \frac{A}{\beta }\int_0^T {{\rm{exp}}(-\frac{{{E_a}}}{{RT}}){\rm{d}}T} $ | (5) |
由于动力学模型处理方法不同,结果也不同。故分别采用Coats-Redfer法和分布活化能模型(DAEM)法对三甘醇的降解行为进行研究,以获得降解过程反应活化能及其分布。
Coats-Redfer法采用近似积分求解动力学参数,可反映降解机理[19, 24, 25]。其积分式如式(6)。
| $ \left\{ \begin{array}{l} n = 1 \;\; {\rm{{\rm{ln}}}}\left[{\frac{{-{\rm{ln}}(1-\alpha )}}{{{T^2}}}} \right] = {\rm{ln}}\left[{\frac{{AR}}{{\beta {E_a}}}\left( {1-\frac{{2RT}}{{{E_a}}}} \right)} \right] - \frac{{{E_a}}}{R}\frac{1}{T}\\ n \ne 1 \;\; {\rm{ln}}\left[{\frac{{{{(1-\alpha )}^{1-n}}-1}}{{(n - 1){T^2}}}} \right] = {\rm{ln}}\left[{\frac{{AR}}{{\beta {E_a}}}\left( {1-\frac{{2RT}}{{{E_a}}}} \right)} \right] -\frac{{{E_a}}}{R}\frac{1}{T} \end{array} \right. $ | (6) |
设n=1,对一般反应区和大部分Ea,
|
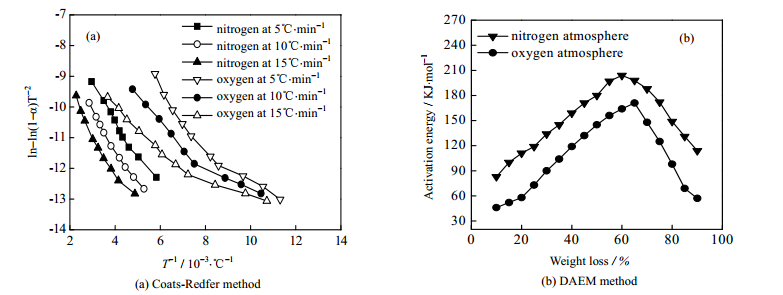
图 6 降解动力学模型的Coats-Redfer法拟合曲线和DAEM法活化能分布曲线 Fig.6 Fitting curves of degradation kinetic models by Coats-Redfer and DAEM methods |
| 表 2 Coats-Redfer法求出的降解动力学参数 Table 2 Kinetic parameters of pyrolysis calculated with Coats-Redfer method |
由表 2可知,氮气气氛下的三甘醇降解反应级数可视为1,氧气气氛下的三甘醇降解可近似视为两段降解级数为1的反应。该拟合曲线的相关系数均大于0.98,故降解级数假设合理。三甘醇在氧气气氛下第二阶段活化能与氮气气氛下的活化能接近,氧气气氛下第一阶段活化能较小。此外,三甘醇降解活化能随升温速率的提高而逐渐减小,这说明升温速率加快会加剧三甘醇的分解。
DAEM法是指分布活化能模型(Distributed Activation Energy Model),该模型认为降解是由无数个互相独立的一级反应构成,可用Gauss分布连续函数来描述其活化能[26, 27]。其积分式如式(7)。
| $ \frac{{{E_a}}}{R} =-\frac{{{\rm{dln}}\beta }}{{{\rm{d}}\left( {1/T} \right)}}-2T $ | (7) |
由不同升温速率下的失重曲线得到同一失重率下不同曲线上的温度,求得这一失重率下的活化能。由于右侧第一项远大于第二项,取温度平均值,将不同失重率对应活化能值作图,即得到失重过程中的活化能变化曲线,见图 6(b)。
由图 6(b)可知,活化能分布反映三甘醇降解包含分子键能断裂的一系列连续、复杂的反应过程。热降解在失重率60 %时有最大活化能204.82 kJ·mol-1,氧化降解在失重率65 %时有最大活化能171.43 kJ·mol-1。
此外,三甘醇氧化降解反应活化能明显低于热降解反应活化能,与Coats-Redfer法得到的规律相同,这说明空气中的氧对三甘醇的降解过程影响明显,三甘醇的氧化降解与热降解相比更容易发生。
综上所述,为了防止三甘醇自身降解,生产过程中应控制重沸器内三甘醇加热再生温度不能超过210℃,避免升温速率过快,并且严格防止氧气窜入再生系统中,造成三甘醇失活。
4 结论(1) 失活三甘醇溶液中的杂质主要包括固体悬浮物、热稳定盐和有机杂质;大部分杂质能加剧三甘醇溶液的失活。其中,乙二酸、甘醇酸类、Mg2+、Ca2+和FeS对三甘醇溶液失活的影响最为显著。应严格控制三甘醇中固体悬浮物(如FeS)、热稳定盐(如Mg2+、Ca2+)和有机杂质(如甘醇酸类)的含量。
(2) 三甘醇热降解是级数为1的一步质量损失过程,而氧化降解是两段级数为1的质量损失过程;升温速率的加快可促使三甘醇热解的初始温度、失重峰温度以及热解终温均向高温方向移动,即加剧三甘醇的分解。应控制重沸器内三甘醇加热再生温度不能超过210℃,并避免升温速率过快。
(3) 三甘醇在氧气气氛下第二阶段活化能与氮气气氛下的活化能接近,氧气气氛下第一阶段活化能较小。三甘醇氧化降解反应活化能明显低于热降解反应活化能,其氧化降解与热降解相比更容易发生。故应严格防止氧气窜入再生系统中,造成三甘醇失活。
符号说明:
| [1] | Satyro M A, Schoeggl F, Yarranton H W, et al. Temperature change from isenthalpic expansion of aqueous triethylene glycol mixtures for natural gas dehydration[J]. Fluid Phase Equilibria , 2011, 305(1): 62-67. DOI:10.1016/j.fluid.2011.03.011. |
| [2] | WEI Shou-xing(魏守幸). Research progress of natural gas dehydration technology(天然气脱水技术的研究进展)[J]. Coal and Chemical Industry(煤炭与化工) , 2015, 38(5): 5-8. |
| [3] | MAO Li-jun(毛立军), WANG Yong-liang(王用良), WU Yan(吴艳), et al. Discussion on new processes and new techniques of natural gas dehydration(天然气脱水新工艺技术探讨)[J]. Guangdong Chemical Industry(广东化工) , 2013, 40(8): 66-69. |
| [4] | Davoudi M, Safadoust A R, Mansoori S A A, et al. The impurities effect on thermal degradation and corrosivity of amine[J]. Journal of Natural Gas Science and Engineering , 2014, 19(19): 116-124. |
| [5] | Abukashabeh A S, Alhseinat E, Al-Asheh S, et al. Thermophysical properties of fresh and lean thermally degraded N-methyldiethanolamine[J]. Journal of Natural Gas Science and Engineering , 2014, 19(7): 317-323. |
| [6] | Shao Q J, Peng J X, Xu Q F, et al. Studyonpyrolysischaracteristicsand kinetics of bamboo underliner heating temperature[J]. ActaEnergiae Solaris Sinica , 2006, 27(7): 671-676. |
| [7] | Liu X G, Li B Q. Theoretical elucidation of distributed activation energy model and its application inchar gasification and simulation distillationsystems[J]. Journal of Fuel Chemistry and Technology , 2001, 29(1): 51-59. |
| [8] | GUO Bin(郭斌), HE Zhan-you(何战友), LIU Xue-rui(刘学蕊), et al. Study on the reason of TEG Vitiation and its recycling technology(郭斌, 何战友, 刘学蕊, 等三甘醇失效原因分析及回收研究)[J]. Natural Gas Industry(天然气工业) , 2006, 26(9): 152-153. |
| [9] | NIE Chong-bin(聂崇斌). The degradation of alcohol amine desulfurization solution and the resurrection(醇胺脱硫溶液的降解和复活)[J]. Oil and natural gas chemical industry(石油与天然气化工) , 2012, 41(2): 164-168. |
| [10] | Fredriksen S B, Jens K J. Oxidative degradation of aqueous amine solutions of MEA, AMP, MDEA, Pz:a review[J]. Energy Procedia , 2013, 37(11): 1770-1777. |
| [11] | YE Qing-guo(叶庆国), ZHANG Shu-sheng(张书圣). The methyldiethanolamine degradation products in desulphurization process for acid waste gas(酸性废气脱硫工艺中N-甲基二乙醇胺降解反应产物的研究)[J]. Journal of Chemical Enginering of Chinese Universities(高校化学工程学报) , 2001, 15(1): 35-39. |
| [12] | CHEN Geng-liang(陈赓良). Technical progress of TEG dehydration process in natural gas industry(天然气三甘醇脱水工艺的技术进展)[J]. Chemical engineering of oil & gas(石油与天然气化工) , 2015, 44(6): 1-9. |
| [13] | LI Chun-hua(李春华), ZHANG Min-hua(张敏华), JIANG Hao-xi(姜浩锡), et al. Thermogravimetric kinetics of polystyrene degradation over BaO(氧化钡催化降解聚苯乙烯的热分析动力学)[J]. Journal of Chemical Enginering of Chinese Universities(高校化学工程学报) , 2009, 23(1): 171-174. |
| [14] | WANG Gang(王刚), LI Ai-ming(李爱民), LI Jian-feng(李建丰). Devolatilization of PLA investigated by TG/FT-IR, Py-GC/MS analysis(基于TG/FT-IR, Py-GC/MS的聚乳酸塑料热降解研究)[J]. Journal of Chemical Enginering of Chinese Universities(高校化学工程学报) , 2009, 23(6): 957-961. |
| [15] | Yin D J, Zhang L Z, Zhao X F, et al. Iron-glutamate-silicotungstate ternary complex as highly active heterogeneous Fenton-like catalyst for 4-chlorophenol degradation[J]. Chinese Journal of Catalysis , 2015, 36(12): 2203-2210. DOI:10.1016/S1872-2067(15)61011-7. |
| [16] | FAN Zheng(范峥), HUANG Feng-lin(黄风林), WANG Di(王迪), et al. Inactivation analysis and degradation mechanism of natural gas desulfurized solutions(天然气脱硫溶液失活原因分析与降解机理研究)[J]. Journal of Chemical Enginering of Chinese Universities(高校化学工程学报) , 2016, 30(6): 1436-1444. |
| [17] | ZHAO Huan-juan(赵欢娟), XIA Yong(夏勇), ZHANG Di(张迪), et al. Influence of contaminants on TEG dehydration performance(杂质对三甘醇脱水能力的影响研究)[J]. Natural Gas Chemical Industry(天然气化工) , 2016, 41(2): 47-51. |
| [18] | CHEN Xiu-na(陈秀娜), FAN Zheng(范峥), LI Wen-hong(李稳宏), et al. Operation analysis and optimization research of natural gas dehydration system(天然气脱水系统现状分析及优化)[J]. Chemical Industry and Engineering Progress(化工进展) , 2012, 31(11): 2449-2454. |
| [19] | ZHENG Zhi-feng(郑志锋), HUANG Yuan-bo(黄元波), JIANG Jian-chun(蒋剑春), et al. Walnut shell pyrolysis characteristic and several dynamic model results(核桃壳热解特性及几种动力学模型结果比较)[J]. ActaEnergiae Solaris Sinica(太阳能学报) , 2011, 32(11): 1677-1682. |
| [20] | Wang C P, Wang F Y, Yang Q R, et al. Thermogravimetric studies of the behavior of wheat straw with added coal during combustion[J]. Biomass and Bioenergy , 2009, 33(1): 50-56. DOI:10.1016/j.biombioe.2008.04.013. |
| [21] | MA Chuan(马川), SUN Lu-shi(孙路石), JIN Li-mei(金立梅), et al. Pyrolysis kinetics modeling of flame retardant HIPS(阻燃HIPS塑料热解动力学模型)[J]. Journal of Chemical Industry and Engineering(化工学报) , 2014, 65(9): 3479-3484. |
| [22] | Wan Nik W B, Ani F N, Masjuki H H. Thermal stabilityevaluation of palm oil as energy transport media[J]. Energy Conversion and Management , 2005, 46(13/14): 2198-2215. |
| [23] | FU Xin-min(付兴民), XU Guo-huan(徐国欢), YANG Di(杨迪), et al. Adhesive waste pyrolysis coke combustion characteristic(不干胶废弃物热解焦燃烧特性)[J]. Chinese Journal of Environmental Engineering(环境工程学报) , 2015, 9(3): 1445-1450. DOI:10.12030/j.cjee.20150375. |
| [24] | ZHOU Cai-rong(周彩荣), SHI Xiao-hua(石晓华), WANG Hai-feng(王海峰), et al. Thermal decomposition and the non-isoththermal decomposition kinetics of DL-2-Naproxen(DL-2-萘普生热分解过程和非等温热分解动力学研究)[J]. Journal of Chemical Enginering of Chinese Universities(高校化学工程学报) , 2011, 25(3): 442-446. |
| [25] | YANG Xiu-shan(杨秀山), DENG Shao-gang(邓少刚), HUANG Peng-hui(黄鹏辉), et al. Thermal analysis kinetics studies on solid-solid reaction of calcium sulfide and phosphogypsum(硫化钙磷石膏固固反应的热分析动力学)[J]. Journal of Chemical Enginering of Chinese Universities(高校化学工程学报) , 2016, 30(3): 589-594. |
| [26] | LI Shuang(李爽), YANG Bin(杨斌), FENG Xiu-yan(冯秀燕), et al. Experimental study of typical Shanbei long flame coals pyrolysis kinetics(典型陕北长焰煤热解行为及其动力学实验研究)[J]. Journal of Dalian University of Technology(大连理工大学学报) , 2013, 53(3): 333-339. DOI:10.7511/dllgxb201303004. |
| [27] | WANG Xiang(王翔), WANG Xu-jiang(王旭江), FAN Yan-rong(范燕荣), et al. Pyrolysis characteristics and kinetics parameters of diesel under different atmosphere(不同气氛下柴油热解及热动力学特性分析)[J]. Journal of Combustion Science and Technology(燃烧科学与技术) , 2014, 20(4): 335-340. |




