2. 中国石油集团安全环保技术研究院, 北京 102206;
3. 太原工业学院 环境与安全工程系, 山西 太原 030008
2. Safety & Environmental Technology Research Institute of China Petroleum Group, Beijing 102206, China;
3. Department of Environmental and Safety Engineering, Taiyuan Institute of Technology, Taiyuan 030008, China
BiVO4是环境友好的光催化材料,带隙宽约2.4 eV,具有良好的可见光响应,但由于电子-空穴复合率高,光催化氧化性能显得不足[1]。通过掺杂和调控形貌,可改善BiVO4空穴的氧化能力,使复合后的催化剂在可见光响应下表现出优异的光催化活性[2]。引入CoOx(Co2O3和Co3O4)修饰BiVO4可有效提高光电流密度[3],因为CoOx属于p型半导体,具有独特的电子结构,易与n型半导体的BiVO4形成p-n异质结,并在异质结构的界面处产生电位差,进而促使光生电子或空穴的有效分离,抑制电子-空穴的复合[4]。高晓明等[5]以Bi(NO3)3·5H2O和NH4VO3为原料,向混合溶液中加乙酸钴,经180 ℃水热反应8 h,洗涤烘干后,对模拟汽油进行催化氧化,脱硫率为86%;黄文迪等[6]利用水热法,将Co(NO3) 2·6H2O加入Bi(NO3)3和NH4VO3混合液中,在220 ℃恒温反应24 h,用乙醇和高纯水去除杂质,冷冻干燥制得固体粉末状CoOx/BiVO4复合催化剂,之后对亚甲基蓝进行催化氧化,降解率达到91.2%;Bacha等[7]利用光化学沉积方法将CoOx覆盖在BiVO4的表面,在可见光的作用下对双酚A的降解率达到99.16%,对比Fe-BiVO4、Ni-BiVO4、Pure-BiVO4和Co-BiVO4,显示出极高的活性。上述研究表明,CoOx/BiVO4在可见光响应下只是对单纯物质溶液且浓度较低的情形下降解效果明显,但对高浓度难降解物质构成的复杂有机工业废水的降解效率,如同其他氧化法,效果并不理想[8-9]。
为探究对高浓度乙硫醇工业废水有效降解的高效光催化氧化技术,本实验在pH值为7.0的磷酸盐中性缓冲溶液中,将含一定浓度的Co(NO3)2通过电化学方法沉积在BiVO4颗粒表面,形成复合催化剂CoOx -Co(PO4)x/BiVO4(记作Co-Pi/BiVO4),在可见光响应下对该工业废水进行降解,以期使溶液化学需氧量(COD)和硫含量得到大幅降低,超过CoOx/BiVO4的作用效果。
合成得到的Co-Pi是一种无定形体,主要包含Co(III)、Co(II)、氧和磷[10],结果表明,与半导体光阳极BiVO4复合时可极大提高催化体系的氧化效率。本研究在实验的基础上,分析阐述Co-Pi的化学作用机理,以及Co-Pi/BiVO4在可见光响应下氧化降解含硫工业废水的动力学方程和降解历程。
2 实验 2.1 主要试剂和仪器分析纯级Co(NO3) 2·6H2O、Bi(NO3) 3·5H2O、NH4VO3,均购于西陇化工股份有限公司(广东汕头);化学纯级无水乙醇、NaH2PO4、NaH2PO4,均购于天津博迪化工有限公司;分析纯十六烷基三甲基溴化铵(CTAB),西亚化学科技(济南)有限公司产。
管式高温炉,BTF-1200C,安徽贝意克设备技术有限公司;行星磨,WJFT-03,长沙无创粉尘技术有限公司;电化学工作站,CHI 630E,上海辰华仪器有限公司;光化学反应仪,PLS-SXE300,北京泊菲莱科技有限公司;COD测定仪,LH-CP3M,广州连华环保科技有限公司;紫外荧光硫测定仪,ZDS-3000A,江苏新高科分析仪器有限公司;硫化物测定仪,ST-1/XS,北京智云达科技股份有限公司;JSM-IT300HR扫描电镜,日本电子株式会社;D8型X射线衍射仪,德国BRUKER-AXS公司;AXIS Supra型X射线光电子能谱仪,英国Kratos公司。
废水来源:山西海鑫石化有限公司含乙硫醇有机废水,pH=7.5,COD初始值约2 000 mg⋅L−1,硫的质量浓度为89.7 mg⋅L−3。
2.2 实验方法(1) BiVO4颗粒的制备
称取1.94 g的Bi(NO3) 3·5H2O于200 mL的去离子水中,超声溶解15 min后,加0.23 g的NH4VO3和0.05 g的CTAB于其中,置于高压釜中,加热至130 ℃,反应12 h,取出冷却至室温。分别用乙醇和去离子水洗涤数次,在800 ℃的温度下烧结4 h,冷却后用行星磨研磨至100 µm左右,待用。
(2) CoOx/BiVO4的制备
电化学工作站内,以Ag/AgCl为参比电极,铂丝为辅助电极,纱布包裹的BiVO4为工作电极,以去离子水作介质,加0.25 mol的Co(NO3) 2·6H2O于其中,相对于Ag/AgCl电极施加1.5 V的偏压,电沉积6 h[11],最终在BiVO4表面形成CoOx膜,然后再用去离子水洗涤膜表面吸附的离子,得到CoOx/BiVO4。
(3) Co-Pi/BiVO4的制备
分别配制0.1 mol⋅L−1的磷酸氢二钠与0.1 mol⋅L−1的磷酸二氢钠溶液各100 mL,以62:38的体积比将两者混匀后置于电化学工作站内,此时缓冲溶液的pH值约为7.0,代替去离子水作介质,以上述相同的方法进行电沉积,最后得到在磷酸盐中性缓冲溶液中生成的CoOx-Co(PO4)x/BiVO4,即Co-Pi/BiVO4。
(4) 废水降解
称取适量的Co-Pi/BiVO4加入含硫有机废水,调节光化学反应仪,选择可见光波长为485 nm进行照射,搅拌反应6 h,每隔一定时间取样测定废水的COD和有机硫化物浓度,分析降解情况。
3 结果与讨论 3.1 Co-Pi/BiVO4复合催化剂的物性表征(1) 形貌分析
为确定CoOx与BiVO4的结合形态,对纯水环境下电沉积得到的CoOx/BiVO4与在中性磷酸盐环境下电沉积得到的Co-Pi/BiVO4分别进行1万倍电镜扫描,如图 1所示。从图中可以看出,CoOx/BiVO4与Co-Pi/BiVO4表面大为不同。(b)图显示,许多CoOx微粒广泛散布在BiVO4的表面,有些嵌入BiVO4粒子之间,表明CoOx与BiVO4复合后形成了异质结构[12],活性位点较多;而(a)图显示,纯水环境下得到的CoOx/BiVO4,CoOx粒子在BiVO4表面分布稀疏,表明活性位点少,异质结构未有效形成。

|
图 1 CoOx / BiVO4及Co-Pi / BiVO4的SEM图 Fig.1 SEM micrographs of CoOx / BiVO4 and Co-Pi / BiVO4 |
电沉积时须注意,太高密度的负载CoOx会覆盖BiVO4表面活性位点,同时阻止了BiVO4对可见光的吸收,降低光生电子和空穴的产生,不利于催化氧化反应的进行,因而Co(NO3)2的加入量、溶液pH值和电沉积时间是重要的影响因素[13]。
(2) 晶型分析
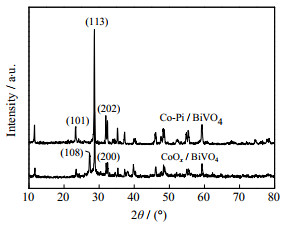
为了分析Co-Pi/BiVO4异质材料的结构特性,分别对CoOx/BiVO4及Co-Pi/BiVO4作了XRD测试,如图 2所示。
|
图 2 CoOx/BiVO4及Co-Pi/BiVO4的XRD图 Fig.2 XRD patterns of CoOx/BiVO4 and Co-Pi/BiVO4 |
纯BiVO4有单斜白钨矿型、四方锥石型和单斜四方型3种晶体结构,单斜白钨矿型相较其他2种晶型具有更高的可见光响应催化活性和氧化特性[14]。从图 2中可以看出,Co-Pi/BiVO4和CoOx/BiVO4的主要特征峰仍为单斜白钨矿型(对比图库BiVO4的标准衍射峰)。比较Co-Pi/BiVO4和CoOx/BiVO4的XRD衍射结果可知,CoOx/BiVO4在28.0°处对应的单斜相晶面(108)已经左移到Co-Pi/BiVO4在24.6°处对应的晶面(101),且磷酸钴盐的生成、掺入使得原有单斜相CoOx/BiVO4位于29.3°处(113)晶面特征衍射峰明显增强,表明Co3(PO4)2、CoPO4已成功嵌入CoOx/BiVO4的内部[15]。同时可以看到CoOx/BiVO4在32.5°处对应的(200)晶面也由于磷酸钴盐的掺入稍有左移,对应于Co-Pi/BiVO4在32°处的晶面(202),说明Co-Pi/BiVO4的晶型结构与CoOx/BiVO4的结构已有所不同。
(3) 化学态分析
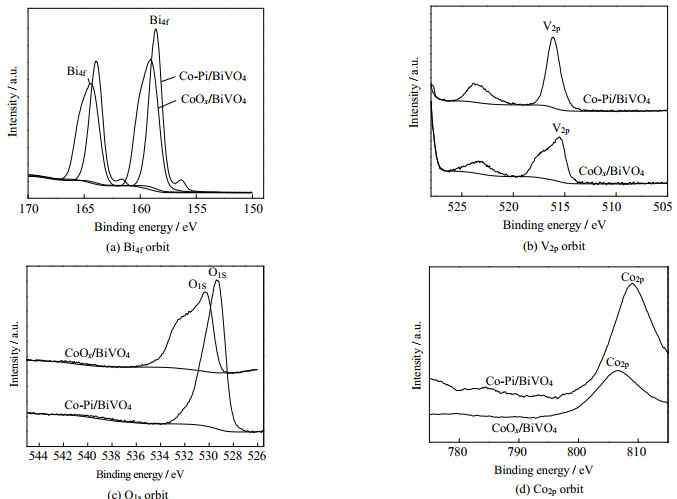
为了分析复合材料Co-Pi/BiVO4的元素特性,分别对CoOx/BiVO4及Co-Pi/BiVO4作了XPS测试,图谱形态如图 3所示。
|
图 3 CoOx / BiVO4及Co-Pi / BiVO4的XPS谱图 Fig.3 XPS spectra of CoOx / BiVO4 and Co-Pi / BiVO4 |
图 3(a)中,Bi元素的Bi4f能谱图表明,Co-Pi/BiVO4复合物在结合能158.0和163.5 eV处的谱峰分别对应Bi4f的2个轨道4f5/2和4f7/2,与CoOx/BiVO4的Bi3+出现的2个谱峰159.5和165 eV相比,分别右移了少许,其电子结合能减弱了一点,但峰的强度显然增加了,表明原子轨道的结合能提高了;图 3(b)是Co-Pi/BiVO4与CoOx/BiVO4 2种物质V元素的2p轨道图谱,从图中可以看出,V2p轨道出现2个谱峰,2个峰的结合能差别不大,但峰值稍有差别,Co-Pi/BiVO4的峰值比CoOx/BiVO4的峰值高;图 3(c)是Co-Pi/BiVO4与CoOx/BiVO4 2种物质的O1s能谱图,从图中可以看出,两者的电子结合能和原子轨道结合能都存在差别,Co-Pi/BiVO4的峰值要高些;从图 3(d)得知,Co-Pi/BiVO4中,Co元素的2p轨道在809.5 eV处出现了较大峰值,比CoOx/BiVO4的Co2p在806.5 eV处出现的峰值似有升高,表明Co-Pi/BiVO4无论是电子结合能,还是原子轨道结合能,均比CoOx/BiVO4要高。同时由掺杂元素XPS谱峰的位置及原子轨道能量升高引起电子受激发推测,2p轨道6个电子中3个激发进入3d轨道并使其占满,余下2p 3个平行轨道由3个单电子独自与氧原子成键,故Co应主要以其三价的Co2O3形态存在于复合催化剂中。综上现象说明,CoOx与BiVO4结合后各元素电子结构确实呈现了一些变化,表明Co-Pi/BiVO4与CoOx/BiVO4 2种物质内部均形成了不同的异质结[16]。
(4) 氧化性与稳定性分析
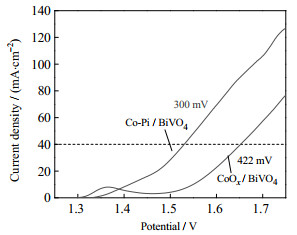
为考证Co-Pi/BiVO4的氧化性与稳定性,分别以CoOx/BiVO4和Co-Pi/BiVO4作工作电极,于电化学工作站内进行电极析氧和电阻抗测试,得到如图 4所示的对比曲线。
|
图 4 2种不同环境合成的催化剂电化学析氧极化曲线 Fig.4 Oxygen-produced polarization curves of catalysts prepared under two different environments |
图 4析氧极化曲线表明,相较于CoOx/BiVO4的析氧过电位422 mV,Co-Pi/BiVO4仅需300 mV的过电位就可以达到40 mA⋅cm−2的电流密度,说明在析氧极化过程中,Co-Pi/BiVO4电荷转移速率更快,反映了该催化剂具有更优良的电化学氧化活性。在一定时间内,电流密度大,积分电荷量就大,表明催化剂电极的活性表面积大,其对废水的光催化氧化能力就强[17],因而在磷酸盐中性缓冲溶液中通过电沉积得到的复合催化剂Co-Pi/BiVO4比在纯水中电沉积得到的CoOx/BiVO4,光氧化能力有明显优势。
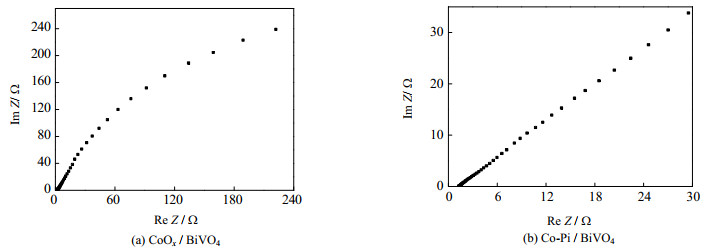
通过测试上述两者催化剂的电化学交流阻抗,探究电化学阻抗对催化剂在析氧极化催化氧化过程中的稳定性,图 5的对比曲线表明了2种催化剂的电化学交流阻抗Nyquist图谱的变化关系。Im Z代表电化学阻抗Z的虚部,Re Z代表Z的实部。
|
图 5 2种不同环境合成的催化剂电阻抗曲线 Fig.5 Electro-resistance curves of catalysts prepared under two different environments |
从图 5(a)中可以看出,催化剂CoOx/BiVO4表现出较大的串联电阻,表明其导电性能不太好,CoOx与基底BiVO4接触欠佳,该催化剂的稳定性不太好;图 5(b)情况显示,Co-Pi/BiVO4表现出较小的串联电阻,表明Co-Pi与BiVO4的接触性良好,该催化剂的稳定性更好[18]。
3.2 磷酸盐中性缓冲溶液的化学作用分析磷酸盐中性缓冲溶液产生的Co-Pi组成不仅含有CoOx,还含有磷酸钴盐。Co-Pi中磷的存在会极大地影响Co的电子特性,从图 3(d)中可以看出,Co-Pi中Co2p的出峰位置为809.5 eV,而CoOx中Co2p的标准出峰位置为806.5 eV[19],前者比后者所处的结合能要高一点,表明Co-Pi中Co元素偏向于高正价态,而P以磷酸根的形式存在,是质子的接受体,能促进PO43− ─H键的形成[20],以及·OH自由基的生成。
第一步,由Co(NO3)2电解产生的CoOx会与HPO42−和H2PO4−作用生成磷酸钴盐CoPO4和Co3(PO4)2沉淀混杂于CoOx中,并附着在BiVO4的表面形成Co-Pi/BiVO4。
第二步,该体系在可见光的响应下,非稳态的CoPO4会转变成稳态的Co3(PO4)2,释放出自由电子。
| $3 \mathrm{CoPO}_4 \rightarrow \mathrm{Co}_3\left(\mathrm{PO}_4\right)_2+\mathrm{PO}_4{ }^{3-}+3 \mathrm{e}^{-}$ | (1) |
第三步,Co-Pi中PO43−结合水中的H+进而产生羟基自由基。
| $\text { Co-Pi }+\mathrm{H}_2 \mathrm{O}+\mathrm{e}^{-} \rightarrow \text { Co-Pi-H }+\cdot \mathrm{OH}$ | (2) |
因此,Co-Pi/BiVO4体系不仅可以降低其电子-空穴的复合几率,而且还能激发出强氧化性基团·OH,故Co-Pi盐也具有很好的可见光助催化氧化效应。
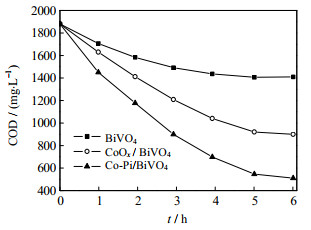
3.3 Co-Pi/BiVO4对乙硫醇废水的降解为比较Co-Pi/BiVO4对高浓度乙硫醇工业废水的降解效果,分别以Co-Pi/BiVO4、CoOx/BiVO4和BiVO4为光阳极,在同等条件下作废水的降解对比试验,常温,调节光化学反应仪可见光波长为485 nm。废水均取500 mL,催化剂的加入量均为1.0 mg⋅L−1,分别得到如图 6所示的COD降解情况,如图 7所示的硫化物脱除情况,图中t为时间。
|
图 6 3种催化剂氧化降解废水的效果 Fig.6 Performance on wastewater degradation of the three catalysts |
|
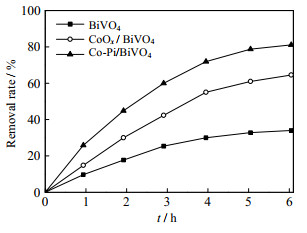
图 7 3种催化剂氧化去除硫化物的效果 Fig.7 Performance of total sulfur removal of the three catalysts |
从图 6中可以看出,Co-Pi/BiVO4催化氧化的效果明显好于CoOx/BiVO4和BiVO4,6 h后COD的降解率达到80%,而CoOx/BiVO4的降解率为55%,BiVO4的则更低。图 7表明,6 h后,脱硫率基本达到极值,BiVO4的脱硫率为32%,CoOx/BiVO4的脱硫率为64%,而Co-Pi/BiVO4的脱硫率最高,大于78%,比CoOx/BiVO4的高出14%,这在高浓度含硫有机废水的处理中,降解效果是很明显的,说明在pH值为中性的磷酸盐缓冲溶液中由电沉积法制备得到的CoOx/BiVO4比纯水电沉法制得的CoOx/BiVO4和单独BiVO4具有更多的空穴,展示出更强的氧化能力。同时也表明,钴离子作为电子的有效受体,可捕获从价带到导带的大量光生电子,促进了BiVO4光生电子与空穴的有效分离[21],从而大幅提高Co-Pi/BiVO4光氧化降解效率。
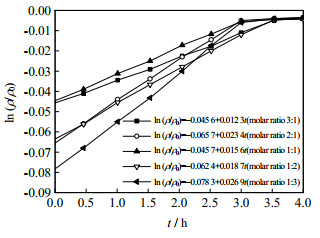
3.4 不同物质的量比制得的Co-Pi/BiVO4降解动力学研究为了考察不同配比的Co(NO3)2与BiVO4构成的Co-Pi/BiVO4复合催化剂对含硫有机物的氧化降解性能,选择Co(NO3)2与BiVO4物质的量比n(Co(NO3)2): n(BiVO4)为3:1、2:1、1:1、1:2、1:3这5种情形制备得到Co-Pi/BiVO4物,测定初始废水中硫化物的质量浓度ρ0和不同降解时间点硫化物的质量浓度ρ,得到拟合的一级动力学方程
|
图 8 不同物质的量比制得的Co-Pi/BiVO4降解一级动力学曲线 Fig.8 The 1st order degradation kinetic curves of Co-Pi / BiVO4 prepared under different material ratios |
从图 8中可看出,当Co(NO3) 2与BiVO4物质的量比为1:3时,得
经分析,所取的含硫有机废水主要成分是乙硫醇C2H5SH,通过CoOx及BiVO4的共效应富空穴作用,C2H5SH最后降解为CH3COOH和SO42−。
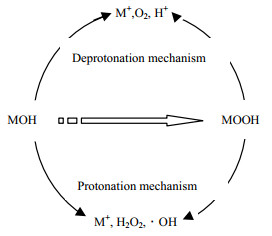
对于反应机理,一般认为CoOx/BiVO4在可见光响应下产生大量空穴,光生空穴从价带注入,将其表面的金属-羟基基团M─OH转化为中间体M─OOH,该中间体再进行去质子化反应,释放出O2,进而完成对废水的催化氧化降解[23]。
| $ \mathrm{MOOH}+4 \mathrm{e}^{-} \rightarrow \mathrm{O}_2+\mathrm{H}^{+}+\mathrm{M}^{+} $ | (3) |
然而由于测定的含硫降解产物中主要存在CH3COO−和SO42−两种酸根形态,由此推测中间体M─OOH可能被质子化产生了H2O2,进而产生˙OH。
| $\mathrm{MOOH}+\mathrm{H}^{+} \rightarrow \mathrm{H}_2 \mathrm{O}_2+\mathrm{M}^{+}+2 \mathrm{e}^{-}$ | (4) |
| $\mathrm{H}_2 \mathrm{O}_2+\mathrm{e}^{-} \rightarrow \mathrm{OH}^{-}+\cdot \mathrm{OH}$ | (5) |
上述2种机理路径如图 9所示。
|
图 9 CoOx/BiVO4光催化降解机理途径分析 Fig.9 Mechanism of CoOx / BiVO4 photocatalytic degradation |
乙硫醇降解为CH3COOH和H2SO4的机理历程如下[24]:
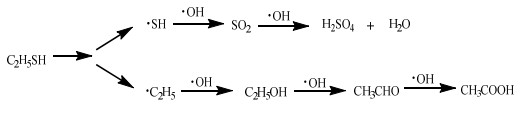
|
Co-Pi/BiVO4复合催化剂降解高浓度乙硫醇工业废水,效果明显,结合该类催化剂性能表征分析与对比结果,得出如下结论:
(1) 在呈中性的磷酸盐缓冲溶液里通过电化学沉积法可制得Co-Pi/BiVO4,制得的CoOx颗粒微小,与BiVO4结合稳定、紧密,当Co(NO3)2与BiVO4物质的量比为1:3时,对乙硫醇废水的降解效果为最佳;
(2) Co-Pi/BiVO4体系催化活性高,空穴与电子的复合程度低,在可见光响应下该体系氧化能力比纯水电沉积法得到的CoOx/BiVO4和单纯BiVO4的氧化能力强,降解乙硫醇工业废水,COD去除率达到80%,脱硫率超过78%;
(3) Co-Pi/BiVO4催化体系稳定、高活性,同时由于Co-Pi与CoOx/BiVO4的叠加效应,导致更多的·OH产生,有利于降解反应的进行。
| [1] |
陈锦森, 刘咏鸽, 陆建兵. 光催化剂钒酸铋BiVO4研究进展[J]. 生物化工, 2020, 6(2): 143-146. CHEN J S, LIU Y H, LU J B. A brief analysis on the research progress of bismuth vanadate BiVO4[J]. Biological Chemical Engineering, 2020, 6(2): 143-146. |
| [2] |
吴江稳, 翟福旺, 陈朝鑫, 等. CuO/BiVO4复合光催化剂的合成及其光催化性能的研究[J]. 广州化工, 2021, 49(4): 37-40. WU J W, ZHAI F W, CHEN C X, et al. Preparation of CuO/BiVO4 Composite photocatalyst and its photocatalytic properties[J]. Guangzhou Chemical Industry, 2021, 49(4): 37-40. |
| [3] |
李蒋, 王雁, 张秀芳, 等. Co3O4/BiVO4复合阳极活化过-硫酸盐强化光电催化降解双酚A[J]. 环境科学, 2018, 39(8): 3713-3718. LI J, WANG Y, ZHANG X F, et al. Enhancement of photoelectrocatalytic degradation of bisphenol-A with peroxymonosulfate activated by a Co3O4 composite photoanode[J]. Environmental Science, 2018, 39(8): 3713-3718. |
| [4] |
WANG Z P, LIN Z L, SHEN S J, et al. Advances in designing heterojunction photocatalytic materials[J]. Chinese Journal of Catalysis, 2021, 42(5): 710-730. DOI:10.1016/S1872-2067(20)63698-1 |
| [5] |
高晓明, 付峰, 武玉飞, 等. Co-BiVO4光催化剂的制备及其用于光催化氧化噻吩[J]. 无机材料学报, 2012, 27(10): 1073-1078. GAO X M, FU F, WU Y F, et al. Preparation of Co-BiVO4 photocatalyst and its application in the photocatalytic oxidative thiophene[J]. Jounral of Inorganic Materials, 2012, 27(10): 1073-1078. |
| [6] |
黄文迪, 孙静, 申婷婷, 等. Co-BiVO4异质结光催化剂的制备及其性能[J]. 化工进展, 2017, 36(11): 4080-4086. HANG W D, SUN J, SHEN T T, et al. Preparation and properties of Co-doped BiVO4 heterojunction photocatalysts fabricated by hydrothermal method[J]. Chemical Industry and Engineering progress, 2017, 36(11): 4080-4086. |
| [7] |
BACHA A U R, NABI I, CHENG H Y, et al. Photoelectrocatalytic degradation of endocrine-disruptor bisphenol-A with significantly activated peroxymonosulfate by Co-BiVO4 photoanode[J]. Chemical Engineering Journal, 2020, 389(6): 124482. |
| [8] |
邵俊龙, 王绍科, 和佼, 等. 高浓度工业有机废水光催化技术[J]. 工业技术创新, 2014, 1(1): 30-35. SHAO J L, WANG S K, HE J, et al. Photocatalytic treatment of high concentration industrial organic wastewater[J]. Industrial Technology Innovation, 2014, 1(1): 30-35. |
| [9] |
高巍. 高浓度难降解有机工业废水处理技术评价[J]. 化工通讯设计, 2020, 46(12): 164-165. GAO W. Technical evaluation of high concentration difficult to degradation organic industrial wastewater treatment[J]. Chemical Engineering Design Communication, 2020, 46(12): 164-165. |
| [10] |
姜晓娟. 钴分子催化剂作为助催化剂前驱体对BiVO4光阳极水氧化性能的调控[D]. 大连: 大连理工大学, 2016. JIANG X J. Molecular Cobalt-based complexes as precursors of aid-catalyst for BiVO4 photoanodes modification [D]. Dalian: Dalian University of Technology, 2016. |
| [11] |
ZHANG A P, ZHANG J Z. Study on synthesis and photocatalytic activity of Cu, Ag, Au doped BiVO4 photocatalysts[J]. Journal of Molecular Catalysts, 2010, 24(1): 51-56. |
| [12] |
SU J, ZUO X X, LI G D, et al. Macroporous V2O5-BiVO4 composites: effect of heterojunction on the behavior of photogenerated charges[J]. The Journal of Physical Chemistry C, 2011, 115(16): 8064-8071. |
| [13] |
MAHSH B V, ABDULLAH K, SINEM A, et al. The significance of the local structure of cobalt-based catalysts on the photoelectrochemical water oxidation activity of BiVO4[J]. Electrochimica Acta, 2021, 366(1): 137467. |
| [14] |
HUO T Y, ZHANG X F, DONG X L, et al. Photonic crystal coupled porous BiVO4 hybrid for efficient photocatalysis under visible light irradiation[J]. Journal of Materials Chemistry A, 2014, 41(2): 17366-17370. |
| [15] |
PILLI S K, DEUTSCH T G, FURTAK T E, et al. Light induced water oxidation on cobalt-phosphate(Co-Pi) catalyst modified semi-transparent, porous SiO2-BiVO4 electrodes[J]. Physical Chemistry Chemical Physics, 2012, 19(14): 7032-7039. |
| [16] |
GU S N, LI W J, WANG F Z, et al. Synthesis of buckhorn-like BiVO4 with a shell of CeOx nanodots: effect of heterojunction structure on the enhancement of photocatalytic activity[J]. Applied Catalysis B: Environmental, 2015, 170/171: 186-194. |
| [17] |
PILLI S K, FURTAK T E, BROWN L D, et al. Cobalt-phosphate(Co-Pi) catalyst modified Mo-doped BiVO4 photoelectrodes for solar water oxidation[J]. Energy & Environmental Science, 2011, 12(4): 5028-5034. |
| [18] |
李雪. 基于BiVO4高效光催化剂的设计制备及其光催化性能增强机理研究[D]. 西安: 西北师范大学, 2021. LI X. Design and preparation of high efficient BiVO4-based photocatalysts and the mechanism of enhanced photocatalytic performance [D]. Xian: Northwest Normal University, 2021. |
| [19] |
崔亮. 负载型纳米阵列的制备及其在催化水解制氢和电化学析氧反应中的应用研究[D]. 青岛: 青岛大学, 2017. CUI L. Preparation of loaded nanoarray and its applied research in producing hydrogen by catalytic hydrolysis as well as electrochemical oxygen evolution [D]. Qingdao: Qingdao University, 2017. |
| [20] |
ESSWEIN A J, SURENDRANATH Y, REECE S Y, et al. Highly active cobalt phosphate and borate based oxygen evolving catalysts operating in neutral and natural water[J]. Energy & Environmental Science, 2011, 4(2): 499-504. |
| [21] |
YIN W Z, WANG W Z, ZHOU L, et al. CTAB-assisted synthesis of monoclinic BiVO4 phoyocatalyst and its highly efficient degradation of organic dye under visible-light irradiation[J]. Journal of Hazardous Materials, 2010, 173(1/2/3): 194-199. |
| [22] |
LUO W J, LI Z S, YU T, et al. Effects of surface electrochemical pretreatment on the photoelectrochemical performance of Mo-doped BiVO4[J]. The Journal of Physical Chemistry C, 2013, 116(8): 5076-5081. |
| [23] |
顾少楠. 稀土离子改性钒酸铋可见光催化材料的合成及机理研究[D]. 北京: 北京科技大学, 2016. GU S N. Synthesis and visible light-driven photocatalytic mechanism of rare-earth ions modified BiVO4 [D]. Beijing: University of Science and Technology Beijing, 2016. |
| [24] |
马香娟. 杂环化合物的电化学氧化行为与降解机理[D]. 杭州: 浙江大学, 2013. MA X J. Electrochemical oxidation behavior and mechanism of heterocyclic compounds [D]. Hangzhou: Zhejiang University, 2013. |




