甲状旁腺素(parathyroid hormone,PTH)是甲状旁腺分泌的维持钙、磷代谢的重要激素之一,其分子为84个氨基酸组成的多肽,在血循环中完整的PTH分子结构成为全段PTH(1-84PTH,iPTH),是体内主要生物活性形式[1-2]。PTH合成和分泌受血清游离钙和25羟维生素D(25 hydroxyvitamin D,25OHD)的调节,如低钙血症和25OHD不足使PTH释放增加,溶解骨钙并释放入血,同时提高肾小管和肠道回吸收钙的能力加强,提高血钙水平。PTH主要在肾脏清除,因此其降解受肾功能的影响,如慢性肾脏疾病(chronic kidney dielace, CKD)患者表现为肾性骨病。随着免疫分析方法的进展,PTH检测已成为相关疾病的常规检测内容,是诊断各种原因引起的原发性或继发性甲状旁腺功能增高或减退所致高钙血症和低钙血症的重要实验室检查,PTH也是CKD的重要监测指标[3-5]。为明确我国人群血清PTH参考区间,并研究年龄、性别及血清25OHD等因素对中国人群PTH的影响,本研究对北京、杭州、广州、大连、乌鲁木齐等5个城市2 449名健康成年人血清PTH水平进行多中心调查。
对象与方法 对象本研究人群为国际临床化学委员会(International Federation of Clinical Chemistry,IFCC)全球多中心参考范围研究的中国研究人群[6]。依据IFCC对于参考区间的规则,2013年5月1日至9月30日来自中国5个城市的共2 627名表观健康人入选,包括北京(北部)、杭州(东部)、广州(南部)、大连(东北部)及乌鲁木齐(西北部),受试者由所在地区的一所医院进行甄选,5所医院分别是北京协和医院、浙江大学附属第二医院、中山大学附属第一医院、大连医科大学附属第一医院和新疆医科大学附属医院。所有受试者均对本试验知情且确保年龄及性别平均分布。本研究获北京协和医院伦理委员会批准。
入选标准:在目标城市生活超过1年;无急性或慢性感染、消化道疾病、肾脏病、代谢病、营养不良性疾病、风湿性疾病、内分泌疾病或者心血管疾病;无近期手术史、近6个月无用药史、献血史及输血史。近期服用维生素D者亦除外。由专业医务人员测量身高、体质量、血压等数据。体质量指数(body mass index,BMI) =体质量(kg)/身高2(m2)。入选标准信息采用问卷形式进行调查。
本研究按不同血清25OHD水平对受试者进行分组,即25OHD严重缺乏(<10 μg/L),25OHD缺乏(10~19.99 μg/L),25OHD不足(20~29.99 μg/L)和25OHD正常(≥30 μg/L)。血清25OHD浓度≥150 μg/L为维生素D中毒[7-8]。
实验室检测标本采集:受试者按要求在采血前1周维持正常饮食摄入,采血前12 h空腹,并避免采血48 h前饮酒及1 h前吸烟。静脉血标本采集在含促凝集采血管中并于2 h内离心(1 200×g,10 min)、分离血清,-80 ℃冻存空运至北京,统一由北京协和医院检验科进行中心化检测。
标本检测:血清PTH检测仪器为Beckman Dx 1800全自动化学发光免疫分析仪(贝克曼库尔特,美国)及其配套试剂、校准品,质控品为伯乐Lyphochek Tumor Marker Plus Control。25OHD检测为北京协和医院检验科建立的同位素稀释超高压液相色谱串联质谱(isotope dilution-ultra performance liquid chromatography-tandem mass sepctrometry, ID-UPLC/MS/MS),仪器为Waters ACQUITY超高效液相色谱仪(沃特世,美国)和ABSCIEX 4000 Q TRAP三重四级杆串联质谱仪(Applied Biosystems,美国),质控品为伯乐LiquichekTM Specialty Immunoassay control。血清Ca、P检测仪器为AU5800全自动生化分析仪(贝克曼库尔特,美国)及其配套试剂、校准品,质控品为伯乐Liquid Assayed Multiqual。所有试剂及校准品均符合厂家要求,所有的测试实验室质量控制均在控。
统计学方法采用SPSS22.0统计软件,连续变量采用均值±标准差(x±s)表示。性别间差异采用独立样本t检验,不同年龄亚组、不同地区及不同25OHD水平人群PTH水平比较采用单因素方差分析,计数资料采用卡方检验。使用Nested ANOVA探讨PTH参考区间的影响因素,以SD比值(the ratio of SD,SDR)是否大于0.3决定是否根据地区、性别、年龄建立不同的参考区间[9]。P<0.05为差异有统计学意义。
结果 一般临床资料剔除受试者信息缺失者后,本研究最终有效受试者为2 449人,平均年龄(40.1±12.2)岁,其中男性1 189人占48.6%,女性1 260人占51.4%。受试者基本信息及不同地区人群血清PTH、25OHD、Ca、P水平见表 1。所有受试者血清PTH浓度为(34.96±14.45)ng/L,血清25OHD浓度为(19.07±6.26)μg/L,血清Ca浓度为(2.30±0.09)mmol/L,血清P浓度为(1.14±0.16)mmol/L。
| 城市 | 男性 [n(%)] | 年龄 (岁) | BMI (kg/m2) | PTH (ng/L) | 25OHD (μg/L) | Ca (mmol/L) | P (mmol/L) | eGFR (mL/min·1.73 m-2) |
| 北京 | 230(46.1) | 40.0±11.9 | 23.6±3.1 | 36.92±14.29 | 16.08±5.98 | 2.30±0.08 | 1.15±0.15 | 108.6±18.6 |
| 杭州 | 241(48.5) | 40.2±12.4 | 22.6±2.9 | 38.16±15.28 | 18.55±5.63 | 2.30±0.08 | 1.15±0.17 | 107.3±19.2 |
| 广州 | 244(50.3) | 40.0±12.0 | 22.7±2.9 | 35.67±13.52 | 20.97±4.75 | 2.29±0.08 | 1.16±0.17 | 107.9±21.2 |
| 大连 | 262(54.4) | 39.9±12.1 | 22.3±2.8 | 26.38±11.67 | 21.71±6.62 | 2.30±0.08 | 1.11±0.15 | 117.7±24.4 |
| 乌鲁木齐 | 212(43.6) | 40.3±12.5 | 23.2±3.2 | 37.49±13.92 | 18.13±6.46 | 2.30±0.09 | 1.12±0.16 | 114.7±20.4 |
| 总计 | 1 189(48.6) | 40±12.2 | 22.9±3.0 | 34.96±14.45 | 19.07±6.26 | 2.30±0.09 | 1.14±0.16 | 111.2±21.2 |
| BMI:体质量指数;PTH:甲状旁腺素;25OHD:25羟维生素D; Ca钙;P:磷; eGFR:估算肾小球滤过率 | ||||||||
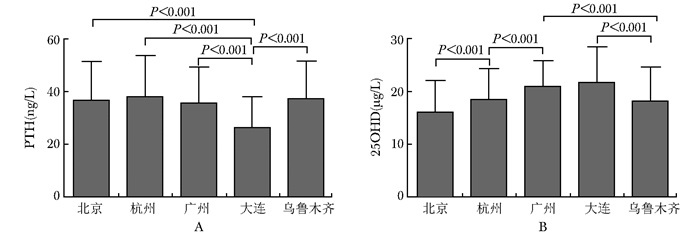
在5个城市中,大连受试者PTH水平显著低于其他城市(图 1A),差异有统计学意义(P=0.000),同时大连受试者血清25OHD水平显著高于北京、杭州及乌鲁木齐(P=0.000),与广州间差异无统计学意义(P=0.054)(图 1B)。5个城市中,大连受试者与乌鲁木齐受试者血清P水平比较,差异无统计学意义(P>0.05),且二者均低于其他3个城市(P<0.01)。
|
| 图 1 不同地域血清PTH水平及25OHD比较 Figure 1 Serum levels of PTH and 25OHD in different cities PTH:甲状旁腺素;25OHD:25羟维生素D |
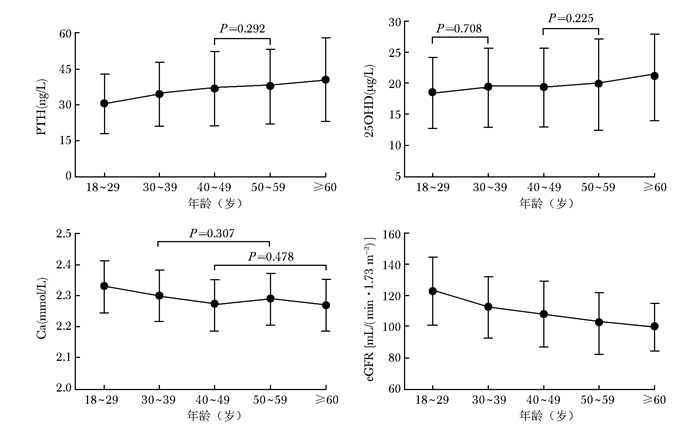
随着年龄的增加,血清PTH水平增加(P<0.01),但40~49岁组与50~59岁组间差异无统计学意义(P=0.292)(图 2)。血清25OHD水平也随年龄增加而增加(P<0.01),但18~29岁组与30~39岁组间及40~49岁组与50~59岁组间比较,差异无统计学意义(P值分别为0.708,0.225)。随着年龄的增加,血清Ca水平降低(P<0.01),但30~39岁组与50~59岁组间及40~49岁组与≥60岁组间比较,差异无统计学意义(P值分别为0.307,0.478)。估算肾小球滤过率(estimated glomerular filtration rate,eGFR)随着年龄增加而显著降低(P<0.01)(图 2)。血清P水平在各年龄组比较,差异无统计学意义(P>0.05)。
|
| 图 2 不同年龄亚组血清PTH,25OHD,Ca,eGFR水平比较 Figure 2 Serum levels of PTH, 25OHD, Ca, and eGFR in different age groups PTH:甲状旁腺素;25OHD:25羟维生素D; Ca:钙;eGFR:估算肾小球滤过率 |
在不同性别分组中,血清PTH均随年龄增加而增加,同一年龄分组性别比较,差异无统计学意义(P>0.05)(表 2)。在不同性别分组中,血清25OHD也随年龄增加而增加,但同一年龄分组中,女性血清25OHD水平低于男性(P<0.05)。在不同性别分组中,血清Ca均随年龄增加而减低,同一年龄分组中女性血清Ca水平低于男性(P<0.05)(表 2)。血清P水平在各年龄亚组差异无统计学意义(P>0.05)。
| 年龄 (岁) | PTH(ng/L) | 25OHD(ng/L) | Ca(mmol/L) | eGFR[mL/(min·1.73 m-2)] | |||||||
| 男性 | 女性 | 男性 | 女性 | 男性 | 女性 | 男性 | 女性 | ||||
| 18~29 | 29.63±12.35 | 30.91±12.04 | 20.43±5.82 | 16.44±4.59* | 2.35±0.08 | 2.31±0.08 | 110.2±21.5 | 126.5±20.5 | |||
| 30~39 | 33.54±12.20 | 35.24±13.97 | 19.84±5.59 | 16.87±5.42* | 2.32±0.08 | 2.27±0.08 | 108.9±18.2 | 116.2±18.8 | |||
| 40~49 | 36.00±15.17 | 37.42±15.16 | 21.53±5.99 | 17.34±5.76* | 2.29±0.08 | 2.26±0.09 | 105.5±21.5 | 111.1±19.4 | |||
| 50~59 | 38.63±16.38 | 36.83±14.20 | 20.85±7.20 | 18.90±7.17* | 2.27±0.08 | 2.30±0.08 | 101.3±18.6 | 103.3±19.9 | |||
| ≥60 | 40.44±19.89 | 40.62±13.65 | 22.47±6.49 | 19.70±6.82# | 2.25±0.07 | 2.28±0.09 | 98.2±15.8 | 97.8±13.6 | |||
| 总计 | 34.49±14.77 | 35.42±14.14 | 20.74±6.17 | 17.49±5.92* | 2.31±0.09 | 2.29±0.09 | 108.7±21.0 | 113.5±21.2 | |||
| PTH:甲状旁腺素;25OHD:25羟维生素D; Ca钙;eGFR:估算肾小球滤过率; 与男性相比, #P<0.05, *P<0.01 | |||||||||||
依据血清维生素D水平对受试者分组,随着血清25OHD水平增高,PTH显著降低(P=0.000),而eGFR随之显著增加(P=0.000)(表 3)。血清25OHD不足及正常人群(≥20 μg/L)血清PTH的2.5~97.5百分位为14.10~65.22 ng/L。血Ca在血清25OHD水平<10 μg/L时低于血清25OHD水平≥20 μg/L时(P<0.05)。血P水平在血清25OHD水平<20 μg/L时明显高于≥20 μg/L(P=0.000)。
| 25OHD (μg/L) | 男性 [n(%)] | PTH (ng/L) | Ca (mmol/L) | eGFR [mL/(min·1.73 m-2)] | P(mmol/L) |
| <10 | 95(62.5) | 43.86±16.91 | 2.28±0.09 | 115.5±20.3 | 1.16±0.16 |
| 10~19.99 | 676(52.8) | 36.11±14.19 | 2.29±0.08 | 113.6±21.6 | 1.15±0.16 |
| 20~29.99 | 367(40.7) | 32.56±13.19 | 2.30±0.08 | 107.9±20.3 | 1.12±0.16 |
| ≥30 | 49(42.6) | 29.72±17.16 | 2.31±0.09 | 103.2±20.3 | 1.09±0.15 |
| P | - | <0.001 | <0.05 | <0.001 | <0.001 |
| 25OHD:25羟维生素D; PTH:甲状旁腺素;Ca钙;eGFR:估算肾小球滤过率; P:磷 | |||||
Nested ANOVA结果显示,地区、性别、年龄的学生化残差(studentized residual, SDR)分别为0.340、0.000和0.270,因此建立中国人群PTH参考区间时可以不考虑性别、年龄因素。地区之间除大连外,其他地区PTH水平无差异,去除大连地区后,建立中国人群血清PTH的参考区间(表 4),中国人群血清PTH浓度为(37.07±14.29)ng/L。
| 25OHD(μg/L) | n | 2.5% | 95% CI | 97.5% | 95% CI |
| <10 | 141 | 22.51 | 17.40~24.00 | 88.47 | 79.62~94.10 |
| 10~19.99 | 1 102 | 17.00 | 15.00~18.00 | 72.09 | 68.00~78.47 |
| 20~29.99 | 658 | 14.74 | 13.43~16.00 | 64.34 | 61.08~68.00 |
| ≥30 | 60 | 8.63 | 6.00~14.10 | 113.70 | 64.25~141.00 |
| 总计 | 1 961 | 16.00 | 15.00~17.00 | 71.96 | 68.00~77.49 |
| 25OHD:25羟维生素D;CI:置信区间 | |||||
甲状旁腺素及维生素D是临床上常用的辅助诊断骨质疏松和原发性甲状旁腺素增多症(primary hyperparathyroidism,pHPT)等骨钙代谢紊乱的实验室指标[10-12]。在正常生理及骨钙代谢紊乱疾病中,PTH通过维生素D和血钙水平的改变而对钙磷代谢进行调节。因此健康人群的甲状旁腺水平对评估骨代谢及营养状况有重要的意义。本研究旨在通过对中国不同地域的城市、不同年龄及性别人群进行多中心调查,以明确中国人群PTH的影响因素和参考区间。
本研究调查结果显示,PTH在不同地区间存在明显差异,主要表现为大连受试者血清PTH水平为5个城市中最低水平,而其他城市间比较,差异无统计学意义(P>0.05)。剔除大连地区,其他所有受试者血清PTH的浓度为(37.07±14.29) ng/L,2.5~97.5百分位数为16.00~71.96 ng/L。大连地区血清25OHD水平为5个城市中最高水平(与广州无差异)。一般认为地理纬度越低接受光照时间越长,则人体内合成25OHD水平越多。北京、杭州和广州人群血清25OHD水平依次增高证实了这种假设。但是大连在5个城市中纬度并非最低,其受试者血清25OHD与最低纬度的广州无差异,考虑可能与其沿海饮食中鱼肉摄入多相关。大量鱼肉的摄入可增加富含维生素D的鱼肝油摄入。因此,受较高水平血清25OHD的调节,大连PTH水平较其他城市低,符合二者的调节关系。而位于我国西北部的乌鲁木齐市,其纬度最高,25OHD水平却非最低,而处于中间纬度的北京市25OHD为最低水平。乌鲁木齐光照时间长,可能是原因之一[13]。东部发达城市人群有更长的室内工作时间,接受相对较少的光照,也会导致北京市人群25OHD水平比乌鲁木齐偏低。
由于在人体正常衰老过程中出现肾脏功能下降,而PTH主要在肾脏清除[14],因此,健康人群的年龄及肾功能可能影响钙磷的代谢。本研究调查结果证实,随着年龄的增加,血Ca水平明显下降,eGFR水平显著降低,血清PTH呈现出升高趋势。Rejnmark等[15]对2 316名行钼靶检查女性人群的调查也发现同样的增长趋势。尽管男女存在性别及性激素水平的差异[16],本研究未发现血清PTH存在性别差异,而且在各年龄亚组中也未见血清PTH存在性别差异。不过25OHD水平在每个年龄亚组均表现出男性高于女性,这可能与男性较女性有更多户外活动和日照时间促进更多维生素D的合成有关。
目前我国人群94.6%存在维生素D不足甚至缺乏[17],受其调节的PTH的变化特点目前尚无大样本调查结果。本研究中,维生素D缺乏人群(<30 μg/L)占总受试者的96.9%,血清25OHD不足及正常人群(≥20 μg/L)的血清PTH的2.5~97.5百分位数为14.10~65.22 ng/L,其参考区间的下限和上限均明显小于整体人群,与之前文献报道[18]一致。主要原因是维生素D的缺乏导致其刺激肠道吸收钙的作用减弱引起血钙水平下降,最终刺激甲状旁腺钙感应受体促进PTH分泌以提高血钙水平[19-20]。因此建立低维生素D水平下PTH的参考区间具有重要的意义。
综上所述,本研究对我国不同地域5个城市2 449例健康人进行调查建立了不同维生素D水平下血清PTH的参考区间。血清PTH水平随年龄增加而增加,但无性别差异。在中国人群普遍存在维生素D缺乏情况下,建立不同维生素D水平下的PTH参考区间是非常必要的。
| [1] | Potts JT. Parathyroid hormone:past and present[J]. J Endocrinol, 2005, 187: 311. DOI:10.1677/joe.1.06057 |
| [2] | Martin KJ, Akhtar I, González EA. Parathyroid hormone:new assays, new receptors[J]. Semin Nephrol, 2004, 24: 3–9. DOI:10.1053/j.semnephrol.2003.08.019 |
| [3] | Ketteler M, Eckardt KU. KDIGO clinical practice guidelines for the diagnosis, evaluation, prevention and treatment of chronic kidney disease related mineral and bone disorders (CKD-MBD)[J]. Der Nephrol, 2009, 4: 437–440. DOI:10.1007/s11560-009-0291-y |
| [4] | AT, VL, DH, et al. Bone disease in predialysis, hemodialysis, and CAPD patients:evidence of a better bone response to PTH[J]. Kidney Int, 1995, 47: 1434–1442. DOI:10.1038/ki.1995.201 |
| [5] | Lehmann G, Stein G, Hüller M, et al. Specific measurement of PTH (1-84) in various forms of renal osteodystrophy (ROD) as assessed by bone histomorphometry[J]. Kidney Int, 2005, 68: 1206. DOI:10.1111/j.1523-1755.2005.00513.x |
| [6] | Ozarda Y, Ichihara K, Barth JH, et al. Protocol and standard operating procedures for common use in a worldwide multicenter study on reference values[J]. Clin Chem Lab Medicine Cclm, 2013, 51: 1027. |
| [7] | Holick MF. Vitamin D deficiency[J]. Nederlands Tijdschrift Voor Geneeskunde, 2007, 150: 1315–1316. |
| [8] | Holick MF, Binkley NC, Bischoffferrari HA, et al. Evaluation, treatment, and prevention of vitamin D deficiency:an Endocrine Society clinical practice guideline[J]. J Clin Endocrinol Metab, 1911, 96: 1911. |
| [9] | Kiyoshi I. Statistical considerations for harmonization of the global multicenter study on reference values[J]. Int J Clin Chem, 2014, 432: 108–118. |
| [10] | Vestergaard P, Mollerup CL, Frøkjaer VG, et al. Cohort study of risk of fracture before and after surgery for primary hyperparathyroidism[J]. Br Med J, 2001, 163: 4875–4878. |
| [11] | Vignali E, Viccica G, Diacinti D, et al. Morpho-metric vertebral fractures in postmenopausal women with primary hyperparathyroidism[J]. J Clin Endocrinol Metab, 2009, 94: 2306. DOI:10.1210/jc.2008-2006 |
| [12] | Bolland MJ, Grey AB, Gamble GD, et al. Association between primary hyperparathyroidism and increased body weight:a meta-analysis[J]. J Clin Endocrinol Metab, 2005, 90: 1525–1530. DOI:10.1210/jc.2004-1891 |
| [13] | 郭艳英, 努荣古丽·买买提, 马福慧, 等. 乌鲁木齐城区健康成年人维生素D营养状况调查分析[J]. 标记免疫分析与临床, 2015, 22: 989–993. |
| [14] | Glassockr J, Los Angeles COGT. Aging and chronic kidney disease[J]. Kidney Blood Pressure Res, 2013, 38: 109. DOI:10.1159/000355760 |
| [15] | Rejnmark L, Vestergaard P, Heickendorff L, et al. Determinants of plasma PTH and their implication for defining a reference interval[J]. Clin Endocrinol, 2010, 47: 37. |
| [16] | Li M, Lv F, Zhang Z, et al. Establishment of a normal reference value of parathyroid hormone in a large healthy Chinese population and evaluation of its relation to bone turnover and bone mineral density[J]. Osteoporos Int, 2016, 27: 1907. DOI:10.1007/s00198-015-3475-5 |
| [17] | Yu S, Fang H, Han J, et al. The high prevalence of hypovitaminosis D in China:a multicenter vitamin D status survey[J]. Medicine, 2015, 94: e585. DOI:10.1097/MD.0000000000000585 |
| [18] | Souberbielle JC, Cormier C, Kindermans C, et al. Vitamin D status and redefining serum parathyroid hormone reference range in the elderly[J]. J Clin Endocrinol Metab, 2001, 86: 3086. |
| [19] | Aloia JF, Dhaliwai R, Shieh A, et al. Vitamin D supplementation increases calcium absorption without a threshold effect[J]. The American journal of clinical nutrition, 2014, 99: 624–631. DOI:10.3945/ajcn.113.067199 |
| [20] | Jamali Z, Asadikaram G, Mahmoodi M, et al. Vitamin D status in female students and its relation to calcium metabolism markers, lifestyles, and polymorphism in vitamin D receptor[J]. Clin Lab, 2013, 59: 407–413. |
| (收稿日期:2017-12-29) |

