2. 712046 陕西咸阳,陕西中医药大学附属医院骨病科
2. Department of Orthopedics, Affiliated Hospital of Shaanxi University of Chinese Medicine, Xianyang 712046, Shaanxi, China
绝经后骨质疏松症(postmenopausal osteoporosis,PMOP)是以妇女绝经后体内雌激素水平急剧下降,所引起的一种常见骨骼疾病,主要以骨量减少、骨的微组织结构退化和遭到破坏为特征,从而导致骨脆性增加,最终诱发骨折[1],甚至危及生命。女性绝经后5~10年为PMOP的一般发生时间[2],流行病学统计显示,患有骨质疏松的50岁以上的人群女性约为15.4%~33.3%,男性约为4.3%~12.5%[3-4]。目前,针对骨质疏松症的治疗用药多以西药为主,其治疗效果肯定,但安全性以及不良反应同样需要关注。女性绝经后,其卵巢衰退以及雌激素的缺乏是骨质疏松发生的关键,一定程度上,骨脆性的增加和骨量的较少均取决于雌激素的水平。研究显示,骨形成和骨吸收指标水平在妇女绝经后分别有不同程度的上升,且幅度较大[5]。
目前国内外骨质疏松各防治指南中,运用西药(主要为雌激素)治疗骨质疏松治疗效果较为肯定,但不良反应、并发症一直以来都是亟待解决的难题[6],因此,在寻求治疗效果的同时不能忽略药物的安全性。中医药治疗PMOP几十年中,特别最近几年,临床研究、相关专题性报道的大量涌现,结论的准确性尚待进一步考证。为进一步观察中医药的安全性、有效性及不良反应等,本研究采用Cochrane系统评价方法,对既往临床研究文献进行梳理和Meta分析,以明确中医药或中西医结合治疗PMOP的治疗效果,为临床运用中医药提供依据,起到一定的指导与服务作用。
材料与方法 纳入、排除标准纳入标准:(1)随机对照试验(randomized controlled trials, RCT);(2)公开发表的文献(限中文和英文);(3)研究对象:患有PMOP;(4)干预措施:观察组给予治疗骨质疏松症的补肾类中医药(包括中药、中成药以及中药合剂等),或中西医联合用药;对照组给予非中医药(包括各种抗骨质疏松药物等);(5)结局指标:骨折数、视觉模拟评分法(visual analogue score, VAS)、腰椎骨密度(bone mineral density,BMD)及髋部BMD(包括股骨颈、粗隆、大转子等)、骨钙素(bone gla protein,BGP)、Ⅰ型原胶原N-端前肽(propeptide of type 1 procollagen,P1NP)、Ⅰ型胶原交联C-末端肽(β cross-linked C-telopeptide of type 1 collagen,β-CTX)等骨代谢指标和雌二醇(estradiol,E2)。
排除标准:(1)动物实验;(2)文献设计方法不当,或不严谨,或重复发表;(3)文献尚未公开发表;(4)患者诊断为非绝经后骨质疏松症;(5)对照组给予中医药或中西医联合用药。
检索策略计算机检索CNKI、VIP、万方、Embase、PubMed、Medline等数据库建库至2019年5月发表的文献;英文检索策略:通过检索词“Chinese medicine for Tonifying kidney”、“osteoporosis”组合检索;中文检索策略:运用检索词“补肾中药”、“骨质疏松”在各数据库中进行检索,条目最多者为最终检索结果,并输录于EndNoteX9软件中。
文献质量评估质量评价:运用Cochrane协作网的偏倚风险评价工具,对所纳入的随机对照试验(randomized controlled trial,RCT)进行测评。包括7个主要项目:随机方法,分配隐藏方案,对研究员与受试者是否采取盲法,结果数据是否完整,选择性报告研究结果,其他偏倚问题来源。
质量评分:运用Cochrane系统评价方法-Jadad评分法[6],对所纳入文献进行质量评分:1~3分低质量;4~5分中等质量;6~7分为高质量(表 1)。
| 文献来源 | 质量评分 | 样本量 | 干预措施 | 结局指标 | 不良反应 | |||
| T/C | 试验组 | 对照组 | 总疗程 | |||||
| 孔西建等[7]2015 | 3分 | 60/58 | 骨松益骨方+CTs | CTs | 6个月 | VAS、骨折发生率 | 未记录不良反应 | |
| 刘国泰等[8]2014 | 2分 | 30/30 | 强骨饮 | CTs | 6个月 | VAS、β-CTX、P1NP | T:1例胃部不适,1例便秘;C:1例便秘 | |
| 卞庆来等[9]2018 | 3分 | 24/24 | 青娥丸+CT | CT | 6个月 | VAS、β-CTX、P1NP、BMD1、BMD2 | 无明显不良反应 | |
| 王均华等[10]2018 | 3分 | 34/34 | 金天格胶囊 | CT | 6个月 | VAS、BMD1、BGP、ALP | T:3例出现口干、1例便秘;C:1例便秘 | |
| 钟秋生等[11]2015 | 3分 | 99/99 | 健脾益气方 | CT | 3个月 | E2 | T:6例出现口干口苦;C:15例恶心、头痛 | |
| 黄海卫等[12]2018 | 2分 | 30/30 | 青娥丸 | CT | 1个月 | VAS、BMD1、BMD2 | 无明显不良反应 | |
| 沈智等[13]2018 | 3分 | 50/50 | 强骨胶囊+CT | CT | 6个月 | BMD1、BGP、ALP、P1NP | 未记录不良反应 | |
| 唐保明[14]2015 | 3分 | 62/62 | 补肾调冲方+CT | CT | 6个月 | VAS、E2、BGP、BMD1 | 未记录不良反应 | |
| 王晓东等[15]2011 | 5分 | 61/61 | 护骨胶囊 | CT | 6个月 | VAS、BGP、BMD1、BMD2 | T:3例出现轻度便秘 | |
| 韩艳等[16]2015 | 2分 | 20/20 | 补肾活血方+CT | CT | 6个月 | VAS、BMD1、BMD2 | 无明显不良反应 | |
| 谭英华等[17]2016 | 2分 | 30/30 | 补脾益肾方+CTs | CTs | 3个月 | E2、BMD1、BMD2、BGP、β-CTX | 未记录不良反应 | |
| 杨通宇等[18]2016 | 2分 | 46/40 | 鹿角壮骨胶囊+CTs | CTs | 6个月 | VAS、P1NP、β-CTX、BMD1、BMD2 | 未记录不良反应 | |
| 余贤斌等[19]2015 | 3分 | 30/30 | 骨康胶囊 | CT | 6个月 | β-CTX、P1NP、BMD1、BMD2 | 未记录不良反应 | |
| 孙艳红等[20]2017 | 2分 | 35/35 | 补肾健骨汤+CTs | CTs | 6个月 | β-CTX、BMD1、BMD2 | 无明显不良反应 | |
| 杜增峰等[21]2016 | 2分 | 55/55 | 骨愈灵胶囊+CT | CT | 2个月 | BGP、BMD1、BMD2 | 无明显不良反应 | |
| 黄付伟等[22]2018 | 3分 | 38/37 | 骨松键骨丸+CT | CTs | 3个月 | VAS、BGP | 未记录不良反应 | |
| 张宝荣等[23]2017 | 2分 | 32/32 | 左归丸+CTs | CT | 3个月 | E2、β-CTX、P1NP | 未记录不良反应 | |
| 徐玉禄等[24]2018 | 3分 | 40/40 | 精骨补骨颗粒 | CT | 6个月 | VAS、E2、BMD1 | 未记录不良反应 | |
| 张鹏贵等[25]2017 | 1分 | 70/70 | 独活寄生汤+CT | CT | 12个月 | BGP、E2 | 无明显不良反应 | |
| 王少锋等[26]2017 | 1分 | 50/50 | 独活寄生汤+CT | CT | 12个月 | E2、BGP、BMD1 | 无明显不良反应 | |
| 付江涛等[27]2017 | 3分 | 46/46 | 补肝益肾方+CTs | CTs | 6个月 | VAS、E2、BMD1 | T:2例出现发热、便秘;C:4例出现发热、便秘 | |
| 王丽丽等[28]2017 | 2分 | 56/56 | 补肾生骨颗粒 | CT | 6个月 | VAS | 未记录不良反应 | |
| 陈悦霞等[29]2017 | 2分 | 50/50 | 强筋壮骨合剂+CTs | CTs | 6个月 | VAS | 无明显不良反应 | |
| 李岩等[30]2013 | 3分 | 123/127 | 劲骨坚颗粒 | CT | 3个月 | E2、ALP、BGP | T:13例出现口干、便秘;C:30例出现口干便秘 | |
| 代轶楠等[31] 2016 | 3分 | 30/30 | 淫羊藿胶囊 | CT | 6个月 | β-CTX、P1NP | 未记录不良反应 | |
| 戴少川等[32] 2018 | 3分 | 79/79 | 杜仲壮骨颗粒+CT | CT | 12个月 | BMD1、BMD2、β-CTX、BGP、ALP、P1NP | T:7例出现胃肠道反应;C:5例出现胃肠道反应 | |
| 陈桂林等[33]2017 | 2分 | 42/42 | 补肾中药+CT | CT | 6个月 | E2、BMD1 | 无明显不良反应 | |
| 万雷[34]2009 | 2分 | 24/24 | 骨康口服液+CTs | CTs | 6个月 | E2、BMD1 | 未记录不良反应 | |
| T:试验组;C:对照组;CT:一种常规药物治疗;CTs:两种及以上常规药物治疗;VAS:视觉模拟评分;β-CTX:Ⅰ型胶原交联C-末端肽;P1NP:Ⅰ型原胶原N-端前肽;E2:雌二醇;BGP:骨钙素;ALP:碱性磷酸酶;BMD1:腰椎骨密度;BMD2:髋部骨密度 | ||||||||
运用RevMan5.3软件进行数据的处理与分析。采用比值比(odds ratio, OR)/相对危险度(relative risk,RR)分析二分类变量;若为连续性变量则采用均数差(mean difference,MD);二者均采用95%置信区间(confidence interval,CI)来表示各效应量。异质性检验采用I2检验,当多个同类研究(P>0.05,I2≤50%),说明有同质性,Meta分析采用固定效应模型;若(P<0.05,I2≥50%),说明各研究间存有异质性,Meta分析则采用随机效应模型。当异质性过大时,可进行描述性分析。针对某项指标,当文献数量≥10篇时,可做漏斗图检测是否存有偏倚。
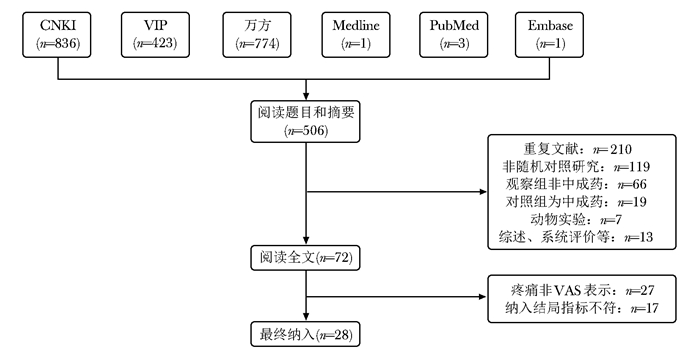
结果 文献筛选流程根据相关关键词检索,初步检索出文献2 038篇,并依据初期的纳入和排除标准对文献进行筛选。通过阅读题目和摘要得到506篇,进一步阅读全文,剔除重复文献、不符合纳入和排除标准的文献、最终共28篇被纳入本评价中,均为中文文献(图 1)。
|
| 图 1 文献检索流程及结果 Figure 1 Flow chart of literature screening VAS:视觉模拟评分 |
纳入的28篇文献中,有两组符合纳入指标的5篇,将这5篇文献进行拆分,计为10项研究,相当于分析33个原始研究。28篇文献共计受试者2 687例,其中1 346例为观察组,1 341例为对照组,127例为最大样本量,20例为最小样本量,具体信息及纳入指标见表 1。
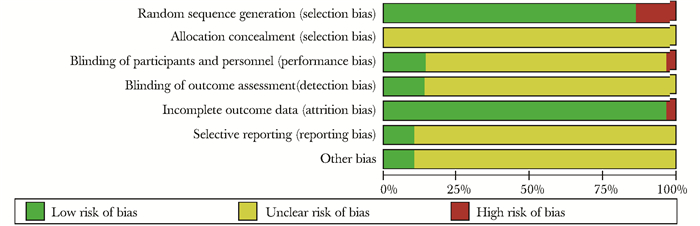
方法学质量所纳入研究均提到了随机方法,其中有4项[12, 21-22, 26]研究按照诊疗方法或就诊顺序进行随机分组,方法失当;1项[15]研究采取了双盲,具体实施方法未交代;有7项[7-8, 16, 20, 22, 24, 31]研究出现了失访及脱落,其中5项[8, 16, 20, 22, 31]研究交代了脱落原因,包括患者的身体因素以及部分患者依从性较差等;纳入的28项研究均未描述分配隐藏,均未交代是否采用盲法对结局进行评估;对选择性报告偏倚、以及其他偏倚来源均不清楚,因此,采用风险偏倚评估工具对纳入研究进行质量评价(图 2)。
|
| 图 2 纳入研究偏倚风险评估图 Figure 2 Risk of bias assessment in the studies |
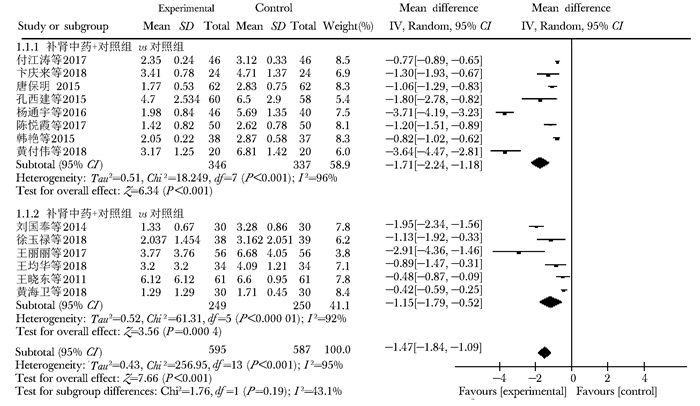
疼痛改善情况:报告两组干预措施治疗前后VAS疼痛评分改变的有14项研究,各研究间异质性检验I2=99%,具有高异质性。按照治疗方式不同进行亚组分析。其中8项为补肾中药与常规治疗对照研究,异质性检验I2=96%,具有高异质性,(MD=-1.71,95% CI:-2.24~-1.18,P<0.001);6项研究为补肾中药+常规治疗与常规治疗对照,异质性检验I2=92%,高异质性(MD=-1.15,95% CI:-1.79~-0.52,P<0.001)。故采用随机效应模型,组间比较差异有统计学意义(图 3)。
|
| 图 3 中医药改善VAS的亚组分析 Figure 3 Subgroup analysis of Chinese medicine improving VAS VAS:视觉模拟评分 |
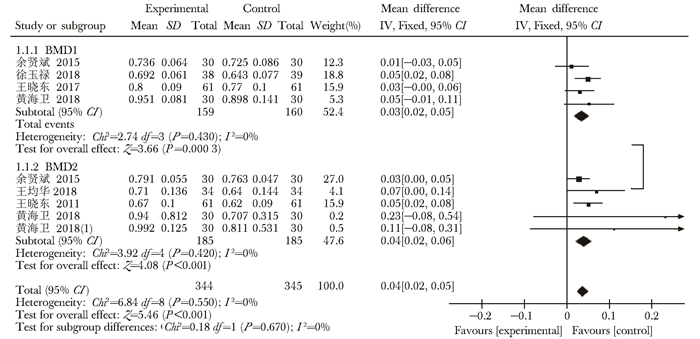
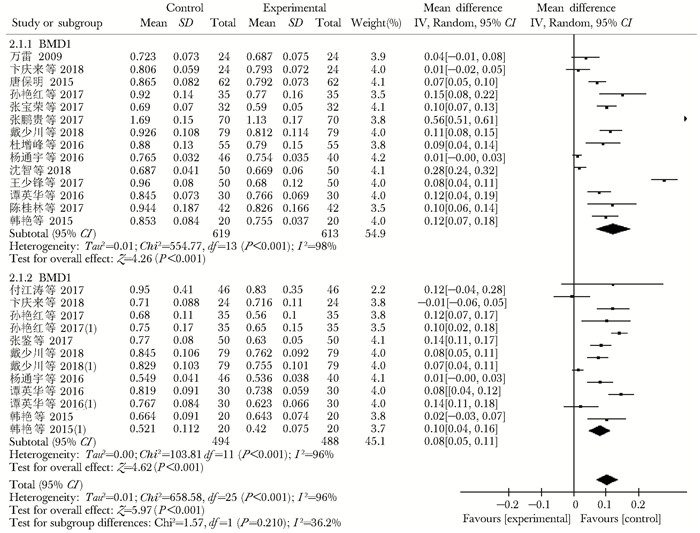
BMD:共18项研究对BMD进行了报告,按不同部位BMD、不同治疗方案分别进行亚组分析。其中有6项研究以补肾中药与常规治疗两种干预措施对不同部位BMD进行了报告,各研究间异质性检验I2=0%,无异质性(MD=0.04,95% CI:0.02~0.05,P<0.001);共12项研究以补肾中药+常规治疗与常规治疗对不同部位BMD进行了报告,各研究间异质性检验I2=96%,异质性较高(MD=0.10,95% CI:0.07~0.11,P<0.001),两组均采用随机效应模型,组间比较差异有统计学意义(图 4,5)。
|
| 图 4 补肾中药与常规治疗BMD亚组比较森林图 Figure 4 Forest plots of BMD subgroup comparison of Chinese medicine for Tonifying kidney plus conventional therapy BMD:骨密度 |
|
| 图 5 补肾中药+常规治疗与常规治疗BMD亚组比较森林图 Figure 5 Forest plots of BMD subgroup comparison of Chinese medicine for Tonifying kidney plus conventional therapy and conventional therapy BMD:骨密度 |
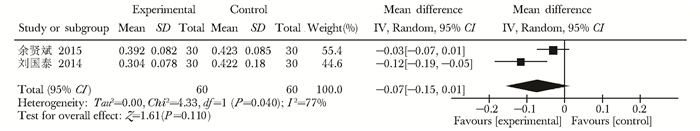
β-CTX:共有8项研究报告了β-CTX,其中补肾中药与常规治疗对照的有2项研究,其异质性检验I2=77%,P=0.040,Meta分析采用随机效应模型(MD=-0.07,95% CI:-0.15~0.01,P=0.110),两组比较差异无统计学意义(图 6)。
|
| 图 6 补肾中药与常规治疗β-CTX水平比较森林图 Figure 6 Forest plots of β-CTX level comparison in Chinese medicine for Tonifying kidney plus conventional therapy β-CTX:Ⅰ型胶原交联C-末端肽 |
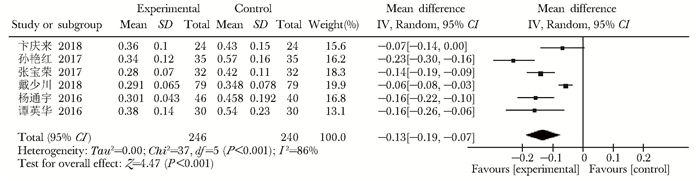
补肾中药+常规治疗与常规治疗对照有6项研究,异质性检验I2=86%,P<0.001,高异质性,Meta分析采用随机效应模型(MD=-0.13,95% CI:-0.19~-0.07,P<0.001),两组比较差异有统计学意义(图 7)。
|
| 图 7 补肾中药+常规治疗与常规治疗β-CTX水平比较森林图 Figure 7 Forestry plots of of β-CTX level comparison in Chinese medicine for Tonifying kidney plus conventional therapy and conventional therapy β-CTX:Ⅰ型胶原交联C-末端肽 |
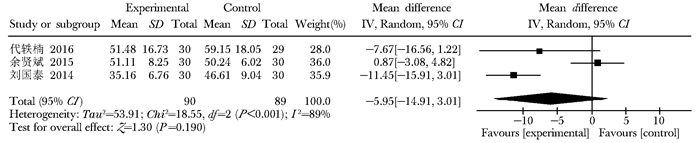
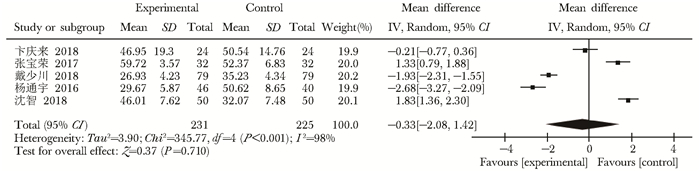
P1NP:共8项研究报告了P1NP,补肾中药与常规治疗对照研究有3项,异质性检验I2=89%,P=0.490,因此Meta分析采用随机效应模型(MD=-5.95,95% CI:-14.91~3.01,P=0.190),两组比较差异无统计学意义(图 8)。补肾中药+常规治疗与常规治疗对照的有5项研究,异质性检验I2=98%,P<0.001,具有高异质性,Meta分析采用随机效应模型(MD=-0.33,95% CI:-2.08~1.42,P=0.710),两组比较差异无统计学意义(图 9)。
|
| 图 8 补肾中药与常规治疗P1NP水平比较森林图 Figure 8 Forest plots of P1NP level comparison of Chinese medicine for Tonifying kidney and conventional therapy P1NP:Ⅰ型原胶原N-端前肽 |
|
| 图 9 补肾中药+常规治疗vs常规治疗P1NP水平比较森林图 Figure 9 Forest plots of P1NP level comparison between Chinese medicine for Tonifying kidney plus conventional therapy vs conventional therapy |
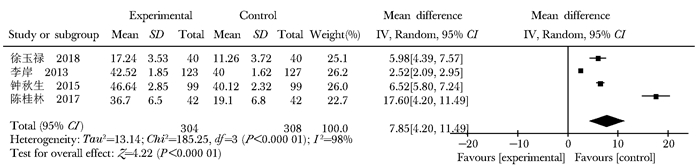
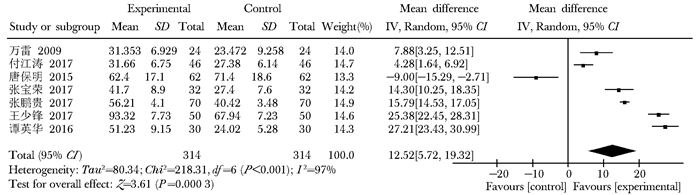
E2:共11项研究报告了E2,干预措施为补肾中药与常规治疗的研究有4项,异质性检验I2=98%,P<0.001,高异质性,因此采用随机效应模型进行Meta分析(MD=7.85,95% CI:4.20~11.49,P<0.001],两组比较差异无统计学意义(图 10)。补肾中药+常规治疗与常规治疗对照的有7项研究,异质性检验I2=97%,P<0.001,具有高异质性,Meta分析采用随机效应模型(MD=12.52,95% CI:5.72~19.32,P<0.001],两组比较差异有统计学意义(图 11)。
|
| 图 10 补肾中药与常规治疗E2水平比较森林图 Figure 10 Forest plots of E2 level comparison of Chinese medicine for Tonifying kidney plus conventional therapy E2:雌二醇 |
|
| 图 11 补肾中药+常规治疗与常规治疗E2水平比较森林图 Figure 11 Forest plots of E2 Level comparison of Chinese medicine for Tonifying kidney plus conventional therapy and conventional therapy E2:雌二醇 |
纳入的28项研究中,仅有1项研究报告了骨折。报告不良反应的研究有7项,记录无明显不良反应的有8项,另外13项未记录不良反应。不良反应所记录患者大多数多表现为胃肠道不适,如便秘、腹泻、恶心、呕吐等;另有的患者服用西药时出现头痛、乏力,甚至有的患者可见心悸;部分患者服药后会见咳嗽、发热、面部潮红、口干等现象。
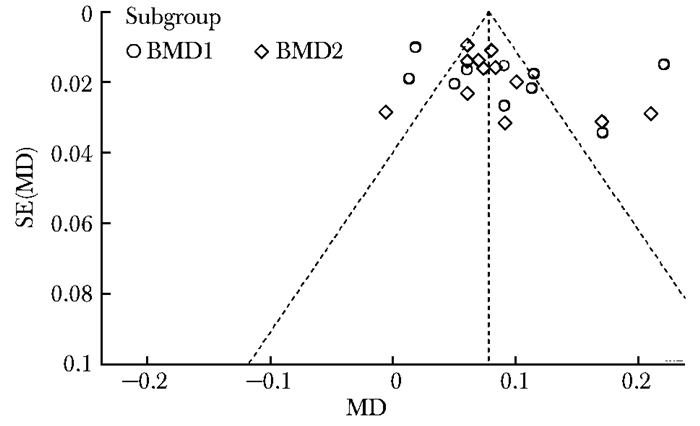
发表偏倚评估在各研究所报告的指标中,补肾中药+常规治疗组中腰椎BMD、髋部BMD涉及研究超过10项,因此,采取了发表偏倚评估:BMD1和BMD2在图中两侧对称性较差,表明有发表偏倚的可能性存在(图 12)。
|
| 图 12 腰椎及髋部BMD漏斗图 Figure 12 BMD funnel diagram of lumbar spine and hip BMD:骨密度 |
针对目前国内尚无统一的关于骨质疏松治疗效果的判断标准,本研究选取了较为常用的指标进行Meta分析。分别从补肾中药治疗PMOP的VAS、提高不同部位骨密度、改善各项骨代谢指标以及降低脆性骨折发生率等方面进行评价、分析。在改善患者骨痛方面补肾中药单用或联合常规治疗使用,效果均优于常规治疗组;提高患者骨密度方面,单用补肾中药或联合常规治疗,其治疗效果亦优于常规治疗组;补肾中药单用在改善CTX治疗水平方面,与常规治疗比较未见明显差异,而补肾中药联合常规治疗时,效果反而优于常规治疗组;在改善Ⅰ型原胶原N-端前肽方面,单用补肾中药治疗效果与常规治疗相当,联合用药较常规治疗较效果较好;但从补肾中药改善CTX和P1NP方面而言,在研究报告有限的情况下,尚不能对其治疗效果进行肯定,有待于进一步考究。
11项对雌二醇的研究表明,补肾中药单用或者联合西药运用,治疗效果较单纯西药治疗更具优势,这说明,中药在调节绝经后女性的雌激素水平方面有一定作用。在安全性方面,7项研究报告了患者在服用中药或西药等抗骨质疏松药物期间发生了不良反应,具体包括手、面部潮红,口干、恶心、头痛、乏力、便秘、心悸以及胃肠道反应等,但所占受试者总体比例较小,且治疗组与对照组均有出现,经一定处理或疗程结束后能自行缓解,因此,不排除与患者自身体质相关,这说明中药的安全性相对较好。
本Meta分析所纳入研究多数为中文文献,相关英文文献缺乏,总体质量偏低,从而导致了范围上的局限性;且主要结局指标——骨折发生率纳入研究较少(仅1项提及),未来需要更多的相关研究,且需对受试患者开展长期随访,以观察骨折发生率;纳入研究在方案设计、方法学上存在一定差异,如纳入的4项随机研究,以就诊顺序进行编码,方法不恰当,很可能导致结果失准;各研究均未使用分配隐藏,大多数未使用盲法;纳入各研究多数未能保证受试者的良好依从性,如患者未能按时、按量服药,也会导致结局指标的检测结果不确切。因此,日后开展相关研究,需要进行临床多中心、大样本量研究等,严谨的方法学设计,严格执行各项标准、保证患者的依从性才是获得确切结果的关键,才能确保临床研究的质量,为以后进行系统评价提供更有利的条件。
| [1] | Szamatowicz M. How can gynaecologists cope with the silent killer-osteoporosis[J]. Prz Menopauzalny, 2016, 15: 189–192. |
| [2] | Burckhardt P, Christiansen C, Fleisch H, et al. Consensus development conference:prophylaxis and treatment of osteoporosis[J]. Am J Med, 1987, 295: 914–915. |
| [3] | 中国健康促进基金会骨质疏松防治中国白皮书编委会. 骨质疏松症中国白皮书[J]. 中华健康管理学杂志, 2009, 3: 148–154. DOI:10.3760/cma.j.issn.1674-0815.2009.03.006 |
| [4] | 中华医学会骨质疏松和骨矿盐疾病分会. 原发性骨质疏松症诊疗指南(2017年)[J]. 中华骨质疏松和骨矿盐疾病杂志, 2017, 5: 1674–2591. |
| [5] | 李薇, 张博, 张雨薇, 等. 雌激素调节骨代谢作用的研究进展[J]. 中国骨质疏松杂志, 2017, 23: 3963–3982. |
| [6] | 李静, 陈德才, 王覃. 2016年《美国内分泌医师协会与美国内分泌协会绝经后骨质疏松症诊疗指南》解读[J]. 中国全科医学, 2017, 20: 891–895. |
| [7] | 孔西建, 李盈盈, 翟远坤, 等. 骨松益骨方联合阿仑膦酸钠治疗脾肾气虚血瘀型原发性骨质疏松症的治疗效果观察[J]. 中医药导报, 2015, 21: 19–24. |
| [8] | 刘国泰, 王建辉, 周莉, 等. 强骨饮治疗绝经后骨质疏松症的临床研究[J]. 中国药物警戒, 2014, 11: 652–656. |
| [9] | 卞庆来, 邹小娟, 沈霖. 青娥丸治疗绝经后骨质疏松症肾虚血瘀证的治疗效果观察[J]. 中华中医药杂志, 2018, 33: 308–312. |
| [10] | 王均华, 肖蔚林, 杨依然, 等. 金天格胶囊对股骨粗隆间骨折患者术后骨密度影响的临床研究[J]. 中国中医骨伤科杂志, 2018, 26: 26–29. |
| [11] | 钟秋生, 韩临晓, 陆向然, 等. 健脾益气方对绝经后女性骨质疏松症的临床治疗效果观察[J]. 世界中西医结合杂志, 2015, 10: 378–380. |
| [12] | 黄海卫, 王宇. 青蛾丸治疗绝经后肾虚血瘀型骨质疏松症临床观察[J]. 辽宁中医药大学学报, 2018, 20: 138–140. |
| [13] | 沈智, 曾景奇, 李益亮, 等. 强骨胶囊联合维D2磷葡钙片治疗老年性骨质疏松症50例总结[J]. 湖南中医杂志, 2018, 34: 7–9. |
| [14] | 唐保明. 补肾调冲方治疗绝经后骨质疏松症62例[J]. 中国实验方剂学杂志, 2015, 21: 191–194. |
| [15] | 王晓东, 邓伟民, 洪曼杰, 等. 护骨胶囊治疗绝经后妇女骨质疏松症的临床研究[J]. 实用医学杂志, 2011, 27: 1662–1664. DOI:10.3969/j.issn.1006-5725.2011.09.058 |
| [16] | 韩艳, 刘娜, 吴春雷, 等. 唑来膦酸配合补肾活血方治疗绝经后骨质疏松临床分析[J]. 中华全科医学, 2015, 13: 402–404. |
| [17] | 谭英华, 熊仁青. 补脾益肾方药治疗围绝经期骨质疏松症的临床研究[J]. 中医药导报, 2016, 22: 64–68. |
| [18] | 杨通宇, 胡建山, 李文忠, 等. 鹿角壮骨胶囊治疗绝经后骨质疏松症患者的临床治疗效果观察[J]. 中国妇幼保健, 2016, 31: 1034–1036. |
| [19] | 余贤斌, 孙辽军, 胡炜. 骨康胶囊治疗绝经后骨质疏松的临床应用及对股转换标志物水平的影响[J]. 中华中医药学刊, 2015, 33: 2970–2972. |
| [20] | 孙艳红, 韩正云, 李建民. 补肾健骨汤对绝经后骨质疏松症患者骨密度及骨代谢指标的影响[J]. 河北中医药学报, 2017, 32: 546–549. |
| [21] | 杜增峰, 贺耀耀, 马晓磊, 等. 骨愈灵胶囊联合注射用骨肽治疗骨质疏松症的临床研究[J]. 现代药物与临床, 2016, 31: 126–129. |
| [22] | 黄付伟, 孔西建, 朱静栋. 骨松健骨丸治疗绝经后骨质疏松症的临床治疗效果观察[J]. 世界中西医结合杂志, 2018, 13: 1116–1122. |
| [23] | 张宝荣, 谭颖颖. 左归丸加味对绝经后骨质疏松症患者骨转换标志物和骨密度的影响[J]. 陕西中医药大学学报, 2017, 40: 48–50. |
| [24] | 徐玉禄, 王群, 邢亚群, 等. 精骨补骨颗粒治疗绝经后骨质疏松症38例临床观察[J]. 中华全科医学, 2018, 16: 1188–1191. |
| [25] | 张鹏贵, 杜耿. 独活寄生汤联合唑来膦酸治疗绝经后骨质疏松肝肾亏虚证70例[J]. 河南中医, 2017, 37: 1446–1448. |
| [26] | 王少锋, 戴浩军. 独活寄生汤辅助治疗绝经后骨质疏松症治疗效果分析[J]. 中贵州医药, 2017, 41: 65–66. |
| [27] | 付江涛, 彭页, 黄永红, 等. 补肝益肾方治疗绝经后骨质疏松症的临床观察[J]. 中国医药导报, 2017, 14: 86–89. |
| [28] | 王丽丽, 房经武, 王金国. 补肾生骨颗粒对肾虚血瘀型绝经后骨质疏松症BMD、E2、BALP、N-MID的影响[J]. 世界中医药, 2017, 12: 293–298. DOI:10.3969/j.issn.1673-7202.2017.02.014 |
| [29] | 陈悦霞, 葛美芳, 朱青. 强筋壮骨祛风合剂对老年原发性骨质疏松症的临床观察[J]. 中草药, 2017, 48: 2266–2268. |
| [30] | 李岩, 李跃华. 劲骨坚颗粒对骨代谢指标的影响[J]. 吉林中医药, 2013, 33: 265–267. DOI:10.3969/j.issn.1003-5699.2013.03.023 |
| [31] | 代轶楠, 向楠, 周广文. 淫羊藿胶囊对绝经后骨质疏松患者骨密度及骨代谢标志物的影响[J]. 湖北中医杂志, 2016, 38: 3–5. |
| [32] | 戴少川. 杜仲壮骨胶囊联合雷洛昔芬治疗绝经后骨质疏松症临床研究[J]. 中国骨质疏松杂志, 2018, 24: 1489–1492. DOI:10.3969/j.issn.1006-7108.2018.11.020 |
| [33] | 陈桂林. 阿仑磷酸钠联合中医治疗老年女性绝经后骨质疏松的安全性及临床治疗效果观察[J]. 黑龙江医药, 2017, 30: 116–118. |
| [34] | 万雷. 十味骨康口服液治疗绝经后骨质疏松症24例[J]. 辽宁中医杂志, 2009, 36: 1926–1927. |
| (收稿日期:2019-01-11) |

