本课题组有关铁蓄积与骨质疏松的前期研究表明,绝经后女性骨质疏松症患者中存在铁蓄积[1-2];铁蓄积可通过活性氧损伤导致骨质疏松症的发生和发展[3-4]。在此研究背景下,本课题组研究使用降低铁蓄积的方法防治绝经后骨质疏松。临床上降低铁蓄积的主要方法是使用铁螯合剂。去铁酮 (deferiprone,DFP) 是2011年由美国食品和药物管理局 (Food and Drug Administration,FDA) 批准在美国上市的一种可口服的铁螯合剂,与铁具有良好的亲和力,可有效地控制体内铁负荷。但是,DFP对骨代谢作用如何,目前尚未有十分全面的研究报道。本研究从DFP对成骨细胞作用的研究入手,使用不同浓度的DFP体外干预小鼠前体成骨样细胞MC3T3-E1,观察DFP对MC3T3-E1细胞增生、分化以及细胞铁代谢的作用,旨为DFP对骨代谢影响的研究提供初步实验资料。
材料与方法 主要材料与仪器小鼠前体成骨样细胞MC3T3-E1(中科院上海细胞库);去铁酮 (美国Selleck公司);改良型α-MEM (美国Gibico公司);胎牛血清 (美国Gibico公司);CCK-8检测试剂盒 (日本DojinDo公司);Trizol (美国Invitrogen公司);碱性磷酸酶 (alkaline phosphatase,ALP) 活性检测试剂盒 (日本Labassay公司);BCA蛋白试剂盒 (南通碧云天公司);荧光定量PCR mix (美国Madison公司);酶标仪 (美国Thermo公司);荧光定量PCR仪 (美国AB applied biosystems公司)。
实验方法细胞培养:小鼠MC3T3-E1细胞常规培养于改良型α-MEM培养基 (含10%的胎牛血清、青霉素100 μg/mL和链霉素100 μg/mL),5% CO2、37 ℃条件培养。根据细胞的培养情况每2~3 d换液1次,细胞密度长至70%~80%时进行传代。
细胞增生检测:采用CCK-8法。MC3T3-E1细胞接种于96孔板中,每孔7 000个。细胞贴壁后更换培养液同时加入终浓度为50 μg/mL抗坏血酸和10 mmol/L β-甘油磷酸钠,同时分别加入终浓度为25、50、100 μmol/L的DFP,细胞分为5组,即DMSO溶剂组、对照组 (加入不含DFP的等量培养基),25 μmol/L DFP组、50 μmol/L DFP组、100 μmol/L DFP组。每组3个复孔。干预48 h后,每孔加入10 μL CCK-8试剂,37 ℃孵育1 h后终止培养。在15 min内用酶标仪测定450 nm波长的各孔吸光度 (A) 值。
ALP活性检测:MC3T3-E1细胞接种于6孔板中,每孔1×105个。细胞贴壁后更换培养液并加入终浓度为50 μg/mL抗坏血酸和10 mmol/L β-甘油磷酸钠,同时分别加入终浓度为25、50、100 μmol/L的DFP,细胞分为4组,即对照组 (加入不含DFP的等量培养基),25 μmol/L DFP组、50 μmol/L DFP组、100 μmol/L DFP组。每组3个复孔。培养10 d后,各孔加75μL Triton X-100裂解细胞,收集上清液,用BCA试剂盒测定总蛋白浓度,用ALP活性测定试剂盒测定ALP含量。用酶标仪测定520 nm波长的各孔的吸光值 (A值),根据测得A值计算单位蛋白浓度中ALP的相对活性。
实时定量PCR检测:采用实时定量PCR 2-△△CT法。MC3T3-E1细胞接种于6孔板中,每孔1×105个。细胞贴壁后更换培养液并加入终浓度为50 μg/mL抗坏血酸和10 mmol/L β-甘油磷酸钠,同时分别加入终浓度为25、50、100 μmol/L的DFP,细胞分为4组,即对照组 (加入不含DFP的等量培养基),25 μmol/L DFP组、50 μmol/L DFP组、100 μmol/L DFP组。每组3个复孔。干预72 h后,使用Trizol试剂常规提取细胞总RNA,经反转录成cDNA。PCR反应体系为20 μL,反应条件:95 ℃ 30 s,60 ℃ 30 s,72 ℃ 30 s,40个循环,同时追加溶解曲线反应检测引物特异性。转铁蛋白受体 (TfR) 引物序列,上游:5′-GGCTACCTGGGCTATTGT-3′,下游:5′-CACGA GGAGTGTATGTATTCTG-3′;内参基因GAPDH引物序列,上游:5′-CCTGGAGAAACCTGCCAAGT A-3′,下游:5′-TCATACCAGGAAATGAGCTTGAC-3′。使用2-△△CT法计算TfR PCR产物的相对值,并使用Step OneTM软件V 2.1进行分析。
统计学方法实验中测定结果重复3次,采用统计分析软件SPSS17.0进行分析,实验所得数据用均数±标准差 (x±s) 表示,采用单因素方差分析 (One-way ANOVA) 进行检验,以P < 0.05为差异有统计学意义。
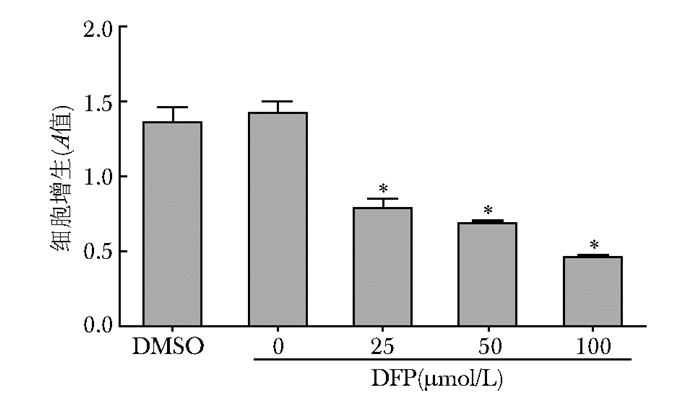
结果 细胞增生检测结果随着DFP干预浓度的增加,A值逐渐降低。DMSO溶剂组、对照组 (0 μmol/L) 和DFP 25、50、100 μmol/L组A值分别为1.36±1.10、1.41±0.09、0.78±0.06、0.68±0.03、0.46±0.01。DFP各浓度组与对照组 (0 μmol/L) 比较,差异有统计学意义 (P < 0.05)(图 1)。
|
| 图 1 不同浓度DFP对MC3T3-E1细胞增生的影响 Figure 1 Effects of various concentrations of DFP on proliferation of MC3T3-E1 cells DFP:去铁酮;与对照组 (0 μmol/L) 比较,*P < 0.05 |
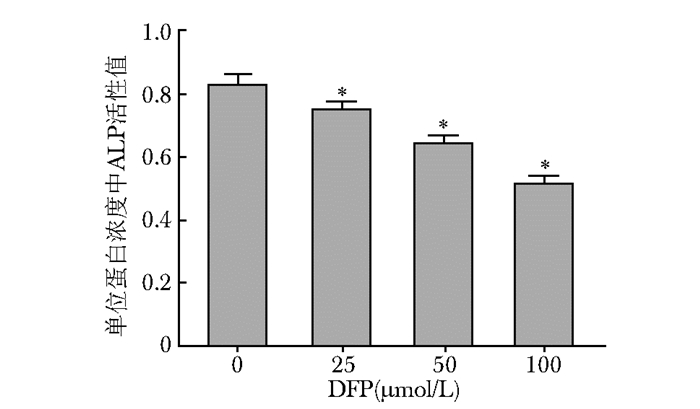
随着DFP干预浓度的增加,ALP活性指标逐渐降低。对照组 (0 μmol/L) 和DFP 25、50、100 μmol/L组ALP活性值分别为0.83±0.05、0.75±0.04、0.64±0.03、0.51±0.03。DFP各浓度组与对照组 (0 μmol/L) 比较,差异有统计学意义 (P < 0.05)(图 2)。
|
| 图 2 不同浓度DFP对MC3T3-E1细胞ALP活性的影响 Figure 2 Effects of various concentrations of DFP on ALP activity of MC3T3-E1 cells DFP:去铁酮;ALP:碱性磷酸酶;与对照组 (0 μmol/L) 比较,*P < 0.05 |
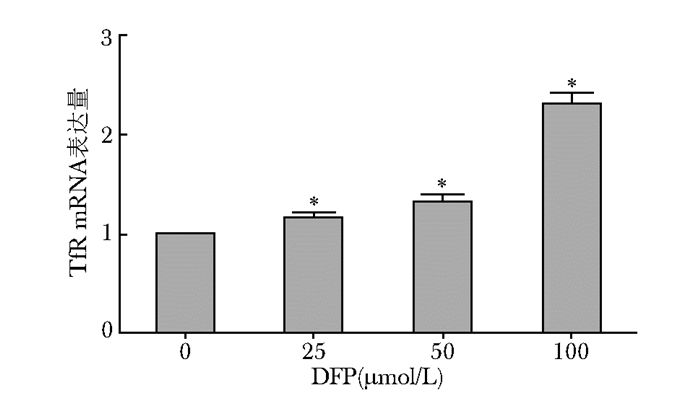
随着DFP干预浓度的增加,TfR mRNA表达量逐渐升高。对照组 (0 μmol/L) 和DFP 25、50、100 μmol/L组表达比分别为1、1.16±0.05、1.32±0.06、2.30±0.11。DFP各浓度组与对照组 (0 μmol/L) 比较,差异有统计学意义 (P < 0.05)(图 3)。
|
| 图 3 不同浓度DFP对MC3T3-E1细胞TfR mRNA表达的影响 Figure 3 Effects of various concentrations of DFP on expression of TfR mRNA in MC3T3-E1 cells DFP:去铁酮;TfR:转铁蛋白受体;与对照组 (0 μmol/L) 比较,*P < 0.05 |
MC3T3-E1细胞是一种小鼠前成骨细胞株,具有在抗坏血酸和β-甘油磷酸钠的作用下单一定向成骨细胞分化的各种生物学特征,被广泛应用于成骨细胞的相关体外研究中[5]。ALP是成骨细胞分化成熟的标志酶,一般认为,ALP活性越高,成骨细胞分化越趋成熟。TfR是细胞膜上的一种重要的铁摄取通道蛋白,其基因表达水平与细胞内铁离子浓度呈负相关,即其表达水平越高细胞内铁离子浓度越低,因此通过检测TfR可间接判断细胞内铁离子水平[6-7]。
在本研究中,使用DFP体外干预MC3T3-E1细胞48 h,细胞增生检测结果显示,随着DFP浓度的增加,细胞的增生逐渐下降;在MC3T3-E1细胞培养7 d即ALP分泌高峰时测定了ALP的活性,结果显示,随着DFP浓度的增加,细胞ALP的活性逐渐降低;DFP细胞干预72 h后,荧光定量PCR结果显示,随着DFP干预浓度增加,TfR mRNA的表达逐渐增加,提示细胞内铁离子逐渐减少因铁被DFP螯合。以上结果提示在本实验浓度内DFP可抑制MC3T3-E1细胞的增生和分化,螯合细胞内的铁离子。
2003年Suarez等[8]用去铁酮干预成骨细胞MG-63,发现高剂量的去铁酮 (180~240 μmol/L) 可抑制1,25OHD3引起的骨钙素分泌。本实验的研究结果与其相似,同样提示DFP对MC3T3-E1细胞的部分生物学活性有抑制作用。本研究组认为,这种抑制作用可能与DFP螯合细胞内的铁有关。DFP是一种可透膜的铁螯合剂,可有效螯合细胞内的铁离子。铁是细胞重要的微量元素,是细胞色素和某些呼吸酶的组成成分,细胞内铁的缺乏会导致细胞障碍。因此,在DFP的铁螯合作用下,MC3T3-E1细胞的部分生物学活性出现明显下降。
本实验是铁螯合剂DFP对成骨细胞作用的初步研究,实验指标简一,没有考虑到复杂的体内环境,这是本研究的局限。DFP对骨质疏松防治的意义究竟如何,尚需全面的研究探讨。
综上所述,本实验发现,DFP可能通过螯合小鼠前成骨细胞MC3T3-E1的铁离子抑制其增生和分化。本实验是DFP对成骨细胞作用的初步研究,为进一步探讨DFP对绝经后骨质疏松的作用提供了部分实验资料。
| [1] | 张林林, 姜习凤, 艾红珍, 等. 绝经后髋部脆性骨折中铁过载指标与骨密度骨转换指标关系的研究[J]. 中华外科杂志, 2013, 51 : 518–521. |
| [2] | 王兵, 赵环, 姜习凤, 等. 绝经后女性股骨头铁含量与骨密度的相关性[J]. 中华骨质疏松与骨矿盐杂志, 2013, 6 : 9–14. |
| [3] | He YF, Ma Y, Gao C, et al. Iron overload inhibits osteoblast biological activity through oxidative stress[J]. Biol Trace Elem Res, 2013, 152 : 292–296. DOI:10.1007/s12011-013-9605-z |
| [4] | 何银锋, 赵理平, 赵国阳, 等. 高铁环境下成骨细胞增生和凋亡与氧化应激的关系[J]. 中华骨质疏松和骨矿盐疾病杂志, 2012, 5 : 125–129. |
| [5] | Choi EM, Lee YS. Involvenment of P13K/Akt/CREB and redox changes in mitochondral defect of osteoblastic MC3T3-E1 cells[J]. Toxicol Vitro, 2011, 25 : 1085–1088. |
| [6] | Kuhn LC. Iron and gene expression: Molecular mechanisms regulating cellular iron homeostasis[J]. Nutr Rev, 1998, 56 : 54–75. |
| [7] | Gambling L, Danzeisen R, Gair S, et al. Effect of iron deficiency on placental transfer of iron transport proteins in vivo and in vitro[J]. Biochem J, 2001, 356 : 883–889. |
| [8] | Suarez IG, Martin JLF, Diaz MN, et al. Effect of desferrioxamine and deteriprone on the 1, 25(OH)(2) D-3-stimulated osteocalcin secretion in osteoblast-like cells[J]. Nefrologia, 2003, 23 : 27–31. |
| (收稿日期:2016-09-13) |

