2. 450052 郑州,郑州大学第一附属医院整形外科;
3. 450052 郑州,郑州大学第一附属医院药学部,河南省高等学校临床医学重点学科开放实验室
2. Department of Plastic Surgery, The First Affiliated Hospital of Zhengzhou University, Zhengzhou 450052, China;
3. Department of Pharmacy, First Affiliated Hospital of Zhengzhou University, Key-Discipline Laboratory of Clinical Medicine, Zhengzhou 450052, China
骨质疏松与肥胖已成为威胁人类健康的两大类慢性疾病。近来研究发现,肥胖可以引起骨折风险增加,可能是导致骨质疏松的另一危险因素[1]。成骨细胞的数量减少和功能降低所导致的骨量减低可引起骨质疏松的发生,其凋亡水平升高也影响骨生成的调节。因此,体内高脂环境诱导的成骨细胞凋亡增加可能是肥胖患者骨量减低的原因之一。在体外环境下,可以运用棕榈酸干预模拟肥胖患者体内高脂环境,研究脂毒性对细胞的影响。已有研究发现,棕榈酸可诱导包括成骨细胞在内的多种细胞凋亡[2-3]。内质网应激(endoplasmic reticulum stress,ERS)是细胞对自身的一种自我保护反应。适度的内质网应激可以维持细胞内稳态,发挥细胞保护作用,但长期或过度内质网应激反应则会造成细胞损伤甚至导致细胞调亡[4]。以往研究已经证明,内质网应激反应在棕榈酸诱导的人脐带间充质干细胞、胰岛细胞凋亡中发挥了重要作用[5-7],然而,在高脂诱导的成骨细胞凋亡的进程中是否有内质网应激的参与目前还不明确。本研究拟建立棕榈酸诱导成骨细胞凋亡的模型,且应用内质网应激抑制剂4-苯基丁酸(4-phenylbutyric acid,4-PBA)预处理细胞,从而进一步探讨内质网应激在此进程中所起到的作用。
材料与方法 材料小鼠成骨细胞MC3T3-E1 14购自中国科学院上海细胞研究所细胞库。
α-MEM培养基、胎牛血清购自GIBCO公司,胰蛋白酶、青-链霉素混合液、牛血清白蛋白购自北京索莱宝公司,二甲基亚砜(DMSO)购自北京鼎国公司,CCK-8检测试剂盒购自日本Dojindo公司,细胞凋亡检测试剂盒购自南京凯基公司,引物由上海生工公司设计并合成,棕榈酸购自上海生工公司,Trizol购自日本Takara公司,RT-PCR检测试剂盒购自日本Toyobo公司,4-苯基丁酸购自美国Sigma公司。
方法CCK-8法检测细胞增生活力:MC3T3-E1 Subclone 14细胞培养于含10%胎牛血清、1%青-链霉素混合液的α-MEM培养基中,置于37 ℃、含5% CO2的恒温培养箱中,隔天换液,每3 d传一代。将处于对数生长期状态良好的细胞以5×104/mL密度接种于96孔板,每孔100 μL,培养箱中预培养24 h后分别换为含BSA或不同浓度棕榈酸(100、250、500 μmol/L)的完全培养基分别孵育成骨细胞24 h;用含500 μmol/L棕榈酸的完全培养基孵育成骨细胞不同时间(0、6、12、24 h);为进一步验证内质网应激的作用,本研究用不同浓度的内质网应激抑制剂4-PBA (0、1.0、2.5、5.0、10.0 mmol/L)预处理细胞6 h后再加入500 μmol/L棕榈酸干预24 h。每组设置5个复孔。培养结束后,弃去旧的培养基,向每孔中加入10 μL CCK试剂,孵育2.5 h后用酶标仪测定各孔450 nm处吸光度(A值)。实验重复3次。
应用流式细胞仪检测细胞凋亡率:取对数生长期细胞计数后按1:3比例接种于75 cm2细胞培养瓶,分组方法与上述相同,每组设3个重复。培养结束后,用不含EDTA的胰酶消化收集各组细胞,采用Annexin V-PI双染法流式细胞术按试剂盒说明进行后续操作。实验重复3次。
反转录聚合酶链反应(real-time quantitative reverse transcription PCR,RT-qPCR)检测CHOP、GRP78和caspase-12 mRNA表达的变化:取对数生长期的细胞计数后按1:3比例接种于25 cm2细胞培养瓶,按照上述处理方法,对细胞进行干预,培养完成后收集各组细胞。Trizol法提取细胞总RNA,测定其浓度、纯度并按试剂盒说明书步骤逆转录为cDNA。引物由上海生工生物公司设计合成,引物名称引物序列扩增片段长度见表 1。PCR反应配置为蒸馏水6.4 μL,SYBR®Green Realtime PCR Master Mix 10 μL,上游引物(10 μmol/L)0.8 μL,下游引物(10 μmol/L)0.8 μL,样品cDNA溶液2 μL,总体积20 μL。
| 名称 | 引物序列 | 片段长度(bp) |
| GRP78 | F:5′-AGCGACAAGCAACCAAAGAT-3′ | |
| R:5′-CCCAGGTCAAACACAAGGAT-3′ | 139 | |
| CHOP | F:5′-GCGACAGAGCCAGAATAACAG-3′ | |
| R:5′-CAAGGTGAAAGGCAGGGACT-3′ | 138 | |
| Caspase-12 | F:5′-AAGGTAGGCAAGACTGGTTCC-3′ | |
| R:5′-AATAGTGGGCATCTGGGTCA-3′ | 147 | |
| GAPDH | F:5′-GGTGAAGGTCGGTGTGAACG-3′ | |
| R:5′-CTCGCTCCTGGAAGATGGTG-3′ | 233 |
配置完成后,将反应液轻轻地震荡混匀,用微型离心机离心30 s后上机,按以下条件进行反应(三步法):95 ℃ 1 min,40个循环:95 ℃ 15 s,60 ℃ 15 s,72 ℃ 45 s。采用2-ΔΔCT法对实验结果进行分析。
统计学方法采用SPSS17.0软件对实验结果进行统计学分析,数据以均数±标准差(x±s)表示。实验数据均进行正态分布检验及方差齐性检验,采用独立样本t检验进行两组间比较,单因素方差分析(one-way ANOVA)行多组间比较,以P < 0.05为差异有统计学意义。
结果 棕榈酸干预对成骨细胞增生活力的影响与对照组相比(A值: 1.015±0.068),250 μmol/L (A值: 0.816±0.108)和500 μmol/L (A值: 0.479±0.050)棕榈酸干预成骨细胞24 h可明显降低细胞增生活力(P < 0.05),而100 μmol/L棕榈酸组则对其增生率无明显影响(P > 0.05)。根据以上结果,本研究选择用具有明显作用的浓度500 μmol/L进行下一步实验。用500 μmol/L的棕榈酸干预6,12,24 h后,与对照组相比,细胞增生活力呈时间依赖性下降(A值: 0.952±0.064,0.788±0.043,0.683±0.044,0.482±0.052,P < 0.05),棕榈酸对成骨细胞增生活性的影响呈时间和剂量依赖性。
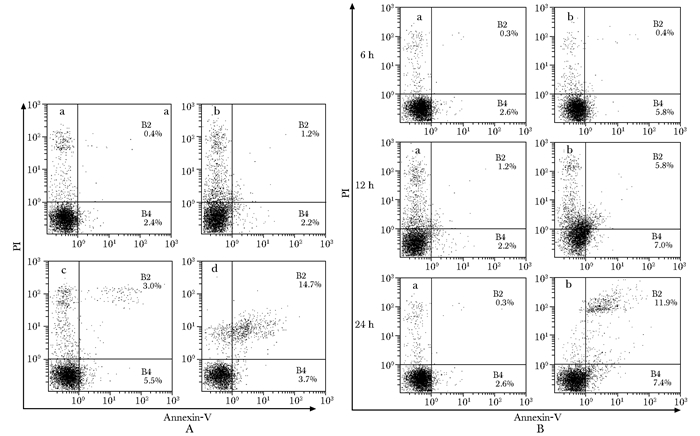
棕榈酸干预对成骨细胞凋亡率的影响用不同浓度棕榈酸作用24 h后,成骨细胞的凋亡率随着棕榈酸浓度的增高而升高,与对照组比较,250 μmol/L PA组增高了6.70%±1.40%,500 μmol/L PA组增高了15.30%±1.28%,差异有统计学意义(P < 0.05)(图 1A)。
|
| 图 1 棕榈酸干预对成骨细胞凋亡的影响 Figure 1 Effects of palmitate on MC3T3-E1 cell apoptosis A:不同浓度棕榈酸对成骨细胞凋亡的影响(a:对照组,b:100 μmol/L PA组,c:250 μmol/L PA组,d:500 μmol/L PA组);B:500 μmol/L棕榈酸作用不同时间对成骨细胞凋亡的影响(a:对照组,b:500 μmol/L PA组); PA:棕榈酸;PI:碘化丙啶棕榈酸对成骨细胞GRP78、CHOP、caspase-12 mRNA表达的影响 |
用500 μmol/L棕榈酸分别干预成骨细胞6,12,24 h后,各组细胞的凋亡率与对照组相比均有所增高且呈时间依赖性规律,分别增高了3.63%±1.45%,9.0%±2.31%,15.7%±0.61%(P < 0.05)(图 1B)。
与对照组相比,用250和500 μmol/L棕榈酸干预成骨细胞24 h后CHOP和GRP78 mRNA的表达水平呈剂量依赖性增高(均P < 0.05),然而caspase-12 mRNA的表达水平则有所降低(P < 0.05),100 μmol/L浓度组无明显差异(P > 0.05)。500 μmol/L棕榈酸分别处理细胞6,12,24 h后,CHOP的表达水平呈时间依赖性增高(P < 0.05);GRP78 mRNA表达水平在12 h开始升高,24 h达到峰值(P < 0.05);caspase-12 mRNA的表达水平则在12 h达到峰值,24 h后开始下降(P < 0.05)(表 2,3)。
| 棕榈酸浓度(μmol/L) | CHOP | GRP78 | Caspase-12 |
| 0(对照组) | 1.00±0.25 | 1.00±0.06 | 1.00±0.04 |
| 100 | 1.41±0.26 | 1.07±0.26 | 1.02±0.23 |
| 250 | 2.71±0.64* | 2.50±1.26* | 0.60±0.05* |
| 500 | 27.21±0.93* | 8.97±2.34* | 0.22±0.04* |
| 与对照组相比,*P < 0.05 | |||
| 干预时间(h) | CHOP | GRP78 | caspase-12 |
| 0 | 1.00±0.36 | 1.00±0.03 | 1.00±0.30 |
| 6 | 6.51±0.91* | 1.40±0.14 | 1.08±0.25 |
| 12 | 8.02±1.05* | 2.20±0.37* | 1.29±0.16* |
| 24 | 25.25±1.72* | 9.55±1.13* | 0.21±0.60* |
| 与0 h组相比,*P < 0.05 | |||
与单纯棕榈酸(500 μmol/L)干预组相比(A值:0.355±0.029),用5 mmol/L的4-PBA预处理细胞6 h后再加入棕榈酸干预细胞24 h可以使细胞的增生活力提高(A值:0.451±0.049,P < 0.05),而10 mmol/L 4-PBA组的这一作用则较为减低(A值:0.429±0.042,P < 0.05)。与对照组相比,单纯4-PBA干预组(5mmol/L)细胞增生活力差异无统计学意义(A值:0.849±0.040,P > 0.05)。
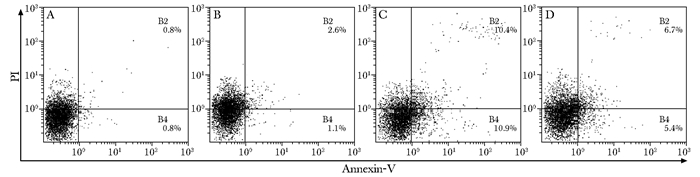
4-PBA预处理对棕榈酸干预成骨细胞凋亡率的影响与单纯棕榈酸干预组相比,用5 mmol/L的4-PBA预处理细胞6 h后再加入棕榈酸干预细胞24 h可以使细胞的凋亡率降低8.6%±2.05%,差异有统计学意义(P < 0.05)。与对照组相比,单纯4-PBA干预组细胞凋亡率无明显变化(P > 0.05)(图 2)。
|
| 图 2 4-PBA预处理对棕榈酸干预成骨细胞凋亡率的影响 Figure 2 Effects of 4-PBA exposure on apoptosis of palmitate treated MC3T3-E1 cells (x±s) A:对照组; B:4-PBA组; C:PA组; D:4-PBA+PA组; PA:棕榈酸;PI:碘化丙啶 |
与对照组相比,4-PBA可以降低棕榈酸引起的GRP78、CHOP mRNA表达增高,升高caspase-12 mRNA的表达减少,呈现与单纯棕榈酸干预组相反趋势(均P < 0.05)(表 4)。
| 组别 | CHOP | GRP78 | caspase-12 |
| 对照组 | 1.00±0.01 | 1.00±0.34 | 1.00±0.23 |
| 4-PBA | 2.25±0.70 | 1.51±0.66 | 1.72±0.63 |
| PA | 28.33±7.31* | 10.68±2.28* | 0.23±0.08* |
| 4-PBA+PA | 3.19±0.65# | 0.89±0.72# | 2.60±0.50# |
| P | < 0.05 | < 0.05 | < 0.05 |
| 与对照组相比,*P < 0.05;与PA组相比,#P < 0.05 | |||
骨质疏松作为21世纪五大疾病之一已经成为不容忽视的世界性公众健康问题。随着我国人口老龄化问题的不断加剧,预计到2020年,骨质疏松患者将达到2.866亿,髋部骨折人数将达163.82万,将会严重影响人民的生活质量。肥胖是一类由遗传因素、周围环境和个人生活方式多种原因引起的复杂代谢性疾病,它不仅是动脉粥样硬化、糖尿病等慢性疾病的独立危险因素,而且与骨质疏松的发生发展密切相关。
肥胖状态下,体内器官或组织脂质沉积过多,脂肪因子分泌谱将趋向炎性改变,脂肪细胞分泌的各种因子(主要为脂肪酸)可对细胞产生脂毒性作用,进而引起细胞功能障碍甚至凋亡[8]。肥胖患者体内脂质大量积累,脂肪酸的动员和利用减少、生成增多,血清游离脂肪酸水平普遍增高[9]。流行病学调查显示,肥胖可引起骨密度减低和骨脆性增高、骨折风险升高等骨质疏松的表现[1, 10]。高脂血症性骨质疏松动物模型的建立也强调了高脂饮食所引起的肥胖可以诱发骨质疏松[11-12]。在一项脂肪细胞与成骨细胞共培养实验中,Elbaz等[13]发现,抑制脂肪细胞内脂肪酸的合成可以对成骨细胞产生保护作用,从而反向验证了脂肪酸对成骨细胞的脂毒性作用。在体外实验中,有研究者运用棕榈酸的干预来模拟肥胖患者体内高脂环境,从而研究脂毒性对细胞的影响:Gunaratnam等[14]发现棕榈酸可以通过引发自噬作用和JNK通路的激活来诱导成骨细胞的凋亡。另一项研究也证实了ERK和AMPK通路在棕榈酸诱导的成骨细胞凋亡过程中的作用[3]。本研究发现,用不同浓度(0、100、250、500 μmol/L)的棕榈酸作用于成骨细胞24 h可以使其增生活力和凋亡率分别成浓度依赖性的降低和升高。取其作用敏感浓度500 μmol/L干预成骨细胞不同时间(0、6、12、24 h),随着作用时间的延长,细胞的增生活力和凋亡水平也分别随之下降和增高。这与之前的研究结果一致[5]。
存在于内质网上的免疫球蛋白结合蛋白(immunoglobulin binding protein,BPI),又称葡萄糖调节蛋白78(glucose-regulated protein 78,GRP78),可以帮助蛋白质正确折叠。高热缺氧、代谢障碍和某些药物的应用会引起内质网上错误折叠蛋白的积累,发生内质网应激。活化转录因子6 (activating transcription factor 6,ATF6),IREl (inositol requiring kinase 1)和蛋白激酶激酶RNA样内质网激酶(protein kinase RNA-like endoplasmic reticulum kinase,PERK)是位于内质网上的3个跨膜蛋白。正常情况下,GRP78可与其结合,使其处于静息状态。当内质网应激发生时,大量未折叠蛋白质在内质网腔内积累,会刺激GRP78,使之与以上3种跨膜蛋白分离并激活,从而使应激信号通过PERK-eIF2α、ATF6和IRE1-XBP-l通路继续向下游传递,通过抑制一般蛋白质合成,增加蛋白质降解等方式减轻内质网压力,对应激状态下的细胞发挥保护作用[15-16]。但是,持续时间过久或过度的内质网应激则可通过CHOP通路、caspase-12通路和JNK通路的激活,引起一系列的下游反应,对细胞功能产生不利影响甚至造成细胞凋亡。Zhong等[17]发现NF-κb的激活在棕榈酸诱导的成骨细胞凋亡过程中也起到了重要作用,而以往研究也证实,内质网应激可以通过调节NF-κb的活性参与疾病的炎性反应过程[18],因此,这从另一个角度解释了内质网应激在此过程中的作用。
为探讨棕榈酸引起成骨细胞凋亡的具体机制,本研究采用RT-qPCR法检测了各组细胞ERS相关基因的表达水平,结果显示,与对照组相比,随着棕榈酸作用浓度的增高和作用时间的延长CHOP和GRP78 mRNA的表达水平增高,然而caspase-12 mRNA的表达水平则在12 h达到峰值,24 h出现降低,这可能是因为在12 h时细胞为了自我保护首先选择程序性死亡,但细胞凋亡的过程持续时间比较短暂,一般持续数小时后即被邻近的细胞或巨噬细胞所吞噬,所以当作用时间延长至24 h后,caspase-12 mRNA的表达水平开始下降[16]。研究结果提示,内质网应激可能参与了棕榈酸诱导的成骨细胞凋亡过程。
内质网应激抑制剂4-苯基丁酸(4-phenylbutyric acid,4-PBA)是一种低分子量的游离脂肪酸,它可以稳定蛋白质的结构并且帮助错误折叠的蛋白质重新正确折叠,从而缓解内质网应激压力,保护细胞免受应激损伤[19-20]。为了进一步明确内质网应激在棕榈酸诱导的成骨细胞凋亡过程中的作用,本研究在棕榈酸干预前应用4-PBA预处理细胞,发现其可以降低内质网应激标志基因的表达并在一定程度上逆转棕榈酸的对成骨细胞的以上有害作用,发挥细胞保护作用。这也进一步验证了内质网应激可能参与了棕榈酸诱导的成骨细胞凋亡过程。
综上所述,棕榈酸可以呈浓度和时间依赖性的降低成骨细胞增生活性,升高凋亡率,增高细胞内ERS相关基因的表达。4-PBA则可在一定程度上逆转棕榈酸的以上作用,从而对高脂环境下的成骨细胞发挥保护作用。这一结果有望对临床上高脂性骨质疏松的治疗提供新的靶点。
| [1] | Cohen A, Dempster DW, Recker RR, et al. Abdominal fat is associated with lower bone formation and inferior bone quality in healthy premenopausal women:a transiliac bone biopsy study[J]. J Clin Endocrinol Metab, 2013, 98 : 2562–2572. DOI:10.1210/jc.2013-1047 |
| [2] | Martino L, Masini M, Novelli M, et al. Palmitate activates autophagy in INS-1E b-cells and in isolated rat and human pancreatic islets[J]. PLoS One, 2012, 7 : e36188. DOI:10.1371/journal.pone.0036188 |
| [3] | Kim JE, Ahn MW, Baek SH, et al. AMPK activator, AICAR, inhibits palmitate-induced apoptosis in osteoblast[J]. Bone, 2008, 43 : 394–404. DOI:10.1016/j.bone.2008.03.021 |
| [4] | 刘宝琴, 王华芹. 内质网应激与未折叠蛋白反应的研究进展[J]. 中华肿瘤防治杂志, 2010, 17 : 869–872. |
| [5] | Lu J, Wang Q, Huang L, et al. Palmitate causes endoplasmic reticulum stress and apoptosis in human mesenchymal stem cells:prevention by AMPK activator[J]. Endocrinology, 2012, 153 : 5275–5284. DOI:10.1210/en.2012-1418 |
| [6] | Zhao Y, Tan Y, Xi S, et al. A novel mechanism by which SDF-1β protects cardiac cells from palmitate-induced endoplasmic reticulum stress and apoptosis via CXCR7 and AMPK/p38 MAPK-mediated interleukin-6 generation[J]. Diabetes, 2013, 62 : 2545–2558. DOI:10.2337/db12-1233 |
| [7] | Simon-Szabó L, Kokas M, Mandl J, et al. Metformin attenuates palmitate-induced endoplasmic reticulum stress, serine phosphorylation of IRS-1 and apoptosis in rat insulinoma cells[J]. PLoS One, 2014, 9 : e97868. DOI:10.1371/journal.pone.0097868 |
| [8] | Sharma S, Tandon VR, Mahajan S, et al. Obesity:friend or foe for osteoporosis[J]. J Mid-Life Health, 2014, 5 : 6–9. DOI:10.4103/0976-7800.127782 |
| [9] | Arner P, Rydén M. Fatty acids, obesity and insulin resistance[J]. Obes Facts, 2015, 8 : 147–155. DOI:10.1159/000381224 |
| [10] | Mazziotti G, Bilezikian J, Canalis E, et al. New understanding and treatments for osteoporosis[J]. Endocrine, 2012, 41 : 58–69. DOI:10.1007/s12020-011-9570-2 |
| [11] | Patsch JM, Kiefer FW, Varga P, et al. Increased bone resorption and impaired bone microarchitecture in short-term and extended high-fat diet-induced obesity[J]. Metabol Clin Exp, 2011, 60 : 243–249. DOI:10.1016/j.metabol.2009.11.023 |
| [12] | Halade GV, Rahman MM, Williams PJ, et al. High fat diet-induced animal model of age-associated obesity and osteoporosis[J]. J Nutr Biochem, 2010, 21 : 1162–1169. DOI:10.1016/j.jnutbio.2009.10.002 |
| [13] | Elbaz A, Wu X, Rivas D, et al. Inhibition of fatty acid biosynthesis prevents adipocyte lipotoxicity on human osteoblasts in vitro[J]. J Cell Mol Med, 2010, 14 : 982–991. DOI:10.1111/j.1582-4934.2009.00751.x |
| [14] | Gunaratnam K, Vidal C, Boadle R, et al. Mechanisms of palmitate-induced cell death in human osteoblasts[J]. Biol Open, 2014, 155 : 108–116. |
| [15] | Boot-Handford RP, Briggs MD. The unfolded protein response and its relevance to connective tissue diseases[J]. Cell Tissue Res, 2010, 339 : 197–211. DOI:10.1007/s00441-009-0877-8 |
| [16] | 张红菊, 赵忠新, 夏斌. 大鼠脑缺血后内质网伴侣蛋白GRP78和GRP94及胱冬酶12表达的改变[J]. 中国脑血管病杂志, 2006, 3 : 163–166. |
| [17] | Zhong X, Xiu L, Wei G, et al. Bezafibrate prevents palmitate-induced apoptosis in osteoblastic MC3T3-E1 cells through the NF-κB signaling pathway[J]. Int J Mol Med, 2011, 28 : 535. |
| [18] | Kitamura M. Biphasic, bidirectional regulation of NF-κB by endoplasmic reticulum stress[J]. Antioxidants Redox Sign, 2009, 11 : 2353–2364. DOI:10.1089/ars.2008.2391 |
| [19] | Yam GH, Gaplovska-Kysela K, Zuber C, et al. Sodium 4-phenylbutyrate acts as a chemical chaperone on misfolded myocilin to rescue cells from endoplasmic reticulum stress and apoptosis[J]. Invest Ophthalmol Vis Sci, 2007, 48 : 1683–1690. DOI:10.1167/iovs.06-0943 |
| [20] | Humeres C, Montenegro J, Varela M, et al. 4-Phenylbutyric acid prevent cytotoxicity induced by thapsigargin in rat cardiac fibroblast[J]. Toxicol In Vitro, 2014, 28 : 1443–1448. DOI:10.1016/j.tiv.2014.07.013 |
| (收稿日期:2016-03-21) |

