扩展功能
文章信息
- 刘应林, 陈丽娟, 柳佳睿, 余震
- LIU Ying-Lin, CHEN Li-Juan, LIU Jia-Rui, YU Zhen
- A型肉毒毒素预防性治疗偏头痛有效性及安全性的随机对照试验的meta分析
- Efficacy and safety of botulinum toxin A inprophylactic treatment of migraine: A meta-analysis of randomized controlled trials
- 国际神经病学神经外科学杂志, 2020, 47(1): 67-72
- Journal of International Neurology and Neurosurgery, 2020, 47(1): 67-72
-
文章历史
收稿日期: 2019-08-05
修回日期: 2019-11-13
偏头痛(migraine)根据每月偏头痛发作频率、严重程度等,可将偏头痛分为慢性偏头痛(chronic migraine, CM)及发作性偏头痛(episodic migraine, EM)[1]。偏头痛常与焦虑、抑郁等疾病共患,还可导致脑白质病变、脑梗死等[2]。
偏头痛的治疗主要包括急性期治疗和发作间期预防性治疗,旨在减少头痛天数、严重程度和相关残疾,并减少对急性药物的需求从而改善生活质量[3]。但是目前预防性治疗存在很大缺陷,主要表现为药物特异性不高,患者口服药物依从性差等[4]。A型肉毒毒素(onabotulinumtoxin A, Botox)是由肉毒梭菌产生的一种嗜神经性细胞外毒素,Botox被美国FDA批准用于成人CM预防性治疗[5]。但是国内关于Botox治疗偏头痛的相关随机对照试验研究甚少,本文采用系统评价的方法,探讨Botox预防性治疗偏头痛的有效性和安全性,以期为临床治疗偏头痛提供循证依据。
1 资料与方法 1.1 研究类型Botox预防性治疗偏头痛的随机对照试验。
1.2 研究对象纳入标准:患者年龄18~65岁,试验对象符合国际头痛协会(IHS)制定的偏头痛诊断标准[1]。
排除标准:①其他原发性偏头痛、继发性偏头痛、复杂性偏头痛;②神经肌肉疾病患者(重症肌无力、Eaton-Lambert综合征和肌萎缩侧索硬化症)以及其他神经肌肉功能障碍病史;③严重的全身性疾病;④进入试验前由于偏头痛、医疗或美容整形的原因注射过肉毒素的患者;⑤患有重大精神障碍(如严重抑郁症、广泛性焦虑症)或正在接受抗精神病药物治疗的患者;⑥孕期或哺乳期的女性患者。
1.3 干预措施试验组药物为Botox,对照组为安慰剂。
1.4 结局指标与基线相比,患者平均每月偏头痛发作频率的变化;与基线相比,平均每月偏头痛日数的变化;与基线相比,急性期头痛用药日数变化;与基患者生活质量评分改变情况;安全性结局指标:不良反应。
1.5 文献排除标准非随机、安慰剂对照、双盲试验;自身对照试验;回顾性研究;病例报道;体外研究;不符合研究对象标准的试验;综述或者系统评价类文献。
1.6 检索策略计算机检索PubMed、Embase、Cochrane Library、SinoMed(CBM)、中国知网、万方等数据库中关于Botox预防性治疗偏头痛有效性和安全性的随机对照试验(randomized controlled trials, RCT),检索时间从建库至2019年5月1日。英文检索词包括:migraine、onabotulinumtoxin A、botulinum toxin type A;中文检索词包括:偏头痛、偏头风、A型肉毒毒素。检索策略采用主题词加自由词结合的方式。
1.7 资料提取及质量评价由2位研究者采用盲法独立进行文献筛选和资料提取,对不一致的文献复核并讨论达成一致。纳入的文献按Cochrane系统评价及Jadad量表评分法进行质量评价(1~7分)[6],由两名研究者独立评分,对有分歧意见的文献,由第三者协助解决。1~3分为低质量,4~7分为高质量。
1.8 统计学分析统计软件采用Cochrane协作网提供的RevMan 5.3。二分类变量用比值比(odds ratio, OR)以及95%可信区间(confidence intervals, CI)表示;计量资料采用均数差(MD)和95%CI作为效应量。采用I2检验和P值对纳入研究进行异质性分析,以P≤0.1、I2≥50%作为存在异质性的检验标准。若各研究间无显著异质性(P>0.1, I2 < 50%),采用固定效应模型分析;若存在显著异质性(P≤0.1, I2≥50%),采用随机效应模型分析。
2 结果 2.1 文献检索结果及质量评价根据检索策略进行检索,共获取2416篇文献,通过去除重复文献、阅读题目、摘要后共纳入文献16篇,通过阅读全文后有4篇文献未找到相关数据,最终纳入12项RCT[7-18],共计4 131例偏头痛患者。文献检索与筛选流程(图 1)。本系统评价纳入的研究均为随机、双盲、安慰剂对照临床试验,其中只有1篇文献未提及随机序列产生方法、分配隐藏及盲法实施具体方法[9]。文献质量评价均采用Cochrane系统评价及Jadad评分,Jadad评分均为大于或等于4分,纳入研究质量均较高(表 1)。

|
| 图 1 文献筛选流程图 |
| 文献 | 基线比较 | 随机序列的产生 | 分配隐藏 | 盲法 | 脱失或退出 | Jadad评分 |
| SheenaK等2006 | 可比 | 交替分配 | 恰当 | 恰当 | 提及 | 5 |
| SKAurora等2010 | 可比 | 电脑生成随机化序列 | 电脑控制 | 恰当 | 提及 | 6 |
| HC Diener等2010 | 可比 | 电脑生成随机化序列 | 电脑控制 | 恰当 | 提及 | 7 |
| DavidW等2010 | 可比 | 电脑生成随机化序列 | 电脑控制 | 恰当 | 提及 | 7 |
| Arthur H等2006 | 可比 | 未提及 | 未提及 | 未提及 | 提及 | 4 |
| S Evers等2003 | 可比 | 电脑生成随机序列 | 电脑控制 | 恰当 | 无脱失及退出 | 7 |
| Susanne等2009 | 可比 | 随机分配表 | 随机分配表 | 恰当 | 提及 | 7 |
| Saper等2007 | 可比 | 未提及 | 未提及 | 未提及 | 提及 | 4 |
| Frederick G等2008 | 未提及 | 随机分配表 | 随机分配表 | 恰当 | 提及 | 7 |
| Vo AH等2007 | 可比 | 电脑生成随机序列 | 电脑控制 | 恰当 | 提及 | 7 |
| Sandrini等2011 | 可比 | 电脑生成随机序列 | 电脑控制 | 恰当 | 提及 | 7 |
| Hollanda等2014 | 可比 | 电脑生成随机序列 | 电脑控制 | 恰当 | 提及 | 7 |
纳入的共12篇文献[7-18]均报道了Botox对偏头痛患者每月偏头痛发作频率的影响,结果显示,与安慰剂相比,Botox在减少每月偏头痛发作频率方面差异无统计学意义(MD=-0.1, 95%CI: -0.41~0.21, P=0.53, I2=47%)。见图 2。

|
| 图 2 Botox与安慰剂对偏头痛患者每月偏头痛发作频率的影响的森林图 |
仔细阅读文献后,考虑到偏头痛类型不同可能导致偏倚增加,故分为EM及CM两个亚组进行分析。在纳入的12篇RCT中,其中有5篇文献[7, 9, 12-13, 17]报道了Botox对EM患者偏头痛发作频率的影响,有7篇文献[8, 10, 11, 14-16, 18]报道了Botox对CM患者偏头痛发作频率的影响。EM亚组meta分析结果显示,与安慰剂相比,Botox在减少偏头痛发作频率方面差异无统计学意义(MD=-0.1, 95%CI: -0.41~0.21, P=0.53, I2=47%),CM亚组meta分析结果显示,与安慰剂相比,Botox在减少偏头痛发作频率方面有显著差异(MD=-0.43, 95%CI: -0.7~-0.17, P=0.001, I2=0%)。见图 3。

|
| 图 3 Botox与安慰剂对偏头痛患者每月偏头痛发作频率的影响的亚组分析的森林图 |
有4篇文献[12, 14-16]报道了Botox对偏头痛患者每月偏头痛天数影响情况,meta分析结果显示,Botox在减少每月偏头痛天数方面优于安慰剂,差异具有统计学意义(MD=-1.42, 95%CI: -2.24~-0.61, P=0.0006, I2=40%)。见图 4。

|
| 图 4 Botox与安慰剂对偏头痛患者每月偏头痛发作天数的影响的森林图 |
有3篇文献[11, 14, 15]报道了Botox对偏头痛患者每月急性期头痛药物使用频率的影响,meta分析结果显示,Botox在减少每月急性期药物服用频率方面优于安慰剂,差异具有统计学意义(MD=-1.20, 95%CI: -2.19~-0.21, P=0.02, I2=0%)。见图 5。

|
| 图 5 Botox与安慰剂对偏头痛患者每月急性期头痛药物服用频率的影响的森林图 |
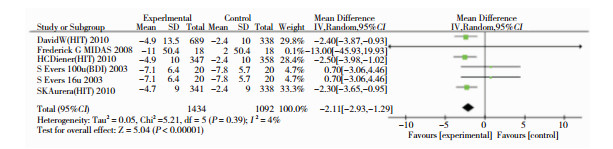
有5篇文献[11-12, 14-16]报道了Botox对偏头痛患者生活质量量表评分的影响,评分量表包括头痛影响测试问卷(HIT-6)、贝克抑郁量表(Beck Depression Inventory, BDI)、偏头痛失能程度问卷(Migraine Disability Assessment, MIDAS),评分越高,代表生活质量越低[19]。meta分析结果显示,Botox在改善偏头痛患者生活质量方面优于安慰剂,差异具有统计学意义(MD=-2.11, 95%CI: -2.93~-1.29, P < 0.00001, I2=4%)。见图 6。
|
| 图 6 Botox与安慰剂对偏头痛患者每月生活质量量表评分的影响的森林图 |
共有9篇文献[7-15]报道了不良反应相关数据,meta分析结果显示,Botox组总不良事件发生率高于安慰剂组(OR=1.38, 95%CI: 1.20~1.58, P < 0.00 001, I2=0%),但不良反应均较轻微且短暂。见图 7。

|
| 图 7 Botox与安慰剂对偏头痛患者总不良反应的森林图 |
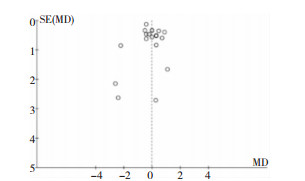
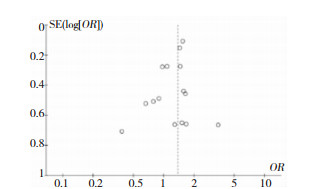
偏头痛患者偏头痛发作频率和不良反应发表偏倚分析显示,漏斗图(略)对称,不存在发表偏倚(图 8、图 9)。其他相关结局指标因纳入文献少,故无法行发表偏倚评估。
|
| 图 8 试验组与对照组偏头痛发作频率对比漏斗图 |
|
| 图 9 试验组与对照组不良反应对比漏斗图 |
本研究结果表明,Botox在减少CM患者患者每月偏头痛发作频率方面优于安慰剂,对于EM,与安慰剂相比,在减少偏头痛患者每月偏头痛发作频率方面趋于有效。Botox在减少偏头痛患者每月偏头痛发作天数、急性期药物使用频率以及改善生活质量方面优于安慰剂。2019年,Bruloy等[20]的一项meta分析结论与本研究一致,但不同的是本文还对偏头痛患者每月急性期药物服用频率进行了分析。
本研究对每月偏头痛发作天数结局指标共纳入4篇文献,其中3篇[14-16]关于CM,1篇[12]关于EM,将4篇文献进行合并分析,虽结果表明优于安慰剂,但若将此1篇文献剔除再进行分析,异质性减小。将此文章进行单独分析,结果表明与安慰剂相比,Botox组与安慰剂组并无差异。同样,针对生活质量量表评分改变情况,共纳入5篇文献,其中包括EM文献1篇[14],虽结果表明优于安慰剂,但若将此文献剔除再进行分析,异质性则减小。因此针对上述两项结局指标,应将CM及EM单独进行meta分析,但因针对EM的研究文献只有1篇无法进行综合合并。期望有更多的针对Botox对EM每月偏头痛发作天数改善情况、生活质量量表评分改变的大样本临床试验,以进一步评价。
不良反应分析显示,Botox组总不良事件发生率高于安慰剂组,在所报告的研究中,常见不良反应包括颈部疼痛、肌肉无力、眼睑下垂、注射部位疼痛、上呼吸道感染等,未见严重不良反应及死亡病例的报道,且这些不良反应多为轻至中度,不会遗留后遗症。
本文的不足之处,本文针对每月偏头痛发作天数、生活质量量表评分改变等结局指标纳入文献较少,会影响分析的准确性;而且本文由于纳入文献对注射剂量、注射部位及注射疗程等相关数据差异较大或者无法获得数据,故未进行综合分析,但推测不同注射剂量、不同的注射部位以及治疗疗程可能会影响疗效,希望将来有相关研究设计对上述方面进行综合分析,以更好的指导临床。
综上所述,Botox能有效减少CM患者每月偏头痛发作频率、每月偏头痛发作天数、急性期药物使用频率以及改善生活质量,但对于EM,则需更多试验数据进行论证,不管CM还是EM患者,均对Botox有较好的耐受性。
| [1] |
Headache Classification Committee of the International Headache Society (IHS). The international classification of headache disorders, 3rd edition[J]. Cephalalgia, 2018, 38(1): 1-211.
|
| [2] |
中华医学会疼痛学分会头面痛学组. 中国偏头痛防治指南[J]. 中国疼痛医学杂志, 2016, 22(10): 721-727. DOI:10.3969/j.issn.1006-9852.2016.10.001 |
| [3] |
Sun-Edelstein C, Rapoport AM. Update on the Pharmacological Treatment of Chronic Migraine[J]. Curr Pain Headache Rep, 2016, 20(1): 6. |
| [4] |
Berger A, Bloudek LM, Varon SF, et al. Adherence with migraine prophylaxis in clinical practice[J]. Pain Pract, 2012, 12(7): 541-549. DOI:10.1111/j.1533-2500.2012.00530.x |
| [5] |
Frampton JE, Silberstein S. OnabotulinumtoxinA:a review in the prevention of chronic migraine[J]. Drugs, 2018, 78(6): 589-600. |
| [6] |
Jadad AR, Moore RA, Carroll D, et al. Assessing the quality of reports of randomized clinical trials:is blinding necessary?[J]. Control Clin Trials, 1996, 17: 1-12. DOI:10.1016/0197-2456(95)00134-4 |
| [7] |
Saper JR, Mathew NT, Loder EW, et al. A Double-Blind, Randomized, Placebo-Controlled Comparison of Botulinum Toxin Type A Injection Sites and Doses in the Prevention of Episodic Migraine[J]. Pain Med, 2007, 8(6): 478-485. DOI:10.1111/j.1526-4637.2006.00168.x |
| [8] |
Sandrini G, Perrotta A, Tassorelli C, et al. Botulinum toxin type-A in the prophylactic treatment of medication-overuse headache:a multicenter, double-blind, randomized, placebo-controlled, parallel group study[J]. Headache Pain, 2011, 12: 427-433. DOI:10.1007/s10194-011-0339-z |
| [9] |
Petria S, Tölleb T, Straube A, et al. Botulinum Toxin as Preventive Treatment for Migraine:A Randomized Double-Blind Study[J]. Eur Neurol, 2009, 62: 204-211. DOI:10.1159/000228987 |
| [10] |
Hollanda L, Monteiro L, Melo A, et al. Botulinum toxin type A for cephalic cutaneous allodynia in chronic migraine:a randomized, double-blinded, placebo-controlled trial[J]. Neurol Int, 2014, 6: 5133. |
| [11] |
Freitag FG, Diamond S, Diamond M, et al. Botulinum Toxin Type A in the Treatment of Chronic Migraine Without Medication Overuse[J]. Headache, 2008, 48: 201-209. |
| [12] |
Evers S, Vollmer-Haase J, Schwaag S, et al. Botulinum toxin A in the prophylactic treatment of migraine-a randomized, double-blind, placebo-controlled study[J]. Cephalalgia, 2004, 24: 838-843. DOI:10.1111/j.1468-2982.2004.00754.x |
| [13] |
Elkind AH, O'Carroll P, Blumenfeld A, et al. A Series of Three Sequential, Randomized, Controlled Studies of Repeated Treatments With Botulinum Toxin Type A for Migraine Prophylaxis[J]. J Pain, 2006, 7(10): 688-696. DOI:10.1016/j.jpain.2006.03.002 |
| [14] |
Dodick DW, Turkel CC, De Gryse RE, et al. OnabotulinumtoxinA for Treatment of Chronic Migraine:Pooled Results From the Double-Blind, Randomized, Placebo-Controlled Phases of the PREEMPT Clinical Program[J]. Headache, 2010, 50: 921-936. DOI:10.1111/j.1526-4610.2010.01678.x |
| [15] |
Diener HC, Dodick DW, Aurora SK, et al. Onabotulinumtoxin A for treatment of chronic migraine:Results from the double-blind, randomized, placebo-controlled phase of the PREEMPT 2 trial[J]. Cephalalgia, 2010, 30(7): 804-814. DOI:10.1177/0333102410364677 |
| [16] |
Aurora SK, Dodick DW, Turke CC, et al. Onabotulinumtoxin A for treatment of chronic migraine:Results from the double-blind, randomized, placebo controlled phase of the PREEMPT 1 trial[J]. Cephalalgia, 2010, 30(7): 793-803. DOI:10.1177/0333102410364676 |
| [17] |
Aurora SK, Gawel M, Brandes JL, et al. Botulinum Toxin Type A Prophylactic Treatment of Episodic Migraine:A Randomized, Double-Blind, Placebo-Controlled Exploratory Study[J]. Headache, 2007, 47: 486-499. |
| [18] |
Vo AH, Satori R, Jabbari B, et al. Botulinum toxin type-a in the prevention of migraine:A double-blind controlled trial[J]. Aviat Space Environ Med, 2007, 78(Suppl): B113-B118. |
| [19] |
周志彬, 于生元. 偏头痛相关评价工具[J]. 中国疼痛医学杂志, 2015, 21(4): 241-244. DOI:10.3969/j.issn.1006-9852.2015.04.001 |
| [20] |
Bruloy E, Sinna R, Grolleau JL, et al. Botulinum Toxin versus Placebo:A MetaAnalysis of Prophylactic Treatment for Migraine[J]. Plast Reconstr Surg, 2019, 143(1): 239-250. DOI:10.1097/PRS.0000000000005111 |
 2020, Vol. 47
2020, Vol. 47




