扩展功能
文章信息
- 徐佳, 张佳乐, 李杨杨, 陆小明
- XU Jia, ZHANG Jia-Le, LI Yang-Yang, LU Xiao-Ming
- 内固定技术在椎管肿瘤切除中的应用
- Application of internal fixation in resection of spinal canal tumors
- 国际神经病学神经外科学杂志, 2019, 46(5): 490-494
- Journal of International Neurology and Neurosurgery, 2019, 46(5): 490-494
-
文章历史
收稿日期: 2019-07-20
修回日期: 2019-09-23
椎管肿瘤是神经外科常见病种,传统的手术方式是后路椎板切除后再行肿瘤切除,此方式的缺点是对于位于脊髓腹侧及椎管内外沟通型的肿瘤切除范围有限,且会影响脊柱稳定性。随着神经脊柱外科的发展,越来越多的神经外科医生开始熟练掌握内固定技术,并逐渐关注后路椎板切除对于脊柱稳定性的影响[1, 2]。我科2016年10月至2019年4月利用显微手术技术及内固定技术治疗各类椎管肿瘤患者21例,现报道如下。
1 资料与方法 1.1 一般资料21例患者中,男性8例,女性13例; 年龄18~65岁; 病程一周至三月; 病变部位:颈段11例,胸段6例,腰段3例,胸腰交界段1例。入组标准:(1)暴露病变时需切除侧方关节; (2)肿瘤已破坏骨质,影响脊柱稳定性; (3)肿瘤合并脊柱退行性病变及椎管狭窄,需同时行后路减压; (4)切除病变时需行不少于三个节段的全椎板及棘突切除。
1.2 临床表现21例患者均有不同程度的神经症状,6例患者以颈部/肩背部/腰部疼痛为主,5例患者以一侧或双侧上肢感觉/运动障碍为主,7例患者以一侧或双侧下肢感觉/运动障碍为主,2例患者表现为四肢感觉及运动障碍,1例患者表现为胸部束带感。术前Frankel分级:A级1例,C级2例,D级2例,E级16例; 术前疼痛视觉模拟量表(visual analogue scale, VAS)评分:0~2分17例,3~6分3例,7~10分1例,平均2.6分。
1.3 影像学检查术前均行MRI平扫加增强扫描,以明确病变位置、病变和脊髓及脊柱的关系,病变有无其他影响脊柱稳定性的因素,有无合并椎间盘突出等退变性疾病的情况; 同时行病变节段的CT检查,并行二维及三维重建,判断椎弓根螺钉的进钉点,精确计算进钉角度、长度; 涉及C1~2部位病变的患者行颈部CTA检查,并行二维及三维重建,判断椎动脉的走行方式,确定进钉点和进钉方向、深度。
1.4 手术治疗所有患者均在全麻下取俯卧位,20例患者采用后正中入路进行手术,1例患者因肿瘤横跨椎管两侧,故采用以病变节段为中心的跨中线横切口进行手术。
1.4.1 制作钉道一般情况下C3~6做侧块螺钉,C1~2及C7以下节段做椎弓根螺钉。全程在电生理监测下操作。充分暴露棘突、椎板及侧块或横突,结合术前CT,确定进钉点。高速磨钻磨除进钉点骨皮质,开路锥沿预定的进钉方向制作钉道。探针随时确认钉道的正确性,直至钉道深度达到预期值,再次探查确定钉道位置准确,骨蜡封闭钉道口以减少出血。如病变侵犯骨质,导致进钉点无法确认,可待去除棘突、椎板后,直视下在硬脊膜外探察椎弓根走行方向并制作钉道; 如骨质破坏严重,无法置钉,可跨过病变节段,并酌情增加固定节段。制作钉道过程中如有疑问应行C臂机定位,根据定位结果及时调整钉道。
1.4.2 切除肿瘤全程在电生理监测下操作。咬除棘突,做全椎板切除,保留椎板和棘突的骨组织,以备植骨融合。一般保留上下关节突,如需充分暴露椎管内外沟通型肿瘤,或需暴露硬脊膜囊侧方,可以高速磨钻取去除关节突部分骨质。置手术显微镜,显微镜下切除肿瘤。如肿瘤位于硬脊膜外,需尽量保持硬脊膜完整,避免出现脑脊液漏; 如肿瘤位于硬脊膜下,可以4-0无损伤缝线悬吊硬脊膜后沿长轴切开,完成肿瘤切除操作后再以该缝线严密缝合硬脊膜,尽量做到水密性; 如肿瘤为硬脊膜内外沟通型,可局部横向切开硬脊膜以增加暴露范围。硬膜缺损处可采用自体肌肉、筋膜及人工硬膜修补,生物蛋白胶加固。对于髓内病变,显露脊髓后,沿后正中线或在距离肿瘤最近的位置纵行切开脊髓,根据电生理监测的波形变化进行操作,沿肿瘤与脊髓的移行界面分离,尽量保护脊髓。止血以压迫及贴敷止血材料为主,尽量减少电凝操作。
1.4.3 固定及融合以丝攻加工钉道后,置入合适长度的螺钉,根据需要调整脊柱曲线,以模棒模拟钛棒的弯曲方向,并制作长度及曲度合适的钛棒,将钛棒置入螺钉中,螺帽临时固定。C臂机摄片确定置钉位置及固定情况满意后,锁紧螺帽。磨除螺钉周围骨质的部分骨皮质,以碎骨屑及人工骨置入钉棒周围行植骨融合。
2 结果所有患者随访3~33个月,平均16个月。肿瘤完全切除19例,2例近全切除,术后复发1例,1例转移至第三脑室内。无手术死亡病例。病变性质:神经鞘瘤8例,血管母细胞瘤2例,海绵状血管瘤2例,室管膜瘤2例,神经根鞘囊肿1例,肠源性囊肿1例,炎性肉芽肿1例,尤文肉瘤1例,血管脂肪瘤1例,骨瘤1例,滑膜腱鞘巨细胞瘤1例。术后Frankel分级:A级恢复至C级1例,C级恢复至D级2例,D级恢复至E级2例,E级16例无变化。术后VAS平均1.3分。20例患者达到骨性融合,融合率95.2%。没有发生内固定材料断裂、松动、脱出的情况。
|
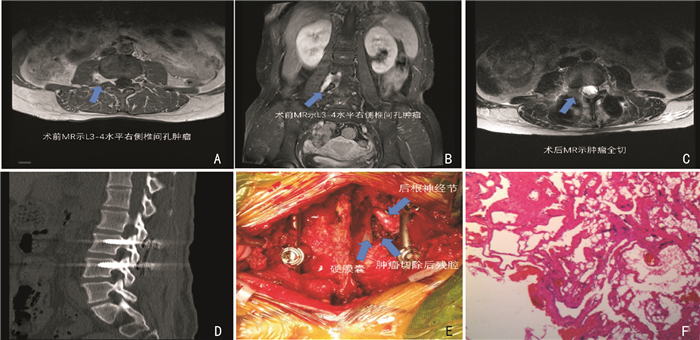
| A、B:术前MR提示肿瘤位于L3-4水平右侧椎间孔区; C:术后MR提示肿瘤全切; D:术后CT提示固定位置满意; E:术中见肿瘤全切,硬膜囊及神经根保留完好; F:病理示血管瘤 图 1 腰椎椎间孔区血管瘤切除+内固定 |
手术切除是椎管肿瘤的首选治疗方式。由于前路手术难以获得足够的手术空间,且椎前静脉丛会阻挡手术视野,所以多数术者采用后路手术切除椎管肿瘤[3]。为了充分暴露肿瘤,在切除肿瘤的同时尽量保护脊髓和神经功能,术中需要切除棘突和椎板,部分病人甚至需要切除关节突,这些操作势必会破坏脊柱及其韧带的完整性,从而影响脊柱稳定性。切除椎板,特别是切除三个节段以上的椎板,术后易发生脊柱不稳、半脱位或脊柱后凸畸形。一般情况下,切除的椎板节段越多,脊柱稳定性破坏越大,特别是儿童和青少年。颈段、颈胸或胸腰交界段及腰段的稳定性不仅仅依靠骨性结构的完整性,由棘上韧带、棘间韧带和棘突组成的张力带对于脊柱的稳定性也很重要。如果该张力带受到破坏,其前拉力会下降,限制脊柱活动的作用也会明显减弱[4]。为了维持术后脊柱的稳定性,部分神经外科医师会采用椎板成形加连接片固定的方式。该术式对于预防手术后术区局部软组织增生对硬膜囊的压迫效果良好,对于仅做椎板切开的患者,其维持脊柱稳定性的效果与内固定相近,但无法恢复因切除棘突、韧带后造成的脊柱后张力带的破坏; 对于需要切除侧方关节以及肿瘤已破坏骨质的患者,单纯的椎板成形无法达到维持脊柱稳定的效果。
在我国,神经外科在脊柱内固定技术方面起步较晚。由于大部分神经外科医生在切除椎管肿瘤时会选择后方入路,因此后路椎弓根螺钉或侧块螺钉固定成为最常用的固定技术。内固定技术的应用可以允许患者早期下床活动、进行功能锻炼,降低因长期卧床导致的各种并发症的发生率[5]。但内固定技术的术后并发症较多,如植入内固定材料所需要的暴露范围较常规手术大,增加手术创伤; 内固定术后患者脊柱活动度下降,伴有明显的异物感; 内固定手术会增加相邻节段椎间盘的退变速度等[6]。因此,内固定的手术适应症要严格把握。我们的经验是:颈段、腰段及颈胸/胸腰连接段相对活动度大,如去除椎板的节段较长(一般大于等于三个节段),需要行固定融合; 肿瘤位于椎旁或脊髓腹侧,为充分暴露肿瘤需要去除部分关节突,导致脊柱稳定性受损,需要行固定融合; 肿瘤明显侵犯骨质,破坏关节突关节、椎弓根或椎体,影响脊柱稳定性,需要行固定融合; 对于肿瘤合并椎间盘突出、导致椎管狭窄的患者,可以经后路减压后行固定融合。由于多节段椎板切除对于脊柱稳定性的影响是一个长期的过程,所以对于65岁以上的患者,我们没有选择行固定融合术。
椎管肿瘤患者如果需行内固定术,术前检查必须完善。该组患者术前均行相应节段MRI平扫+增强检查,明确病变具体节段与硬脊膜及脊髓的关系以及病变是否有影响脊柱稳定性的因素,或者是否合并脊柱退行性病变、椎管狭窄等。病变节段附近椎管的CT平扫+二维(三维)重建也是必要的,可以用来明确病变是否侵犯椎管骨质、是否影响脊柱稳定性,并通过测量确定进钉点及进钉的方向和深度,C1-C2节段患者可以通过颈部CTA检查判断椎动脉与椎管之间的关系,制定相应的置钉计划[7]。
感染对于有植入物的手术患者而言是灾难性的结果,可能直接导致手术失败。因此预防感染至关重要。该组病例中,我们在切皮前半小时使用头孢呋辛钠2.25 g静脉滴注,手术时间大于3小时追加一次预防用抗生素。术中严格要求无菌操作,尽量减少手术室人员流动,使用C臂机透视时以大块的手术巾单保护切口及手术附近区域,并注意保护洗手护士的器械台。术中冲洗水以每8万单位庆大霉素加入500 ml生理盐水的比例配制,并在手术结束前以大量冲洗水反复冲洗创面。术后预防性使用抗生素,密切监测患者体温情况,观察切口生长状况,尽量减少皮下引流管留置时间。本组病例无患者发生感染。
在手术操作过程中,应根据术前影像学资料制定手术计划,严格按照术前计划进行操作。切除硬脊膜外肿瘤时,应注意保护硬脊膜完整性,如有破损,需以自体筋膜或脂肪组织修补,使用4-0无损伤线缝合至水密性,辅以生物蛋白胶加固; 如需打开硬脊膜,建议沿脊髓长轴切开硬膜,并以4-0无损伤线悬吊,切除肿瘤后可以4-0无损伤线连续缝合硬膜至水密性,必要时辅以生物蛋白胶加固[8]。在置入椎弓根螺钉时,严格按照术前的置钉计划准确寻找进钉点,可在去除棘突和椎板之前先制作钉道,以免失去骨性标志造成置钉困难; 以直径2 mm左右的磨钻去除进钉点表面皮质,使用钝性的开路锥沿术前计划的方向和深度制作钉道,可分数次以球形探子确定钉道准确性,直至到达预计深度,如遇疑问,随时以定位钉做C臂机定位; 植入螺钉并以C臂机定位确定置钉位置满意后,应根据脊柱自然弧度制作钛棒并固定牢靠,特别是颅颈交界、颈椎及颈胸交界处,应先调整头架恢复自然弧度位置,然后再制作钛棒; 切除的椎管骨质都应保留,去除表面软组织后,制作成尽量细小的骨屑,钉棒系统植入完毕后,应磨除钉棒周围结构的骨皮质,以带抗生素的生理盐水反复冲洗术区后,以上述骨屑行植骨融合,如骨屑量少,应辅以异体骨或人工骨。切口缝合前确定无活动性出血,如硬膜保持完成,应在硬膜外放置负压引流管,否则放置普通引流管,然后按照解剖层次分层严密缝合切口,缝合时注意尽量减小死腔,可使用2-0大针微荞线进行间断缝合,每针间距在1 cm左右,缝合皮下组织和皮肤时应注意保持合适的松紧度,避免术后切口缺血坏死[9]。
电生理监测在该组患者术中起到重要的指导作用。对于硬脊膜外肿瘤,如肿瘤位于椎间孔区,电生理监测可在手术影响到神经根时做出及时的反应,可以避免对神经根的进一步损伤; 对于髓外硬脊膜下肿瘤,电生理监测可在判断是否为过路神经根、神经根是否存在重要功能等方面起到作用,尽可能保留神经功能; 对于髓内肿瘤,电生理监测可在肿瘤切除过程中指导术者减少对脊髓的过度牵拉或直接损伤; 在内固定过程中,电生理监测可以在脊髓或神经根受到影响时及时报警,避免进一步的损伤[10]。
内固定患者术后管理对于手术的成功非常重要。由于手术切口位于背侧,术后应尽量避免切口受压,定期轴线翻身,同时根据伤口情况决定换药频率,确保切口一期愈合; 皮下引流管根据引流液性状及引流量决定拔除时间,尽量在72 h内拔除皮下引流管,如引流液为脑脊液成分,为减少拔除引流管后皮下积液,可行腰大池置管持续引流; 鼓励术后患者早期下床活动,以避免下肢静脉血栓等并发症的发生,同时有利于功能锻炼,下床前需佩戴合适的支具。内固定患者术后需要定期随访复查,以便观察肿瘤是否复发、内固定系统是否移位、脱落,以及融合效果如何。该组患者均获得随访,最长时间33月,最短3月,影像学复查结果提示1例颈段血管母细胞瘤在颈胸交界段复发,1例颈段尤文肉瘤转移至三脑室内,其余肿瘤均未见明显复发征象。20例患者达到骨性融合,其中13例为双侧融合,7例为单侧融合,1例术后随访3月,未见骨性融合。部分病例术中去除的自体骨较少,用于植骨融合的骨屑量不够,影响了融合的效果。
随着科学技术的进步,许多新技术已被融入到内固定手术中,为椎管肿瘤切除后的内固定带来了创新。吴玉仙等[11]采用3D打印导板辅助多节段椎弓根螺钉置入进行颈椎管内肿瘤切除,能提高颈椎椎弓根螺钉的置钉精确度,明显缩短手术时间,减少手术出血量。Kantelhardt等[12]采用微创小切口置钉,进一步缩小了手术暴露范围,减少了术后感染的发生率。Lonjon等[13]采用手术机器人辅助置钉,置钉位置及深度更为精准,减少了手术并发症的发生。朱双芳等[14]认为椎板复位内固定术相对于单纯的钉棒固定,发生螺钉松动、断钉、断棒等现象的概率降低。Iacopino等[15]认为内固定技术是提高巨大哑铃型颈椎管神经鞘瘤手术切除率的关键技术。王林锋等[16]利用棘突椎板复合体回植联合空心螺钉固定在治疗胸腰椎椎管内肿瘤方面取得了良好的效果。
综上所述,内固定技术结合显微手术,在切除椎管肿瘤的过程中,对于肿瘤的暴露、脊髓和神经根的保护,以及维持脊柱稳定性等方面具有重要作用,使经后路切除椎管肿瘤更为安全,对于脊髓脊柱专业方向的神经外科医师而言是一种需要掌握的技能。
| [1] |
菅凤增. 脊柱稳定性与脊柱内固定[J]. 中华神经外科杂志, 2013, 29(9): 865-866. DOI:10.3760/cma.j.issn.1001-2346.2013.09.001 |
| [2] |
陈赞, 菅凤增. 椎管内肿瘤与脊柱稳定性[J]. 中国现代神经疾病杂志, 2013, 13(12): 986-987. |
| [3] |
Matsumoto T, Imagama S, Ito Z, et al. Total spondylectomy following carbon ion radiotherapy to treat chordoma of the mobile spine[J]. Bone Joint J, 2013, 95-B(10): 1392-1395. DOI:10.1302/0301-620X.95B10.31269 |
| [4] |
Sagan LM, Lickendorf MB. Posterior cervical lateral mass fixation for the management of insufficient anterior stabilization[J]. Ann Acad Med Stetin, 2005, 51(1): 23-26. |
| [5] |
Maheshwari GU, Chauhan S, Kumar S, et al. Access osteotomy for infratemporal tumors:two cases reports[J]. Ann Maxillofac Surg, 2012, 2(1): 77-81. DOI:10.4103/2231-0746.95330 |
| [6] |
Mazel C, Balabaud L, Bennis S, et al. Cerbical and thoracic spine tumor management:surgical indications, techniques, and outcomes[J]. Orthop Clin North Am, 2009, 40(1): 75-92. DOI:10.1016/j.ocl.2008.09.008 |
| [7] |
刘炳智, 谢延平, 颜继英, 等. 不同椎管内肿瘤切除术对神经功能恢复及胸椎稳定性的影响[J]. 山西医药杂志, 2015, 44(20): 2426-2428. |
| [8] |
Mohindra S, Savardekar A. Unilateral hemilaminectomy:The surgical approach of choice for juxta-medullary spinal tumors[J]. Neurol India, 2015, 63(2): 230-236. DOI:10.4103/0028-3886.156289 |
| [9] |
赵国, 宋晓斌, 沈勇, 等. 颈椎解剖学重建在颈椎椎管内肿瘤手术中的应用[J]. 临床神经外科杂志, 2015, 12(5): 354-357. DOI:10.3969/j.issn.1672-7770.2015.05.009 |
| [10] |
田学丰, 冯春国, 张科, 等. 脊柱内固定技术在切除多节段椎管内肿瘤的应用[J]. 中国临床神经外科杂志, 2016, 21(11): 673-675. |
| [11] |
吴学仙, 李建民, 纪玉清, 等. 3D打印导板辅助多节段椎弓根螺钉置入在颈椎管内原发肿瘤手术中的应用[J]. 中华骨与关节外科杂志, 2018, 11(7): 498-502. DOI:10.3969/j.issn.2095-9958.2018.07.004 |
| [12] |
Kantelhardt SR, Keric N, Conrad J, et al. Minimally invasive instrumentation of uncomplicated cervical fractures[J]. Eur Spine J, 2016, 25(1): 127-133. DOI:10.1007/s00586-015-4194-5 |
| [13] |
Lonjon N, Chan-seng E, Costalat V, et al. Robot-assisted spine surgery:feasibility study through a prospective case-matched analysis[J]. Eur Spine J, 2016, 25(3): 947-955. DOI:10.1007/s00586-015-3758-8 |
| [14] |
朱双芳, 黄学良, 周初松, 等. 230例椎管内肿瘤的诊断及手术治疗经验[J]. 中国矫形外科杂志, 2019, 27(3): 230-234. |
| [15] |
Iacopino DG, Giugno A, Guli C, et al. Surgical nuances on the treatment of giant dumbbell cervical spine schwannomas:description of a challenging case and review of the literature[J]. Spinal Cord Ser Cases, 2016, 2: 15042. DOI:10.1038/scsandc.2015.42 |
| [16] |
王林锋, 陆成武, 林伟明, 等.棘突椎板复合体回植联合空心螺钉固定在胸腰椎椎管内肿瘤切除术中的应用[J].2017, 27(9): 795-799. http://www.cnki.com.cn/Article/CJFDTOTAL-ZJZS201709006.htm
|
 2019, Vol. 46
2019, Vol. 46



