扩展功能
文章信息
- 陈立久, 颜伟, 李文涛, 张军霞, 尤永平
- CHEN Li-jiu, YAN Wei, LI Wen-tao, ZHANG Jun-xia, YOU Yongping
- 胶质母细胞瘤手术切除程度与患者生存预后的相关性分析
- Association of extent of surgical resection with survival and prognosis in patients with glioblastoma
- 国际神经病学神经外科学杂志, 2019, 46(2): 154-158
- Journal of International Neurology and Neurosurgery, 2019, 46(2): 154-158
-
文章历史
收稿日期: 2019-02-25
修回日期: 2019-04-16
胶质母细胞瘤是最致命的原发性颅内肿瘤[1, 2],总生存期为15~18个月,2年生存率为25%[3, 4]。影响预后的因素包括年龄、神经功能状态、手术切除程度、分子生物学特性、放化疗等[5, 6]。目前手术切除是胶质母细胞瘤最有效的治疗方法,可有效延长患者的生存期限。但是目前基于影像学的胶质母细胞瘤手术切除范围仍有争议。为此,本研究回顾性分析南京医科大学第一附属医院自2012年07月至2017年07月收治的有完整术前术后MRI数据和随访信息的48例原发性胶质母细胞瘤患者的临床资料,探讨肿瘤手术切除范围对患者生存预后的影响,现报道如下。
1 资料与方法 1.1 一般资料选取南京医科大学第一附属医院神经外科2012年07月至2017年07月收治有完整临床资料并进行长期跟踪随访的原发性胶质母细胞瘤患者48例,所有入组患者均无其它器官功能不全等严重的基础疾病,亦无明显的手术禁忌证。所有患者均经术后病理证实,主要以颅内压增高、癫痫和运动障碍为初始症状。本研究获得了南京医科大学第一附属医院伦理委员会的批准。
1.2 研究方法及观察指标研究分为两步,首先探讨T1增强像是否全切对患者生存期的影响,进一步探讨在T1增强像已经达到全切的患者亚组中,基于Flair像的手术切除程度对患者生存期的影响。比较两组间患者年龄、性别及首发症状、术后生存质量(KPS评分)、中位生存期、术后并发症(记忆力减退、性格改变等)等因素。
1.3 影像扫描及肿瘤体积计算方法所有患者均要求完成术前及术后72 h内头颅MRI(GE3.0T Signa HDX,GE Medical Systems,美国)扫描,扫描序列包括T1/T2平扫、T1增强像、Flair像、DTI、DWI等,其中横断位T1增强像、Flair像的图像参数:层厚5.0 mm,层间距0.5 mm。肿瘤体积的测量:基于横断位T1增强像及Flair像,逐层手动勾画肿瘤边界,取各层面截面积之和乘以层厚-层间距之和,计算肿瘤体积。Flair像异常体积定义为除去T1增强像肿瘤体积以外的异常区域。
1.4 统计学方法选择SPSS 20.0软件进行数据统计。计量资料以均数±标准差来表示,采用t检验; 率的比较采用χ2检验。生存分析采用Kaplan-Meier法,生存曲线的比较采用Log-rank检验,最佳分离阈值采用分类与回归分析法,P<0.05为差异有统计学意义。
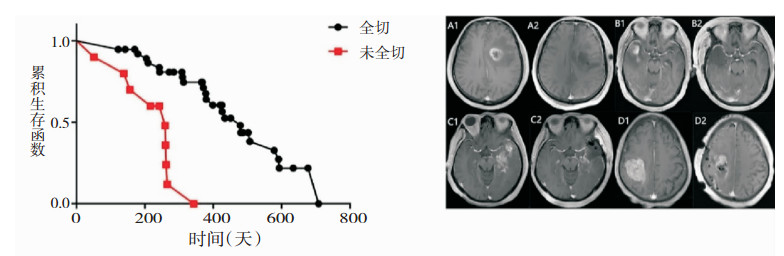
2 结果 2.1 基于T1增强像的胶质母细胞瘤切除程度与患者生存预后的相关性分析在本研究中,共有长期跟踪随访及术前术后磁共振影像数据完整的48例胶质母细胞瘤患者纳入分析,其中38例为T1增强像全切的患者,其余10例为T1增强像未全切的患者,两组患者年龄、性别及首发症状一般资料比较,差异均无统计学意义(P>0.05),提示两组间数据并无偏倚,具有可比性,详见表 1。为了比较T1增强像全切与未全切对胶质母细胞瘤患者生存期的影响,如图 1所示,我们绘制了Kaplan-Meier曲线,结果显示:T1增强像全切的患者中位生存期显著长于未全切患者的中位生存期(16.2月VS 8.6月),差异有统计学意义(P < 0.01)。进一步我们比较了两组患者术后生存质量(KPS评分)、生存期、术后并发症(记忆力减退、性格改变),详见表 2。结果显示:术后1周KPS评分T1增强像全切患者明显低于未全切患者(78.42±5.47分VS 87.00±4.83分),差异有统计学意义(t=4.514,P < 0.05)。而术后3个月KPS评分两组间差异无统计学意义(t=1.755,P>0.05)(T1增强像全切组:未全切组VS 87.89±6.22分:92.00±7.89分)。两组患者术后并发症情况比较均无统计学意义(P>0.05)。
|
| 图 1 T1对比增强像未全切与全切胶质母细胞瘤患者的生存预后差异 |
| 项目 | T1增强像全切 | T1增强像未全切 | 统计值 | P |
| 患者人数 | 38 | 10 | ||
| 平均年龄(岁) | 55.37±11.57 | 60.90±6.39 | t=1.447 | 0.155 |
| 性别(男/女) | 24/14 | 7/3 | - | 1.000 |
| 首发症状 | ||||
| 头痛、头晕 | 30 | 7 | - | 0.675 |
| 癫痫 | 20 | 7 | - | 0.478 |
| 精神障碍 | 4 | 2 | - | 0.591 |
| 运动障碍 | 11 | 4 | - | 0.703 |
| 语言障碍 | 10 | 3 | - | 1.000 |
| 注:“-”表示采用Fisher的精确检验,无统计值。 | ||||
| 项目 | T1增强像全切 | T1增强像未全切 | 统计值 | P |
| 患者人数 | 38 | 10 | ||
术后1周KPS 评分(分) | 78.42±5.47 | 87.00±4.83 | t=4.514 | 0.001 |
| 术后3个月KPS 评分(分) | 87.89±6.22 | 92.00±7.89 | t=1.755 | 0.083 |
| 术后并发症 | ||||
| 记忆力减退 | 4 | 2 | - | 0.591 |
| 性格改变 | 3 | 1 | - | 1.000 |
| 注:“-”表示采用Fisher的精确检验,无统计值。 | ||||
T1对比增强序列全切的患者(切除程度100%)中位生存期(16.2月)显著长于未全切患者(< 100%)的中位生存期(8.6月)(P < 0.01)。A1~A2全切增强像术前、术后,B1~B2全切增强像术前、术后,C1~C2未全切增强像术前、术后,D1~D2未全切增强像术前、术后。
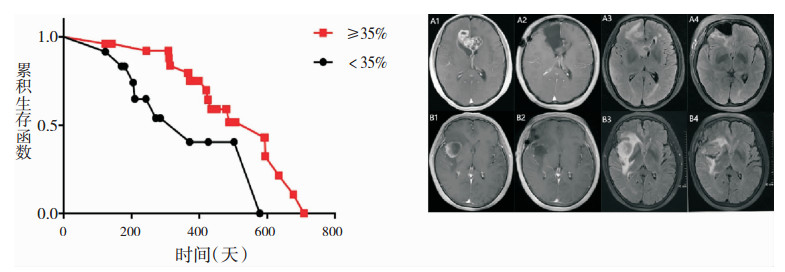
2.2 基于Flair像的胶质母细胞瘤手术切除程度对患者生存预后的影响为了进一步探讨胶质母细胞瘤手术切除程度对患者生存期的影响,我们在T1增强像全切的38名患者中,进一步分析了基于Flair像手术切除率和术后生存期的相关性。运用分类与回归分析法找出了最佳分离阈值(手术切除率35%)。如图 2所示,即Flair像手术切除率≥35%的患者术后生存期明显长于手术切除率<35%的患者生存期,最终以此为依据将该38名患者分成预后截然不同的两个亚组,一组为手术切除率≥35%,另一组为手术切除率<35%,两组的术前一般情况比较无差异统计学意义(P>0.05),提示两组间数据并无偏倚,具有可比性,如表 3所示。Kaplan-Meier曲线分析结果显示:Flair像手术切除率≥35%患者的中位生存期明显长于手术切除率<35%患者的中位生存期(19.7月VS 12.4月),差异有统计学意义(P<0.05)。进一步我们分析了基于Flair像手术切除程度对术后患者生活质量影响,我们比较了基于Flair像手术切除率不同的两组患者术后KPS评分及并发症,结果发现Flair像手术切除率≥35%患者的术后1周KPS评分低于手术切除率<35%患者(79.62±5.28分VS 75.83±5.15分),差异有统计学意义(t=2.069,P<0.05)(表 4)。术后3个月KPS评分两组间差异无统计学意义(t=0.292,P>0.05)(Flair像手术切除率≥35%组:手术切除率<35%组VS 87.69±6.51分:88.33±5.77分)。
|
| 图 2 基于Flair像手术切除率不同对胶质母细胞瘤患者生存预后的影响 |
| 项目 | 切除率≥35% | 切除率<35% | 统计值 | P |
| 患者人数 | 26 | 12 | ||
| 平均年龄(岁) | 53.56±11.42 | 59.82±11.23 | t= 1.540 | 0.132 |
| 性别(男/女) | 25/15 | 1/4 | - | 0.146 |
| 首发症状 | ||||
| 头痛、头晕 | 21 | 9 | - | 0.689 |
| 癫痫 | 13 | 7 | - | 0.734 |
| 精神障碍 | 3 | 1 | - | 1.000 |
| 运动障碍 | 7 | 4 | - | 0.714 |
| 语言障碍 | 7 | 3 | - | 1.000 |
| 注:“-”表示采用Fisher的精确检验,无统计值 | ||||
| 项目 | 切除率≥35% | 切除率<35% | 统计值 | P |
| 患者人数 | 26 | 12 | ||
术后1周KPS 评分(分) | 79.62±5.28 | 75.83±5.15 | t=2.069 | 0.046 |
| 术后3个月KPS 评分(分) | 87.69±6.51 | 88.33±5.77 | t=0.292 | 0.772 |
| 术后并发症 | ||||
| 记忆力减退 | 3 | 1 | - | 1.000 |
| 性格改变 | 2 | 1 | - | 0.338 |
| 注:“-”表示采用Fisher的精确检验,无统计值 | ||||
结果显示基于Flair像手术切除率≥35%患者的中位生存期(19.7月)显著长于手术切除率<35%的患者(12.4月)(P<0.05)。A1~A4切除率≥35%增强像术前、术后,Flair像术前、术后,B1~B4切除率<35%增强像术前、术后,Flair像术前、术后。
3 讨论胶质母细胞瘤是一种具有高死亡率的侵袭性脑肿瘤,主要是由于复发的必然性[7]。手术切除是现在胶质母细胞瘤最主要的治疗方式以及其他治疗有效的基础[8, 9, 10]。但是目前基于影像学的胶质母细胞瘤手术切除范围,国内外学者一直在探讨。2001年,Lacroix等回顾性分析了1993年6月至1999年6月在德克萨斯大学安德森癌症中心的胶质母细胞瘤患者416例,发现T1增强像手术切除率≥98%,患者的中位生存期为13.0月[11]。2011年,Sanai等在加利福尼亚大学旧金山分校统计分析了1997年至2009年500例胶质母细胞瘤患者,结果提示T1增强像全切可使患者的中位生存期达到16.0月[12]。2014年,Oppenlander等也做了类似的研究发现,T1增强像切除率≥80%,患者中位生存期为19.2月,T1增强像切除率≥97%,患者中位生存期为30月[13]。上述研究提示T1增强像切除程度越大,患者术后的中位生存期越长。除此之外,Brown等对胶质母细胞瘤手术切除程度与生存预后的Meta分析显示:胶质母细胞瘤T1增强像全切可以延长患者的无进展生存期和总体生存期[14]。在本研究中,48例患者共有38例(79%)完成了全切,中位生存期为16.2月,相比较未全切的患者(21%)的中位生存时间(8.6月)显著延长,差异有统计学意义,但本研究入组的病例数较少,有较多患者仍存活,以致本研究中T1增强像全切组患者的中位生存期较短。我们将继续扩大入组样本量,延长随访时间,进一步完善后续研究,获得大样本高质量数据,指导胶质母细胞瘤手术治疗。
近几年,国内外学者在T1增强像全切基础上引入Flair像作为胶质母细胞瘤的手术切除范围[15]。2016年,Li等在德克萨斯大学安德森癌症中心分析了1993年6月至2012年12月间1229例胶质母细胞瘤患者,其中新诊断的胶质母细胞瘤患者117例,发现Flair像手术切除率≥53.21%的患者的中位生存期为23.0月[16]。2017年,Pessina等也发表了282例胶质母细胞瘤患者的研究报道,认为Flair像手术切除率≥45%的患者,患者中位生存期可达到24.5月[5]。本研究也探讨了基于T1增强像全切的Flair像切除率对生存期的影响,结果显示:Flair像手术切除率≥35%的患者术后中位生存期为19.7月,手术切除率<35%的患者术后中位生存期只有12.4月,差异有统计学意义。因此,我们认为对于胶质母细胞瘤患者在T1增强像全切基础上进一步切除部分Flair像,可以有效延长了胶质母细胞瘤患者生存期。胶质母细胞瘤的T1增强像之外的Flair像异常信号,即为瘤周水肿带。目前认为,瘤周水肿程度与胶质瘤的预后、复发关系密切。我们课题组回顾性分析97例幕上胶质瘤患者术前影像学资料并随访,结果发现水肿距离T1增强病灶边缘≤1 cm患者的生存率高于水肿距离病灶边缘>l cm患者,差异有统计学意义[17]。Petrecca总结了20例T1增强像全切后复发的胶质母细胞瘤患者,有17例(85%)复发局限于切除边缘,即瘤周水肿带区域[18]。因此,Sughrue提出了胶质母细胞瘤扩大切除的概念,即T1增强像全切加瘤周1cm水肿带[19]。Pessina提出了胶质母细胞瘤超大切除的概念,即T1增强像全切加Flair像全切[5]。
那么胶质母细胞瘤扩大切除是否会显著影响患者术后生存质量?胶质母细胞瘤的手术切除重点应该是最大限度地切除肿瘤,同时防止术后神经功能损伤或其它并发症。Li和Sughrue的研究结果都提示胶质母细胞瘤扩大切除对患者术后30天神经功能并发症并无差异[16, 19]。我们研究发现,Flair像切除率≥35%的患者术后一周的KPS评分低于切除率<35%的患者,差异有统计学意义。Flair像切除率≥35%的患者术后3个月的KPS评分有所回升,与后者比较,差异无统计学意义。我们认为:手术早期部分患者术后出现神经功能的障碍,可能和扩大切除了更多的脑组织有关。然而,大脑功能具有一定的功能代偿,加上患者后期经过一段时间的康复锻炼等治疗,神经功能障碍可以得到一定程度的恢复。因此,在充分考虑神经功能的前提下,胶质母细胞瘤扩大切除不会显著影响患者术后生存质量。
综上所述,本研究提示胶质母细胞瘤手术切除程度与预后关系密切。胶质母细胞瘤T1增强像全切基础上Flair像切除率≥35%能够明显延长患者的生存期,对胶质母细胞瘤手术策略制定有着重要的指导意义。
| [1] |
Kreisl TN. Chemotherapy for malignant gliomas[J]. Semin Radiat Oncol, 2009, 19(3): 150-154. DOI:10.1016/j.semradonc.2009.02.003 |
| [2] |
Grossman SA, Ye X, Piantadosi S, et al. Survival of patients with newly diagnosed glioblastoma treated with radiation and temozolomide in research studies in the United States[J]. ClinCancerRes, 2010, 16(8): 2443-2449. |
| [3] |
Brower V. Early-stage progress on glioma vaccines[J]. J Natl Cancer Inst, 2011, 103(18): 1361-1362. DOI:10.1093/jnci/djr363 |
| [4] |
Kubben PL, ter Meulen KJ, Schijns OE, et al. Intraoperative MRI-guided resection of glioblastoma multiforme:asystematicreview[J]. LancetOncol, 2011, 12(11): 1062-1070. |
| [5] |
Pessina F, Navarria P, Cozzi L, et al. Maximize surgical resection beyond contrast-enhancing boundaries in newly diagnosed glioblastoma multiforme:is it useful and safe? A single institution retrospective experience[J]. J Neurooncol, 2017, 135(1): 129-139. DOI:10.1007/s11060-017-2559-9 |
| [6] |
Stupp R, Tonn JC, Brada M, Pentheroudakis G; ESMO Guidelines Working Group. High-grade malignant glioma:ESMO Clinical practice Guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2010, 21(Suppl 5): v190-193. |
| [7] |
Mampre D, Ehresman J, Pinilla-Monsalve G, et al. Extending the resection beyond the contrast-enhancement for glioblastoma:feasibility, efficacy, and outcomes[J]. Br J Neurosurg, 2018, 32(5): 528-535. DOI:10.1080/02688697.2018.1498450 |
| [8] |
Klepper LIa. Method of calculating the equivalent tumor dose as a function as to irradiated tumor tissue volume[J]. Med Tekh, 2001(4): 15-20. |
| [9] |
Emmanuel C, Lawson T, Lelotte J, et al. Long-term survival after glioblastoma resection: hope despite poor prognosis factors[J].J Neurosurg Sci. 2018, Jan 23.[Epub ahead of print] http://www.ncbi.nlm.nih.gov/pubmed/29363298
|
| [10] |
Fukui A, Muragaki Y, Saito T, et al. Volumetric Analysis Using Low-Field Intraoperative Magnetic Resonance Imaging for 168 Newly Diagnosed Supratentorial Glioblastomas:Effects of Extent of Resection and Residual Tumor Volume on Survival and Recurrence[J]. World Neurosurg, 2017, 98: 73-80. DOI:10.1016/j.wneu.2016.10.109 |
| [11] |
Lacroix M, Abi-Said D, Fourney DR, et al. A multivariate analysis of 416 patients with glioblastoma multiforme:prognosis, extent of resection, and survival[J]. J Neurosurg, 2001, 95(2): 190-198. DOI:10.3171/jns.2001.95.2.0190 |
| [12] |
Sanai N, Polley MY, McDermott MW, et al. An extent of resection threshold for newly diagnosed glioblastomas[J]. J Neurosurg, 2011, 115(1): 3-8. DOI:10.3171/2011.2.JNS10998 |
| [13] |
Oppenlander ME, Wolf AB, Snyder LA, et al. An extent of resection threshold for recurrent glioblastoma and its risk for neurological morbidity[J]. J Neurosurg, 2014, 120(4): 846-53. DOI:10.3171/2013.12.JNS13184 |
| [14] |
Brown TJ, Brennan MC, Li M, et al. Association of the Extent of Resection With Survival in Glioblastoma:A Systematic Review and Meta-analysis[J]. JAMA Oncol, 2016, 2(11): 1460-1469. DOI:10.1001/jamaoncol.2016.1373 |
| [15] |
Emblem KE, Farrar CT, Gerstner ER, et al. Vessel caliber-a potential MRI biomarker of tumor response in clinical trials[J]. Nat Rev Clin Oncol, 2014, 11(10): 566-584. DOI:10.1038/nrclinonc.2014.126 |
| [16] |
Li YM, Suki D, Hess K, et al. The influence of maximum safe resection of glioblastoma on survival in 1229 patients:Can we do better than gross-total resection[J]. J Neurosur, 2016, 124(4): 977-988. DOI:10.3171/2015.5.JNS142087 |
| [17] |
李文涛, 颜伟, 张军霞, 等. 基于磁共振图像的脑胶质瘤影像学临床分型及意义[J]. 中华神经医学杂志, 2015, 14(12): 1205-1209. DOI:10.3760/cma.j.issn.1671-8925.2015.12.004 |
| [18] |
Petrecca K, Guiot MC, Panet-Raymond V, et al. Failure pattern following complete resection plus radiotherapy and temozolomide is at the resection margin in patients with glioblastomas[J]. J Neurooncol, 2013, 111(1): 19-23. DOI:10.1007/s11060-012-0983-4 |
| [19] |
Sughrue ME, Glenn CA, Baker CM, et al. An Examination of the Role of Supramaximal Resection of Temporal Lobe Glioblastoma Multiforme[J]. World Neurosurg, 2018, 114: e747-e755. DOI:10.1016/j.wneu.2018.03.072 |
 2019, Vol. 46
2019, Vol. 46




