扩展功能
文章信息
- 李晓娜
- LI Xiao-Na
- 下调硫氧还蛋白相互作用蛋白表达对急性脑梗死大鼠脑保护作用
- Cerebral protection effect of downregulation of thioredoxin-interacting protein in rats with acute cerebral infarction
- 国际神经病学神经外科学杂志, 2019, 46(1): 65-69
- Journal of International Neurology and Neurosurgery, 2019, 46(1): 65-69
-
文章历史
收稿日期: 2018-05-22
修回日期: 2018-09-04
急性脑梗死作为神经内科常见的危重症,近年来发病率呈升高趋势,具有较高的致残率和致死率[1],治疗的关键在于尽早促使梗阻血管供血区脑组织恢复血供,但临床实际工作中发现,在解除血管梗阻,恢复血流灌注后反而加重了脑损伤,即发生了缺血-再灌注损伤[2]。研究发现[3],再灌注诱发大量活性氧(ROS)产生,加速细胞凋亡是缺血再灌注损伤重要机制。硫氧还蛋白相互作用蛋白(thioredoxin-interacting protein, TXNIP)作为机体内硫氧还蛋白的天然拮抗剂,是氧化应激途径中关键性调控蛋白,可通过与硫氧还蛋白结合而抑制该蛋白的抗氧化功能,在调节氧化还原平衡中发挥重要作用[4],研究表明[5],ROS可促使TXNIP由胞核转移至胞质,激活凋亡信号调节激酶1(apoptosis signal-regulating kinase 1, ASK-1)、天冬氨酸特异的半胱氨酸蛋白酶-1(cysteinyl aspartate-specific proteinase-1, caspase-1)等凋亡相关分子,最终导细胞凋亡。动物实验表明[6],大鼠肝脏缺血-再灌注后产生大量的ROS,TXNIP表达上升,但硫氧还蛋白活性降低。本研究拟利用小分子干扰RNA(small interfering RNA, siRNA)技术特异性下调急性脑梗死大鼠脑缺血区组织中TXNIP基因表达,观察其对脑神经功能的保护作用。
1 资料与方法 1.1 实验动物及主要试剂和设备 1.1.1 实验动物及分组清洁级健康雄性SD大鼠48只购自上海斯莱克实验动物有限公司[合格证号:SCXK(沪)2017-0005],体质量260~300 g,饲养于标准条件下,自由进食和饮水,适应性饲养7 d。利用随机数字表随机分为假手术组、模型组、阴性对照组和TXNIP干扰组,每组12只。
1.1.2 主要试剂和设备TXNIP和内参引物由上海生工生物公司设计合成;TXNIP干扰序列和阴性对照序列由上海吉凯基因化学技术公司设计合成;Trizol总RNA提取试剂盒购自美国Invitrogen公司;逆转录和PCR试剂盒购自德国Qiagen公司;2, 3, 5-氯化三苯基四氮唑(TTC)试剂购自美国Sigma公司;TUNEL细胞凋亡检测试剂盒购自美国Roch公司;兔抗TXNIP多克隆抗体购自美国Santa Cruz公司;ASK1及磷酸化-ASK1(p-ASK1)单克隆抗体购自美国CST公司;兔抗鼠caspase-1多克隆抗体购自武汉博士德生物公司;实时荧光定量PCR仪购自瑞士Roche公司;凝胶电泳系统购自美国Alpha Innotech公司。
1.2 方法 1.2.1 动物模型构建参照文献[7]中介绍的方法构建大鼠缺血再灌注损伤模型:10%水合氯醛腹腔注射麻醉,固定后,消毒,沿颈部正中线切开,使左侧颈总动脉充分暴露,沿血流方向将颈内动脉和颈外动脉分离,对颈外动脉远心端及近心端进行结扎,并从两结扎点之间将血管剪断,对颈总动脉及颈内动脉进行夹闭,在颈外动脉游离端剪一切口,并将线栓插入颈内动脉约19 mm,对伤口缝合,缺血120 min后恢复灌注。假手术组大鼠仅暴露左侧颈总动脉而不结扎。待大鼠清醒后,根据Zea-Longa评分标准对神经功能进行评分[8],以评分1~3分为合格。建模过程中,模型组和阴性对照组各有1只大鼠死亡,进行了补充。
TXNIP干扰组:于恢复灌注前15 min,将5 nmol的TXNIP siRNA溶于10 μL生理盐水中,经侧脑室注射;TXNIP siRNA序列:5’-GCCCUUAGGAUCCUGGCUUTT-3’。阴性对照组:于恢复灌注前15 min,将等量的阴性对照序列经侧脑室注射;阴性对照序列:5’-UUCUCCGAACGUGUCACGUTT-3’。模型组则以同样的方法给予等量的生理盐水。
1.2.2 神经功能评分各组大鼠于建模3 d时,再次根据Zea-Longa评分标准对神经功能损伤情况进行评分[8]。
1.2.3 TTC法检测各组大鼠脑梗死面积各组大鼠于再次进行神经功能评分后,各组随机取6只大鼠,麻醉处死,留取脑组织,置于-20℃冰箱20 min,取出后沿冠状位连续切6片,厚度约2 mm,浸入1% TTC中进行37℃水浴20 min。取出后用多聚甲醛固定,4℃固定24 h,拍照,用Image pro Plus 6.0软件对图片进行分析,计算脑梗死面积百分比(%)=梗死脑组织总面积/脑组织总面积×100%。
1.2.4 TUNEL法检测脑组织中神经细胞凋亡水平各组大鼠于再次进行神经功能评分后,将各组剩余的6只大鼠麻醉处死,留取脑组织,多聚甲醛固定,行冠状位切片,常规脱水后,用石蜡包埋,用切片机按4 μm的厚度进行切片,按照TUNEL试剂盒进行操作。对切片常规脱蜡、再水合,用蛋白酶K(10 mmol/L)处理15 min,滴加TUNEL液在37℃下孵育60 min,PBS冲洗3次,DAB染色,苏木素复染。用光学显微镜观察,TUNEL阳性凋亡细胞胞核或胞质被染色棕黄色,随机取5个视野计数凋亡细胞数,计数神经细胞凋亡率(%)=TUNEL阳性细胞数/总细胞数×100%。
1.2.5 实时荧光定量PCR技术检测脑组织中TXNIP基因表达取脑组织,研磨后加入裂解液,按Trizol总RNA提取试剂盒说明提取总RNA并检测纯度。按逆转录试剂盒说明将总RNA逆转录成cDNA,按PCR试剂盒说明,用实时荧光定量PCR仪对引物进行扩增。引物序列:TXNIP:上游:5’-CAAGTTCGGCTTTGAGCTTC-3’,下游:5’-GCCATTGGCAAGGTAAGTGT-3’;β-actin:5’-AAGGTGACAGCAGTCGGTT-3’,下游:β-actin:5’-TGTGTGGACTTGGGAGAGG-3’。反应条件:94℃ 3 min,92℃ 30 s,92℃ 30 s,60℃ 30 s,76℃ 30 s,连续循环38次。每个样品设3个平行复孔。用2-△△Ct法计算脑组织中TXNIP mRNA相对表达量。
1.2.6 Western blot法检测脑组织中TXNIP、ASK1、p-ASK1和caspase-1蛋白表达取脑组织,研磨后加入含蛋白酶抑制剂及广谱磷酸酶抑制剂的裂解液,按总蛋白提取试剂盒说明提取总蛋白,按BCA蛋白浓度测定试剂盒说明检测总蛋白浓度。取50 mg总蛋白,行SDS-聚丙烯酰胺凝胶电泳分离,电转移至聚偏氟乙烯膜上,5%脱脂奶粉封闭2 h,分别将一抗兔抗TXNIP多克隆抗体、ASK1及p-ASK1单克隆抗体和兔抗鼠caspase-1多克隆抗体(稀释比例:1:800、1:1 000、1:500和1:1 200)加入,4℃过夜孵育,TBST洗膜3次,加入二抗,室温条件下孵育2 h,TBST洗膜3次,暗室下加入化学发光试剂反应20 min,拍照,使用Image J图像软件分析,获得脑组织中TXNIP、ASK1、p-ASK1和caspase-1蛋白相对表达量。
1.3 统计学方法使用SPSS 21.0统计软件分析,计量资料以均数±标准差(x±s)表示,多组间比较采用单因素方差分析和LSD-t检验,以P<0.05为差异有统计学意义。
2 结果 2.1 各组大鼠神经功能评分假手术组、模型组、阴性对照组和TXNIP干扰组大鼠建模3 d时,神经功能评分分别为(0.14±0.05)分、(2.22±0.55)分、(2.49±0.97)分和(1.65±0.10)分,差异有统计学意义(F=42.046, P=0.000)。模型组、阴性对照组和TXNIP干扰组大鼠建模3 d时,神经功能评分均高于假手术组,差异有统计学意义(P<0.05)。模型组和阴性对照组大鼠建模3 d时,神经功能评分无差异(P=0.239)。TXNIP干扰组大鼠建模3 d时,神经功能评分低于模型组和阴性对照组,差异有统计学意义(P<0.05)。
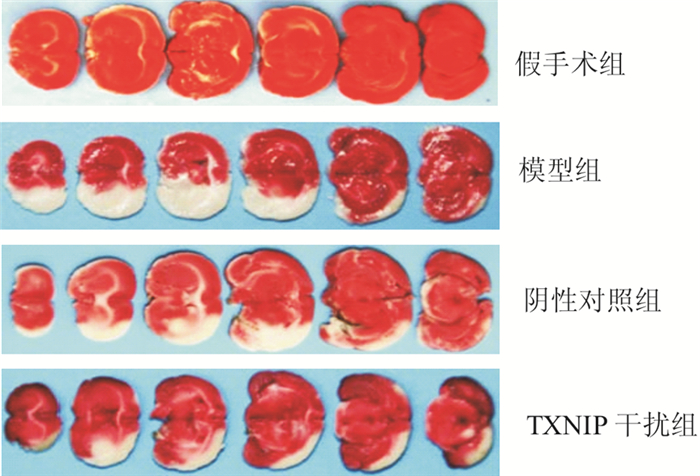
2.2 各组大鼠脑梗死面积假手术组、模型组、阴性对照组和TXNIP干扰组大鼠脑梗死面积分别为(0.99±0.08)%、(24.74±2.38)%、(23.48±2.72)%和(16.40±1.32)%,差异有统计学意义(F=192.936, P=0.000)。模型组、阴性对照组和TXNIP干扰组大鼠脑梗死面积高于假手术组,差异有统计学意义(P<0.05)。模型组和阴性对照组大鼠脑梗死面积无差异(P=0.271)。TXNIP干扰组大鼠脑梗死面积低于模型组和阴性对照组,差异有统计学意义(P<0.05)。见图 1。
|
| 图 1 TTC法检测大鼠脑梗死面积 |
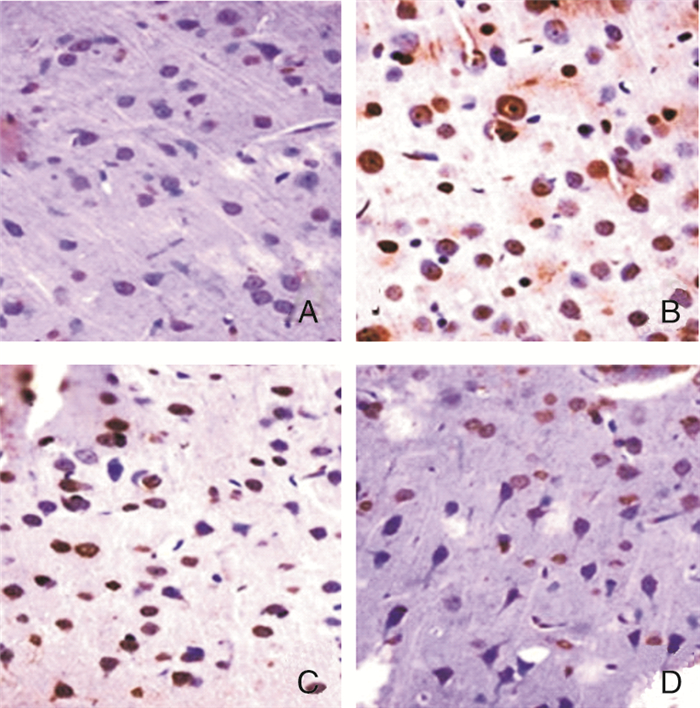
假手术组、模型组、阴性对照组和TXNIP干扰组大鼠脑组织中神经细胞凋亡率分别为(4.92±1.43)%、(71.53±6.25)%、(68.23±3.05)%和(22.61±2.33)%,差异有统计学意义(F=473.627, P=0.000)。模型组、阴性对照组和TXNIP干扰组大鼠脑组织中神经细胞凋亡率高于假手术组,差异有统计学意义(P<0.05)。模型组和阴性对照组大鼠脑组织中神经细胞凋亡率无差异(P=0.143)。TXNIP干扰组大鼠脑组织中神经细胞凋亡率低于模型组和阴性对照组,差异有统计学意义(P<0.05)。见图 2。
|
| 图 2 TUNEL法检测脑组织中细胞凋亡情况(放大倍数×400) 注:A:假手术组;B:模型组;C:阴性对照组,D:TXNIP干扰组 |
假手术组、模型组、阴性对照组和TXNIP干扰组大鼠脑组织中TXNIP mRNA相对表达量分别为(1.03±0.14)、(2.61±0.09)、(2.65±0.11)和(1.55±0.10),差异有统计学意义(F=301.979, P=0.000)。模型组、阴性对照组和TXNIP干扰组大鼠脑组织中TXNIP mRNA相对表达量高于假手术组,差异有统计学意义(P<0.05)。模型组和阴性对照组大鼠脑组织中TXNIP mRNA相对表达量比较,差异无统计学意义(P=0.515)。TXNIP干扰组大鼠脑组织中TXNIP mRNA相对表达量低于模型组和阴性对照组,差异有统计学意义(P<0.05)。
2.5 各组大鼠脑组织中TXNIP、ASK1、p-ASK1和caspase-1蛋白表达模型组、阴性对照组和TXNIP干扰组大鼠脑组织中TXNIP、p-ASK1和caspase-1蛋白相对表达量高于假手术组,而ASK1蛋白相对表达量低于假手术组,差异有统计学意义(P<0.05)。模型组和阴性对照组大鼠脑组织中TXNIP、ASK1、p-ASK1和caspase-1蛋白相对表达量比较,差异无统计学意义(P值分别为0.188、0.420、0.255和0.251)。TXNIP干扰组大鼠脑组织中TXNIP、p-ASK1和caspase-1蛋白相对表达量低于模型组和阴性对照组,而ASK1蛋白相对表达量高于模型组和阴性对照组,差异有统计学意义(P<0.05)。见表 1。
| 组别 | 例数(n) | TXNIP蛋白 | ASK1蛋白 | p-ASK1蛋白 | caspase-1蛋白 |
| 假手术组 | 6 | 0.23±0.06 | 0.83±0.08 | 0.30±0.06 | 0.20±0.09 |
| 模型组 | 6 | 0.81±0.04a | 0.26±0.06a | 0.86±0.04a | 0.66±0.06a |
| 阴性对照组 | 6 | 0.77±0.07a | 0.29±0.02a | 0.78±0.10a | 0.72±0.07a |
| TXNIP干扰组 | 6 | 0.40±0.05abc | 0.54±0.09abc | 0.53±0.18abc | 0.42±0.12abc |
| F | 158.508 | 86.693 | 33.039 | 46.554 | |
| P | 0.000 | 0.000 | 0.000 | 0.000 | |
| 注:a为与假手术组比较,P<0.05;b为与模型组比较,P<0.05;c为与阴性对照组比较,P<0.05 | |||||
急性脑梗死是致残、致死的主要疾病之一,目前尚无特效的治疗手段,关键在于尽早恢复血管血流,减少缺血半暗带区组织损伤,以改善患者预后[9],但在血管复流过程中不可避免的会发生缺血-再灌注损伤,反而会加重脑组织损伤[10]。近年来研究发现[11],硫氧还蛋白与缺血-再灌注损伤密切相关,在平衡氧化还原状态、抗凋亡、抗炎中发挥重要作用。TXNIP则是存在于机体内硫氧还蛋白的天然拮抗剂,可与其结合而抑制其抗氧化活性,在氧化应激反应中发挥重要作用,有研究指出[12],TXNIP表达上调可促进炎症或凋亡相关分子表达而在细胞凋亡及炎症反应中发挥重要作用。本研究通过构建急性缺血-再灌注大鼠模型,并对脑组织中TXNIP基因表达进行干预,结果显示,TXNIP干扰组大鼠脑组织中TXNIP mRNA和蛋白相对表达量均低于模型组和阴性对照组,说明通过侧脑室注射TXNIP siRNA的方法可有效抑制脑组织中TXNIP表达。
本研究结果显示,TXNIP干扰组大鼠建模3 d时,神经功能评分低于模型组和阴性对照组,说明下调TXNIP基因表达可改善大鼠神经功能,本研究结果显示,TXNIP干扰组大鼠脑梗死面积和脑组织中神经细胞凋亡率均低于模型组和阴性对照组,说明下调TXNIP基因表达可有效减少缺血-再灌注大鼠脑梗死面积及神经细胞凋亡,这些结果提示TXNIP基因参与了大鼠脑缺血-再灌注损伤过程,抑制该基因表达则可有效保护脑组织。ASK1作为细胞凋亡通路中一种重要的蛋白,在细胞因子和应激诱导细胞凋亡中发挥关键性作用[13],caspase-1是一种炎症相关caspase,不仅在调控炎症反应中发挥重要作用,而且介导了程序性细胞死亡,在促进细胞凋亡中发挥重要作用[14],本研究结果显示,模型组、阴性对照组和TXNIP干扰组大鼠脑组织中TXNIP、p-ASK1和caspase-1蛋白相对表达量高于假手术组,而ASK1蛋白相对表达量低于假手术组,TXNIP干扰组大鼠脑组织中TXNIP、p-ASK1和caspase-1蛋白相对表达量低于模型组和阴性对照组,而ASK1蛋白相对表达量高于模型组和阴性对照组,说明在急性缺血-再灌注大鼠脑组织中存在TXNIP、p-ASK1和caspase-1蛋白高表达,抑制TXNIP表达则可减少p-ASK1和caspase-1蛋白表达,提示TXNIP可能通过促进凋亡蛋白ASK1磷酸化表达而加速细胞凋亡。
综上所述,下调TXNIP基因表达可改善急性脑梗死大鼠神经功能,减少脑梗死面积和神经细胞凋亡,其机制可能与抑制促进凋亡相关蛋白ASK1磷酸化介导的细胞凋亡有关,但具体作用机制尚待进一步研究明确。
| [1] |
吉训明, 吴川杰. 急性脑梗死后颈动脉血运重建手术时机的探讨[J]. 中华神经外科杂志, 2017, 33(4): 325-327. DOI:10.3760/cma.j.issn.1001-2346.2017.04.001 |
| [2] |
Beker MC, Caglayan AB, Kelestemur T, et al. Effects of normobaric oxygen and melatonin on reperfusion injury:role of cerebral microcirculation[J]. Oncotarget, 2015, 6(31): 30604-30614. |
| [3] |
Wu MY, Yiang GT, Liao WT. Current mechanistic concepts in ischemia and reperfusion injury[J]. Cell Physiol Biochem, 2018, 46(4): 1650-1667. DOI:10.1159/000489241 |
| [4] |
莫与琳, 杨亚军, 崔燎. TXNIP介导的氧化应激在疾病中的作用机制[J]. 中国药理学通报, 2018, 34(1): 16-19. DOI:10.3969/j.issn.1001-1978.2018.01.005 |
| [5] |
Kumar A, Mittal R. Mapping Txnip:Key connexions in progression of diabetic nephropathy[J]. Pharmacol Rep, 2017, 70(3): 614-622. |
| [6] |
杜津, 王倩, 李庆明, 等. 硫氧还蛋白系统在硫化氢抗大鼠肝缺血再灌注损伤中的变化[J]. 中华医学杂志, 2012, 92(37): 2607-2610. DOI:10.3760/cma.j.issn.0376-2491.2012.37.005 |
| [7] |
孙寒静, 刘志和, 吴艳华, 等. 川芎嗪对急性脑梗死大鼠CD40/CD40L信号通路的影响及机制探讨[J]. 中西医结合心脑血管病杂志, 2016, 14(10): 1087-1090. DOI:10.3969/j.issn.1672-1349.2016.10.010 |
| [8] |
李晓云, 王立新, 牛建一, 等. miR-126在糖尿病大鼠脑缺血损伤组织中的表达及在血管再生中的意义[J]. 中华神经医学杂志, 2016, 15(9): 908-912. DOI:10.3760/cma.j.issn.1671-8925.2016.09.007 |
| [9] |
冷辉林, 蔡龙. 骨髓间质干细胞移植减轻犬急性脑梗死模型的缺血性脑损伤研究[J]. 国际神经病学神经外科学杂志, 2017, 44(3): 266-269. |
| [10] |
Li W, Suwanwela NC, Patumraj S. Curcumin prevents reperfusion injury following ischemic stroke in rats via inhibition of NF?κB, ICAM-1, MMP-9 and caspase-3 expression[J]. Mol Med Rep, 2017, 16(4): 4710-4720. DOI:10.3892/mmr.2017.7205 |
| [11] |
Li Y, Xiang Y, Zhang S, et al. Intramyocardial injection of thioredoxin 2-expressing lentivirus alleviates myocardial ischemia-reperfusion injury in rats[J]. Am J Transl Res, 2017, 9(10): 4428-4439. |
| [12] |
Monteiro HP, Ogata FT, Stern A. Thioredoxin promotes survival signaling events under nitrosative/oxidative stress associated with cancer development[J]. Biomed J, 2017, 40(4): 189-199. |
| [13] |
Guo X, Namekata K, Kimura A, et al. ASK1 in neurodegeneration[J]. Adv Biol Regul, 2017, 66(11): 63-71. |
| [14] |
Lee H, Shin EA, Lee JH, et al. Caspase inhibitors:a review of recently patented compounds (2013-2015)[J]. Expert Opin Ther Pat, 2018, 28(1): 47-59. DOI:10.1080/13543776.2017.1378426 |
 2019, Vol. 46
2019, Vol. 46



