扩展功能
文章信息
- 中国医师协会神经内科分会癫痫专委会
- 成人全面性惊厥性癫痫持续状态治疗中国专家共识
- 国际神经病学神经外科学杂志, 2018, 45(1): 1-4
-
文章历史
癫痫持续状态(status epilepticus, SE)是严重的神经科急症,其中全面性惊厥性癫痫持续状态(generalized convulsive status epilepticus, GCSE)具有潜在致死性,如何采取有效手段迅速终止临床发作和脑电图的痫样放电是降低死亡率和改善预后的关键[1, 2]。长期以来,由于缺乏高质量的随机对照(randomized controlled trial, RCT)研究,各家单位多根据经验和习惯制定自己的SE治疗方案,因此,医疗机构间实施的具体方案差异较大,影响了SE的整体救治水平。近年来,国内外专业学术组织根据已有的RCT研究结果,相继发表了4个有代表性的基于循证医学的SE处理的指导文件,它们分别是2010年欧洲神经病学学会联盟《成人癫痫持续状态处理指南》[3]、2016年美国癫痫学会《儿童和成人的惊厥性癫痫持续状态治疗指南》[4]、2012年美国神经重症学会的《癫痫持续状态的评估与处理指南》[5]和2014年中华医学会神经病学分会神经重症协作组的《惊厥性癫痫持续状态监护与治疗(成人)中国专家共识》[6]。然而,由于绝大多数研究来自国外,据此制定的指南并不完全适合我国的医疗现状,比如初始治疗中的劳拉西泮注射剂及鼻腔、直肠粘膜给药的苯二氮卓类药物均在国内无法获取。而《惊厥性癫痫持续状态监护与治疗(成人)中国专家共识》[6]则是重症医学专家从其专业角度提供的指导意见。目前,国内癫痫学术团体尚未推出关于GCSE治疗的指导性文件。为此,中国医师协会神经内科分会癫痫专委会组织相关专家,在已发表临床指南的高级别证据基础上,结合我国实际情况,讨论并撰写《成人全面性惊厥性癫痫持续状态治疗中国专家共识》,供神经内科、神经外科、急诊科、重症医学科和院前急救的同道参考。
1 定义和适用范围尽管各个指南采取的证据评价系统不统一,收录的研究语种和年限也有所差异,但所入选的高等级证据研究的重叠性很高。因此,推荐意见具有较高一致性。
采用Lowenstein等[7]提出的临床实用的GCSE操作定义,即每次全身性强直-阵挛(generalized tonic-clonic seizure, GTC)发作持续5 min以上,或2次以上发作,发作间期意识未能完全恢复。不区分原发性或继发性GTC。GCSE可分为3个阶段[4]:GTC发作超过5 min,为第一阶段GCSE,启动初始治疗,最迟至发作后20 min评估治疗有无明显反应;发作后20~40 min属于第二阶段GCSE,开始二线治疗;发作后大于40 min进入第三阶段GCSE,属难治性癫痫持续状态(refractory SE, RSE),转入重症监护病房进行三线治疗。超级难治性癫痫持续状态(super-RSE):2011年在英国牛津举办的第3届伦敦-因斯布鲁克SE研讨会上首次被提出。当麻醉药物治疗SE超过24 h,临床发作或脑电图痫样放电仍无法终止或复发时(包括维持麻醉剂或减量过程中),定义为super-RSE[8]。
本专家共识主要涵盖院前和院内终止GCSE的方案选择及安全性评价,super-RSE的探索性处理,不涉及其它类型SE、神经重症监护和SE病因学评估与治疗。
2 第一阶段GCSE的初始治疗共有3项多中心RCT研究比较了不同的初始药物方案对成人GCSE的疗效。美国退伍军人事务SE协作组于1990~1995年进行了国际上第一个关于SE治疗的多中心RCT研究,研究结果于1998年发表。该研究总共纳入384例显著GCSE(定义为发作持续时间超过10 min)患者,比较了4种静脉注射药物方案,即劳拉西泮(0.1 mg/kg)、或苯巴比妥(15 mg/kg)、或苯妥英钠(18 mg/kg)、或地西泮(0.15 mg/kg)后续苯妥英钠(18 mg /kg)对终止发作的成功率。当用药后20 min内发作终止且60 min内不复发被定义为治疗成功。头对头比较分析发现劳拉西泮组优于苯妥英钠组(P=0.001),而其他组间比较则无显著性差异。2001年美国1项研究纳入205例GCSE患者,由院前急救人员在救护车上分别对患者静脉注射2 mg劳拉西泮、5 mg地西泮和安慰剂,结果劳拉西泮和地西泮的发作控制率相当,分别为59.1%和42.6%[10]。2012年的RAMPART试验是1项院前多中心非劣效RCT研究[11],纳入748名成人患者,显示肌肉注射10 mg咪达唑仑和静脉注射劳拉西泮4 mg的发作控制率分别为73.4%和63.4%(P < 0.01),提示肌肉注射咪达唑仑的疗效不劣于静脉注射劳拉西泮,而前者在无静脉通路情况下显然占有优势。以上三项研究还显示肌注咪达唑仑、静注地西泮、静注劳拉西泮和静注苯妥英钠的呼吸、心血管不良反应(低通气、低血压和心律失常)无显著差异[9-11]。
此外,2项开放标签小规模RCT研究比较了静注丙戊酸与静注苯妥英钠的发作控制率[12, 13],1项研究显示丙戊酸优于苯妥英钠(丙戊酸,66% vs苯妥英钠,42%;P=0.046),而另1项则显示两者疗效相当。
根据以上研究结果,可得到以下结论[4]:对于GCSE成人患者的初始治疗, 肌注咪达唑仑、静注劳拉西泮、静注地西泮(不论是否后续苯妥英钠)和静注苯巴比妥均能有效终止发作(A级证据);静注地西泮和静注劳拉西泮的有效性相当。未建立静脉通路情况下,肌注咪达唑仑的有效性优于静注劳拉西泮(A级证据);当发作持续时间大于10 min时,静注劳拉西泮的有效性优于静注苯妥英钠(A级证据)。
建议:由于国内尚不生产劳拉西泮注射剂,苯妥英钠注射剂也获取困难。初始治疗首选静注10 mg地西泮(2~5 mg/min),10~20 min内可酌情重复一次,或肌注10 mg咪达唑仑。院前急救和无静脉通路时,优先选择肌注咪达唑仑。
3 第二阶段GCSE的治疗当苯二氮卓类药物的初始治疗失败后,可选择其他AEDs治疗。美国退伍军人事务SE协作组的多中心RCT研究中,比较了初始治疗失败后续以二线治疗的4组方案的发作控制率,分别是:劳拉西泮失败后续以静注苯妥英钠、苯巴比妥失败后续以静注苯妥英钠、苯妥英钠失败后续以劳拉西泮和静注地西泮加苯妥英钠失败后续以劳拉西泮,结果显示4组间的总控制率无显著性差异[9]。2007年印度1项单中心RCT研究[14],纳入100例地西泮2次静脉注射控制GCSE失败患者,静注丙戊酸组(20 mg/kg)和静注苯妥英钠组(20 mg/kg)的控制率分别为88%和84%(P>0.05)。2011年我国宣武医院1项RCT研究共纳入66例静脉注射地西泮(0.2 mg/kg)控制GCSE失败的患者,结果显示丙戊酸(30 mg/kg)静脉注射后续静脉泵注维持和地西泮(0.2 mg/kg)静脉注射后续静脉泵注(4 mg/h)维持的控制率分别为50%和56%,两组控制率相当[15]。2015年另1项来自印度的RCT研究纳入150名初始劳拉西泮治疗失败的GCSE患者,分别续以静注苯妥英钠(20 mg/kg)、丙戊酸(30 mg/kg)和左乙拉西坦(25 mg/kg),每组各50名患者,结果显示发作控制率分别为苯妥英钠组(68%)、丙戊酸组(68%)和左乙拉西坦组(78%),3组间无显著性差异[16]。
建议:初始苯二氮卓类药物治疗失败后,可选择丙戊酸15~45 mg/kg静脉推注后续1~2 mg/(kg·h)静脉泵注,或苯巴比妥15~20 mg/kg(50~100 mg/min)静脉注射,或苯妥英钠18 mg/kg(< 50 mg/min)或左乙拉西坦1000~3000 mg静脉注射。
4 第三阶段RSE的治疗大约三分之一的GCSE患者将进入RSE。此时,需转入重症监护病房,立即静脉输注麻醉药物,以持续脑电图监测呈现爆发-抑制模式或电静息为目标。同时应予以必要的生命支持与器官保护,防止因惊厥时间过长导致不可逆的脑损伤和重要脏器功能损伤[6]。
该阶段主要治疗方案为静脉输注咪达唑仑、静脉输注异丙酚和静脉输注戊巴比妥。咪达唑仑较难实现脑电图的爆发-抑制模式,异丙酚则可能产生输注综合征,戊巴比妥心血管不良反应较大且国内难以获得。优先选取哪种方案,目前尚缺乏高质量的RCT研究证据。
建议:咪达唑仑[0.2 mg/kg负荷量静注,后续持续静脉泵注0.05~0.40 mg/(kg·h)],或者丙泊酚[2 mg/kg负荷量静注,追加1~2 mg/kg直至发作控制,后续持续静脉泵注1~10 mg/(kg·h)]。
5 super-RSE的治疗对于super-RSE的治疗,尚处于临床探索阶段,多为小规模回顾性观察研究。可能有效的手段包括:氯胺酮麻醉、吸入性麻醉剂、电休克、免疫调节、低温、外科手术、经颅磁刺激和生酮饮食等[4]。
建议:权衡利弊后,谨慎使用。
6 终止GCSE后的处理终止标准为临床发作停止、脑电图痫样放电消失和患者意识恢复。
当在初始治疗或第二阶段治疗终止发作后,建议立即予以同种或同类肌肉注射或口服药物过渡治疗,如苯巴比妥、卡马西平、丙戊酸、奥卡西平、托吡酯和左乙拉西坦等;注意口服药物的替换需达到稳态血药浓度(5~7个半衰期),在此期间,静脉药物至少持续24 h。
当第三阶段治疗终止RSE后,建议持续脑电监测直至痫样放电停止24~48 h,静脉用药至少持续24~48 h,方可依据替换药物的血药浓度逐渐减少静脉输注麻醉药物。
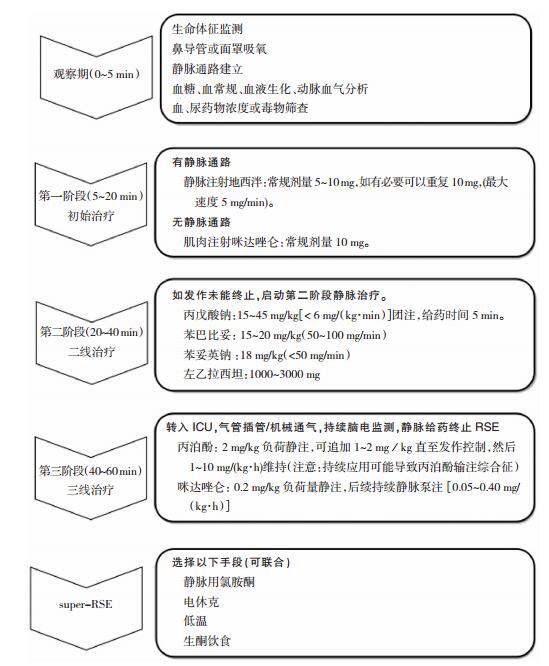
7 终止成人GCSE的推荐流程图结合我国医疗现状,我们将终止成人GCSE的建议流程概括成图 1。
|
| 图 1 终止全面性惊厥性癫痫持续状态的推荐流程图 |
参与共识讨论的专家(按姓氏笔画顺序排列):
丁美萍、王小珊、王天成、王中原、王玉、王玉平、王世民、王学峰、王晓飞、王康、王湘庆、王微微、王群、邓学军、朱雨岚、朱遂强、伍国锋、任连坤、任惠、刘玉玺、江文、孙红斌、连亚军、肖波、吴原、汪昕、宋治、宋毅军、张敬军、陈阳美、周东、周列民、周盛年、郑荣远、孟红梅、赵永波、赵传胜、郝晓婷、洪震、徐祖才、黄华品、黄志凌、廖卫平
共识执笔专家:王学峰、王康、肖波
| [1] |
Hauser WA. Status epilepticus:Epidemiologic considerations[J]. Neurology, 1990, 40(5 Suppl 2): 9-13. |
| [2] |
Chen JWY, Wasterlain CG. Status epilepticus:pathophysiology and management in adults[J]. Lancet Neurol, 2006, 5(3): 246-256. DOI:10.1016/S1474-4422(06)70374-X |
| [3] |
Meierkord H, Boon P, Engelsen B, et al. EFNS guideline on the management of status epilepticus in adults[J]. Eur J Neurol, 2010, 17(3): 348-355. DOI:10.1111/j.1468-1331.2009.02917.x |
| [4] |
Glauser T, Shinnar S, Gloss D, et al. Evidence-Based Guideline:Treatment of Convulsive Status Epilepticus in Children and Adults:Report of the Guideline Committee of the American Epilepsy Society[J]. Epilepsy Curr, 2016, 16(1): 48-61. DOI:10.5698/1535-7597-16.1.48 |
| [5] |
Brophy GM, Bell R, Claassen J, et al. Guidelines for the evaluation and management of status epilepticus[J]. Neurocrit Care, 2012, 17(1): 3-23. DOI:10.1007/s12028-012-9695-z |
| [6] |
中华医学会神经病学分会神经重症协作组. 惊厥性癫痫持续状态监护与治疗(成人)中国专家共识[J]. 中华神经科杂志, 2014, 47(9): 661-666. |
| [7] |
Lowenstein DH, Alldredge BK. Status epilepticus[J]. N Engl J Med, 1998, 338(14): 970-976. DOI:10.1056/NEJM199804023381407 |
| [8] |
Shorvon S. Super-refractory status epilepticus:an approach to therapy in this difficult clinical situation[J]. Epilepsia, 201l, 52(Suppl 8): 53-56. |
| [9] |
Treiman DM, Meyers PD, Walton NY, et al. A comparison of four treatments for generalized convulsive status epilepticus. Veterans Affairs Status Epilepticus Cooperative Study Group[J]. N Engl J Med, 1998, 339(12): 792-798. DOI:10.1056/NEJM199809173391202 |
| [10] |
Alldredge BK, Gelb AM, Isaacs SM, et al. A comparison of lorazepam, diazepam, and placebo for the treatment of out-of-hospital status epilepticus[J]. N Engl J Med, 2001, 345(9): 631-637. DOI:10.1056/NEJMoa002141 |
| [11] |
Silbergleit R, Durkalski V, Lowenstein D, et al. Intramuscular versus intravenous therapy for prehospital status epilepticus[J]. N Engl J Med, 2012, 366(7): 591-600. DOI:10.1056/NEJMoa1107494 |
| [12] |
Gilad R, Izkovitz N, Dabby R, et al. Treatment of status epilepticus and acute repetitive seizures with i.v. valproic acid vs phenytoin[J]. Acta Neurol Scand, 2008, 118(5): 296-300. DOI:10.1111/ane.2008.118.issue-5 |
| [13] |
Misra UK, Kalita J, Patel R. Sodium valproate vs phenytoin in status epilepticus:A pilot study[J]. Neurology, 2006, 67(2): 340-342. DOI:10.1212/01.wnl.0000224880.35053.26 |
| [14] |
Agarwal P, Kumar N, Chandra R, et al. Randomized study of intravenous valproate and phenytoin in status epilepticus[J]. Seizure, 2007, 16(6): 527-532. DOI:10.1016/j.seizure.2007.04.012 |
| [15] |
Chen WB, Gao R, Su YY, et al. Valproate versus diazepam for generalized convulsive status epilepticus:A pilot study[J]. Eur J Neurol, 2011, 18(12): 1391-1396. DOI:10.1111/ene.2011.18.issue-12 |
| [16] |
Mundlamuri RC, Sinha S, Subbakrishna DK, et al. Management of generalised convulsive status epilepticus (SE):A prospective randomised controlled study of combined treatment with intravenous lorazepam with either phenytoin, sodium valproate or levetiracetam-Pilot study[J]. Epilepsy Res, 2015, 114: 52-58. DOI:10.1016/j.eplepsyres.2015.04.013 |
 2018, Vol. 45
2018, Vol. 45


