扩展功能
文章信息
- 李莎, 曹晓雨, 范卫明, 刘庆新, 周晓生, 陈金波
- LI Sha, CAO Xiao-Yu, FAN Wei-Ming, LIU Qing-Xin, ZHOU Xiao-Sheng, Chen Jin-Bo
- 急性高血压脑出血患者血浆CXCL12水平与脑水肿的相关性研究
- Correlation between plasma CXCL12 level and brain edema in patients with acute hypertensive intracerebral hemorrhage
- 国际神经病学神经外科学杂志, 2017, 44(3): 275-279
- Journal of International Neurology and Neurosurgery, 2017, 44(3): 275-279
-
文章历史
收稿日期: 2016-10-28
修回日期: 2017-05-30
脑出血(intracerebral hemorrhage, ICH)指非外伤性脑实质内出血。脑出血的常见病因是高血压合并动脉硬化,而高血压脑出血的好发部位是基底节区,发生率约占60%,常继发多种并发症,死亡率高[1]。脑出血后继发性脑损伤是导致神经功能恶化的主要原因,其中最重要的病理变化是继发性脑水肿。目前认为炎症因子在脑水肿的形成过程中扮演了重要角色[2]。趋化因子被认为是急性和慢性炎症的调节因子[3]。我们前期临床及基础研究发现血浆中趋化因子CXCL12水平的改变与脑梗死预后有关[4-5]。目前关于趋化因子CXCL12与脑出血的临床研究报道少见,本研究通过动态检测脑出血后患者血浆CXCL12水平,观察趋化因子CXCL12水平对ICH患者预后的影响,探讨血浆CXCL12在脑水肿形成过程中的作用,以期为脑水肿的治疗提供新的理论依据。
1 研究对象与方法 1.1 研究对象脑出血组:选取2015年9月至2016年1月在本院住院治疗的急性高血压脑出血患者34例,男性20例,女性14例,年龄36~69岁,平均(54.62±8.86) 岁。入选标准:既往有高血压病史或入院后确诊为高血压病;首次发病并于发病24小时内到达医院;完善头颅CT检查确诊为脑出血;能配合完成调查并同意对其进行随访的患者。排除标准:各种原因引起的继发性脑出血患者,包括颅脑外伤、动脉瘤破裂、动-静脉畸形、长期口服抗凝药及脑梗死溶栓所导致的颅内出血;无法计算出血体积的患者,比如蛛网膜下腔出血或血肿破入脑室;近期有手术史、感染史、输血史和心肌梗死病史;肝肾功能损害严重或发现有恶性肿瘤;脑出血患者需要及时行手术治疗;患者及家属不能配合完成调查者。
对照组:同期在本院进行体检的健康者25例,男16例,女9例,年龄40~72岁,平均年龄(57.64±9.08) 岁。既往无心脑血管疾病和肝肾、恶性肿瘤等疾病,血液检查结果不存在炎症或病毒感染。
对照组与脑出血组患者的性别、年龄相匹配。
1.2 研究方法 1.2.1 血浆CXCL12水平测定脑出血组分别于入院24小时内、第3天、第7天和第14天,对照组于体检当日清晨空腹抽取静脉血约2 mL存于EDTA抗凝管中,以3000 rmp/min离心20 min,吸取上层血浆置EP管中,储存于-80℃冰箱待测。ELISA试剂盒购自南京森贝伽生物科技有限公司。
1.2.2 脑出血患者早期预后评估方法于发病30天后对脑出血患者进行改良Rankin量表(modified Rankin Scale, mRS)评分,根据mRS评分将患者分为预后良好组(mRS≤2分)和预后不良组(mRS>2分)[6]。
1.2.3 相对水肿体积的计算脑出血患者分别于入院24小时内、第3天和第7天完善颅脑CT检查。釆用多田公式计算体积,体积=(长径×宽径×层厚×层数×π/6) 计算,病灶体积=血肿体积+周围水肿体积。相对水肿体积=(病灶体积-血肿体积)/血肿体积[7]。
1.3 统计学分析采用SPSS 13.0进行统计学分析,对符合正态分布的计量资料用均数±标准差(x±s)来描述,组间比较采用t检验;非正态分布资料用中位数(最小值-最大值)描述,组间比较采用秩和检验。计数资料比较行χ2检验。数据相关性行Pearson相关性分析。P < 0.05为差异有统计学意义。
2 结果 2.1 脑出血组与对照组血浆CXCL12水平的比较脑出血组24小时内血浆CXCL12水平(19.85±1.84)μg/L明显高于对照组(11.34±2.23)μg/L,差异有统计学意义,P < 0.01。
2.2 脑出血组血浆CXCL12水平的整体变化脑出血组血浆CXCL12水平在第3天快速上升(22.56±1.56)μg/L,在第7天达高峰(23.38±1.53)μg/L,第14天时开始下降(22.64±1.78)μg/L,但仍高于对照组(P < 0.01)。
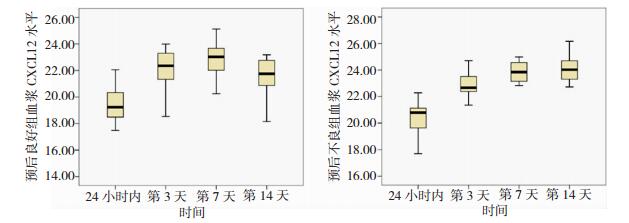
2.3 预后良好组和预后不良组血浆CXCL12水平及差异根据mRS评分将脑出血患者分为预后良好组(19例)和预后不良组(15例),预后良好组与整体的变化趋势一致,各时间点的血浆CXCL12水平均高于对照组,差异均有统计学意义(P < 0.01)。预后不良组血浆CXCL12水平在第14天时未见下降。预后不良组血浆CXCL12水平在各时间点均高于预后良好组,两组血浆CXCL12水平在第7天时和第14天时比较差异均有统计学意义,P值分别 < 0.05和 < 0.01。见表 1和图 1。
| 组别 | 例数 | 24小时内 | 第3天 | 第7天 | 第14天 |
| 预后良好组 | 19 | 19.36±1.82 | 22.14±1.39 | 22.92±1.27* | 21.58±1.34** |
| 预后不良组 | 15 | 20.46±1.75 | 23.10±1.64 | 23.96±1.66 | 23.98±1.30 |
| 注:*为第7天与预后不良组比较,P < 0.05;**为第14天与预后不良组比较,P < 0.01。 | |||||
|
| 图 1 预后良好组和预后不良组不同时间血浆CXCL12(μg/L)变化趋势 |
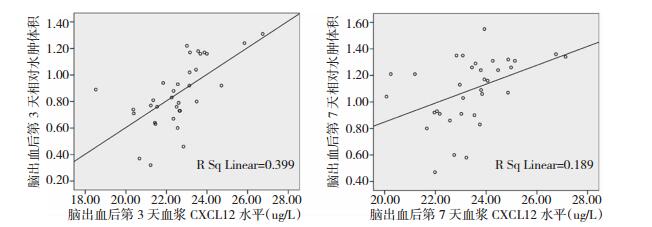
Pearson相关性分析显示,脑出血组24小时内血浆CXCL12水平与相对水肿体积无相关性(r=0.224, P>0.10),第3天和第7天血浆CXCL12水平与相对水肿体积呈正相关,相关系数分别为(r=0.631, P < 0.01) 和(r=0.435, P < 0.05)。见图 2。
|
| 图 2 Pearson相关性分析图 |
本研究发现脑出血患者血浆CXCL12水平在24小时内较对照组明显升高,ICH后第3天血浆CXCL12水平快速上升,第7天时达到高峰,在第14天虽开始下降,但仍高于对照组。预后良好组血浆CXCL12水平变化趋势与整体趋势一致,各时间点的血浆CXCL12水平均高于对照组。预后不良组血浆CXCL12水平在第14天时未见下降,预后不良组血浆CXCL12水平在不同时间均高于预后良好组,两组血浆CXCL12水平在第7天和第14天时差异具有统计学意义,说明脑出血后血浆CXCL12水平越高的患者预后越差。Pearson相关性分析显示脑出血后24小时内血浆CXCL12水平与相对水肿体积无相关性,第3天和第7天时血浆CXCL12水平与相对水肿体积呈正相关。
急性高血压脑出血(acute hypertensive intracerebral hemorrhage, AHICH)后脑水肿体积通常在脑出血发生后24小时增加75%,第5~6天达高峰,并持续至第14天[6]。有研究发现炎症反应在脑出血后脑水肿的形成过程中起重要作用[8]。趋化因子CXCL12有CXCR7和CXCR4两种受体,这两种受体均属于G蛋白偶联受体,CXCR7的表达有利于细胞的生长、存活及黏附,而活化的CXCR4的表达有利于细胞的增值和迁移。研究发现趋化因子CXCL12及其受体CXCR4在关节炎的模型中发挥着促炎效应,而CXCR4是促炎效应的必要条件[9]。也有文献报道,在哮喘状态下CXCL12表达明显上升,并趋化更多的炎症细胞到达肺组织,从而加重肺部严重损伤[10]。应用CXCR4的拮抗剂AMD3100能够抑制SDF-l对各种炎性细胞的趋化作用,减轻呼吸道炎症[11],以上研究说明CXCL12-CXCR4生物轴在介导炎症反应中起着重要作用。
研究发现急性脑梗死患者血清CXCL12水平明显升高,趋化因子CXCL12水平与梗死灶体积和卒中严重程度密切相关[12],患者入院时血清CXCL12水平与梗死后1年内卒中再发风险也密切相关[13]。趋化因子CXCL12既可以通过诱导免疫细胞和炎症因子到达大脑局部缺血部位加重组织损伤[14]又可以趋化神经干细胞(neural stem cells, NSC)从脑室下区(subventricular zone, SVZ)向受损部位募集,促进神经功能恢复[15]。Jun等[16]研究发现,趋化因子CXCL12通过趋化炎症细胞浸润和促进缺血区炎症因子表达加重组织损伤,应用CXCL12受体拮抗剂AMD3100后,能显著抑制缺血区炎症反应以及减轻血脑屏障破坏。我们前期基础研究发现CXCL12在大鼠短暂性局灶性脑缺血早期可以通过自由基过氧化和降低缺血脑组织中各种能量代谢酶活性加重脑组织损伤,在发病6 h内使用AMD3100可以改善脑缺血的预后[5]。最近Wu等[17]研究发现CX549作为CXCR4的一个新型拮抗剂,它与CXCR4的亲和力比AMD3100更强,能够显著减少小胶质细胞的活化,抑制炎症介质的表达,促进卒中后神经功能恢复。而Yamaguchi等[18]研究发现,过度表达的CXCL12能募集内皮祖细胞(endothelial progenitor cells, EPCs)到缺血区,参与缺血组织血管再生,促进受损组织神经功能恢复。黎柏源等[19]对大鼠脑出血模型的研究中发现,体外给予SDF-1能明显上调血肿周围组织SDF-1 mRNA及SDF-1蛋白水平的表达,可减少脑出血后受损区域细胞的凋亡;在大鼠皮质神经元凋亡模型中发现SDF-1通过CXCR4下调凋亡相关蛋白caspase-3表达,对神经细胞起到保护作用。
近期Shen等[20]研究发现,脑出血后患者血清CXCL12水平显著升高,血清CXCL12水平不仅与患者入院时的美国国立卫生研究院卒中量表评分(National Institute of Health stroke scale, NIHSS)和血肿体积呈正相关,还与患者6个月的死亡率、整体存活率和预后不良独立相关。在本研究中同样发现脑出血患者血浆CXCL12明显升高,血浆CXCL12水平持续较高的患者预后不良,这可能与趋化因子CXCL12介导的炎症损伤有关,也可能是CXCL12介导的炎症损伤作用大于神经保护作用。此外本研究发现脑出血患者血浆CXCL12水平动态变化趋势与脑水肿高峰期大致相同,并且在第3天和第7天时血浆CXCL12水平与相对脑水肿体积呈正相关。由此可见,通过动态检测血浆CXCL12水平可大致预测脑水肿变化趋势,CXCL12受体拮抗剂有可能成为未来治疗脑水肿的新型药物。
综上所述,脑出血后血浆CXCL12水平明显升高,血浆CXCL12水平持续升高的患者预后较差;血浆CXCL12动态变化趋势与脑水肿高峰一致,通过动态检测血浆CXCL12水平能够为脑水肿的评估和治疗提供依据。本研究不足之处在于收集的样本量较少,随访时间较短,未来应增大样本量并对患者的长期预后进行分析,使结果更具有说服力。
| [1] |
周焜, 黄冠又, 梁郸, 等. 非手术治疗自发性基底节区脑出血预后因素分析[J]. 国际神经病学神经外科学杂志, 2013, 40(1): 5-9. |
| [2] |
Aronowski J, Zhao X. Molecular Pathophysiology of cerebral hemorrhage:secondary brain injury[J]. Stroke, 2011, 42(6): 1781-1786. DOI:10.1161/STROKEAHA.110.596718 |
| [3] |
Lazennec G, Richmond A. Chemokines and chemokine receptors:new insights into cancer-related inflammation[J]. Trends Mol Med, 2010, 16(3): 133-144. DOI:10.1016/j.molmed.2010.01.003 |
| [4] |
肖新兴, 刘庆新, 邹雪飞, 等. 急性脑梗死患者血浆CXCL12水平的改变及其对临床预后的影响[J]. 临床神经病学杂志, 2015, 28(2): 91-94. |
| [5] |
王聪聪, 刘睿, 袁淑绘, 等. CXCL12在大鼠短暂性局灶性脑缺血损伤超早期中的作用[J]. 中风与神经疾病杂志, 2015, 32(12): 1095-1098. |
| [6] |
Qureshi AI, Mendelow AD, Hanley DF. Intracerebral haemorrhage[J]. Lancet, 2009, 373(9675): 1632-1644. DOI:10.1016/S0140-6736(09)60371-8 |
| [7] |
Gupta M, Verma R, Parihar A, et al. Perihematomal edema as predictor of outcome in spontaneous intracerebral hemorrhage[J]. Neurosci Rural Pract, 2014, 5(1): 48-54. DOI:10.4103/0976-3147.127873 |
| [8] |
Wang J, Doré S. Inflammation after intracerebral hemorrhage[J]. J Cereb Blood Flow Metab, 2007, 27(5): 894-908. DOI:10.1038/sj.jcbfm.9600403 |
| [9] |
Chung SH, Seki K, Choi BI, et al. CXC chemokine receptor 4 expressed in T cells plays an important role in the development of collgen-induced arthritis[J]. Arthritis Res Ther, 2010, 12(5): 1-14. |
| [10] |
Negrete-García MC, Velazquez JR, Popoca CA, et al. Chemokine (C-X-C motif) ligand 12/stromal cell-derived factor-1 is associated with leukocyte recruitment in asthma[J]. Chest, 2010, 138(1): 100-106. DOI:10.1378/chest.09-2104 |
| [11] |
Lukacs NW, Berlin A, Schols D, et al. AMD3100, a CXCR4 antagonis, attenuates allergic lung inflammation and airway hyperreactivity[J]. Am J Pathol, 2002, 160(4): 1353-1360. DOI:10.1016/S0002-9440(10)62562-X |
| [12] |
Liu P, Xiang JW, Jin SX. Serum CXCL12 levels are associated with stroke severity and lesion volumes in stroke patients[J]. Neurol Res, 2015, 37(10): 853-858. DOI:10.1179/1743132815Y.0000000063 |
| [13] |
Gu XL, Liu L, Lu XD, et al. Serum CXCL12 Levels as a Novel Predictor of Future Stroke Recurrence in Patients with Acute Ischemic Stroke[J]. Mol Neurobiol, 2016, 53(5): 2807-2814. DOI:10.1007/s12035-015-9151-0 |
| [14] |
Ruscher K, Kuric E, Liu Y, et al. Inhibition of CXCL12 signaling attenuates the post ischemic immune response and improves functional recovery after stroke[J]. J Cereb Blood Flow Metab, 2013, 33(8): 1225-1234. DOI:10.1038/jcbfm.2013.71 |
| [15] |
Filippo TRM, Galindo LT, Barnabe GF, et al. CXCL12 N-terminal end is sufficient to induce chemotaxis and proliferation of neural stem/progenitor cells[J]. Stem Cell Res, 2013, 11(2): 913-925. DOI:10.1016/j.scr.2013.06.003 |
| [16] |
Jun H, Yaning L, Yaohui T, et al. CXCR4 antagonist AMD3100 protects blood-brain barrier integrity and reduces inflammatory response after focal ischemia in mice[J]. Stroke, 2013, 44(1): 190-197. DOI:10.1161/STROKEAHA.112.670299 |
| [17] |
Wu KJ, Yu SJ, Shia KS, et al. A Novel CXCR4 Antagonist CX549 Induces Neuroprotection in Stroke Brain[J]. Cell Transplant, 2017, 26(4): 571-583. DOI:10.3727/096368916X693563 |
| [18] |
Yamaguchi J, Kusano KF, Masuo O, et al. Stromal cell-derived factor-1 effects on ex vivo expanded endothelial progenitor cell recruitment for ischemic neovascularization[J]. Circulation, 2003, 107(9): 1322-1328. DOI:10.1161/01.CIR.0000055313.77510.22 |
| [19] |
黎柏源, 白万胜, 赵永博, 等. 基质衍生因子-1对大鼠脑出血后神经细胞凋亡的作用及其机制研究[J]. 中国现代医学杂志, 2015, 25(1): 21-25. |
| [20] |
Shen J, Chen B, Zheng GR, et al. Detection of high serum concentration of CXC chemokine ligand-12 in acute intracerebral hemorrhage[J]. Clin Chim Acta, 2017, 471: 55-61. DOI:10.1016/j.cca.2017.05.022 |
 2017, Vol. 44
2017, Vol. 44




