扩展功能
文章信息
- 方立, 单国用, 张松, 高松涛, 张道培
- FANG li, SHAN guo-yong, ZHANG song, GAO song-tao, ZHANG dao-pei
- 伽玛刀治疗三叉神经痛显效、复发时间及安全性的生存分析
- A survival analysis of patients with trigeminal neuralgia undergoing gamma knife surgery: time to marked response, time to recurrence, and safety
- 国际神经病学神经外科学杂志, 2017, 44(3): 252-256
- Journal of International Neurology and Neurosurgery, 2017, 44(3): 252-256
-
文章历史
收稿日期: 2017-03-02
修回日期: 2017-04-24
2. 郑州人民医院神经内科, 河南 郑州 450000
2. Department of Neurology, Zhengzhou people's Hospital, Zhenghou 450000, china
伽玛刀(Gamma knife surgery,GKS)作为一种非侵入性手术方法,目前证实其在治疗TN上具有良好的疗效和较高的安全性。被推荐应用于治疗药物难治性TN或作为其他治疗方法失败时的辅助替代治疗[1]。但对于影响其术后的预后、复发因素目前尚仍有争议。因此,我们通过郑州人民医院GKS治疗中心2012年6月至2015年2月期间确诊的TN并行GKS治疗的患者预后、复发及不良反应情况进行随访研究,探讨与患者术后预后及复发相关的影响因素。
1 资料与方法 1.1 资料 1.1.1 纳入排除标准纳入标准2012年6月至2015年8月在我院确诊的TN患者,符合国际头面痛学会分会委员会制定的诊断标准:(1) 阵发性发作的面部疼痛,持续数秒。(2) 疼痛至少包含以下5种标准:① 疼痛只限于三叉神经的一支或多支分布区;② 疼痛为突然的、强烈的、尖锐的、皮肤表面的刺痛或烧灼痛;③ 疼痛程度严重;④ 刺激扳机点可诱发疼痛;⑤ 具有痉挛发作间歇期。(3) 无神经系统损害表现。(4) 每次发作形式刻板。(5) 排除其他引起面部疼痛的疾患。对于疑为继发性三叉神经痛患者,应进行详细的体格检查,必要时行头颅平片、CT及/或MRI检查。
1.1.2 排除标准GKS术后随访期间,再行其他三叉神经相关手术治疗。
1.2 临床资料特点92例入选患者术后随访中3例患者失联,1例术后再行其他手术而退出试验。共88例完成随访。男26例,女62例;年龄35~92岁,中位年龄59岁,其中 < 70岁53例,≥70岁35例;中心剂量最小65Gy, 最大90Gy,中位中心剂量75.35Gy,70Gy~90Gy 64例,65Gy~70Gy 24例;非典型性疼痛34例,典型性疼痛54例;靶点位置距离脑干边缘最小6 mm,最大12 mm,中位靶点距脑干距离8.65 mm,< 8 mm 34例,≥8 mm 54例,按靶点位置分组时,中心剂量范围为65Gy~90Gy,两组间剂量比较经t检验无统计学差异(p < 0.05);三叉神经手术史8例,血管减压术史5例,射频消融史3例,无手术史80例;卡马西平等抗癫痫药物应用史76例,无药物应用史12例;磁共振检查三叉神经与血管接触密切者51例,无接触者37例;三叉神经痛病程1月~12年,中位病程3.64年,< 3年57例,≥3年31例。具体如表 1。
| 分组 | 例数 | 中位显效时间 | χ2 | p值 |
| 年龄 | ||||
| < 70岁 | 53 | 1 | 0.174 | 0.676 |
| ≥70岁 | 35 | 1 | ||
| 性别 | ||||
| 男 | 26 | 3 | 3.760 | 0.052 |
| 女 | 62 | 1 | ||
| 中心剂量 | ||||
| < 70 Gy | 24 | 3 | 7.951 | 0.005 |
| ≥70 Gy | 64 | 1 | ||
| 疼痛特点 | ||||
| 非典型疼痛 | 33 | 1 | 4.504 | 0.034 |
| 典型疼痛 | 55 | 3 | ||
| 靶点位置距离脑干边缘 | ||||
| < 8 mm | 34 | 1 | 12.543 | 0.000 |
| ≥8 mm | 54 | 3 | ||
| 手术史 | ||||
| 有 | 8 | 4.5 | 19.150 | 0.000 |
| 无 | 80 | 1 | ||
| 药物治疗史 | ||||
| 有 | 76 | 1 | 2.149 | 0.143 |
| 无 | 12 | 1 | ||
| 神经与血管接触 | ||||
| 有 | 51 | 1 | 0.118 | 0.731 |
| 无 | 37 | 1 | ||
| 病程 | ||||
| < 3年 | 57 | 1 | 27.255 | 0.000 |
| ≥3年 | 31 | 3 |
在局麻下安装Leksell立体定向框架,头略俯以使三叉神经根走行与Y轴平行。排除干扰因素,采用3.0TMRI(3D-TOF)序列,0.7mm薄层无间距定位扫描三叉神经区域,充分显示三叉神经根部。使用深圳玛西普公司SRRS型治疗系统进行治疗规划。选用4mm准直器,沿患侧三叉神经感觉根脑桥段(REZ)设置靶点,调节权重,采用50%等剂量曲线包绕三叉神经根部,靶区中心剂量为65~90Gy,将20%等剂量曲线限定在脑干外缘最深不超过3mm,使脑干边缘剂量不高于16Gy。最后,记录靶点至脑干边缘距离(沿三叉神经根径向)。至术后常规应用20%甘露醇及地塞米松针预防脑干水肿。
1.4 疗效评价采用巴罗神经学研究所(BNI)评分系统,其中Ⅰ级~Ⅲ级为治疗有效。Ⅳ级为无效。术后疼痛再发或复发并程度达Ⅳ级为复发。统计治疗有效率,且记录显效时间及复发时间。
1.5 随访患者GKS术后第1、3、6、12、24个月时分别进行电话或门诊随访,复发也作为随访终点。
1.6 统计学方法所有数据均采用SPSS 19.0软件进行分析。计数资料的描述采用率或构成比,采用Kaplan-Meier法进行显效时间及复发时间的单因素生存分析,用log-rank法对其中的分组资料进行比较,对筛选出的相关因素代入Cox风险比例模型中进行多因素分析,确定影响预后及复发的因素。对影响预后风险因素分组,组内的不良反应率间比较应用χ2检验,p < 0.05为差异有统计学意义。
2 结果 2.1 显效、复发时间情况所有入组患者术后1月、3月、6月、12月、24月的治疗有效率分别为56.8%、79.5%、87.5%、93.18%、89.77%。最短显效时间为术后3小时。最长显效时间为术后第16个月。中位起效时间为2个月。1月、3月、6月、12月、24月的复发率分别为0%、0%、2.27%、3.41%、6.82%,其中术后最短复发时间为术后第4个月。最长复发时间为术后24个月。中位复发时间为13.5个月。术后出现不良反应的为16例,不良反应率为18.18%,主要为面部麻木或面部发凉感,无死亡病例。
2.2 影响显效时间的单因素分析经Kaplan-Meier法单因素分析,且经log-rank法进行比较,其中中心剂量、靶点位置、疼痛特点、手术史、病程与GKS治疗TN的显效时间相关(p值均 < 0.05)。如表 1。
2.3 影响显效时间的多因素分析将单因素分析中有统计学意义的因素纳入Cox风险模型中,病程、靶点、手术史是影响TN患者GKS术后显效时间的独立风险因素(p值均 < 0.05)。病程 < 3年、靶点脑桥缘距离 < 8mm、既往无手术史的患者GKS术后显效时间明显提前。如表 2。生存函数关系见图 1、图 2、图 3。
| 因素 | β | SE | Wald值 | RR值 | 95%CI | p值 |
| 病程 | -0.682 | 0.271 | 6.350 | 0.505 0.297 | 0.859 | 0.012 |
| 靶点 | -0.587 | 0.262 | 5.021 | 0.556 0.333 | 0.929 | 0.025 |
| 手术史 | 1.634 | 0.550 | 8.847 | 5.127 1.746 | 15.052 | 0.003 |

|
| 图 1 病程与显效时间关系的生存函数图。 |
|
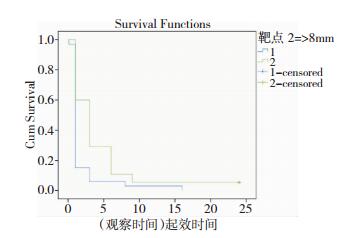
| 图 2 靶点位置与显效时间关系的生存函数图。 |
|
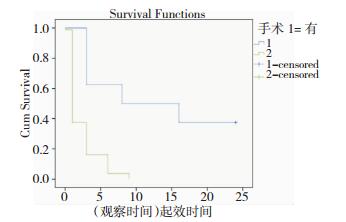
| 图 3 手术史与显效时间关系的生存函数图。 |
既往手术史(χ2=5.628, p值=0.018) 及病程(χ2=3.863, p值=0.049) 与GKS治疗TN的复发时间相关。如表 2。
2.5 影响复发时间的多因素分析将单因素分析中有统计学意义的因素纳入Cox风险模型中,采取向前引入法,手术史(p=0.089) 剔除出模型中。病程纳入模型后,无统计学意义(p=0.458)。如表 3。
术后24个月共出现不良反应16例(其中面部麻木10例,面部发凉3例,面部感觉减退1例,口角歪斜1例、上睑下垂伴口角歪斜1例),不良反应发生率为18.18%。按病程分组,病程 < 3年组与病程≥3年组的不良反应率间比较,差异均无统计学意义(p值>0.05);按手术史分组,有手术史组与无手术史组的不良反应率间比较,差异均无统计学意义(p值>0.05);而靶点距脑干边缘 < 8mm组较≥8mm组的不良反应率高,差异有统计学意义(p值 < 0.05)。如表 4。
| 分组 | 麻木 | 发凉 | 感觉减退 | 口角歪斜 | 上睑下垂 | 总例数(组内%) | χ2 | p值 |
| 病程 | ||||||||
| < 3年 | 5 | 2 | 1 | 0 | 1 | 9(15.79) | 0.623 | 0.430 |
| ≥3年 | 5 | 1 | 0 | 1 | 7(22.58) | |||
| 靶点位置 | ||||||||
| < 8 mm | 8 | 3 | 1 | 1 | 1 | 14(25.45) | 19.694 | 0.000 |
| ≥8 mm | 2 | 2(6.06) | ||||||
| 既往手术史 | ||||||||
| 有 | 1 | 1(12.5) | 0.191 | 0.662 | ||||
| 无 | 9 | 3 | 1 | 1 | 1 | 15(18.75) |
GKS治疗TN的机制可能是通过GKS局部照射三叉神经根部,可引起三叉神经根部周围的接触责任血管闭塞退变萎缩及旁路神经尤其触觉传入纤维伪突触连接的传导阻滞,提高痛觉阈值,降低神经电信号的敏感性,从而使得疼痛缓解[2]。
最近的一项研究发现TN患者GKS术后较好的疗效可能与以下因素有关:高龄,女性,病程早期(病程 < 3年),典型的疼痛特征,存在血管压迫,既往无微血管减压或射频消融等手术史,较大的辐射剂量和药物应用史等[1, 10, 12]。
国外的研究发现BNI评分Ⅰ-ⅢA期TN患者在疼痛病程早期(小于3年)接受GKS治疗,显效时间较早,且无痛期(无药物应用情况下)较长,并能维持很长的疼痛缓解期(BNI评分维持在Ⅰ-ⅢA期之间)[3]。也有人认为治疗前疼痛病史较长,可能是部分TN患者转化为难治性TN的原因[4]。本研究发现病程 < 3年的患者GKS术后显效时间明显提前。目前比较普遍的观点认为动脉压迫是TN发病的主要原因[15]。发现三叉神经受压程度与时间(病程)成正比,病程越长,粘连越多,受压越重[5]。因此,我们推测病程早期患者三叉神经受压及与周围血管或软组织粘连较轻,神经暴露较为充分,组织结构更为清晰,GKS定位更为精准,因此应用GKS治疗时显效较早。
GKS治疗常用的靶点是在三叉神经根近桥脑处。Brisman等人通过辐射剂量及范围变化直方图分析靶点脑干间距离与疗效的关系,发现产生良好效应的辐射目标是接近脑干边缘[6]。Tyler Kabara等人比较90 Gy(30%的等剂量线在脑干边缘)和90 Gy(50%等剂量线在脑干边缘)两组患者,接受50%等剂量线在脑干边缘的患者,疼痛缓解显效最早[8]。从病理特点上分析,三叉神经靠近脑干边缘部分是神经远端的施旺细胞向近端少突胶质细胞的过渡点,三叉神经对放射的敏感性在此发生变化,从神经远端向靠近脑干边缘的近端逐渐增强。这可能就是靠近脑干边缘部分作为合适靶点的原因[1]。从局部解剖结构上看,三叉神经从小脑中脚发出处称REZ, 该段包括有较大的感觉根和较小的运动根。该段行程较直,REZ也是血管压迫的关键部位[9]。此处正是感觉神经纤维汇聚的“最后共同通路”,在此处照射不仅能使所有的感觉神经纤维获得同步照射,而且从能量消耗上来讲也最为经济。从影像特点上看,REZ恰穿越颅后窝脑脊液,在此容易获得良好的对比度,因而对REZ的立体定位更精确[5]。我们的研究中,靶点脑桥缘距离最短的患者为6mm。调试中发现,小于6mm时,20%等剂量曲线很容易超越脑干外缘3mm。靶点脑桥缘距离 < 8mm患者的显效时间明显提前。与国外的研究基本一致。也有研究认为,脑干附近辐射剂量达到15Gy以上的患者术后疼痛明显改善[6]。而我们靶点脑桥缘距离最长为12mm。调试中发现,大于8mm时,脑干边缘剂量下降。使得脑干边缘附近受照射程度不够。这也部分解释了大于8mm组显效较晚的原因。
一项复发性TN患者重复放射治疗研究显示,既往TN相关外科手术史少于3个的患者有更大概率获得完全或适当的疼痛缓解[11]。一项立体定向放射治疗TN研究显示,较差的治疗反应与患者曾接受过三叉神经相关手术有关[13]。我们的研究中发现无手术史患者较既往有过三叉神经相关手术史患者显效时间明显提前。研究中有2例TN患者射波刀术后再发,4例微血管减压术后复发,还有1例脑桥胶质瘤术后,术后患者的GKS治疗效果较差,显效时间延后。我们认为手术影响显效时间的原因可能是:① 手术后改变了三叉神经通路与周围组织结构关系,术后三叉神经周围组织压迫、粘连、炎症程度较高,导致三叉神经脊束核发生突触再塑,导致GKS再次治疗时的显效时间延迟。② 手术改变了三叉神经入脑桥缘处放射敏感区范围或敏感性的变化,导致伽玛刀再次定位的准确性发生变化。
此时,我们发现手术史及病程与GKS治疗TN的复发时间相关。随访中发现有2例TN患者,及1例脑胶质瘤术后继发TN患者,曾先后多次行过微血管减压术及射频消融术,但再次行GKS术后疼痛缓解较晚,且缓解时间较短,复发较早。但经COX回归分析,手术史及病程等并非有统计意义的独立影响因素。可能是受样本例数少或观察时间短的影响,还需后续扩大样本量及延长观察时间继续研究。
一项450例TN研究中发现,GKS术后55%患者会感到面部麻木,但只有2%的患者不能耐受麻木症状[7]。也有建议将靶点定位在距离脑干5~8毫米之间,能在使用较高的剂量更好地控制疼痛和形成三叉神经功能障碍等局限性不良影响之间达到最佳平衡[14]。有研究认为较好的GKS治疗效果与TN治疗的副反应有关,而该副反应的发生与辐射是否侵袭脑干有关[1]。我们发现靶点距脑干边缘小于8mm组较大于8mm组的不良反应率高,但主要为面部感觉异常如麻木。从解剖与生理学角度分析,靶点距离脑干较近,此处为三叉神经入脑桥段,感觉纤维相对密集。且传导痛温觉的纤维和传导触觉的纤维混合组成三叉神经,属感觉纤维更为密集区,很难只毁损传导痛觉的纤维,而不损伤传导触觉的Aa和Aβ类纤维,而后者的损伤正是术后麻木的主要原因[16]。我们发现2例GKS术后口角歪斜,他们的靶点脑桥缘距离均小于8mm,对应的20%等剂量线覆盖脑桥边缘较多,可能导致同侧穿行于脑桥腹侧的面神经受损。因此,较好的靶点位置设定可能还需要进一步的研究证实。
综上总结,病程小于3年、靶点距离脑桥缘较短、既往无手术史是影响TN患者GKS术后显效时间的独立积极影响因素。而靶点距离脑桥缘较短可能导致不良反应相对增多。
| [1] |
Niranjan A, Lunsford LD. Radiosurgery for the management of refractory trigeminal neuralgia[J]. neurology India, 2016, 64(4): 624-629. DOI:10.4103/0028-3886.185393 |
| [2] |
Chen JF, Lee ST. Comparison of percutaneous trigeminal ganglion compression and microvascular decompression for the management of trigeminal neuralgia[J]. Clin Neurol Neurosurg, 2003, 105(3): 203-208. DOI:10.1016/S0303-8467(03)00012-X |
| [3] |
Mousavi SH, Niranjan A, Huang MJ, et al. Early radiosurgery provides superior pain relief for trigeminal neuralgia patients[J]. Neurology, 2015, 85(24): 2159-2165. DOI:10.1212/WNL.0000000000002216 |
| [4] |
Dai ZF, Huang QL, Liu HP, et al. Efficacy of stereotactic gamma knife surgery and microvascular decompression in the treatment of primary trigeminal neuralgia:a retrospective study of 220 cases from a single center[J]. J Pain Res, 2016, 9: 535-542. DOI:10.2147/JPR |
| [5] |
潘绵顺, 王鹏, 汪业汉. 原发性TN发病机制及放射外科治疗. 第二届国际肿瘤靶向治疗大会暨中法靶向放疗论坛会议论文选编[C]; 2008年.
|
| [6] |
Brisman R, Mooij R. Gamma knife radiosurgery for trigeminal neuralgia:Dose-volume histograms of the brainstem and trigeminal nerve[J]. J Neurosurg, 2000, 93(Suppl 3): 155-158. |
| [7] |
刘晓民, 徐德生, 刘阿力, 等. 第十五届国际Leksell伽玛刀年会纪要[J]. 国际神经病学神经外科学杂志, 2010, 37(4): 318-319. |
| [8] |
Tyler-Kabara EC, Kassam AB, Horowitz MH, et al. Predictors of outcome in surgically managed patients with typical and atypical trigeminal neuralgia:comparison of results following microvascular decompression[J]. J Neurosurg, 2002, 96(3): 527-531. DOI:10.3171/jns.2002.96.3.0527 |
| [9] |
廖洪飞. TNGKS治疗长期随访疗效及起效时间多因素分析. [D]. 四川. 泸州医学院. 2012: 27.
|
| [10] |
Kondziolka D, Zorro O, Lobato-Polo J, et al. Gamma Knife stereotactic radiosurgery for idiopathic trigeminal neuralgia[J]. J Neurosurg, 2010, 112(4): 758-765. DOI:10.3171/2009.7.JNS09694 |
| [11] |
Kano H, Kondziolka D, Yang HC, et al. Outcome predictors after gamma knife radiosurgery for recurrent trigeminal neuralgia[J]. Neurosurgery, 2010, 67(6): 1637-1644. DOI:10.1227/NEU.0b013e3181fa098a |
| [12] |
Maesawa S, Salame C, Flickinger JC, et al. Clinical outcomes after stereotactic radiosurgery for idiopathic trigeminal neuralgia[J]. J Neurosurg, 2001, 94(1): 14-20. DOI:10.3171/jns.2001.94.1.0014 |
| [13] |
Martínez Moreno NE, Gutiérrez-Sárraga J, Rey-Portolés G, et al. Long-Term Outcomes in the Treatment of Classical Trigeminal Neuralgia by Gamma Knife Radiosurgery:A Retrospective Study in Patients With Minimum 2-Year Follow-up[J]. Neurosurgery, 2016, 79(6): 879-888. DOI:10.1227/NEU.0000000000001404 |
| [14] |
Massager N, Lorenzoni J, Devriendt D, et al. Gamma knife surgery for idiopathic trigeminal neuralgia performed using a far-anterior cisternal target and a high dose of radiation[J]. J Neurosurg, 2004, 100(4): 597-605. DOI:10.3171/jns.2004.100.4.0597 |
| [15] |
刘国平, 曾群, 杨治权, 等. 显微血管减压术治疗三叉神经痛和面肌痉挛的技术差别(附37例报告)[J]. 国际神经病学神经外科学杂志, 2014, 41(6): 522-525. |
| [16] |
陈文亚. 三叉神经痛治疗中视频温度和针尖长度对视频热凝术疗效的影响[J]. 国际神经病学神经外科学杂志, 2015, 42(2): 121-125. |
 2017, Vol. 44
2017, Vol. 44



 ,
,