扩展功能
文章信息
- 严利, 周文胜, 王佳
- YAN Li, ZHOU Wen-Sheng, WANG Jia
- 过氧化氢干预下Rab30在PC12细胞中的表达及促凋亡通路
- Expression of Rab30 in PC12 cells and related pro-apoptotic pathways under hydrogen peroxide intervention
- 国际神经病学神经外科学杂志, 2016, 43(6): 516-520
- Journal of International Neurology and Neurosurgery, 2016, 43(6): 516-520
-
文章历史
收稿日期: 2016-06-20
修回日期: 2016-11-14
2. 湘潭市第一人民医院老年医学科, 湖南省湘潭市 411101;
3. 湖南省人民医院/湖南省老年医学研究所,湖南省长沙市 410016
神经退行性疾病是指一组由慢性进行性的中枢神经组织退行性变性而发生的疾病的总称。虽然这类疾病的发病机制及病变部位各不相同,神经元的损伤和凋亡(apoptosis) 是引起神经退行性疾病的共同原因。近年来,人们对神经细胞退变发病机理的研究越来越多,研究表明诱导神经细胞死亡的机制主要包括:炎症反应、兴奋性氨基酸毒性、线粒体结构及功能障碍、氧化应激及自由基增多、细胞凋亡等[1-2]。现在更有研究认为高尔基体出现应激反应,其结构的碎裂也是神经元凋亡的机制,但高尔基体碎裂是如何发生和发展的尚不明确[3]。Rab30作为一种重要的调节型的运输蛋白,参与维持非神经细胞高尔基体结构完整[4],可能也参与损伤机制下神经细胞高尔基体碎裂的调控,从而导致神经元丧失。因此,本研究通过检测Rab30在PC12细胞经过氧化氢(H2O2) 损伤干预下的表达情况,并利用MTT法检测细胞存活率、Annexin V-FITC/PI双染法检测细胞凋亡、Western-blot检测JNK3、GM130和Caspase-3蛋白表达,探究H2O2损伤干预下Rab30在PC12细胞中的表达及可能的促凋亡通路。
1 材料与方法 1.1 材料PC12细胞购自中国科学院上海生物细胞研究所;1640培养基(Hyclone公司);胎牛血清与胰蛋白酶(来自Gibco公司);H2O2(国药集团北京有限公司);Rab30抗体(ORIGENE公司);JNK3和GM130抗体(Proteintech公司);Caspase-3抗体(CST公司);二抗(Proteintech公司);MTT (Sigma公司);Annexin V-FITC/PI双染细胞凋亡试剂盒(长沙维尔生物有限公司);BCA蛋白定量试剂盒(Wellbio);显影液-定影液(WellBiology);Super ECL Plus超敏发光液(Thermo pierce公司);25 cm2培养瓶-6孔板(cyagen公司);Tris、APS、SDS、TEMED、甘氨酸、丽春红等均来自美国Sigma公司。
1.2 方法 1.2.1 细胞培养和分组用含有10%胎牛血清的1640完全培养基,在5%CO2、37℃恒温恒湿培养箱培养PC12细胞。待细胞融合至80%~90%即可传代,取细胞形态良好、对数增殖期培养的细胞用于后续实验。实验分为正常培养5 h组(正常组) 和200 Μm H2O2处理5 h组(H2O2组)。
1.2.2 MTT检测细胞存活率两组细胞各设3个复孔,每孔加入20 μl 5 mg/ml的MTT溶液,37℃,5%CO2饱和湿度培养箱中培养。4 h后取出,弃掉上清,在每孔中加入150 μl二甲基亚砜,缓慢摇晃10 min左右用酶联免疫检测仪在490 nm处测定其吸光度值(A值),计算出PC12细胞的存活率。用每组A值与空白对照组A值的比值来计算细胞存活率,实验重复6次,最后取平均值。
1.2.3 Annexin V-FITC/PI双染法检测细胞的凋亡率两组细胞处理5 h后,用不含EDTA的胰蛋白酶进行消化,以冰冷的PBS洗涤2次,离心(2000 rpm/min,5 min) 后收集细胞,收集约1×105~5×105细胞。除去上清液,滴入500 μl Binding buffer悬浮细胞,加入5 μl Annexin V-FITC及5 μl PI使用液使其混匀,置于室温下避光5~15 min后,1 h内采用流式细胞仪检测其荧光强度。正常活的细胞(双阴性细胞) 主要分布在流式细胞分析图中的左下象限(LL),Annexin V-FITC及PI均低染(Annexin V-PI-);早期凋亡的细胞或死亡的细胞分布在流式分析图的右下象限(LR),Annexin V-FITC高染而PI低染(Annexin V+PI-);晚期死亡或凋亡的细胞分布在图的右上象限(UR),AnnexinV-FITC及PI均高染(Annexin V+PI+)[5]。总凋亡率=早期凋亡细胞百分数(LR)+晚期凋亡细胞百分数(UR)。采用专业软件Cell Quest对所得到的数据进行收集、储存和分析。
1.2.4 Western-blot检测Rab30、JNK3、GM130、Caspase-3的蛋白表达收集两组细胞,使用蛋白提取试剂盒提取总蛋白,测量其蛋白浓度。蛋白变性后进行SDS-聚丙烯酰胺凝胶电泳,用半干转移法将凝胶电泳分离的蛋白分子转移到PVDF膜上。5%牛血清白蛋白室温封闭1 h,加入相应一抗,抗Rab30(1 :500)、JNK3(1 :500)、GM130(1 :1000)、Caspase-3(1 :1000)、β-actin (1 :4000),4℃孵育过夜。用TBST洗3次,每次10 min。加入相应二抗37℃孵育1 h,TBST漂洗4次,ECL显影和采图。Quantity one软件分析各条带吸光度值,计算相对表达量。实验重复4次,取均值做统计学分析。
1.3 统计学分析所有数据应用SPSS 17.0统计软件进行统计学分析。数据均采用均数±标准差(x±s) 表示,两组间比较用LSD-t检验,以P < 0.05为差异有统计学意义。
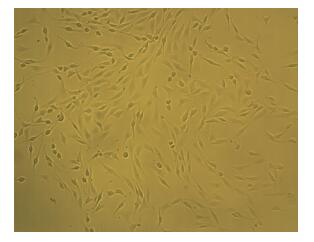
2 结果 2.1 PC12细胞的培养显微镜下观察PC12细胞形态为多角型细胞,贴壁不稳,易成团,胞体周围有晕光,折光度强,成簇生长,培养5~7 d后PC12细胞形成密集的细胞簇,布满整个培养瓶。见图 1。
|
| 图 1 显微镜下正常培养条件下PC12细胞形态结构(10×40)。 |
经200 Μm H2O2处理5 h后的PC12细胞存活率较正常培养的细胞明显减少。H2O2组的吸光度A值(0.1577±0.0100) 与正常组(0.2553±0.0084) 比较明显减少,差异有统计学意义(P < 0.05)。见表 1。
| 实验分组 | N | A值 |
| 正常组 | 6 | 0.2553±0.0084 |
| H2O2组 | 6 | 0.1577±0.0100a |
| 注:a为与正常组比较,P < 0.05。 | ||
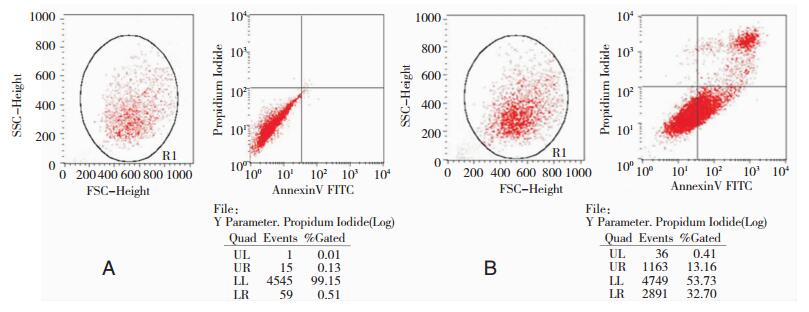
结果显示正常组PC12细胞绝大部分均为双阴性细胞(图 1A,左下象限),正常组细胞结构完整,无明显细胞凋亡或死亡;而经H2O2损伤干预后PC12细胞的凋亡率明显增加(图 1B,右上象限和右下象限),即H2O2组(32.7500±1.0485;46.1167±1.1501) 的早期凋亡率及总凋亡率与正常组(0.5033±0.0216;0.6333±0.0450) 的比较显著增加,差异有统计学意义(P < 0.05)。见表 2和图 2。
| 组别 | N | 早期凋亡率 | 总凋亡率 |
| 正常组 | 6 | 0.5033±0.0216 | 0.6333±0.0450 |
| H2O2组 | 6 | 32.7500±1.0485a | 46.1167±1.1501b |
| 注:a为与正常组的早期凋亡率比较,P < 0.05;b为与正常组的总凋亡率比较,P < 0.05。 | |||
|
| 图 2 Annexin V-FITC/PI法检测PC12细胞的凋亡率流式细胞分析图。 注:A:正常组;B:H2O2组;左下象限:正常活的PC12细胞(双阴性细胞);右上象限:晚期凋亡或死亡的PC12细胞;右下象限:早期凋亡的PC12细胞;左上象限:细胞碎片、损伤的PC12细胞。 |
H2O2损伤干预后,Rab30、GM130在PC12细胞的表达明显下降,而JNK3、Caspase-3在PC12细胞中表达明显增加。即,H2O2组中的Rab30(0.0570±0.0014) 的蛋白表达与正常组(0.2272±0.0020) 比较,差异有统计学意义(P < 0.05);H2O2组中的JNK3(0.6904±0.0211) 蛋白表达与正常组(0.1167±0.0024) 比较,差异有统计学意义(P < 0.05);H2O2组中的GM130(0.0821±0.0038) 的蛋白表达与正常组(0.2704±0.0053) 比较,差异有统计学意义(P < 0.05);H2O2组中的Caspase-3(0.8620±0.0198) 的蛋白表达与正常组(0.3232±0.0006) 比较,差异有统计学意义(P < 0.05)。见表 3。
| 组别 | N | Rab30/β-actin | JNK3/β-actin | GM130/β-actin | Caspase-3/β-actin |
| 正常组 | 4 | 0.2272±0.0020 | 0.1167±0.0024 | 0.2704±0.0053 | 0.3232±0.0006 |
| H2O2组 | 4 | 0.0570±0.0014a | 0.6904±0.0211a | 0.0821±0.0038a | 0.8620±0.0198a |
| 注:β-actin为内参指数;a为与正常组比较,P < 0.05。 | |||||
神经退行性疾病的本质是神经元的丧失,高尔基体的形态改变或破裂是神经退行性疾病共同出现的特征。一旦高尔基体的结构及功能遭受破坏,将会导致蛋白质、脂质结构和转运的异常,神经元细胞功能紊乱,最终导致疾病的发生[6]。在病理条件和损伤机制(兴奋毒性氨基酸、钙超载、炎症因子、氧自由基等) 时,高尔基体会出现应激反应,其超微结构发生变化,甚至发生碎裂[3]。氧化应激在神经退行性疾病中起着非常重要的作用,H2O2作为一种氧化应激诱导剂,常被应用于诱导细胞氧化应激的模型。现阶段认为高尔基体发生破裂可能存在以下机制:① 与氧化应激密切相关[7]。氧化应激主要是通过3个途径介导高尔基体的碎裂:氧化应激导致高尔基体微管蛋白的损伤;氧化应激可清除高尔基体结构蛋白的凋亡蛋白酶,如Caspase-2、Caspase-3或Caspase-7等;氧化应激可引起Ca2+释放,导致胞内钙离子浓度增加。② 错误蛋白的折叠或异常蛋白的聚积与积累,包括突变的SOD1、stathmin、a-synuclein和tau等,它们被认在发病过程中起了关键的作用[8]。③ 钙离子稳态失衡[9]。
Rab蛋白是一类小分子调节型GTP结合蛋白(small GTP-binding proteins),主要参与细胞内的蛋白、脂质的转运过程,包括囊泡的形成、迁移及融合。当胞内某些特定的蛋白运输出现错误时,就会导致某些疾病的发生,这是由于Rab蛋白调控因子发生突变或蛋白功能出现紊乱引起的[10]。Rab30是一个广泛表达、分子量为23 KD的GTP结合蛋白,位于11号染色体中,是从人类的黑素细胞cDNA首先鉴定出来[11]。最近的研究表明Rab30主要定位于高尔基体中,并且在非神经细胞中是维持高尔基体其结构完整所必须的,通过Rab30的沉默表达可导致正常高尔基体弓形结构破裂成片[4]。在我们实验中发现,Rab30经H2O2损伤干预后在PC12细胞中的表达下调,因此,我们推断Rab30有可能同样参与了神经细胞中高尔基体破裂的调控作用。
高尔基体基质蛋白130(Golgi matrix protein 130, GM130) 是高尔基体顺面网状结构中一个重要的基质蛋白,可作为高尔基体结构定位的标记物,GM130表达量下降可作为高尔基体破坏比较敏感的分子标志。赵黔鲁等[12]用鱼藤酮干预PC12细胞,发现GM130表达明显下调,且高尔基体结构也出现了变化。王艳等[13]证实了在脑缺血再灌注实验模型中,TGF-β1表达增加,GM130表达下降,高尔基体结构受损。Nakagomis等[3]发现高尔基体的破裂是先于神经细胞死亡的。GM130作为反应高尔基体结构及功能破坏敏感的分子标志,在本实验中经H2O2损伤干预后的PC12细胞存活率减少,凋亡率增加,GM130蛋白表达较正常组明显下降。因此,我们推断H2O2损伤干预很可能了影响了PC12细胞高尔基体的形态及结构,甚至发生了高尔基体碎裂。
Rab30是c-Jun氨基末端激酶(c-Jun N-terminal kinase, JNK) 的一个靶基因,JNK是丝裂原活化蛋白激酶(mitogen-activatedproteinkinases, MAPKs) 家族中的重要成员,主要参与了细胞存活与凋亡、增殖与分化等多个生物学过程[14]。JNK主要包括JNK1、JNK2和JNK3三个成员,其中JNK3是JNK信号通路中非常重要的异构体之一,主要分布在中枢神经脑组织中,与神经元的凋亡关系密切,大量的炎性介质、细胞因子、应激可以激活JNK3及其后的信号转导。JNK3可介导百草枯和鱼藤酮诱导的多巴胺能神经元死亡,故抑制JNK3的表达,可以显著减少神经元的死亡[15]。本研究发现PC12细胞经H2O2损伤干预可激活JNK3的表达。
综上所述,H2O2损伤干预可下调神经细胞中Rab30的表达,其促凋亡通路可能是通过H2O2激活JNK3的表达而靶向下调Rab30,致使高尔基体结构破碎,并激活Caspase-3的活性,从而诱导神经细胞的凋亡。但由于本次实验没有做Rab30沉默和过表达的干预,Rab30所起的具体机制还有待进一步的研究。
| [1] | Domise M, Vingtdeux V. AMPK in Neurodegenerative Diseases. EXS, 2016, 107: 153–177. |
| [2] | 齐倩倩, 吕佩源. NADPH氧化酶在神经退行性疾病中的作用. 国际神经病学神经外科学杂志, 2015, 42(4): 370–373. |
| [3] | Nakagomi S, Barsoum MJ, Bossy-Wetzel E, et al. A Golgi fragmentation pathway in neurodegeneration. Neurobiol Dis, 2008, 29(2): 221–231. DOI:10.1016/j.nbd.2007.08.015 |
| [4] | Kelly EE, Giordano F, Horgan CP, et al. Rab30 is required for the morphological integrity of the Golgi apparatus. Biol Cell, 2012, 104(2): 84–101. DOI:10.1111/boc.v104.2 |
| [5] | 佟俊杰, 苗清, 王志国, 等. TUNEL法和Annexin V-FITC流式细胞分析法检测成纤维细胞凋亡的对比研究. 口腔医学, 2014, 34(4): 12–15. |
| [6] | Fujita Y, Okamoto K. Golgi apparatus of the motor neurons in patients with amyotrophic lateral sclerosis and in mice models of amyotrophic lateral sclerosis. Neuropathology, 2005, 25(4): 388–394. DOI:10.1111/neu.2005.25.issue-4 |
| [7] | Jiang Z, Hu Z, Zeng L, et al. The role of the Golgi apparatus in oxidative stress:is this organelle less significant than mitochondria?. Free Radic Biol Med, 2011, 50(8): 907–917. DOI:10.1016/j.freeradbiomed.2011.01.011 |
| [8] | Fan J, Hu Z, Zeng L, et al. Golgi apparatus and neurodegenerative diseases. Int J Dev Neurosci, 2008, 26(6): 523–534. DOI:10.1016/j.ijdevneu.2008.05.006 |
| [9] | Vanoevelen J, Raeymaekers L, Dode L, et al. Cytosolic Ca2+ signals depending on the functional state of the Golgi in HeLa cells. Cell Calcium, 2005, 38(5): 489–495. DOI:10.1016/j.ceca.2005.07.003 |
| [10] | Liu S, Storrie B. How Rab proteins determine Golgi structure. Int Rev Cell Mol Biol, 2015, 315: 1–22. DOI:10.1016/bs.ircmb.2014.12.002 |
| [11] | Chen D, Guo J, Miki T, et al. Molecular cloning of two novel rab genes from human melanocytes. Gene, 1996, 174(1): 129–134. DOI:10.1016/0378-1119(96)00509-4 |
| [12] | 赵黔鲁.鱼藤酮损伤P12细胞的机制研究.邯郸:河北工程学院, 2005. |
| [13] | 王燕.丹红注射液对脑缺血再灌注大鼠高尔基体影响的研究.长沙:中南大学, 2011. |
| [14] | Irving EA, Bamford M. Role of mitogen-and stress-activated kinases in ischemic injury. J Cereb Blood Flow Metab, 2002, 22(6): 631–647. |
| [15] | Choi WS, Abel G, Klintworth H, et al. JNK3 mediates paraquat-and rotenone-induced dopaminergic neuron death. J Neuropathol Exp Neurol, 2010, 69(5): 511–520. DOI:10.1097/NEN.0b013e3181db8100 |
 2016, Vol. 43
2016, Vol. 43




