扩展功能
文章信息
- 陈祖芝, 任志霞, 史晓红, 李书剑, 时英英, 张杰文, 向莉
- CHEN Zu-Zhi, et al REN Zhi-Xia, et al SHI Xiao-Hong, et al LI Shu-Jian, et al SHI Ying-Ying, et al ZHANG Jie-Wen, et al XIANG Liet al
- 河南地区两个腓骨肌萎缩症家系PMP22基因突变研究
- A study of PMP22 gene mutation in two families with Charcot-Marie-Tooth disease in Henan, China
- 国际神经病学神经外科学杂志, 2016, 43(4): 287-291
- Journal of International Neurology and Neurosurgery, 2016, 43(4): 287-291
-
文章历史
收稿日期: 2016-03-17
修回日期: 2016-07-18
腓骨肌萎缩症(Charcot-Marie-Tooth disease, CMT)最早由Charcot、Marie以及Tooth于1886年首先报道,发病率1/2500[1],病程缓慢,基本不影响患者的寿命,是具有高度的临床和遗传异质性的周围神经病变之一。在以往研究中有超过70个基因已经被报道为CMT的发病原因[2],在17p11.2-1上PMP22大片段重复突变导致过度编码蛋白而致CMT1A,主要表现为肌肉无力、远端肢体感觉障碍、手脚畸形、神经传导速度减慢和洋葱样改变。PMP22髓鞘磷脂是一种跨膜糖蛋白组成部分,所以对维持髓鞘结构的完整性、调节细胞周期等很重要。从遗传学角度来说,CMT大多是常染色体显性遗传,少数是常染色体隐性遗传、X-性连锁显性遗传、X-性连锁隐性遗传[3]。本研究中我们在郑州大学人民医院神经内科收集两个家系患者,从基因检测方面确诊两个CMT1A常染色体显性遗传的家系,具体介绍如下。
1 研究对象及方法 1.1 研究对象两个家系均来自河南省,无外地居住史,无糖尿病等可能会加重CMT症状的神经病变。所有研究者的纳入标准参考Dyck1993[4]。本研究经郑州大学医学伦理委员会批准,受试者本人或监护人知情并同意。
1.1.1 家系一家系一中4代共4例发病者,发病年龄17~48岁不等,病程缓慢,主要表现为四肢远端感觉减退,呈手套-袜套样,程度及范围逐渐加重,且伴双下肢无力,蹲下后难站起,平素易疲劳,有弓形足畸形。所有患者均未见明显的肌肉萎缩,这与国内外文献报道有一定差异。体格检查:所有患者均有双下肢腱反射消失或减弱,双上肢腱反射对称存在,伴有弓形足等足部畸形,余未见明显的阳性体征。
患者Ⅱ5(先证者):现48岁,1月余前无明显诱因出现右侧足底麻木,1周后左足出现麻木,双足麻木程度及范围逐渐加重,3~4天后合并有双手指端麻木,呈手套-袜套样,且患者自觉双下肢无力,常表现为蹲下后不能站立需要他人扶起,咳嗽或站立时感双手麻木加重,且偶伴有前胸部及背部麻木,平素易疲劳,四肢无疼痛,无肌肉萎缩,无自主神经功能障碍,行血、尿、粪常规、血清肌酸激酶、头颅磁共振检查均无明显异常。
患者Ⅱ7: 45岁发病,主要表现为四肢远端麻木伴双下肢进行性无力,且出现不同程度的弓形足畸形。
患者Ⅲ11:现20岁,发病年龄17岁,主要表现为双下肢麻木,弓形足,行走呈“跨阈步态”,跑步困难,易被绊倒,18岁时行弓形足矫正手术,效果尚可,易被绊倒的现象明显减少,其余症状也稍有减轻。
患者Ⅰ1:自幼弓形足,43岁时出现四肢远端麻木,家属自述72岁时故于急性心肌梗死。
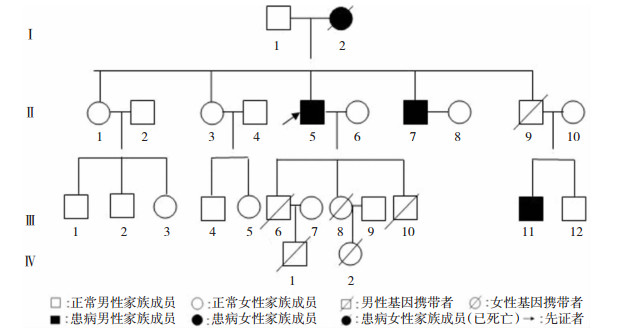
|
| 图 1 家系一 |
家系二中4代共5例发病者,患者Ⅱ9(先证者)现52岁,30岁时出现行走不稳,逐渐加重,行走时垂足(上下楼梯更明显),呈跨阈步态,伴有弓形足;双下肢自觉无力,表现为上楼梯需扶扶手,情绪激动紧张时无法站立;无肌肉萎缩、无肢体感觉障碍、无自主神经功能障碍。
患者Ⅱ3:现62岁,40岁逐渐出现行走不稳,现已无法行走,长期卧床,生活质量严重下降。
患者Ⅱ11和Ⅲ7:自幼有弓形足,上下楼梯时呈跨阈步态,体育较差,平素易疲劳。
患者Ⅰ1:自幼有弓形足,现已故,死因不详。
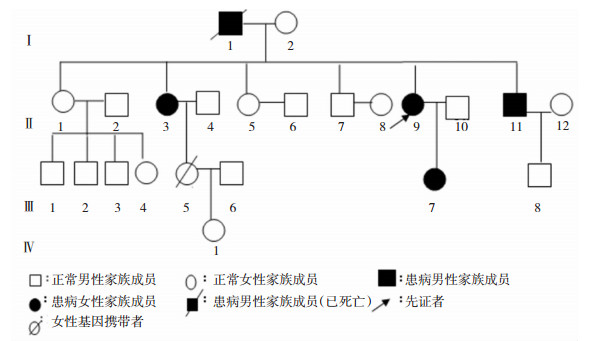
|
| 图 2 家系二 |
采集两家系21名成员和50名健康人的外周血各5 ml,收集在乙二胺四乙酸(EDTA)-K2抗凝试管,应用血液基因组DNA提取试剂盒提取基因组DNA,存入-20度冰箱,且用分光光度计检测DNA的浓度。
1.3 PCR-双酶切法检测PMP22基因引物由生工生物工程(上海)股份有限公司合成。引物设计原理详见参考文献[Kon-Ping Lin, 2006][5],引物名称分别是Hot-F1、Hot-R1、Hot-F2、Hot-R 2,序列分别为5’-TTGGATTCAAAGATATTAGTGTTAT-3’;5’-TAGTAGAGCTCACTCTACAG--3’;5’-TTGGATTCACAGAGACATTAGTTAC--3’;5’-TAGTAGAGTGAGTACAGTGGAC-3。PCR反应体系中分别加入DNA5 μL、2XGC Buffer I 25 μL、dNTPs 4 μL(2.5 mmol/L)、TaqDNA多聚酶0.4 μL(5 U/μL)、Hot-F1和Hot-R2各2.5 μL,加灭菌水至50μL体系。94℃预变性3 min后,进入循环。循环参数:.94℃变性30 s,56℃退火60 s,30个循环后72℃延伸5 min。取PCR产物进行DNA纯化,取纯化后的产物10 μL,分别加EcoR I 0.5 μL、Nsi I 1 μL、buffer 3.1 2.5 μL、灭菌水6 μL,37 ℃水浴酶切过夜,80℃失活3 min。1.5%(体积分数)琼脂糖凝胶电泳,GoldView I型核酸染色剂染色,存入凝胶成像分析系统。参照DNA 2000 bp Marker相对分子质量标准,1760 bp条带为特异性酶切片段,有此片段诊断为基因重复。
2 结果 2.1 临床资料分析家系一中临床表现主要以四肢远端肢体感觉障碍为主,家系二中主要以行走不稳,呈“跨阈步态”为主,所有患者均未见常见的双下肢肌肉萎缩(呈“鹤腿”或“香槟腿”)。
2.2 遗传分子学分析由图 3可见,所有被研究者均经等位基因特异性PCR-双酶切方法检测,其中14名成员有PMP22基因的重复突变(即1760bp片段),其7名患病者(家系一Ⅱ5、Ⅱ7、Ⅲ11,家系二Ⅱ3、Ⅱ9、Ⅱ11、Ⅲ7),其基因携带者有7名(家系一中Ⅱ9、Ⅲ6、Ⅲ8、Ⅲ10、Ⅳ1、Ⅳ2,家系二中Ⅲ5)。
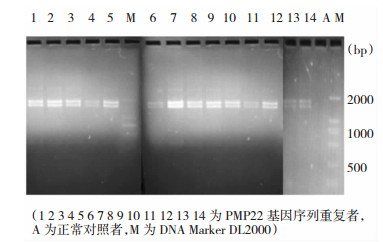
|
| 图 3 等位基因特异性PCR-双酶切方法检测出的PMP22基因的重复突变 |
该研究中7例患者双侧上肢正中神经和尺神经传导速度均 < 38 m/s(平均16 m/s)、感觉神经传导速度均无波形,上下肢被检肌肉均有纤颤电位、正锐波,提示重度神经源性损害;7例基因携带者双侧正中神经的运动神经传导速度 < 38 m/s(平均28 m/s)、感觉神经传导速度均无波形,被检肌肉未见明显异常;研究中7例健康人的神经传导和肌电图均未见明显异常。所有患者均未行神经肌肉活检。
3 讨论CMT是一组常见的具有高度临床和遗传异质性的周围神经单基因遗传病,发病年龄大部分在儿童期或青春期,小部分在成年时发病[6],基本上不影响患者的寿命。该两家系中明确有4例患者发病年龄均在30岁以后,另外5例患者幼时发病,其中2例已故,未采集到血液样品而无法进行PMP22基因验证。这可能是由于本研究的样本量偏少或者是该家系的个体差异。根据CMT致病基因的不同,分成CMT1A、CMT1B、CMT1C、CMT1D、CMT1F共5种亚型[9]。其中CMT1A型病程进展缓慢,通常在20~30年,且下肢的症状比上肢出现得早[7]。常见的临床特征是进行性、对称性肢体远端无力和肌肉萎缩,而家系一中患者主要表现为双下肢远端麻木伴进行性无力,逐渐蔓延至双上肢,远端肢体感觉减退,家系二患者主要以行走不稳,呈“跨阈步态”为主,两家系中患者均出现弓形足畸形,但均无明显的四肢肌肉萎缩,下肢腱反射均消失或减弱,该研究的患者今后是否出现四肢肌肉萎缩,还需我们长期的随访。Colomban等[8]研究表明临床症状是有性别差异的,女性比男性更易残疾,更易出现首发的临床表现,生活质量更差。本研究家系二中女性比男性发病早且严重,这与上诉文献报道相符合,但家系一中临床症状男性比女性出现得早且严重,这不相符合,可能是本研究的样本量偏少,存在一定的差异,也可能是该家系临床特殊性及异质性。曾有报道表明在CMT1A患者中可合并心脏功能异常、自主神经功能障碍、脊柱侧凸、震颤、腕管综合征、呼吸睡眠暂停综合征、腿部溃疡和轻至中度听力下降等不太常见临床特征,而家系一中Ⅰ1患者家属自诉死于心肌梗死,由于未取得相关临床检查资料及血液样品,无法明确两者之间是否存在相关性。
在本研究中7例患者(家系一Ⅱ5、Ⅱ7、Ⅲ11,家系二Ⅱ3、Ⅱ9、Ⅱ11、Ⅲ7)双侧上肢正中神经和尺神经传导速度均 < 38 m/s(平均16 m/s)、感觉神经传导速度均无波形,而7例基因携带者双侧正中神经的运动神经传导速度 < 38 m/s (平均28 m/s)、感觉神经传导速度均无波形。上述的神经电生理结果均符合CMT1A型典型特征,且与基因突变分析结果完全相符,是发现携带有PMP22基因重复突变、尚未出现临床症状的儿童和无临床症状病人的可靠手段。其中Ⅱ9基因携带者具有CMT1A特征性电生理改变,可能轻微的临床表现我们尚且未发现,这与之子(Ⅲ11)患病是符合常染色体显性遗传方式。
在本研究中所有患者均未进行肌肉神经病理检查,所以初步诊断是根据电生理特点分型考虑为CMT1型,其CMT1A、CMT1B、CMT1C、CMT1D和CMT1F亚型的致病基因分别为PMP22、MPZ、LITAF、EGR2和NEFL,两个家系中先证者分别先进行上述基因点突变筛查,结果未发现异常,又进行PMP22基因重复片段的筛查,结果发现患者有PMP22基因重复突变(即1760bp片段),随后剩余19名成员进行该基因筛查。本研究中检测到14名成员有PMP22基因的重复突变,其中7名为患病者,另7名为基因携带者,余7名成员及50名健康人均未发现异常重复片段。目前已证实CMT1的交换热点位于30 kb的CMT1A-REP上1.7 kb的区域,并且75%以上的CMT1患者交换热点位于该区域;对断裂点设计特定的引物经行扩增酶切获得特异性酶切片段即可诊断为基因重复异常[10, 11]。
目前,CMT1A暂无标准的治疗方法,大剂量的维生素C等内科治疗、物理疗法和纠正畸形的外科手术都在研究中,其中维生素C[11]、姜黄素[12]、神经因子3[13]和最近的P18 P2X7嘌呤受体拮抗剂[14]都在小鼠模型和培养的施万细胞中证实有效,但是这些药的有效作用在人类的研究中还未确定[15],需要更进一步的探究。利用矫形器来辅助步行及预防畸形现已常用于临床中,对于考虑外科手术治疗的CMT1A患者时间很重要,因为早期轻微的畸形比晚期严重的更易纠正,而有早期轻微的畸形的患者在临床上是易被漏诊,故早期基因的诊断有无可取代的地位[16]。对有家族史的患者进行基因诊断有重大意义,相比其他检查发现早,准确性高,携带者可及时进行早期的预防,提高他们未来的生活质量。
| [1] | Braathen GJ. Genetic epidemiology of Charcot-Marie-Tooth disease. Acta Neurol Scand Suppl , 2012 (193) : iv–22. |
| [2] | Rossor AM, Polke JM, Houlden H, et al. Clinical implications of genetic advances in Charcot-Marie-Tooth disease. Nat Rev Neurol , 2013, 9 (10) : 562–571. DOI:10.1038/nrneurol.2013.179 |
| [3] | Shin JS, Chung KW, Cho SY, et al. NEFL Pro22Arg mutation in Charcot-Marie-Tooth disease type 1. J Hum Genet , 2008, 53 (10) : 936–940. DOI:10.1007/s10038-008-0333-8 |
| [4] | Dyck PJ, Chance P, Lebo R. Here ditary motor and sensory neuropathy.Philadephia: WB Saunders, 1993, 1094–1132. |
| [5] | Lin KP, Chou CH, Lee HY, et al. Allele-specific all-or-none PCR product diagnostic strategy for Charcot-Marie-Tooth 1A and hereditary neuropathy with liability to pressure palsies. J Chin Med Assoc , 2006, 69 (2) : 68–73. DOI:10.1016/S1726-4901(09)70116-9 |
| [6] | Jani-Acsadi A, Krajewski K, Shy ME. Charcot-Marie-Tooth neuropathies:diagnosis and management. Semin Neurol , 2008, 28 (2) : 185–194. DOI:10.1055/s-2008-1062264 |
| [7] | Colomban C, Micallef J, Lefebvre MN, et al. Clinical spectrum and gender differences in a large cohort of Charcot-Marie-Tooth type 1A patients. J Neurol Sci , 2014, 336 (1-2) : 155–160. DOI:10.1016/j.jns.2013.10.029 |
| [8] | Al-Thihli K, Rudkin T, Carson N, et al. Compound heterozygous deletions of PMP22 causing severe Charcot-Marie-Tooth disease of the Dejerine-Sottas disease phenotype. Am J Med Genet A , 2008, 146A (18) : 2412–2416. DOI:10.1002/ajmg.a.v146a:18 |
| [9] | Vital A, Latour P, Sole G, et al. A French family with Charcot-Marie-Tooth disease related to simultaneous heterozygous MFN2 and GDAP1 mutations. Neuromuscul Disord , 2012, 22 (8) : 735–741. DOI:10.1016/j.nmd.2012.04.001 |
| [10] | Jones EA, Brewer MH, Srinivasan R, et al. Distal enhancers upstream of the Charcot-Marie-Tooth type 1A disease gene PMP22. Hum Mol Genet , 2012, 21 (7) : 1581–1591. DOI:10.1093/hmg/ddr595 |
| [11] | Kaya F, Belin S, Bourgeois P, et al. Ascorbic acid inhibits PMP22 expression by reducing cAMP levels. Neuromuscul Disord , 2007, 17 (3) : 248–253. DOI:10.1016/j.nmd.2006.12.008 |
| [12] | Khajavi M, Shiga K, Wiszniewski W, et al. Oral curcumin mitigates the clinical and neuropathologic phenotype of the Trembler-J mouse:a potential therapy for inherited neuropathy. Am J Hum Genet , 2007, 81 (3) : 438–453. DOI:10.1086/519926 |
| [13] | Pleasure DE, Chance PF. Neurotrophin-3 therapy for Charcot-Marie-Tooth disease type 1A. Neurology , 2005, 65 (5) : 662–663. DOI:10.1212/01.wnl.0000179404.82539.d7 |
| [14] | Nobbio L, Visigalli D, Mannino E, et al. The didanosine homodinucleotide P18 improves invitro myelination in experimental Charcot-Marie-Tooth disease type 1A. J Cell Biochem , 2014, 115 (1) : 161–167. DOI:10.1002/jcb.v115.1 |
| [15] | Reilly MM, de Jonghe P, Pareyson D. 136th ENMC International Workshop:Charcot-Marie-Tooth disease type 1A (CMT1A) 8-10 April 2005, Naarden, The Netherlands. Neuromuscul Disord , 2006, 16 (6) : 396–402. DOI:10.1016/j.nmd.2006.03.008 |
| [16] | Hui-Chou HG, Hashemi SS, Hoke A, et al. Clinica implications of peripheral myelin protein 22 for nerve compression and neural regeneration:a review. J Reconstr Microsurg , 2011, 27 (1) : 67–74. DOI:10.1055/s-0030-1267832 |
 2016, Vol. 43
2016, Vol. 43




