扩展功能
文章信息
- 解媛媛, 肖波
- XIE Yuan-Yuan, XIAO Bo
- 中国汉族人群SLC6A11基因多态性与耐药性癫痫的相关性研究
- Association between SLC6A11 gene polymorphisms and drug-resistant epilepsy in Chinese Han population
- 国际神经病学神经外科学杂志, 2016, 43(3): 219-223
- Journal of International Neurology and Neurosurgery, 2016, 43(3): 219-223
-
文章历史
收稿日期: 2016-04-18
修回日期: 2016-06-22
癫痫是最常见而且严重的慢性神经系统疾病之一,目前中国大约有9000癫痫患者[1, 2]。目前主要的治疗手段是服用抗癫痫药物。尽管近年来新的抗癫痫药物在癫痫治疗方面已取得长足的进步,但迄今仍有大约30%的癫痫患者对抗癫痫药物耐药[3]。耐药性癫痫的机制目前尚未完全明确,有研究表明抗癫痫药物与靶点的敏感性和亲和力的改变有关[4]。抗癫痫药物的靶点包括钠、钙、钾离子等通道和神经递质受体,转运体等[5]。GABA是中枢神经系统中最主要的抑制性神经递质,在神经网络的兴奋性调节中起关键作用,与癫痫的发生发展密切相关。GABA转运体(GAT)是一种主要存在于神经元和神经胶质细胞膜上的糖蛋白,参与GABA在中枢神经系统的转运与释放过程[6]。GAT3是主要的GABA转运体,主要表达与哺乳动物的星型胶质细胞[7]。一项在韩国人群中的研究发现,编码GAT3的SLC6A11基因与癫痫耐药性之间存在关联性[8]。而在中国汉族人群中SLC6A11基因与癫痫耐药性之间的关系尚无相关研究报道。因此本研究拟探索中国汉族人群SLC6A11基因多态性与耐药性癫痫的相关性。
1 材料和方法 1.1 研究对象所有病例选自2010年5月~2012年10月期间中南大学湘雅医院神经内科门诊癫痫患者,均为无血缘关系的汉族人群。本研究得到中南大学湘雅医院伦理委员会的批准,所有受试者在实验前签署知情同意书。每例患者详细记录基本信息、临床发作情况、药物使用情况、药物不良反应、个人史、既往史、家族史,并进行详细体格检查,记录MRI、脑电图等辅助检查结果。
耐药性癫痫组纳入标准(2010年国际抗癫痫联盟[9]):应用足量足疗程的两种或两种以上合理的抗癫痫药物治疗,癫痫发作仍未能完全控制的患者。
药物敏感组癫痫纳入标准:合理应用抗癫痫药物治疗,依据最近12个月内癫痫发作的最长间隔,3倍最长发作间隔(≥12月)无癫痫发作患者。
排除标准:①有酒精相关性癫痫病史,或服用抗肿瘤药物、细胞毒性药物、类固醇化合物等;②患者依从性欠佳,严重的癫痫药物不良反应,肿瘤、外伤、血管畸形、脑血管病、感染、中毒、寄生虫等引起的癫痫及假性发作;③患有严重器质性病变,如高血压、心脏病、血液病、肝肾功能不全;④有进行性疾病、变性疾病、先天性代谢异常疾病或中枢神经系统疾病者。
每位受试者抽取肘静脉血5 mL置于EDTA抗凝管中,用苯酚-氯仿萃取法提取全基因组DNA。
1.2 单核苷酸多态性选择和基因分型从Hapmap数据库中选取14个SLC6A11基因的单核苷酸多态性(single nucleotide polymorphism,SNP):122.2 kilo-base pairs [kbp],HapMap Data Rel 24/phase II Nov08,on NCBI B36 asembly dbSNP b126。
SLC6A11基因候选SNP位点的选择基于以下标准:①最小等位基因频率(MAF)≥10%;②采用Haploview软件(version 4.2)选择SNP,连锁参数(pair-wise r2) r2≥0.8;③对于文献已有报道,在启动子区、外显子区、3’-非编码区具有潜在的功能性突变位点我们亦将其纳入目标SNP;④美国Illumina公司SNP位点评分尽量大于0.6。
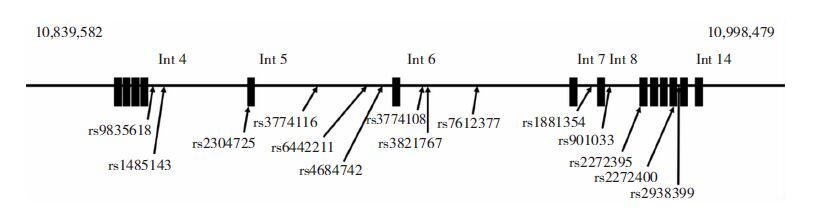
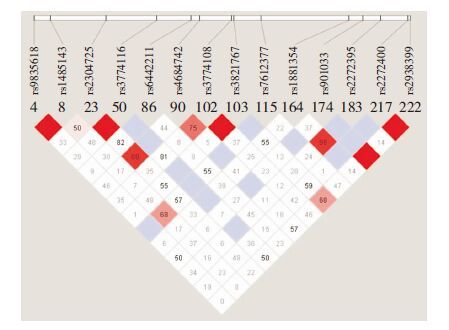
人群的基因分布频率均符合Hardy-Weinberg平衡,目标SNP的基本参数和特征见表 1和图 1。SLC6A11基因的候选SNP的连锁情况如图 2所示。对研究对象应用Illumina Golden Gate定制芯片对所选的SNP进行基因型鉴定。
| SNPs | 等位基因 | 最小等位基因频率(%) | 功能 | 评分 |
| rs2304725 | C/ T | 48 | Synonymous-codon | 0.598 |
| rs2272395 | C/ T | 13 | Synonymous-codon | 0.572 |
| rs2272400 | T/ C | 13 | Synonymous-codon | 0.682 |
| rs3774116 | G/ A | 16 | Intron | 0.877 |
| rs9835618 | G/ T | 34 | Intron | 0.95 |
| rs7612377 | A/ G | 29 | Intron | 0.974 |
| rs901033 | T/ C | 17 | Intron | 0.919 |
| rs4684742 | A/ G | 32 | Intron | 0.935 |
| rs6442211 | T/ C | 23 | Intron | 0.831 |
| rs3821767 | A/ G | 30 | Intron | 1.1 |
| rs3774108 | G/ T | 44 | Intron | 0.907 |
| rs2938399 | T/ C | 49 | Intron | 0.808 |
| rs1881354 | G/ A | 33 | Intron | 0.625 |
| rs1485143 | A/ T | 41 | Intron | 0.925 |
|
| 图 1 SLC6A11基因候选SNPs示意图 |
|
| 图 2 SLC6A11基因SNPs的连锁情况 |
应用SPSS软件包(Ver 21.0,SPSS Inc.,Chicago,IL)进行数据分析。计量资料均以均数±标准差(x±s) 表示。计数资料均以例数(相对百分数)表示。Hardy-Weinberg平衡使用卡方检验分析或者Fisher’s exact test;在耐药组与反应组中年龄比较用Student’s t-test。性别和其他特征资料比较用χ2检验。对年龄,性别和发作类型进行校正后,各种基因型与药物反应之间关系用二元logistic回归分析。连锁不平衡和单倍型分析用SHEsis软件 (http://analysis.bio-x.cn/myAnalysis.php)[10, 11]。P<0.05为差异有统计学意义。
2 结果 2.1 人口统计学信息及临床资料本研究共纳入了480个癫痫患者,均为汉族人群。其中敏感组288人,平均年龄(23.3±13.4)岁;耐药组192人,平均年龄(24.1±13.4)岁。两组之间的年龄、性别、发作类型没有统计学差异,说明两组人群配对良好。见表 2。
| 特征 | 敏感组(n=288) | 耐药组(n=192) | 总计(n=480) | P值 |
| 年龄(年) | 23.3±13.4 | 24.1±13.4 | -23.6±13.4 | 0.574 |
| 男性 | 176(61.1) | 125(65.1) | 301(62.7) | 0.672 |
| 抗癫痫药物使用[n(%)] | ||||
| 卡马西平 | 96(35.2) | 62(30.0) | 158(32.9) | |
| 丙戊酸 | 75(27.5) | 130(62.8) | 205(42.7) | |
| 奥卡西平 | 92(33.7) | 95(45.9) | 187(39.0) | |
| 拉莫三嗪 | 49(17.9) | 73(35.3) | 122(25.4) | |
| 左乙拉西坦 | 27(9.9) | 37(17.9) | 64(13.3) | |
| 托吡酯 | 25(9.2) | 13(6.3) | 38(7.9) | |
| 苯妥英钠 | 20(7.3) | 51(24.6) | 71(14.8) | |
| 苯巴比妥 | 18(6.6) | 22(10.6) | 40(8.3) |
纳入研究的288个抗癫痫药物反应患者与192个抗癫痫药物耐受患者中,通过对所选的14个SNP进行基因分型,我们所研究的14个位点多态分布在癫痫病人人群中均符合Hardy-Weinberg平衡,SLC6A11基因的14个SNP位点均与耐药无明显相关(P>0.05)。见表 3。
| SNP | 敏感组(n=288) | 耐药组(n=192) | OR值 | P值 | |
| rs6442211 | AA | 7(0.024) | 4(0.021) | ||
| GA | 112(0.390) | 57(0.297) | 0.212-1.142 | 0.877 | |
| GG | 168(0.585) | 130(0.677) | 0.298-1.688 | 0.554 | |
| G | 448 | 317 | |||
| A | 126 | 65 | 0.062 | ||
| rs7612377 | AA | 13(0.045) | 11(0.057) | ||
| GA | 138(0.479) | 108(0.562) | 0.332-2.682 | 0.913 | |
| GG | 137(0.476) | 73(0.380) | 0.222-2.615 | 0.666 | |
| G | 412 | 254 | |||
| A | 164 | 130 | 0.076 | ||
| rs1881354 | TT | 93(0.323) | 70(0.365) | ||
| TC | 146(0.507) | 95(0.495) | 0.598-1.843 | 0.865 | |
| CC | 49(0.170) | 27(0.141) | 0.6629~1.1228 | 0.959 | |
| T | 332 | 235 | |||
| C | 244 | 149 | 0.2719 | ||
| rs2304725 | TT | 145(0.503) | 89(0.464) | ||
| TC | 105(0.365) | 73(0.380) | 0.672-1.702 | 0.778 | |
| CC | 38(0.132) | 30(0.156) | 0.526-2.244 | 0.823 | |
| T | 395 | 251 | |||
| C | 181 | 133 | 1.1038~1.8927 | 0.299 | |
| rs2272395 | TT | 194(0.688) | 120(0.628) | ||
| TC | 85(0.301) | 69(0.361) | 0.592-1.752 | 0.947 | |
| CC | 3(0.011) | 2(0.010) | 0.086-4.827 | 0.669 | |
| T | 473 | 309 | |||
| C | 91 | 73 | 0.8743-1.7247 | 0.2356 | |
| rs2272400 | AA | 66(0.230) | 40(0.208) | ||
| GA | 61(0.213) | 52(0.271) | 0.991-3.796 | 0.053 | |
| GG | 160(0.557) | 100(0.521) | 0.856-3.052 | 0.139 | |
| G | 381 | 252 | |||
| A | 193 | 132 | 0.8098 | ||
| rs901033 | AA | 4(0.014) | 3(0.016) | ||
| GA | 98(0.340) | 53(0.277) | 0.171-5.228 | 0.948 | |
| GG | 186(0.646) | 135(0.707) | 0.212-7.209 | 0.813 | |
| G | 470 | 323 | |||
| A | 106 | 59 | 0.235 | ||
| rs2938399 | TT | 91(0.316) | 77(0.405) | ||
| TC | 152(0.528) | 81(0.426) | 0.329-0.931 | 0.066 | |
| CC | 45(0.156) | 32(0.168) | 0.385-1.766 | 0.620 | |
| T | 334 | 235 | |||
| C | 242 | 145 | 0.235 | ||
| rs4684742 | TT | 33(0.115) | 21(0.109) | ||
| TC | 151(0.528) | 81(0.424) | 0.330-1.789 | 0.541 | |
| CC | 102(0.357) | 89(0.464) | 0.339-3.131 | 0.833 | |
| T | 217 | 123 | |||
| C | 355 | 259 | 0.07 | ||
| rs3821767 | TT | 39(0.136) | 25(0.131) | ||
| TC | 114(0.399) | 67(0.351) | 0.404-1.545 | 0.492 | |
| CC | 133(0.465) | 99(0.518) | 0.477-1.946 | 0.917 | |
| T | 192 | 117 | |||
| C | 380 | 265 | 0.342 | ||
| rs9835618 | AA | 133(0.463) | 102(0.534) | ||
| CA | 141(0.491) | 74(0.387) | 0.396-1.001 | 0.050 | |
| CC | 13(0.045) | 15(0.079) | 0.536-3.970 | 0.460 | |
| C | 167 | 104 | |||
| A | 407 | 278 | 0.5300 | ||
| rs3774108 | TT | 95(0.330) | 43(0.224) | ||
| TG | 144(0.500) | 111(0.578) | 0.999-3.248 | 0.050 | |
| GG | 49(0.170) | 38(0.198) | 0.477-2.748 | 0.761 | |
| T | 334 | 197 | |||
| G | 242 | 187 | 0.0413 | ||
| rs3774116 | AA | 217(0.753) | 135(0.703) | ||
| GA | 67(0.233) | 50(0.260) | 0.584-2.307 | 0.670 | |
| GG | 4(0.014) | 7(0.036) | 0.349-10.592 | 0.453 | |
| G | 75 | 64 | |||
| A | 501 | 320 | 0.1158 | ||
| rs1485143 | AA | 146(0.507) | 91(0.476) | ||
| TA | 114(0.396) | 86(0.450) | 0.682-1.760 | 0.706 | |
| TT | 28(0.097) | 14(0.073) | 0.218-1.313 | 0.172 | |
| T | 170 | 114 | |||
| A | 406 | 268 | 0.913 |
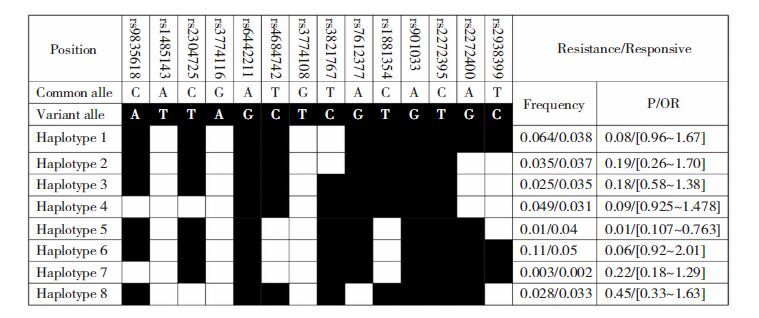
在单体型分析中,我们发现单体型5在耐药性癫痫中的频率明显低于敏感组(1% vs. 4%; OR=2.56 [0.107-0.763]; P=0.01)(图 3)。然而,经过Bonferroni多重分析后,发现单体型5和耐药性癫痫无明显相关性(P>0.05/8)。
|
| 图 3 敏感组和耐药组癫痫患者SLC6A11基因SNP单体型频率 |
癫痫是最常见而严重的神经系统疾病之一,目前临床上主要应用抗癫痫药物来控制发作。尽管近年来有不同作用机制的新药相继上市,但仍有20%~30%的患者对这些药物不敏感或耐药,发作得不到有效控制[12]。耐药性癫痫的治疗手段十分有限,如生酮饮食会给患者带来不适,且依从性差[13]。药物基因组学研究发现药物的疗效与基因密切相关。用药物基因组学方法找出基因多态性在个体和群体对抗癫痫药物反应差异中的规律,为基因指导的药物治疗和个体化治疗提供科学依据,具有重要的临床意义[14, 15]。
GAT是位于神经元和胶质细胞上的重要糖蛋白,是突触间隙和细胞外液的GABA清除的唯一途径。通过抑制GAT可减慢GABA的重摄取过程,延长GABA能信号的持续时间。GABA被重摄取后的命运取决于被什么细胞摄取,被星形胶质细胞摄取的GABA多数被降解,被神经元摄取的GABA则更可能会被重新利用成为神经递质[16]。最近一项研究表明,抑制星形胶质细胞对GABA重摄取能有效抑制痫性放电,而抑制神经元对GABA的摄取则没明显作用[17]。这一研究提示星形胶质细胞对GABA的重摄取在GABA能神经元的活动中起重要作用。2011年韩国学者Kim等[8]首次研究了编码GAT3的SLC6A11基因多态性对抗癫痫药物疗效的影响。结果发现位于SLC6A11的12号外显子上rs2272400位点如果带有T等位基因,则该患者对抗癫痫药物产生耐药性的风险至少增加1.5倍。然而rs2272400的C等位基因与T等位基因编码的氨基酸相同,属于同义突变,Kim等[8]认为其可能通过改变启动子活性影响基因的结构和功能。基于Kim等[8]的研究结果,本实验首次在中国汉族人群中对SLC6A11基因多态性与耐药性癫痫的相关性进行了研究,结果发现在耐药癫痫组中rs2272400位点的TT和CT等位基因的频率(35.7%)要高于敏感组(31.5%),这和Kim等[8]的研究结果一致,但是通过统计学分析显示该SNP基因型分布在两组间无差异。因此,我们没能发现SLC6A11基因多态性与中国汉族人群耐药性癫痫之间的关联性。我们的结果提示SLC6A11基因多态性可能与中国汉族人群耐药性癫痫无关。
癫痫是一种复杂的神经系统疾病,其产生耐药的机制也复杂多样,SLC6A11基因可能仅参与耐药性癫痫的一部分机制,为了能在统计学上检验出这些因素,还需进一步增加实验的样本量。而且SLC6A1基因参与癫痫耐药的具体机制仍不十分清楚,它们可能与一些特殊类型的癫痫有更密切相关,因此,今后还可对不同类型的癫痫进行研究。
| [1] | Cavalleri GL, Mccormack M, Alhusaini S, et al. Pharmacogenomics and epilepsy:the road ahead. Pharmacogenomics , 2016, 12 (10) : 1429–1447. |
| [2] | Wang WZ, Wu JZ, Wang DS, et al. The prevalence and treatment gap in epilepsy in China an ILAE/IBE/WHO study. Neurology , 2003, 60 (9) : 1544–1545. DOI:10.1212/01.WNL.0000059867.35547.DE |
| [3] | Fisher RS, Boas WVE, Blume W, et al. Epileptic seizures and epilepsy:definitions proposed by the International League Against Epilepsy (ILAE) and the International Bureau for Epilepsy (IBE). Epilepsia , 2005, 46 (4) : 470–472. DOI:10.1111/epi.2005.46.issue-4 |
| [4] | Kwan P, Schachter SC, Brodie MJ. Drug-resistant epilepsy. N Engl J Med , 2011, 365 (10) : 919–926. DOI:10.1056/NEJMra1004418 |
| [5] | Meldrum BS, Rogawski MA. Molecular targets for antiepileptic drug development. Neurotherapeutics , 2007, 4 (1) : 18–61. DOI:10.1016/j.nurt.2006.11.010 |
| [6] | Madsen KK, White HS, Schousboe A. Neuronal and non-neuronal GABA transporters as targets for antiepileptic drugs. Pharmacol Therap , 2010, 125 (3) : 394–401. DOI:10.1016/j.pharmthera.2009.11.007 |
| [7] | De Biasi S, Vitellaro-Zuccarello L, Brecha NC. Immunoreactivity for the GABA transporter-1 and GABA transporter-3 is restricted to astrocytes in the rat thalamus. A light and electron-microscopic immunolocalization. Neuroscience , 1998, 83 (3) : 815–828. DOI:10.1016/S0306-4522(97)00414-4 |
| [8] | Kim DU, Kim MK, Cho YW, et al. Association of a synonymous GAT3 polymorphism with antiepileptic drug pharmacoresistance. J Hum Genet , 2011, 56 (9) : 640–646. DOI:10.1038/jhg.2011.73 |
| [9] | Kwan P, Arzimanoglou A, Berg AT, et al. Definition of drug resistant epilepsy:consensus proposal by the ad hoc Task Force of the ILAE Commission on Therapeutic Strategies. Epilepsia , 2010, 51 (6) : 1069–1077. |
| [10] | Shi YY, He L. Shesis, a powerful software platform for analyses of linkage disequilibrium, haplotype construction, and genetic association at polymorphism loci. Cell Res , 2005, 15 (2) : 97–98. DOI:10.1038/sj.cr.7290272 |
| [11] | Li Z, Zhang Z, He Z, et al. A partition-ligation-combination-subdivision EM algorithm for haplotype inference with multiallelic markers:update of the SHEsis (http://analysis.bio-x.cn). Cell Res , 2009, 19 (4) : 519–523. DOI:10.1038/cr.2009.33 |
| [12] | Rogawski MA, Löscher W. The neurobiology of antiepileptic drugs. Nature Reviews Neuroscience , 2004, 5 (7) : 553–564. DOI:10.1038/nrn1430 |
| [13] | Lee E, Kang HC, Kim HD. Ketogenic Diet for Children with Epilepsy:A Practical Meal Plan in a Hospital, 2016, 5(1):60-63. |
| [14] | Cavalleri GL, McCormack M., Alhusaini S, et al. Pharmacogenomics and epilepsy:the road ahead. Pharmacogenomics , 2011, 12 (10) : 1429–1447. DOI:10.2217/pgs.11.85 |
| [15] | 冯海燕, 李筱瑜, 郑乃智. 药物基因组学在难治性癫痫早期诊断和治疗中的应用进展. 国际神经病学神经外科学杂志 , 2014, 41 (3) : 265–268. |
| [16] | Schousboe A, Sarup A, Bak LK, et al. Role of astrocytic transport processes in glutamatergic and GABAergic neurotransmission. Neurochem Int , 2004, 45 (4) : 521–527. DOI:10.1016/j.neuint.2003.11.001 |
| [17] | Galvan A, Villalba RM, West SM., et al. GABAergic modulation of the activity of globus pallidus neurons in primates:in vivo analysis of the functions of GABA receptors and GABA transporters. J Neurophysiol , 2005, 94 (2) : 990–1000. DOI:10.1152/jn.00068.2005 |
 2016, Vol. 43
2016, Vol. 43




