扩展功能
文章信息
- 何双英, 许宏伟, 王爱民, 谭红, 唐红宇
- HE Shuang-Ying, XU Hong-Wei, WANG Ai-Min, TAN Hong, TANG Hong-Yu
- 载脂蛋白(a)基因增强子DHⅢ多态性与湖南地区汉族人群动脉粥样硬化血栓性脑梗死的相关性
- Association between polymorphism in apolipoprotein (a) gene enhancer (DHIII) and atherothrombotic cerebral infarction in Han population in Hunan Province, China
- 国际神经病学神经外科学杂志, 2015, 42(4): 329-332
- Disease Surveillance, 2015, 42(4): 329-332
-
文章历史
- 收稿日期: 2015-06-28
- 修回日期: 2015-08-20
2. 中南大学湘雅医院老年病科, 湖南省长沙市 410008
载脂蛋白(a)[Apolipoprotein (a),Apo(a)]基因的多态性是导致脂蛋白(a)[lipoprotein(a),LP(a)]水平变化的主要原因[1]。由于Lp(a)与动脉粥样硬化有关的各类疾病有紧密关系[2],因此,被国内外学者认为是与其它血脂代谢无关的脑卒中独立危险因素[3, 4]。以动脉粥样硬化性狭窄和斑块不稳定为病理基础的动脉粥样硬化血栓性脑梗死(atherothrombotic cerebral infarction,ATCI)是人群缺血性脑卒中的最常见类型,具有高发病率、高死亡率、高致残率和高复发率的特点,严重影响人类生存质量、危害健康[5]。
2003年Puckey等[6]发现DHⅢ增强子-1230G等位基因能将增强子功能放大2.5倍,成为影响Lp(a)的因素之一。迄今为止,对载脂蛋白(a)基因DHⅢ增强子-1230A/G多态性与ATCI 关系的研究国内外尚未见报道。本文应用聚合酶链式反应-限制性片段长度多态性技术及DNA序列测定法检测湖南地区汉族ATCI、正常人群的Apo(a)基因 DHⅢ增强子-1230A/G多态性,旨在探索Apo(a)增强子基因多态性与ATCI 的关系,为ATCI 的遗传易感性及其发病机制研究提供科学依据。
1 资料和方法 1. 1 研究对象 1.1.1 ATCI组共134例,其中男77例,女57例,平均年龄(59.19±10.52)岁。为2004年10月至2006年12月湘雅医院神经内科住院病人,祖籍为湖南地区,均为汉族,无血缘关系,符合全国第四届脑血管病学术会议修订的诊断标准,经头颅CT和/或MRI确诊的动脉粥样硬化血栓性脑梗死,不包括动脉炎、外伤、血液病、药物、肿瘤、脑血管畸形或动脉瘤所引起的脑梗死。排除梗死后出血,出血后梗死、肝肾疾病,自身免疫性疾病,服用雌激素者及妊娠者,半年内有过降脂治疗者及确诊为冠心病者。
1.1.2 对照组中南大学湘雅医院健康体检者共110例,祖籍湖南地区,均为汉族,无血缘关系,其中男56例,女54例,平均年龄57.27±7.86岁,排除有冠心病、脑血管病、心脑血管疾病家族史、肝肾疾病、血液病、自身免疫性疾病、妊娠、半年内有过降脂治疗者。
1. 2 研究方法 1. 2. 1 人基因组DNA样品的制备抽取研究对象外周静脉血4 ml,肝素抗凝,利用常规酚/氯仿抽提法提取DNA。
1. 2. 2 Apo(a)基因型检测扩增Apo(a)基因增强子-1230A/G的引物由Puckey等[6]提供,并用GCG软件作Blast确定其特异性高,引物序列为:上游为5’-GCTTGGCTGGGAAAACCTATT-3’,下游为5’-TGTTGGAATACCCAGCCGTG -3’。反应在PE4800型PCR仪(美国PE公司)上进行,反应条件为94℃预变性10 min,94℃变性30 s,51℃退火30 s,72℃延伸1 min,32个循环,最后72℃充分延伸10 min。RFLP分析过程:取8 μl经2%琼脂糖凝胶电泳验证为特异性好的Apo(a)增强子-1230A/G PCR产物,加入1 μl限制性内切酶BglⅡ、2 μl的10×Buffer及9 μl的ddH2O,配成20 μl的反应体系37℃酶切4 h。然后经2.5%琼脂糖凝胶电泳,用Eagle Eye II型凝胶图像分析处理系统观察电泳结果并确定基因型。DNA测序分析:取酶切结果显示为一条带、二条带、三条带的模版gDNA标本各10个,PCR扩增后进行DNA正反双向测序,测序结果在Genebank和SNP的数据库中进行比较分析。
1.2.3 血脂测定应用氧化酶法测定甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC);测定高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)先用沉淀剂沉淀,再用酶法测定上清液中的胆固醇;低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C),由公式(LDL-C)=(TC)-(HDL-C)-(TG/5)求出;免疫比浊法测定Lp(a)。
1.3 统计学方法所有资料在Dbase软件中建立数据库,采用SPSS 13.0软件进行统计分析。基因型频率和等位基因频率的差异用χ2检验或Fisher确切概率法。Lp(a)组间比较用Mann-Wheitney非参检验;其它计量资料两组比较采用t检验,两组以上比较采用方差分析。按Hardy-Weinberg平衡法检验样本的群体代表性。
2 结果 2.1 ATCI组和对照组的一般临床资料ATCI组和对照组在年龄、性别、体重指数、吸烟史、饮酒史无显著性差异(P>0.05),提示对照组与病例组具有可比性。见表 1。
组别 | 例数 (n) | 年龄 (岁) | 性别 (男/女) | 体重指数 (kg/m2) | 吸烟史 (%) | 饮酒史 (%) |
| ATCI组 | 134 | 59.19±10.52 | 77/57 | 23.07±2.18 | 32.2 | 13.4 |
| 对照组 | 110 | 57.27±7.86 | 56/54 | 22.66±2.74 | 27.3 | 10.1 |
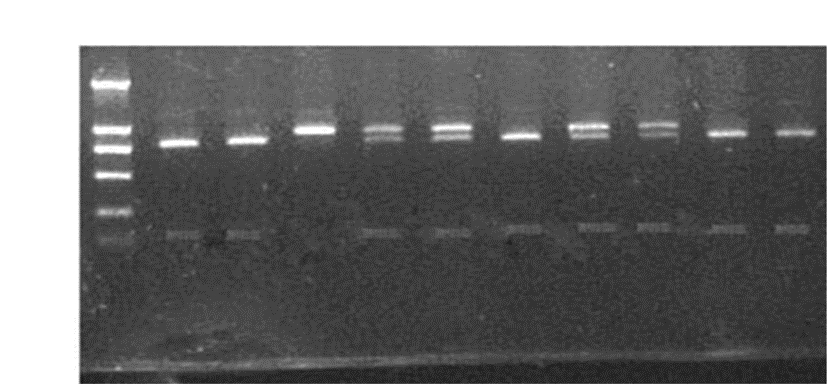
PCR-RFLP分析显示Apo(a) 基因 DHⅢ增强子-1230A/G有3种不同的基因型,分别为AA、GG、AG。见图 1、图 2、图 3。
|
| 图 1 Apo(a)DHⅢ增强子-1230A/G PCR产物酶切后电泳图。M:Marker;3:纯合子AA型;1、2、6、9、10:纯合子GG型;4、5、7、8:杂合子AG型。 |
|
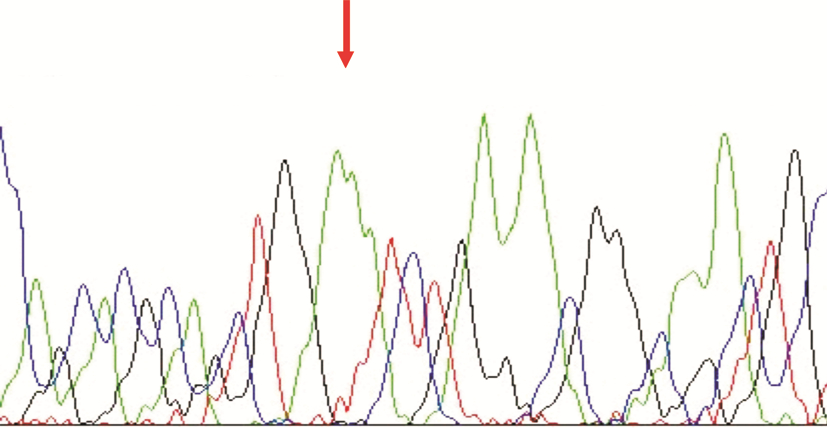
| 图 2 Apo(a)DHⅢ增强子-1230A等位基因测序图 |
|
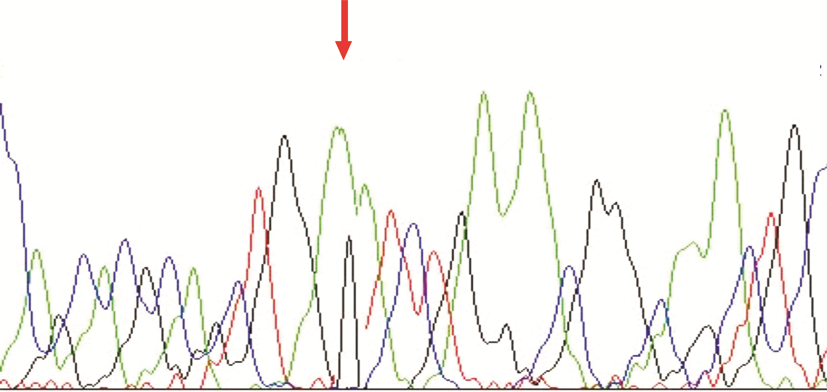
| 图 3 Apo(a)DHⅢ增强子-1230G等位基因测序图 |
对照组及ATCI组基因型及等位基因频率分布均符合Hardy-Weinberg平衡检验(P>0.05),表明来自同一人群达到遗传平衡。
2.4 Apo(a)基因DHⅢ增强子-1230A/G基因型与血脂的关系ATCI组各基因亚型血清Lp(a)水平均明显高于对照组,差异具有统计学意义(P<0.05)。而其他血脂指标:TG、TC、HDL-C、LDL-C在同一基因型的组间差异无统计学意义(P>0.05)。同时比较ATCI组不同基因型Lp(a)水平,发现AA、GG、AG基因型中虽然以GG型Lp(a)水平最高,但在不同基因型间差异无统计学意义(P>0.05)。见表 2。
| 组别 | 基因型(例数) | TG(mmol/l) | TC(mmol/l) | HDL-C(mmol/l) | LDL-C(mmol/l) | Lp(a)(mg/l) |
| ATCI组 | AA(6) | 1.55±0.47 | 4.97±1.02 | 1.25±0.23 | 3.01±1.08 | 138.9(1344.9)* |
| GG(67) | 1.82±1.21 | 4.81±1.08 | 1.22±0.33 | 2.74±0.87 | 284.4(1280.8)* | |
| AG(61) | 1.92±1.25 | 4.56±1.17 | 1.26±0.51 | 2.67±0.95 | 193.6(1186.5)* | |
| 对照组 | AA(18) | 1.89±0.92 | 5.23±0.66 | 1.52±0.38 | 2.48±0.74 | 49.25(150.4) |
| GG(44) | 1.54±0.56 | 5.00±1.06 | 1.57±0.66 | 2.36±0.70 | 53.20(98.3) | |
| AG(48) | 1.24±0.37 | 5.00±0.87 | 1.53±0.33 | 2.32±0.71 | 52.05(102.7) | |
| 注:*为与对照组相比,P<0.05。 | ||||||
ATCI组基因型AA、GG、AG的比率分别为4.5%、50.0 %、45.5%;等位基因A、G的频率分别为27.2%和72.8%。对照组基因型AA、GG、AG的比率分别为16.4%、40.0 %、43.6%;等位基因A、G的频率分别为38.2%和61.8%。ATCI组与对照组组间比较结果显示,GG型频率、G等位基因频率显著高于对照组(P=0.006,P=0.01,OR=1.65)。见表 3。
| 组别 | 例数(n) | 基因型[n(%)] | 等位基因频率[n(%)] | |||
| AA | GG | AG | A | G | ||
| ATCI组 | 134 | 6(4.5) | 67(50.0) | 61(45.5) | 73(27.2) | 195(72.8) |
| 对照组 | 110 | 18(16.4) | 44(40.0) | 48(43.6) | 84(38.2) | 136(61.8) |
| χ2 | 10.05 | 6.63 | ||||
| P | 0.006 | 0.01 | ||||
Apo(a)作为Lp(a)的特异性载脂蛋白,在动脉粥样硬化与血栓形成中占主要地位[1],通过以下几种途径发挥作用:①作为纤溶酶原同源体的Apo(a)竞争有活性的纤溶酶原受体而干扰血凝过程、延长血栓。②Apo(a)与富含脯氨酸或羟脯氨酸的胶原质、弹性蛋白等细胞外基质结合。③Apo(a)通过对纤溶酶原活性及激发的依赖纤溶酶激活的转化生长因子-β的抑制,刺激人类平滑肌细胞的增殖和迁移,增加氧化脂质作用,从而促使动脉硬化的发展。④在转基因动物模型中Apo(a)能影响血小板功能、促使内皮功能紊乱、抑制残余乳糜微粒的清除[7]。
目前已确定的影响血浆Lp(a)水平的Ape(a)多态主要有四种[8],包括Apo(a) kringle IV-2数目可变串联重复序列(variable number of tandem repeats,VNTR)、位于5’端调控区的五核苷酸TTTTA重复序列(pentanucleotide TTTTA repeats,PNTR)、位于启动子下游93位的G/T突变、位于DHⅢ增强子的-1230A/G突变。低重复数目的Apo(a)Kringle IV VNTR可独立预测脑卒中、冠心病、进展期动脉粥样硬化等心脑血管疾病[9]。孙莉等[10]2000年开始对3642例中国人回顾性病例对照研究发现,Apo(a) PNTR与血浆Lp(a)呈微弱负相关、低重复数目的PNTR片段与脑血栓和脑出血独立相关,可使脑卒中发病风险提升32%,提示此多态性在中国人部分脑卒中患者中可能有预测发病的价值。位于Apo(a)上游的DHⅢ增强子-1230位点A→G,可导致Apo(a)基因的转录增加2.5倍,使Lp(a)的水平升高70%[6]。该位点在人群中的突变率大于20%[6]。关于该位点的研究,在国外仅见于2003年Puekey等[6]对362例健康白种高加索人的研究和2006年Zidkova等[11]对713例脂质障碍的捷克门诊病人的研究。以上两项研究均提示DHⅢ增强子-1230位点A→G影响血浆中Lp(a)水平。
本研究首次把Apo(a)上游DHⅢ增强子的-1230位点A/G多态同以动脉粥样硬化为主要病理基础的ATCI联系起来。研究发现Lp(a)水平在ATCI组显著高于对照组,而两组间的TG、TC、HDL-C、LDL-C均无显著性差异,提示Lp(a)水平升高可能与ATCI的发病有关,这一结论与LP(a)是与其它血脂代谢无关的脑卒中独立危险因素的观点相一致[3, 4]。进一步研究发现,ATCI组与对照组Apo(a) DHⅢ增强子-1230的基因型AA、GG、AG百分比分别为6.6/16.4、50.2/40.0和43.2/43.6;等位基因频率A/G分别为28.2/38.2和71.8/61.8。ATCI组与对照组比较,Apo(a) DHⅢ增强子-1230 A/G基因型分布和等位基因频率有显著性差异,GG基因型及G等位基因频率在ATCI组明显高于对照组。由此推测Apo(a) DHⅢ增强子-1230 A/G多态性与中国湖南汉族人群ATCI的发病有关,G等位基因可能是其易感基因,其患ATCI的发病风险是A等位基因的1.65倍。
总之,本研究结果提示Apo(a) DHⅢ增强子-1230 A/G多态性与湖南汉族人群ATCI的发病有一定的关联。因此,研究Apo(a) DHⅢ增强子-1230 A/G多态性有助于湖南地区汉族易感人群的筛选,对ATCI的早期防治具有重要意义。
| [1] | Pati U, Pati N. Lipoprotein(a), Atherosclerosis, and Apolipoprotein(a)Gene Polymorphism. Mol Genet Metab, 2000, 71(1-2):87-92. |
| [2] | 段朋仓,刘俊艳.颅内外动脉粥样硬化的易感性与相关危险因素.国际神经病学神经外科学杂志, 2014, 41(2):152-155. |
| [3] | Sacco RL. Newer risk factors for stroke. Neurology, 2001, 57(5 Suppl 2):S31-S34. |
| [4] | 游咏,杨期东,成志,等.脑卒中患者脂蛋白(a)水平及其相关性.中国动脉硬化杂志, 2003, 11(2):163-164. |
| [5] | 姚德斌,万慧.动脉粥样硬化性脑梗死与侧支循环研究进展.江西医药, 2014, 49(9):926-930. |
| [6] | Puckey LH, Knight BL. Sequence and functional changes in a putative enhancer region upstream of the Apolipoprotein(a) gene. Atherosclerosis, 2003, 166:119-127. |
| [7] | Koschinsky ML. Novel insights into Lp(a) physiology and pathogenicity:More questions than answers? Cardiovasc Hematol Disord Drug Targets, 2006, 6(4):267-278. |
| [8] | Beneš P. Polymorphisms in the Apolipoprotein(a) Gene, Plasma Lp(a) and Cardiovascular Risk. Heart Drug, 2003, 3:217-224. |
| [9] | Chiu L, Hamman RF, Kamboh MI. Apolipoprotein A polymorphisms and plasma lipoprotein(a) concentrations in non-Hispanic Whites and Hispanics. Hum Biol, 2000, 72(5):821-835. |
| [10] | Sun L, Li ZH, Zhang HY, et al. Pentanucleotide TTTTA Repeat Polymorphism of Apolipoprotein(a) Gene and Plasma Lipoprotein(a) Are Associated With Ischemic and Hemorrhagic Stroke in Chinese:A Multicenter Case-Control Study in China. Stroke, 2003, 34(7):1617-1622. |
| [11] | Zídková K, Kebrdlová V, Zlatohlávek L, et al. Detection of variability in Apo(a) gene transcription regulatory sequences using the DGGE method. ClinChim Acta, 2007, 376(1-2):77-81. |
 2015, Vol. 42
2015, Vol. 42


