扩展功能
文章信息
- 李立, 许桢源, 郭利娜, 杨杰
- LI Li, XU Zhen-Yuan, GUO Li-Na, YANG Jie
- 全反式维甲酸对缺血再灌注大鼠血脑屏障通透性的影响
- Effects of all-trans retinoic acid on blood-brain barrier permeability in rats with cerebral ischemia/reperfusion injury
- 国际神经病学神经外科学杂志, 2015, 42(3): 238-243
- Disease Surveillance, 2015, 42(3): 238-243
-
文章历史
- 收稿日期: 2015-03-18
- 修回日期: 2015-06-09
众所周知,在缺血再灌注(ischemia/reperfusion,I/R)的早期,血脑屏障( blood-brain barrier,BBB)的不可逆破坏会导致血管源性脑水肿,后者在继发性脑损伤中起重要作用。大量研究证明,炎症、自由基及其它众多因子均参与血脑屏障的破坏[1]。全反式维甲酸(all trans-retinoic acid,ATRA)可以通过抗炎、抗氧化、促进神经再生等多种机制起到脑保护作用[2]。本课题拟采用免疫组化和免疫印迹方法检测全反式维甲酸对缺血再灌注大鼠MMP-9表达的影响,结合脑组织EB含量和TTC染色,探讨全反式维甲酸对缺血后血脑屏障通透性影响,为全反式维甲酸的临床应用提供实验依据。
1 实验材料 1.1 实验动物清洁级Sprague-Dawley雄性大鼠,购自中南大学动物实验中心,10~12周龄,体重200~250 g。饲料由中南大学动物实验中心提供,洁净饮水,昼夜循环照明,室温度控制在20~25℃,湿度控制在50%~70%。每3只大鼠1笼,每2天更换笼舍,每天更换垫料。
1.2 主要材料0.26 μm I/R栓线(北京沙东生物技术有限公司);0.45 μm immobilon PVDF膜(美国Millipore公司);96孔细胞培养板(美国 Corning公司)。
1.3 主要试剂anti-β-Actin 抗体、兔抗羊 IgG-HRP、羊抗兔 IgG-HRP、WB二抗稀释液、WB一抗稀释液、免疫染色(非荧光)二抗稀释液、免疫染色-抗稀释液(南京凯基生物);二甲基亚砜(国药集团化学试剂有限公司);MMP-9 Antibody (C-20)(美国Santa Cruz Biotechnology公司);EB染液(上海恒远生物科技有限公司);TTC染液(南京建成生物工程研究所);全反式维甲酸ATRA(美国SIGMA公司)。
1.4 主要仪器TS-8水平脱色摇床(海门市其林贝尔公司);Eppendorf5242离心机、Eppendorf5810R冰冻离心机(德国Eppendorf公司);TECAN酶标仪(澳大利亚Tecan公司);BIO-RAD化学发光仪(美国伯乐公司)。
2 实验方法 2.1 试验分组与给药大鼠随机分三组:sham组、I/R组和ATRA组,每组各60只。其中I/R组和ATRA组大鼠按ZeaLonga法制造局灶性脑缺血再灌注模型,sham组只行颈部手术,不行血管栓塞。ATRA组大鼠术后立即每日腹腔注射全反式维甲酸(30 mg/kg),sham组和I/R组大鼠每日注射等量二甲基亚砜的溶剂(dimethyl sulfoxide,DMSO),分别于手术后1 d、3 d和7 d取大鼠脑组织标本,根据取材时间每个大组随机分为3个亚组:1 d组、3 d组和7 d组。各亚组根据实验技术不同再分为4个小组,每小组5只大鼠,分别进行TTC染色测脑梗死体积,伊文思蓝染色测EB含量,免疫组化染色和免疫印迹法测MMP-9表达。
2.2 模型制备与评价I/R组和ATRA组大鼠麻醉、固定、消毒,参照ZeaLonga法制作动物模型[3],缺血60 min后,将栓塞线稍向外拔出完成缺血再灌注模型制备。假手术组仅分离颈总动脉未行切口。术后6 h用Bederson法行神经功能评分,1~3分表示造模成功。见表 1。
| Bederson神经功能评分 | |
| 0分 | 无神经功能丧失,活动正常 |
| 1分 | 不能完全伸展左侧前爪 |
| 2分 | 爬行时出现左侧转圈 |
| 3分 | 行走时身体向左侧倾倒 |
| 4分 | 不能行走神智丧失 |
将各组大鼠固定、取脑,将脑组织置于-20℃冰箱中20~30 min,之后自额前极向后连续做冠状切片5片,厚度为2 mm。将脑片置于含有1% TTC染液的培养皿中,37℃恒温避光孵育30 min,然后置于4%多聚甲醛中固定,最后用相机拍照。应用imagepro-plus软件计算各层脑片脑梗死面积之和和各层脑片全脑面积之和。脑梗死比(%)=(梗死部分面积之和/全脑面积之和)×100%。
2.4 伊文思蓝染色从大鼠尾静脉注射2%伊文思蓝溶液2 ml/kg,其黏膜、四肢等表浅部位瞬间变蓝。30 min后,麻醉并暴露大鼠心脏,将输液皮条针头从心尖处插入主动脉根部,用止血钳固定针头位置,眼科剪剪开右心耳,向其内快速滴注生理盐水约300 ml,直至右心耳流出清澈液体。之后取出大鼠脑组织用4℃生理盐水冲洗,滤纸吸去残余水分。待称量完大鼠右侧大脑半球湿重后,将其放入3 ml二甲基甲酰胺溶液中,60℃恒温孵育48 h,10000 r/min离心20 min,取200 μl上清液加入96孔酶标板中,于630 nm处测定吸光度值。对倍稀释法制作伊文思蓝标准曲线,测得的回归方程为Y=0.0975+1.2736x(x为标准液浓度,y为吸光度,R2=0.9503)。根据标准曲线求得各实验组伊文思蓝含量:EB含量(μg/g)=A(μg/ml)×甲酰胺量(ml)÷脑湿重,其中A为测得的伊文思蓝含量。
2.5 免疫组化检测MMP-9大鼠脑组织用多聚甲醛固定后制备石蜡切片。使用SABC法进行MMP-9染色,切片脱蜡后行抗原修复后,滴入一抗抗体(1∶50)37℃恒温2 h,PBS洗4×5 min后,加一滴生物素化二抗溶液,37℃恒温30 min,PBS洗4×5 min后,加一滴SABC即用型试剂,37℃恒温孵育15 min,PBS洗4×5 min。最后DAB显色、苏木精复染、酒精脱水、中性树胶封片。每只大鼠抽取3张接近于连续层面的切片,用Image pro plus软件测定MMP-9阳性细胞的累积光密度和目标区域的面积,两者相除计算每张切片的平均光密度值,最后计算3张切片平均值做统计分析。
2.6 免疫印迹法测MMP-9表达 2.6.1 组织蛋白提取及浓度测定取大鼠右侧大脑半球视交叉至视交叉后0.4 cm脑组织,放入研钵中,研磨至白色粉末。加入适量RIPA+PMSF裂解液,冰上静置30 min。移至预冷的离心管中,10000 r/min,4℃离心5 min,取上清液备用。向96孔酶标板加入待测样品1 μl,重复加样2次,再加入相应剂量去离子水配成总量为20 μl的混合液,再加入200 μl BCA工作液,震荡30 s,37℃恒温孵育15 min。于562 nm处测定吸光度。绘制标准曲线并用以计算待测样品蛋白含量(μg),除以稀释样品总体积(20 ul),即为样品实际浓度(μg/ul)。
2.6.2 凝胶电泳将组织蛋白样品与5×SDS-PAGE以4∶1体积比混匀,沸水浴加热10 min。进行聚丙烯酰胺凝胶电泳后,取出凝胶,根据目的蛋白MMP-9的分子量和内参β-actin分子量切割凝胶,并裁剪大小相当的PVDF膜,将PVDF膜浸泡于100%甲醇中5 min、去离子水2 min、转膜缓冲液15 min。将滤纸、海绵浸泡于转膜液15 min。将三明治(从负极至正极分别为海绵,3层滤纸,胶,PVDF膜,三层滤纸,海绵)和冰袋共同放入转膜槽中,300 mA恒流转膜100 min。取出PVDF膜,5%脱脂奶粉,室温封闭2 h。PVDF膜分别放入1∶500 MMP-9稀释抗体和1∶500 β-actin抗体中,4℃孵育过夜,TBST溶液洗3×10 min。加入1∶5000二抗溶液,室温孵育1 h,TBST洗涤3×10 min。将PVDF膜放入干净干燥的培养皿中,用滤纸洗净PVDF膜上水分,加入发光液,静置1 min。用image lab软件成像。
2.7 统计处理采用统计软件SPSS 16.0进行统计分析,数据均以均数±标准差表示。多组计量资料间的比较采用单因素方差分析,组间差异比较用LSD法。若P<0.05,则差异有统计学意义。
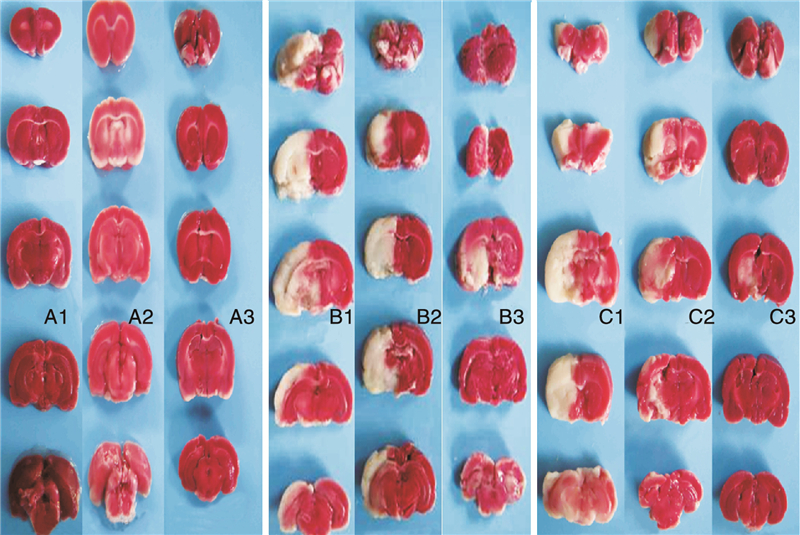
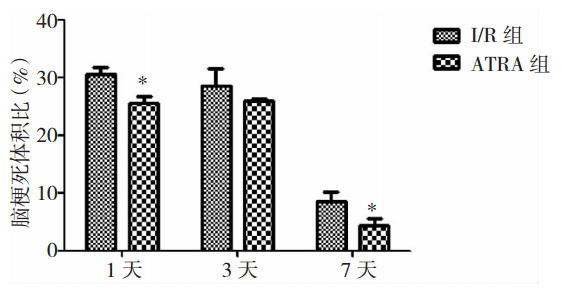
3 结果 3.1 脑梗死体积TTC染色后,正常脑组织呈现鲜红色,缺血梗死部位呈现苍白色,和正常脑组织界限清楚,见图 1。Sham组大鼠脑组织TTC染色无梗死区域,I/R组和ATRA组梗死主要集中于一侧半球。1天、7天时ATRA组脑梗死体积与I/R组比较明显缩小(P<0.05),见图 2。
|
| 图 1 脑组织TTC染色。A:Sham组;B:I/R组;C:ATRA组。1:1天;2:3天;3:7天。 |
|
| 图 2 I/R组和ATRA组梗死体积比(n=5)。注:*为与I/R组对应时间点比较,P<0.05。 |
脑组织EB含量再灌注后1天最高,3天和7天逐渐降低,但7天未降至正常水平。ATRA组和I/R组EB含量各时间点和假手术组相应的时间点相比,含量均明显增高(P<0.05);1天和7天时ATRA组EB含量明显低于I/R组(P<0.05),见图 3。

|
| 图 3 脑组织伊文思蓝含量(n=5, μg/g)。注:△为与假手术组对应时间点比较,P<0.05;*为与I/R组对应时间点比较,P<0.05。 |
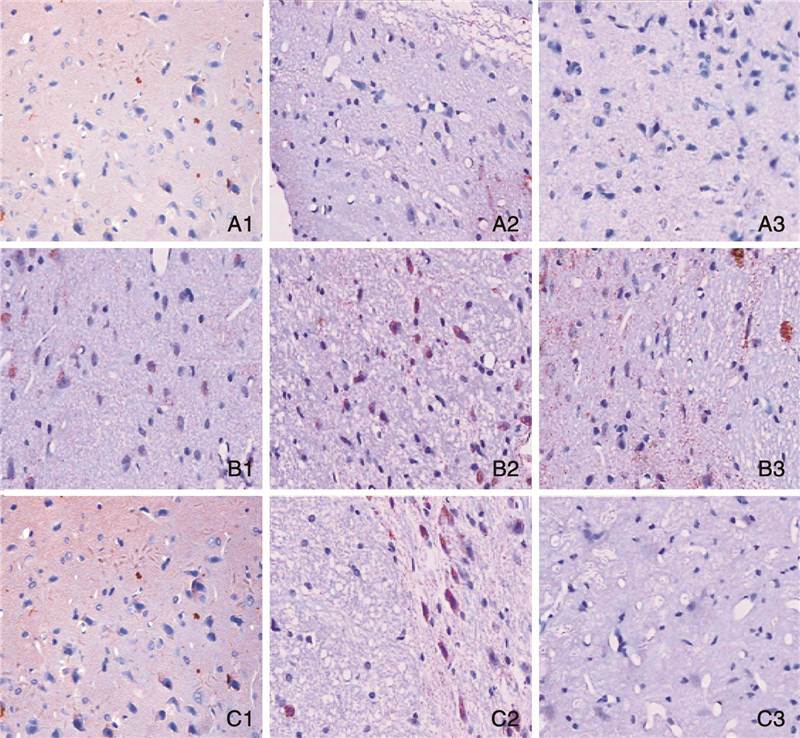
MMP-9在小胶质细胞、缺血神经元、内皮细胞、中性粒细胞中表达,免疫阳性细胞呈现淡棕黄色,见图 4。缺血再灌注后,MMP-9表达于第3天达高峰,后逐渐下降,第7天尚未至正常水平。I/R组和Sham组各对应时间点相比,3天和7天组MMP-9表达明显增高(P<0.05)。ATRA组与I/R组各对应时间点相比,3天和7天组MMP-9表达明显降低(P<0.05),见图 5。
|
| 图 4 免疫组化MMP-9在脑组织中表达。A:Sham组;B:I/R组;C:ATRA组。1:1天;2:3天;3:7天。 |

|
| 图 5 MMP-9蛋白平均光密度值(n=5)。注:△为与假手术组对应时间点比较,P<0.05;*为与I/R组对应时间点比较,P<0.05。 |
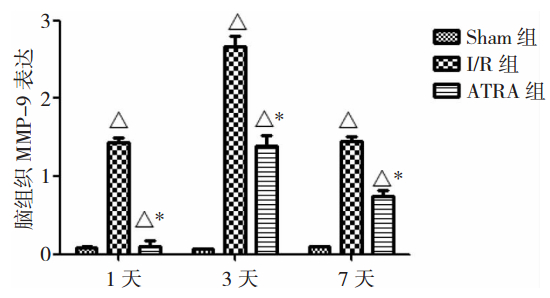
MMP-9相对表达量=(MMP-9条带蛋白灰度值/β-actin条带蛋白灰度值)。MMP-9及β-actin条带见图 6。Sham组与I/R组、ATRA组与I/R组各时间点相比,MMP-9表达差别均有统计学意义(P<0.05),见图 7。

|
| 图 6 Western-blot示脑组织MMP-9表达。 |
|
| 图 7 Western-blot脑组织MMP-9蛋白表达的动态变化(n=5)。注:△为与假手术组对应时间点比较,P<0.05;*为与I/R组对应时间点比较,P<0.05。 |
全反式维甲酸(ATRA)是维生素A的一种活性代谢产物,介导维生素A的绝大部分生物学功能。实验发现,维甲酸在血脑屏障的形成中起重要作用[4]。大鼠脑缺血再灌注后立即腹腔注射ATRA,可明显降低大鼠脑梗死体积,而缺血再灌注前使用ATRA则无此改变[5]。ATRA干预后,ATRA实验组大鼠和I/R组相比,脑梗死体积、伊文思蓝含量明显低于I/R组,说明ATRA可以减轻缺血再灌注后血脑屏障的破坏。
ATRA的血脑屏障保护作用的确切机制尚未明确,可能与影响基因转录有关。目前已经证明脑血管系统平滑肌细胞和内皮细胞均有维甲酸受体(retinoic acid receptor,RAR)的表达。研究表明,维甲酸和RAR结合后,激活的RAR和定位于启动子上的维甲酸反应元件(retinoic acid response element,RARE)结合可促进组织金属蛋白酶抑制剂(tissue iInhibitors of meralloproteinases,TIMPS)表达,调节MMPs/TIMP比例,降低MMP-9的表达;ATRA亦促进核抑制因子NFκB表达,而NFκB和MMP-9启动子结合后,可抑制MMP-9表达[6, 7, 8]。MMP-9通过整合素介导机制改变内皮细胞间的紧密连接,促进内皮细胞从基底膜上脱落,致周细胞、内皮细胞等凋亡,从而增加血脑屏障通透性[9, 10]。进一步研究发现,MMP-9可通过增加转化生长因子β1(transforming growth factor β1,TGF-β1)的含量,从而破坏血脑屏障[11]。本次实验中,缺血再灌注后,MMP-9阳性细胞主要位于梗死区和梗死区周围,MMP-9的表达随缺血时间增加而增加,术后第3天达高峰,7天时仍未降至正常水平。ATRA实验组大鼠和I/R组相比,MMP-9表达显著下降,并且缺血后脑组织伊文思蓝含量和MMP-9的表达有一致性,说明MMP-9和急性期BBB破坏有关,和既往研究结果基本一致[12]。这些说明ATRA可能通过降低MMP-9的含量,从而达到血脑屏障保护作用。
在本次研究中,缺血再灌注后,脑梗死体积及EB含量均于第1天达高峰,MMP-9的表达于第3天达高峰,在相应指标的高峰期,ATRA组相应指标均明显低于I/R组。但MMP-9含量达高峰时(3天时),ATRA组与I/R组脑梗死体积及EB含量差异却无统计学意义,可能与试验误差有关,也可能与MMP-9达高峰时ATRA剂量不足或ATRA药效不足有关,因此需进一步试验论证ATRA的使用剂量,并可将药物作用时间进一步细分以找到更明确的药物作用时间。
| [1] | 侯景明,黎海涛.血脑屏障破坏与脑水肿发生研究进展.国际神经病学神经外科学杂志, 2010, 37(3): 260-263. |
| [2] | Kim JH, Yu KS, Jeong JH, et al. All-trans-retinoic acid rescues neurons after global ischemia by attenuating neuroinflammatory reactions. Neurochem Res, 2013, 38(12): 2604-2615. |
| [3] | Longa EZ, Weinstein PR, Carlson S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats. Stroke, 1989, 20(1): 84-91. |
| [4] | Mizee MR, Wooldrik D, Lakeman KA, et al. Retinoic acid induces blood-brain barrier development. J Neurosci, 2013, 33(4): 1660-1671. |
| [5] | Sato Y, Meller R, Yang T, et al. Stereo-selective neuroprotection against stroke with vitamin A derivatives. Brain Res, 2008, 1241(1):188-192. |
| [6] | Lackey DE, Hoag KA. Vitamin A upregulates matrix metalloproteinase-9 activity by murine myeloid dendritic cells through a nonclassical transcriptional mechanism. J Nutr, 2010, 140(8): 1502-1508. |
| [7] | Dutta A, Sen T, Banerji A, et al. Studies on Multifunctional Effect of All-Trans Retinoic Acid (ATRA) on Matrix Metalloproteinase-2 (MMP-2) and Its Regulatory Molecules in Human Breast Cancer Cells (MCF-7). J Oncol, 2009, 2009: 627840. |
| [8] | Dutta A, Sen T, Chatterjee A. All-trans retinoic acid (ATRA) downregulates MMP-9 by modulating its regulatory molecules. Cell Adh Migr, 2010, 4(3): 409-418. |
| [9] | Bauer AT, Burgers HF, Rabie T, et al. Matrix metalloproteinase-9 mediates hypoxia-induced vascular leakage in the brain via tight junction rearrangement. J Cereb Blood Flow Metab, 2010, 30(4): 837-848. |
| [10] | Yang Y, Thompson JF, Taheri S, et al. Early inhibition of MMP activity in ischemic rat brain promotes expression of tight junction proteins and angiogenesis during recovery. J Cereb Blood Flow Metab, 2013, 33(7): 1104-1114. |
| [11] | McMillin MA, Frampton GA, Seiwell AP, et al. TGFβ1 exacerbates blood-brain barrier permeability in a mouse model of hepatic encephalopathy via upregulation of MMP9 and downregulation of claudin-5. Lab Invest, 2015, doi: 10.1038. |
| [12] | Gasche Y, Fujimura M, Morita-Fujimura Y, et al. Early appearance of activated matrix metalloproteinase-9 after focal cerebral ischemia in mice: a possible role in blood-brain barrier dysfunction. J Cereb Blood Flow Metab, 1999, 19(9): 1020-1028. |
 2015, Vol. 42
2015, Vol. 42


