扩展功能
文章信息
- 苏卢海, 张世渊, 沈波, 胡昌辰
- 垂体腺瘤伴钙化2例诊治报告
- 国际神经病学神经外科学杂志, 2015, 42(2): 166-169
- Disease Surveillance, 2015, 42(2): 166-169
-
文章历史
- 收稿日期:2015-02-05
- 修回日期:2015-04-09
2. 山西省人民医院神经外科, 山西 太原 030012
鞍区肿瘤常见有垂体腺瘤、颅咽管瘤、脑膜瘤等,影像学上伴有钙化表现的临床以颅咽管瘤及脑膜瘤多见[1]。钙化是垂体腺瘤的少见表现,伴有广泛钙化者尤其罕见。2014年我科共收治2例伴有钙化的垂体腺瘤病例,现将诊治情况报告如下。
1 病例报告例1,女,27岁,主因“手指脚趾粗大2年,月经异常伴泌乳1年余”入院。查体:手指脚趾粗大,鼻唇轻度肥厚,头发粗黑,毛发增多,挤压乳头可见乳白色分泌物排出。视力视野及眼底检查:OD 0.2,OS 0.1,双眼中心视野大致正常,双眼周边视野颞上暗点,眼底未见异常改变。激素检查:FT33.34 pg/ml(参考值范围为1.76~6.79),FT40.53 ng/dl(参考值范围为0.6~1.69),PRL33.02 ng/ml(参考值范围为3.34~26.72),hGH36.00 ng/ml(参考值范围为0.010~3.607),TSH0.57 uIU/ml(参考值范围为0.34~5.6),FSH3.76 mIU/ml(参考值范围为4.54~22.51),LH2.80 mIU/ml(参考值范围为19.18~103.03)。甲状腺超声检查示:甲状腺右侧叶囊实性结节。术前头颅CT检查示:蝶鞍扩大,鞍区内可见一类圆形软组织密度影,大小约1.6 cm×1.8 cm,鞍背及鞍底可见部分骨质结构受压变薄,并可见一斑片状骨性密度影,边界较清,并向下突入蝶窦(见图 1A)。颅脑MR检查示:蝶鞍、鞍上池及右侧鞍旁可见一不规则形不均匀长T1低信号、长T2高信号肿块影,大小约1.5 cm×2.3 cm×2.4 cm,轮廓欠清晰,病灶内可见结节显著长T1、短T2低信号影,轮廓欠清晰(见图 1B)。术前诊断为垂体腺瘤(生长激素型)伴钙化。完善术前检查后,在全麻下应用神经导航辅助行内镜下经鼻蝶入路肿瘤切除术。术中切开硬膜见瘤组织质地较软,血供一般,可见鞍底中线近斜坡处钙化团块,桑葚状,质地硬,未予强行切除钙化斑块组织,仔细刮圈刮除瘤组织,可见鞍隔塌陷,脑搏动良好,肿瘤达次全切除。术后光镜下见:细胞增生活跃,可见核分裂像,免疫组化:ACTH(-),TSH(-),FSH(-),hGH(散在+),LH(-),PRL(弱+),Ki-67(+约5%),P53(散在少许+),病理诊断:符合非典型垂体腺瘤(见图 1C、D)。术后次日患者出现口渴及尿量增多等症状,给予积极补液及弥凝治疗。术后1周复查颅脑MR检查示肿瘤次全切除。术后15日患者一过性尿崩症状痊愈,复查激素示hGH及PRL均在正常参考值范围,遂出院。
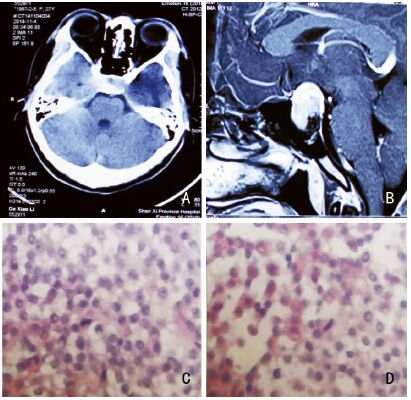
|
| 图 1 A示术前头颅CT检查显示钙化病灶;B示术前颅脑MR检查中钙化病灶;C与D均为切除肿瘤标本术后病理检查涂片。 |
例2,女,22岁,主因“闭经2年余”入院。查体:满月脸,轻度水牛背,锁骨上脂肪增多,向心性肥胖,下腹、腰背及大腿部出现紫纹,颈背部痤疮,面颊与外耳道前方毳毛增多,自诉体重近1年来增加约10 kg。患者睡眠增多,精神稍淡漠。视力视野及眼底检查示:OD 0.5;OS 0.9,均为矫正视力,双眼颞上象限缺损,眼底未见异常改变。激素检查:T30.46 ng/ml(参考值范围为0.88~1.8),T42.23ug/dl(参考值范围为6.04~12.11),FT33.39 pg/ml(参考值范围为1.76~6.79),FT40.28 ng/dl(参考值范围为0.6~1.69),PRL7.23 ng/ml(参考值范围为3.34~26.72),hGH0.065 ng/ml(参考值范围为0.010~3.607),TSH0.71 uIU/ml(参考值范围为0.34~5.6),FSH2.36 mIU/ml(参考值范围为4.54~22.51),LH2.01 mIU/ml(参考值范围为19.18~103.03),ACTH66.718 pg/ml(参考值范围为6.0~40)。术前头颅CT检查示:蝶鞍扩大,鞍区可见一类圆形软组织密度影,边界较清,大小约1.6 cm×1.3 cm,其内可见多发斑点状钙化影,病变向上突入鞍上池,鞍背骨质轻度受压(见图 2A、B)。颅脑MR检查示:蝶鞍内及鞍上池可见大小约2.2 cm×1.5 cm×2.6 cm的不规则形不均匀T1、T2等信号肿块影,轮廓清晰;注射造影剂后,上述病灶呈明显不均匀异常强化;视交叉受压、上抬,双侧海绵窦无受侵(见图 2C)。术前诊断为垂体腺瘤(ACTH腺瘤)伴钙化。完善术前检查,给予优甲乐补充替代治疗后,在全麻下行经眉弓锁孔入路肿瘤切除术。术中见瘤组织质地坚韧,血供一般,可见部分钙化,刮圈刮除瘤组织及小块钙化病灶。再次刮除剩余钙化时出血明显,遂留取部分钙化病灶未予完全切除,肿瘤组织次全切除。术后病理活检结果示:免疫组化:ACTH(小灶状+),TSH(-),FSH(-),hGH(-),LH(-),PRL(+)。病理诊断为:符合垂体腺瘤(见图 2D)。患者术后第二天出现一过性的尿量增多,给予弥凝及补液对症治疗,两日后尿量逐渐恢复正常。术后1周复查颅脑MR检查结果提示肿瘤次全切除。术后两周复查ACTH及皮质醇节律均在正常范围内,遂出院。
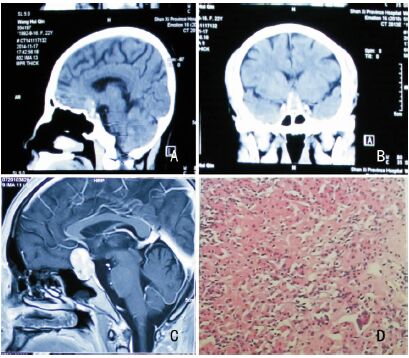
|
| 图 2 A与B示术前头颅CT检查显示钙化病灶;C示术前颅脑MR检查中钙化病灶;D为切除标本术后病理检查涂片。 |
颅内生理性钙化最常见于基底神经节、松果体、大脑镰、脉络丛和小脑幕等部位,直径一般不超过1 cm,病理性钙化主要与外伤、手术、放射、肿瘤、甲状旁腺功能亢进或减退等有关[2]。鞍区的钙化主要发生在颅咽管瘤、脑膜瘤、动脉瘤、视神经与下丘脑胶质瘤、生殖细胞瘤,以及少数拉克氏囊肿。发生在垂体腺瘤者较少见,发生率约0.2%~14%[3, 4, 5, 6]。垂体腺瘤钙化的影像学表现一般为2种外观:瘤内垂体石与蛋壳样钙化。作者复习相关文献,发现与本文病例类似大小及外观特征的垂体腺瘤钙化鲜有报道。
一般认为,垂体瘤的钙化属于营养不良性钙化。在肿瘤生长过程中,由于肿瘤生长过快及体积增大,使肿瘤局部的血液供应不足,无法满足肿瘤的营养需求,产生肿瘤局部组织坏死,细胞内碱性磷酸酶释放,同时又有钙离子及磷酸根离子在局部的沉积,形成钙化斑块。钙化可以发生于任何类型的垂体瘤,但有功能的垂体瘤相对多见,尤其是泌乳素腺瘤。所以有学者认为钙化与肿瘤细胞的自分泌和旁分泌有关[7, 8, 9],加之血管内皮生长因子和骨钙素的参与,进一步促进钙化的形成。此外,尚有部分学者认为钙化是肿瘤细胞发生淀粉样变性的结果[3]。我们查阅相关文献,并结合影像学图像及术中所见,考虑本组病例的钙化可能涉及另一种类型的营养不良性钙化。患者在发现垂体瘤前的“带瘤生存”状态时,曾因某些因素导致亚临床或症状轻微的垂体瘤卒中的发生,出血坏死的细胞通过上述机制及机体的吸收纤维化逐步形成钙化病灶。颅脑MR检查虽无法精确评估钙化的程度,但MR相关技术对含铁血黄素具有特殊表现。仔细阅读术前影像学图像,证实了我们的推断。另外,肿瘤的生长压迫导致鞍内压力增高引起继发性钙化,也可能参与了垂体瘤钙化的发生。对于PRL腺瘤,长期高剂量溴隐亭治疗亦会造成瘤组织的纤维化、钙化,其详细机制尚有待阐明。
通过本组病例,提醒我们遇到伴有钙化的鞍区实性占位病变时,不能单纯考虑颅咽管瘤、脑膜瘤等常见病变,还应考虑垂体瘤的可能。对于此类病变,术前常规行头颅CT及颅脑MR检查,发现钙化的存在,并与其它病变相鉴别,充分了解钙化的部位、程度等详细情况,为手术方案的制定提供至关重要的依据。笔者认为,对于此类患者,必要时候还可以行头颅CTA检查,既可以弥补CT、MRI无法识别的钙化、骨化病灶,还可以排除鞍区巨大动脉瘤的可能,为进一步的治疗提供相对安全的保证。
随着微侵袭神经外科的发展,鞍区肿瘤绝大多数采用经鼻蝶入路手术[10, 11, 12, 13]。对于鞍区伴有钙化的垂体腺瘤,国外学者多主张经鼻蝶入路,但国内学者更倾向于开颅手术。因为经鼻蝶入路术野狭小,术中因有钙化斑,瘤壁不易塌陷,切除钙化斑有困难,且斑块与邻近重要结构的关系不清,术中切除斑块时易伤及颈内动脉和视神经。充分全面评估患者术前的影像学资料后,对本组两例患者,我们分别采用了内镜下经鼻蝶入路和显微镜下经眉弓锁孔入路手术。对于病例1,患者的钙化病灶虽然较大,但未压迫毗邻重要结构,尚未造成明显的占位效应;同时,病灶因钙化已经失去了分泌相应激素的能力,不存在产生hGH的可能。患者迫切希望通过微创手术进行治疗,故我们权衡后采用了内镜下经鼻蝶手术。术中仔细刮除瘤组织,因钙化病变靠近斜坡处,质地坚硬,为防重要结构损伤,未予强行磨除钙化病灶。对于病例2,通过术前影像学表现,我们分析认为钙化为垂体瘤卒中引起,且很大一部分肿瘤位于鞍上区,肿瘤明显的在双侧视神经之间向前上生长,因为视交叉可在肿瘤的后方找到,即后置型视交叉。因此,我们考虑垂体柄也位于肿瘤的后方。肿瘤的鞍上部分位于鞍结节附近,不能在切除了鞍内部分之后完全下降。所以,我们放弃了经鼻蝶入路的打算,转而采用经眉弓锁孔入路手术。这样就能部分控制鞍上肿瘤后方的结构,通过轻微的脑牵拉即可使鞍上区的病灶一览无余,使得肿瘤的鞍内部分可在直视下从双侧视神经之间切除。术中由于钙化与临近血管粘连紧密,剥离过程中出血较多,且电凝时钙化病灶不易收缩止血,故鞍下钙化部分的肿瘤不得不残留。既然这部分瘤组织不引起压迫症状,且失去了分泌激素的功能,考虑到病人的年龄和安全,不再打算进一步切除残余的钙化瘤组织。
本组病例术后均出现一过性的尿崩症状,主要表现为烦渴、多饮、多尿、尿比重和尿渗透压低,经过积极的对症处理及弥凝治疗后,上述症状逐渐缓解,至患者出院时,两例患者的一过性尿崩症状均消失。通过本组病例的分析,我们认为对于钙化的垂体腺瘤进行手术治
疗过程中,并发症较无钙化的垂体瘤更容易发生。这些并发症包括术中出血、术后尿崩(一过性与永久性)、术中重要血管神经的损伤等,而且术中止血更加困难。因为瘤中或瘤周钙化质地硬韧,无论开颅还是经鼻内镜下切除均较困难,术中反复观察、刮圈分离刮除、磨钻磨除,增加了对正常垂体组织的牵拉刺激,也增加了对周围重要解剖结构的误伤,必然增加了术中及术后并发症的发生率。因此,术前仔细查阅影像资料、术中熟练的应用导航定位,以及手术操作时尽可能的轻柔,可以减少手术并发症的发生。
另外,IGF-1和OGTT后的hGH测定对于生长激素型垂体腺瘤的诊疗评估作用已得到公认[14],但由于条件所限,对于本组病例1,我们未能进行这些检验,这是我们案例的缺陷。
虽然引起钙化的详细机制尚未完全阐明,但是,伴随着影像技术的进展和手术方式的多样化,伴有钙化的垂体瘤的诊断和治疗越来越容易,这为钙化的进一步研究提供了重要条件,相信不久明确的机制必将被阐明。
| [1] | 李增跃, 艾立明, 赵广军, 等.鞍区肿瘤CT分析与鉴别诊断(附53例报告).遵义医学院学报, 2005, 28(2):172-173. |
| [2] | Kasliwal MK, Sharma BS. A rare case of pituitary adenoma with calcification: a case report. Turk Neurosurg, 2008, 18(3):232-235. |
| [3] | Yamaguchi S1, Sasajima T, Takahashi M, et al. A case of pleomorphic TSH-producing pituitary adenoma with calcification. No Shinkei Geka, 2004, 32(9):961-967. |
| [4] | Ho DM, Liu HC.Prolactin-containing pituitary adenomas.Their characteristics and comparative study with non-prolactin adenomas.Pathol Res Pract, 1992, 188(3):296-302. |
| [5] | Kato T, Kuwayama A, Takahashi T, et al.Calcification in pituitary adenomas. Neurol Med Chir, 1983, 23(8):633-637. |
| [6] | Webster J, Peters JR, John R, et al.Pituitary stone.Two cases of densely calcified thyrotrophin-secreting pituitary adenomas.Clin Endocrinol, 1994, 40(1):137-143. |
| [7] | 文传志, 赖召攀, 高伯元.垂体瘤伴钙化1例.第三军医大学学报, 2009, 31(8):1538-1544. |
| [8] | Yuriz B, Kazunori A, Hirofumi H, et al.Prolactin-producing pituitary adenomas with abundant spherical amyloid deposition masquerading as extensive calcification.Neurol Med Chir, 2010, 50(11):1023-1026. |
| [9] | Bononi PL, Martinez AJ, Nelson PB, et al. Amyloid deposits in prolactin-producing pituitary adenomas.Endocrinol Invest, 1993, 16(5):339-343. |
| [10] | Cappabianca P, Cavallo L M, Colao A, et al. Endoscopic endonasal transsphenoitlal approach: outcome analysis of 100 consecutive cases. Minim Invasive Neurosurg, 2002, 45(4):193-200. |
| [11] | Wormald PJ, 著.韩德民, 译.内镜鼻窦外科学, 北京:人民卫生出版社, 2006:176-177. |
| [12] | Kabil MS, 著. 张亚卓, 译. 内镜颅底外科, 北京:科学出版社, 2010:39-41. |
| [13] | 张清平, 陈建良.神经内镜下单鼻孔经鼻蝶入路垂体肿瘤的手术治疗.国际神经病学神经外科学杂志, 2006, 33(5): 429-432. |
| [14] | 曹磊, 张亚卓.生长激素型垂体腺瘤的药物治疗现状.中华神经外科杂志, 2013, 29(10):1076-1078. |
 2015, Vol. 42
2015, Vol. 42

 ,
,