扩展功能
文章信息
- 陈玫, 李静
- CHEN Mei, LI Jing
- 静脉注射免疫球蛋白与血浆置换治疗重症肌无力的meta分析
- Intravenous immunoglobulin and plasma exchange in treatment of myasthenia gravis: a meta-analysis
- 国际神经病学神经外科学杂志, 2015, 42(2): 113-117
- Disease Surveillance, 2015, 42(2): 113-117
-
文章历史
- 收稿日期:2015-01-16
- 修回日期:2015-03-23
重症肌无力(myasthenia gravis,MG)是一种由主要由抗乙酰胆碱受体(AchR)抗体介导,细胞免疫依赖,补体参与的神经系统自身免疫性疾病,临床主要表现为骨骼肌的易疲劳感。严重者可累及咽喉肌和呼吸肌,导致咀嚼、吞咽困难及呼吸困难等症状,常危及生命[1]。临床上常采用静脉注射免疫球蛋白(intravenous immunoglobulin,IVIg)或血浆置换(plasma exchange,PLEX)来达到迅速缓解症状的目的。另外,这两种治疗方法也常用于胸腺切除手术的术前准备以及不能耐受或采用其他免疫抑制疗法无效的患者[2]。国内外均有学者对二者治疗MG的疗效及治疗相关不良反应进行了研究,但是,到目前为止还没有相关系统分析方面的文献。因此,我们采用meta分析的方法对已发表的相关研究进行系统分析,以期为临床工作提供循证方面的依据。[KG)][FL)] 1 资料和方法 1.1 检索策略
检索的数据库包括the Cochrane Library、Pubmed、Embase、CNKI和万方数据库。外文数据库检索词为“IV immunoglobulin”、“IVIg”、“plasma exchange”、“PLEX”、“Plasmaspheris”、“myasthenia”、“myasthenia gravis”,中文数据库检索词为“血浆置换”、“免疫球蛋白”、“丙种球蛋白”和“重症肌无力”。检索时间为1977年1月1日至2014年12月30日,语种限制为英语和简体汉语,并对文献的参考文献进行回溯性检索和引文检索。 1.2 纳入与排除标准
纳入标准:①纳入对象为经临床、新斯的明试验、神经电生理检查、AChR或MuSK抗体检测确诊的MG患者;②干预措施分别为IVIg和PLEX;③研究类型:随机对照试验、半随机对照试验及对照试验;④文章有治疗后缓解情况以及治疗相关不良反应等数据;⑤能够获得全文。
排除标准:①研究对象非MG患者;②文章中治疗方法仅为IVIg或PLEX,而不是针对两种治疗方法的疗效及不良反应进行比较;③个案报道或综述类文章;④同一数据重复发表,只选信息最全的一篇。 1.3 质量评价 1.3.1 非随机试验
采用Newcastle.Ottawa Scale (NOS)标准进行质量评价[3]。评分标准:①研究对象选择(4分):病例组定义是否明确?病例组是否有代表性?对照组选择是否合理?对照组定义是否明确?②研究对象的可比性(2分);③结果评价(3分):两组治疗及暴露情况是否记录明确?两组的效果评估方法是否一致?对治疗的反应是否明显记录? 1.3.2 随机对照研究
采用Cochrane Handbook version 5.0.1质量手册[4]方法进行评价。评价内容包括:①分配方案是否随机;②方案是否隐藏;③研究对象和实施方法是否采用盲法;④结果的评估是否采用盲法;⑤是否描述退出和失访情况,并且是否采用了意向分析法;⑥有无选择性报告结局指标;⑦有无其他偏倚来源。若以上标准均表达清楚,则存在相应偏倚风险的可能性低,评为A级;若有1条或1条以上的质量评价标准不清楚,则该研究存在相应偏倚的中度可能性,评为B级;若有1条或1条以上的质量评价标准未提及或不正确,则存在相应偏倚的高度可能性,评为C级。 1.4 资料提取
用事先设计好的资料提取表格提取资料,包括研究类型、样本量、资料的一般情况、治疗方法、临床疗效、治疗期间及随访期间发生的不良反应发生情况及随访时间。由两个研究员独立提取数据,若对数据有不同意见,通过协商解决。 1.5 统计学方法
采用Cochrane协作网提供的Revman v 5.2统计软件进行数据分析。分类变量采用比值比(OR)为效应量,并以95%CI表示。纳入研究结果间的异质性检验采用χ2 检验,以α=0.1为检验水准,当I2<50%时可认为各研究结果之间异质性较小,采用固定效应模型;当I2≥50%时认为各研究结果之间异质性较大,采用随机效应模型。 2 结果 2.1 检索结果
共检索到449篇相关文献,经筛选后共纳入9篇[5, 6, 7, 8, 9, 10, 11, 12, 13, 14],其中6篇为随机对照研究[5, 8, 10, 11, 12, 13],3篇为非随机对照研究[6, 7, 9],1项涉及儿童[9],其余的研究对象均为成人[1, 2, 3, 4, 5, 6, 7, 8, 10, 11, 12, 13],共计2132例样本,其中包括17例青少年MG。5篇为英文文献,4篇为中文文献,发表时间为1998年至2014年。纳入文献基本资料见表 1。
| 文献 | 基线特征 | 研究设计 | IVIg/PLEX组人数 | 随访时间 |
| Gajdos1998 | 年龄、性别、药物治疗情况差异无统计学意义 | 随机对照研究 | 46/41 | 2周 |
| Qureshi1999 | 年龄、性别、病程、重症肌无力严重程度量表评分、高血压、心脏病、肺部疾病的共病率等差异均无统计学意义 | 非随机对照研究 | 24/27 | 4周 |
| Mandawat2010 | 年龄、性别、肤色、疾病严重程度、其他疾病的共病率等差异均无统计学意义 | 非随机对照研究 | 340/1266 | - |
| Barth2011 | 年龄、性别、病程、用药史、重症肌无力严重程度量表评分、肌电图结果、抗体阳性率等差异均无统计学意义 | 随机对照研究 | 41/43 | 60 d |
| Liew2014 | 年龄、性别、抗体类型、药物治疗情况、需手术干情况等差异均无统计学差异 | 非随机对照研究 | 10/7 | 1年 |
| 郝同琴2009 | 年龄、性别、病程、Osserman分型等差异无统计学差异 | 随机对照研究 | 16/13 | 1周 |
| 罗伟汀2012 | 年龄、性别、病程、Osserman分型等差异均无统计学差异 | 随机对照研究 | 40/40 | 1年 |
| 韩雪飞2013 | 年龄、性别、病程、胸腺瘤切除术、各种药物使用情况等差异均无统计学差异 | 随机对照研究 | 27/29 | 21周 |
| 王杰 2014 | 年龄、性别等差异无统计学差异 | 随机对照研究 | 61/61 | - |
3篇非随机试验均为为回顾性研究[6, 7, 9],可比性均较强,NOS质量评分在8~9分,非随机试验中研究质量高。6篇随机试验均未对随机方法进行描述,Barth等[8]的研究提及了分配方法隐藏,其余研究未说明分配方案的隐藏,Barth等[8]的研究在实施过程均采用了盲法,其余研究均未采取盲法,所有研究均提及了结果数据完整性和选择性报告研究结果,均无其他偏倚来源。故随机对照试验质量均为B至C级。文献质量评价结果详见表 2、表 3。
| 文献 | 随机方法 | 分配隐藏 | 使用盲法 | 退出/失访 | 选择性报告结果 | 其他偏移 | 质量等级 |
| Gajdos (1998) | 不清楚 | 不清楚 | 不清楚 | 无 | 无 | 不清楚 | B |
| Barth (2011) | 不清楚 | 是 | 是 | 是 | 无 | 无 | B |
| 郝同琴(2009) | 未提及 | 不清楚 | 未提及 | 无 | 无 | 不清楚 | C |
| 罗伟汀(2012) | 未提及 | 不清楚 | 未提及 | 无 | 无 | 不清楚 | C |
| 韩雪飞(2013) | 未提及 | 不清楚 | 未提及 | 无 | 无 | 不清楚 | C |
| 王杰(2014) | 未提及 | 不清楚 | 未提及 | 无 | 无 | 不清楚 | C |
| 文献 | 研究对象的选择 | 研究对象的可比性 | 结果评价 | 质量评价 |
| Qureshi (1999) | 3 | 1 | 3 | 8 |
| Mandawat (2010) | 4 | 1 | 3 | 9 |
| Liew (2014) | 4 | 1 | 3 | 9 |
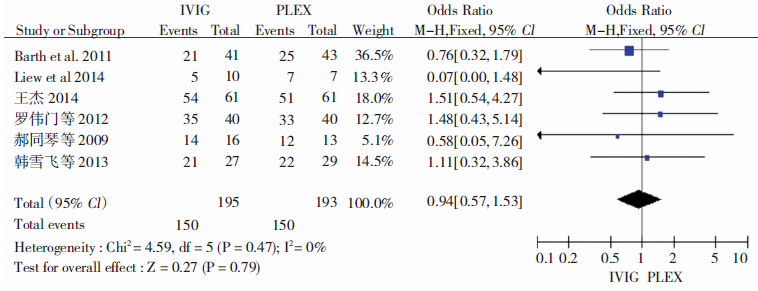
7篇文献比较了IVIg与PLEX治疗MG的有效性,但Gajdos等[5]的研究数据不全,无法用于该meta分析,故我们对其余6篇文献的研究结果进行了分析。其异质性检验结果为I2=0%,可认为各研究结果之间异质性较小,故采用固定效应模型分析,结果显示,IVIg与PLEX治疗MG的有效性无明显差异[OR=0.94,95%CI (0.57,1.32),P=0.79]。见图 1。
|
| 图 1 IVIg与PLEX治疗MG疗效的meta分析 |
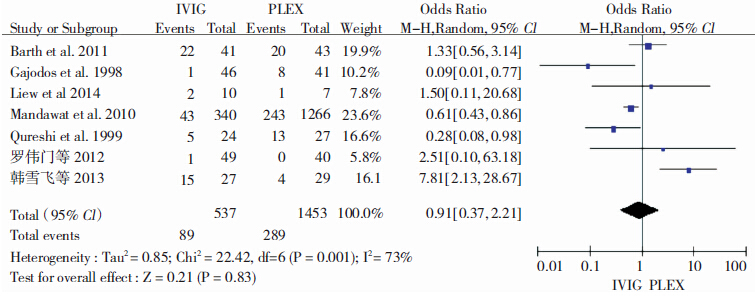
IVIg治疗相关的早期不良反应主要有过敏反应、恶心、呕吐、头痛及发热等,PE治疗相关的早期不良反应主要有枸橼酸盐反应、静脉状态差导致的延误治疗、血管痉挛以及血管迷走反射等。Mandawat等[7]的研究还讨论了两种治疗对心脏、肾脏、感染、血栓形成等的影响。异质性检验结果为I2=73%,认为各研究结果的异质性较大,从而采用随机效应模型进行分析,结果显示IVIg治疗MG的不良反应发生率与PLEX无明显差异[OR=0.91,95%CI (-0.37,2.21),P=0.83]。见图 2。
|
| 图 2 IVIg与PLEX治疗MG不良反应发生率的meta分析 |
目前认为MG是一种由AChR抗体、MuSK抗体、Rynidine抗体等多种抗体介导的,细胞免疫依赖的,补体参与的自身免疫性疾病[1],因此,免疫治疗成为本病治疗的主要方法。IVIg及PLEX是临床上最主要的两种免疫调节治疗方法,尤其应用于疾病恶化需要快速缓解症状、胸腺切除术的术前准备及或患者不能耐受其他免疫抑制剂或其他免疫抑疗法效果不佳时[2]。自1977年第一次应用于治疗MG[14]以来,血浆置换治疗已成为治疗MG的一种常用的治疗方法,通过置换血浆,去除血浆中致病的AChR抗体、MuSK抗体等抗体以及异常的免疫成分,达到迅速缓解症状的目的,对患者的影响较小。但是,血浆置换需要特殊的仪器,操作环境要求无菌化,当患者静脉条件不佳时无法进行该治疗,并且置换的血浆来源于外界有可能会导致患者因换血而感染到其他血液方面的传染性疾病。因此,在治疗重症肌无力的临床应用上存在着一定的局限性。与经典的PLEX相比,IVIg用于临床的时间较晚,其于1983年开始应用于治疗MG[15],其机制主要为中和致病的抗体、与抗体竞争性地与靶向组织部位结合等。与PLEX相比,其治疗方式更为简单,治疗费用相对较低,Heatwole等[16]的研究表明,采用IVIg治疗与采用PLEX治疗相比,每位患者约可节约22326美元的费用。二者应用于MG的治疗均已有30余年,但直到近年来国内外学者才对二者的疗效及治疗相关不良反应进行了研究,并且到目前为止还没有相关系统分析方面的文献。因此,我们采用meta分析的方法对已发表的相关研究进行系统评价,为临床工作提供询证医学方面的依据。
循证医学(evidence-based medicine,EBM)即“遵循证据的医学”,是近年来国际临床医学领域迅速发展起来的一种学说,其核心思想是:医疗决策应尽量以客观研究结果为依据[17]。Meta分析是将系统评价中的多个不同结果的同类研究合并为一个量化指标的统计学方法[17],其作为一种文献研究分析方法,能系统、客观地对多个研究结果进行综合评价和定量分析,提高检验统计效能,增加证据的说服力。本meta分析结果显示,IVIg与PLEX治疗MG的有效性无明显差异,故从循证医学方面验证了IVIg治疗MG的有效性,另外,IVIg治疗相关的早期不良反应主要有过敏反应、恶心、呕吐、头痛及发热等,PE治疗相关的早期不良反应主要有枸橼酸盐反应、静脉状态差导致的延误治疗、血管痉挛以及血管迷走反射等。Meta分析结果显示二者不良反应的发生率无明显的差异,表明IVIg在MG的治疗中是安全可靠的。加之Heatwole等[16]的研究表明采用IVIg治疗可较大程度的节约医疗费用,并且其对设备及环境要求低,治疗方式相对简单。因此该治疗方式值得在临床工作中进行推广。
Meta分析的结论比单个研究较为合理,是临床决策的重要参考,但Meta 分析不能代替大规模、多中心的临床流行病学研究。本研究因纳入研究的设计、IVIg及PLEX的治疗方案在各研究中的差异以及患者年龄、随访时间等因素的差异,势必会对结果产生一定的影响。并且纳入的样本含量不够多,纳入的研究质量参差不齐,也影响结局的可靠性。因此,本研究结论尚需更多更高质量、大样本的随机对照研究来进一步证实。
| [1] | Vincent A, Palace J, Hilton-Jones D. Myasthenia gravis. Lancet, 2001, 357(9274): 2122-2128. |
| [2] | Meriggioli MN, Sanders DB. Autoimmune myasthenia gravis: emerging clinical and biological heterogeneity. Lancet Neurol, 2009, 8(5): 475- 490. |
| [3] | Wells GA, Shea BO, Connell D, et al. The Newcastle-Ottawa Scale (NOS) for assessing the quality of nonrandomized studies in meta-analyses. 2010, http://www.ohri.ca/programs/clinical-.epidemiology/oxford.htm. |
| [4] | Higgins J, Green S. Cochrane handbook for systematic reviews of intervensions 5.1.0. Cochr Collabor, 2011, http://handbook.cochrane.org/. |
| [5] | Gajdos P, Chevret S, Clair B, et a1. Plasma exchange and intravenous immunoglobulin in autoimmune myasthenia gravis. Ann N Y Acad Sci, 1998, 841: 720-726. |
| [6] | Qureshi AI, Choudhry MA, Akbar MS, et a1. Plasma exchange versus intravenous immunoglobulin treatment in myasthenic crisis. Neurology, 1999, 52(3): 629-632. |
| [7] | Mandawat A, Kaminski HJ, Cutter G, et al. Comparative analysis of therapeutic options used for myasthenia gravis. Ann Neurol, 2010, 68(6): 797-805. |
| [8] | Barth D, Nabavi Nouri M, Ng E, et a1. Comparison of IVIg and PLEX in patients with myasthenia gravis. Neurology, 2011, 76(23): 2017-2023. |
| [9] | Liew WK, Powell CA, Sloan SR, et al. Comparison of Plasmapheresis and Intravenous Immunoglobulin as Maintenance Therapies for Juvenile Myasthenia Gravis. JAMA Neurol, 2014, 71(5): 575-580. |
| [10] | 郝同琴, 李闯, 刘建萍.丙种球蛋白与血浆置换治疗重症肌无力的疗效比较.医学信息(内·外科版), 2009, 22(3): 212-214. |
| [11] | 罗伟汀.大剂量静注免疫球蛋白对危重重症肌无力的疗效观察.当代医学, 2012, 18(19): 11-13. |
| [12] | 韩雪飞, 郭莹, 张红, 等.免疫调节疗法治疗重症肌无力临床观察.临床荟萃, 2013, 28(12): 1355-1357. |
| [13] | 王杰.大剂量静注免疫球蛋白对危重重症肌无力的疗效观察.中国卫生产业, 2014, 11(13): 117-118. |
| [14] | Finn R, Coates PM. Plasma exchange in myasthenia gravis. Lancet, 1977, 1(8004): 190-191. |
| [15] | Dau PC. Immune globulin intravenous replacement after plasma exchange. J Clin Apher, 1983, 1(2): 104-108. |
| [16] | Heatwole C, Johnson N, Holloway R, et al. Plasma exchange versus intravenous immunoglobulin for myasthenia gravis crisis: an acute hospital cost comparison study. J Clin Neuromuscul Dis, 2011, 13(2): 85-94. |
| [17] | 李幼平, 李静.循证医学.第2版.北京:高等教育出版社, 2009. |
 2015, Vol. 42
2015, Vol. 42


