扩展功能
文章信息
- 鲁东
- LU Dong
- 复方血栓通胶囊对动脉阻塞致缺血性脑卒中小鼠cPKCγ表达水平及神经功能损伤程度的影响
- Effect of compound Xueshuantong capsules on expression level of conventional protein kinase C γ and degree of nerve injury in mice with artery occlusion-induced ischemic stroke
- 国际神经病学神经外科学杂志, 2015, 42(2): 109-112
- Disease Surveillance, 2015, 42(2): 109-112
-
文章历史
- 收稿日期:2015-01-09
- 修回日期:2015-03-23
血管再通治疗是目前治疗缺血性脑卒中重要的手段及方法,再灌注后脑水肿是导致脑卒中患者病情加重的重要原因之一[1]。有效减轻脑水肿对改善脑卒中患者病情,提高患者治疗效果具有积极的意义[2]。近年相关研究指出[3],脑水肿的形成及发展与脑内源性经典型蛋白激酶Cγ亚型(conventional protein kinase C γ,cPKCγ)表达水平下调有密切的关系。复方血栓通胶囊具有抑制血小板聚集,降低血小板活性,提高纤维蛋白溶解酶活性,减少缺血血管进一步损伤,增强血管舒张功能的作用,可有效改善脑卒中后再灌注[4]。本研究将通过建立缺血性脑卒中小鼠模型探讨复方血栓通胶囊防治缺血性脑卒中的效果及作用机制,旨在为临床用药提供指导。 1 材料与方法 1.1 实验动物
选取60只健康成年昆明小鼠(山东中医药大学实验动物中心提供;许可证号:SCXK(鲁))为实验研究材料,雌雄兼用,年龄为6~8周,体重为15~20 g,所有小鼠给予常规饲料正常喂养。 1.2 试剂及仪器
复方血栓通胶囊(广东众生药业股份有限公司,国药准字:Z20030017);尼莫地平(扬子江药业集团有限公司,国药准字:H20045275);戊巴比妥(湖北恒业化工有限公司);兔源性抗cPKCγ、β-tublin一抗、辣根过氧化物酶标记的羊抗兔二抗(美国Sigma公司);细胞漂洗液(美国BioDev Tech公司);ECL试剂(上海晶美生物公司提供)。EL204电子天平(上海精密仪器有限公司);DGX-924513-2烘箱(上海福马精密仪器有限公司)。 1.3 动物分组及模型制备
根据随机数字表将小鼠分为假性手术组、模型对照组、尼莫地平组(0.4 g/kg)及复方血栓通胶囊低剂量组(0.75 g/kg)、中剂量组(1.50 g/kg)及高剂量组(2.25 g/kg),每组各10只。
各组小鼠灌胃给药,1次/d,持续用药7 d,末次用药后1 h,以50 mg/kg戊巴比妥溶液腹腔注射麻醉,颈部正中切口将右侧颈外动脉及总动脉暴露,分离、结扎颈总动脉近心端、颈外动脉,游离颈外动脉远心端,将颈内动脉结扎,缺血30 min后拔出鱼线再行灌注。假性手术组只将右侧颈外动脉及总动脉暴露,不进行结扎。尼莫地平组、复方血栓通胶囊低剂量组、中剂量组、高剂量组小鼠于开始灌注时点立刻灌胃给药,假性手术组、模型对照组,以后每12 h灌胃一次,持续用药48 h。假性手术组、模型对照组于相同时间点给予等量生理盐水灌胃,所有小鼠造模后均正常喂养。 1.4 神经功能评分
采用改良Bedersen法,0分:无脑功能缺损;1分:对侧前肢屈曲;2分:拉尾时动物对侧前肢抓力下降;3分:拉尾时小鼠向对侧旋转,且小鼠自发向各个方向运动;4分:小鼠向对侧自发性旋转。同时记录不同缺血时间点(1 h、6 h、12 h、24 h和48 h)小鼠神经功能评分。 1.5 脑含水量测定
实验结束后将各组小鼠脱臼处死,取出缺血侧大脑组织后称取湿重,并放入100℃烤箱中恒温烘烤24 h后称重。含水量=(湿重-干重)/湿重×100%。 1.6 Western blot法测定cPKCγ蛋白表达
按照每侧大脑半球加入0.3 ml细胞漂洗液的比例,将脑组织置入4℃匀浆机中搅拌,离心处理15 min弃去上清液,并加入组织蛋白裂解液0.4 ml,冰浴孵育60 min,离心处理后收集上清液,测定蛋白浓度后,以每份150 μL与上样缓冲液50 μL混合,置于100℃下加热5 min,并置于室温下冷却。每组取出40 μg总蛋白进行电泳(20~30 mA,10% SDS-PAGE)及转膜(40 mA)1 h。分别加入兔源性抗cPKCγ、β-tublin一抗、辣根过氧化物酶标记的羊抗兔二抗,并进行免疫杂交,采用ECL试剂染色,并于暗室下行X线曝光、显影及定影。 1.7 统计学方法
采用SPSS 17.0数据软件进行统计分析,计量资料采用均数标准差(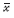 ± s)表示,组间计量资料采用成组t检验,进一步两两比较采用LSD-t法,P<0.05为差异具有统计学意义。
2 结果
2.1 实验情况
± s)表示,组间计量资料采用成组t检验,进一步两两比较采用LSD-t法,P<0.05为差异具有统计学意义。
2 结果
2.1 实验情况
模型对照组小鼠实验过程中有2只术中出血过大而死亡,尼莫地平组有1只小鼠麻醉后死亡,复方血栓通胶囊低剂量组有1只麻醉后死亡,中剂量组及高剂量组各有1只因手术大量出血而死亡。模型对照组有4只小鼠测定了脑含水量,有4只小鼠行Western blot测定,尼莫地平组、复方血栓通胶囊低剂量、中剂量及高剂量组均有5只小鼠测定了脑含水量,有4只小鼠行Western blot测定。 2.2 各组小鼠不同时间点神经功能评分比较
复方血栓通低、中、高剂量组在缺血后12 h、24 h和48 h神经功能损伤评分显著低于假性手术组(P<0.05),见表 1。
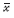 ± s)
± s)
| 组别 | 只数 | 剂量(g/kg) | 各时间点神经功能评分 | ||||
| 1 h | 6 h | 12 h | 24 h | 48 h | |||
| 假性手术组 | 10 | – | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 |
| 模型对照组 | 8 | – | 2.43±1.25 | 3.78±0.96 | 3.82±1.03 | 3.86±1.14 | 3.92±0.98 |
| 尼莫地平组 | 9 | 0.4 | 2.52±1.18 | 3.48±1.09 | 3.12±0.96 | 2.82±0.82 | 2.69±0.98 |
| 复方血栓通胶囊组 | |||||||
| 低剂量组 | 9 | 0.75 | 2.54±1.25 | 3.59±0.96 | 2.48±1.02ab | 2.26±0.89ab | 2.22±0.82ab |
| 中剂量组 | 9 | 1.50 | 2.48±0.96 | 3.48±1.05 | 2.12±0.93abc | 2.02±0.86abc | 1.12±0.79abc |
| 高剂量组 | 9 | 2.25 | 2.47±0.92 | 3.67±1.12 | 2.09±0.87abc | 1.92±0.78abc | 1.45±0.56abc |
| 注:a为与假性手术组比较,差异具有统计学意义,P<0.05;b为与模型对照组比较,差异具有统计学意义,P<0.05;c为与与低剂量组比,差异具有统计学意义,P<0.05。 | |||||||
实验结束时复方血栓通中、高剂量组脑含水量低于模型对照组,差异有统计学意义(P<0.05),见表 2。
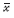 ± s)
± s)
| 组别 | 只数 | 剂量(g/kg) | 含水量 |
| 假性手术组 | 4 | – | 77.12±0.45 |
| 模型对照组 | 4 | – | 79.96±0.42 |
| 尼莫地平组 | 4 | 0.4 | 77.32±0.38a |
| 复方血栓通胶囊 | |||
| 低剂量组 | 4 | 0.75 | 77.84±0.29a |
| 中剂量组 | 4 | 1.50 | 77.15±0.18a |
| 高剂量组 | 4 | 2.25 | 77.98±0.32a |
| F值 | 5.986 | ||
| P值 | 0.008 | ||
| 注:a为与模型对照组比较,差异具有统计学意义,P<0.05。 | |||
实验结束后复方血栓通各组脑cPKCγ蛋白水平均高于模型对照组,差异有统计学意义(P<0.05),见表 3。
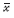 ± s)
± s)
| 组别 | 只数 | 剂量(g/kg) | cPKCγ蛋白水平 |
| 假性手术组 | 4 | – | 92.36±3.23 |
| 模型对照组 | 4 | – | 44.18±4.72 |
| 尼莫地平组 | 4 | 0.4 | 72.02±5.78ab |
| 复方血栓通胶囊 | |||
| 低剂量组 | 4 | 0.75 | 70.12±6.02ab |
| 中剂量组 | 4 | 1.50 | 84.18±4.72ab |
| 高剂量组 | 4 | 2.25 | 83.56±3.86ab |
| F值 | 8.123 | ||
| P值 | 0.000 | ||
| 注:a为与假性手术组比较,差异具有统计学意义,P<0.05;b为与模型对照组比较,差异具有统计学意义,P<0.05。 | |||
脑水肿是指脑实质液体异常聚集导致脑组织惠普细胞体积增大,引起脑卒中后水肿的原因包括血管源性水肿及细胞毒性水肿[5]。前者是由于脑组织缺血缺氧导致血脑屏障损伤使得液体进入脑组织所致[6];后者由于细胞能量代谢障碍导致组织离子泵功能障碍,导致细胞内K+、Na+失衡引起细胞内渗透压增高导致细胞水肿[7]。本研究通过结扎单侧颈总动脉建立小鼠缺血性脑卒中模型,让小鼠一侧大脑缺血30 min后拔出鱼线再行灌注使得基底节局部组织梗死,从而造成大脑明显水肿。一般水肿高峰发生在缺血再灌注后48 h,这一过程与人类卒中后再灌注所致的水肿形成过程相似,同时缺血30 min可有效避免缺血时间过长导致小鼠脑组织大面积梗死液化而影响脑水肿的观察及测量。
蛋白激酶C(PKC)是一类可使得苏氨酸残基及蛋白分子内丝氨酸残基发生磷酸化的蛋白激酶[8]。cPKCγ是最具特征性的亚型之一,它主要在脊髓及大脑神经元中表达,因此可作为缺血性脑损伤的重要分子。它在长时程增强及长时间抑制形成、受体功能调节、突触可塑性及细胞凋亡、缺血及低氧性脑病等生理病理性行为中发挥着重要的作用[9]。Gulati等[10]研究指出,乙醇作为强力神经保护剂,能有效减少急性缺血性脑卒中大鼠脑梗死面积,并能有效改善大鼠神经行为学功能,而这一作用可能与大鼠体内cPKCγ蛋白被激活有关。潘志刚等[11]研究发现,cPKCγ具有脑保护作用,能有效抑制低氧预处理诱导继发性缺血损伤,可有效保护脑神经功能。
复方血栓通胶囊主要成分包括黄芪、三七、丹参、玄参等。其中三七、丹参活血化瘀,玄参养阴、凉血、清热,黄芪益气补气。相关研究指出[12],复方血栓通能有效抑制血小板聚集,降低血液黏稠度,提高纤维蛋白溶解酶活性,减少血管内皮舒张功能,保护血管内皮。同时复方血栓通胶囊具有改善钙离子通道阻断作用,促进神经功能恢复的作用。本研究发现,在复方血栓通干预下,小鼠缺血再灌注后12 h、24 h和48 h的神经功能评分及脑含水量显著低于假性结扎组及阳性对照组,从而表明该药对于脑组织病变细胞有明显促进局部血液循环、改善缺血缺氧状态,从而促使受损细胞逐渐恢复,改善脑组织功能。多项药效学研究证实,复方血栓通胶囊能改善大鼠中动脉缺血模型神经症状,延长大鼠跳台潜伏期和减少出错次数及脑梗死面积,病理检查证实脑组织皮质坏死灶面积明显小于模型组,并可见新生毛细血管和肌质细胞增生。本研究发现复方血栓通胶囊可能通过促使cPKCγ蛋白表达而起到减轻脑缺血再灌注后脑水肿的作用,从而有效改善小鼠神经功能,这为分子水平研究脑卒中缺血机制及发现新的治疗靶点提供指导。分析其可能作用机制与复方血栓通胶囊黄芪中的皂苷可通过对糖元高能磷酸化合物的利用,增强乳酸、丙酮酸代谢,降低能耗,抑制凋亡,诱导cPKCγ表达,抗低氧、抗水肿、清除自由基,提高脑内超氧化物歧化酶(SOD)活性,阻滞钙离子通道,抑制过氧花化物释放,从而能有效减少血小板聚集,改善血液凝固有关。综上所述,复方血栓通胶囊能有效改善缺血性脑卒中小鼠脑水肿程度,减轻神经功能损伤,其作用机制可能与其促进cPKCγ蛋白水平表达有关。
| [1] | 赵雅宁, 高锦云, 吴玉静, 等.缺血性脑卒中患者执行功能障碍影响因素研究.重庆医学, 2012, 41(20): 2058-2061. |
| [2] | 李洁霏, 章欣欣, 钟洁, 等.脑内源性cPKC gamma水平影响缺血性卒中小鼠脑梗死体积和神经功能损伤.基础医学与临床, 2013, 33(11): 1452-1459. |
| [3] | 韩松, 张楠, 尹艳玲, 等.蛋白激酶Cγ在低氧预适应脑保护中的作用及其缺血性卒中鼠脑半影区内相互作用蛋白鉴定.首都医科大学学报, 2013, 34(5): 698-703. |
| [4] | 梁洁萍, 刘忠政, 彭维, 等.复方血栓通胶囊HPLC指纹图谱质量控制方法研究.中药材, 2012, 35(11): 1854-1858. |
| [5] | 魏凯.β-Arrestin对血管收缩功能及缺血性脑卒中的影响.第二军医大学, 2013. |
| [6] | Vagal AS, Khatri P, Broderick JP, et al. Time to Angiographic Reperfusion in Acute Ischemic Stroke: Decision Analysis. Stroke, 2014, 12(2): 123-125. |
| [7] | Wang WL, Li M, Chen Q, et al. Hemorrhagic Transformation after Tissue Plasminogen Activator Reperfusion Therapy for Ischemic Stroke: Mechanisms, Models, and Biomarkers. Mol Neurobiol, 2014, 5(7): 23-25. |
| [8] | Lucke-Wold BP, Turner RC, Logsdon AF, et al. Common Mechanisms of Alzheimer's Disease and Ischemic Stroke: The Role of Protein Kinase C in the Progression of Age-Related Neurodegeneration. J Alzheimers Dis, 2014, 11(2): 42-46. |
| [9] | Shao B, Bayraktutan U. Hyperglycaemia promotes cerebral barrier dysfunction through activation of protein kinase C-β. Diabetes Obes Metab, 2013, 15(11): 993-999. |
| [10] | Gulati P, Singh N.Neuroprotective mechanism of ischemic postconditioning in mice: a possible relationship between protein kinase C and nitric oxide pathways. J Surg Res, 2014, 189(1): 174-183. |
| [11] | 潘志刚, 刘康达, 胡美玉, 等.蛋白激酶C在肝细胞生长因子诱导血管内皮生长因子表达过程中的作用.中国临床医学, 2011, 18(5): 595-598. |
| [12] | 张波, 秦佰焰.济生肾气丸联合复方血栓通胶囊治疗早期糖尿病肾病.中国实验方剂学杂志, 2012, 18(15): 316-317. |
 2015, Vol. 42
2015, Vol. 42
